【话险危夷】脂肪堆积增加可能与重症患者的严重肌肉萎缩有关:一项前瞻性观察研究
时间:2026-05-06 19:25:45 热度:37.1℃ 作者:网络
简介
这项前瞻性观察研究旨在探究危重症患者脂肪堆积与肌肉萎缩的关系,挑战了传统的“肥胖悖论”。研究纳入108名重症监护病房患者,通过CT测量脂肪面积,超声监测股直肌横截面积变化。结果发现,肥胖组(尤其皮下脂肪堆积者)的严重肌肉萎缩发生率(48%)显著高于消瘦组(27%),且肥胖是肌肉萎缩的独立危险因素(校正比值比2.52)。机制分析显示,肥胖患者早期β-羟基丁酸水平较低,可能与酮体生成减少有关。结论提示,脂肪堆积增加反而加剧肌肉萎缩,不支持肥胖在危重症中的保护作用。
目的:肥胖症被认为能减轻危重症患者的肌肉萎缩,原因在于其能增强酮体生成。本研究旨在探究危重症患者脂肪量、酮体与肌肉萎缩之间的关联。
方法:我们于2021 年 11 月至2023 年 10 月在急诊重症监护病房(ICU)开展了一项前瞻性研究,纳入了预计在ICU 住院时间≥7 天且入院24 小时内进行了腹部计算机断层扫描(CT)的成年患者。根据CT 测量的脂肪面积,将患者分为肥胖组和消瘦组。主要结局指标为严重肌肉萎缩,定义为从第1 天到第7 天,通过超声测量的股直肌横截面积减少超过10%。
结果:在134 名入组患者中,108 名患者可评估(57%为男性,中位年龄73 岁)。肥胖组严重肌肉萎缩的发生率(48%)高于消瘦组(27%,p = 0.023)。多变量分析证实肥胖组肌肉萎缩的风险更高(校正比值比2.52,p = 0.034)。β-羟基丁酸(BHB)水平与脂肪面积呈负相关,并与肌肉萎缩风险降低相关。
结论:与我们的假设相反,肥胖增加了肌肉萎缩的风险,这可能是由于酮体生成减少所致。
一、前言
重症监护病房(ICU)出院后持续存在的功能障碍是ICU 生存者面临的一个重大问题,包括认知、心理和身体方面的损伤。身体损伤最常见的是ICU 获得性肌无力(ICU-AW),其特征是由于危重症导致的全身性、对称性肌肉无力。肌肉萎缩是ICU-AW 的典型特征,在ICU 住院的头7 天内,骨骼肌质量每天减少近2%。肥胖症的特征是脂肪过度堆积,通常与多种疾病和死亡风险增加有关。然而,在某些情况下,肥胖却具有保护作用,比如在危重症中,这种现象被称为“肥胖悖论”。肥胖对肌肉萎缩和ICU获得性肌无力也有保护作用,肥胖个体中脂解和酮体生成的增加可能介导了这种保护作用。然而,在大多数之前评估肥胖悖论的临床研究中,肥胖仅依据过高的体重指数(BMI)来定义。由于BMI不仅反映脂肪组织,还反映其他瘦组织,如骨骼肌,因此这些保护作用是否源于脂肪堆积增加仍不清楚。因此,评估肌肉萎缩与脂肪堆积之间的直接关系至关重要。我们假设脂肪堆积增加会减轻重症监护病房(ICU)住院期间的肌肉萎缩,这是由于脂肪分解和酮体生成增加所致。由于脂肪组织的多种功能会因其分布(即皮下脂肪和内脏脂肪)的不同而有所差异,我们还假设脂肪堆积与肌肉萎缩之间的关联会受到脂肪分布的影响。为了验证这一假设,我们开展了一项单中心前瞻性队列研究。
二、材料与方法
研究环境与研究对象
我们在山口大学医院的20 张床位的急诊重症监护室(ICU)进行了一项单中心前瞻性队列研究。我们筛选了2021 年 11 月至2023 年 10 月期间入住ICU 且预计ICU 住院时间7 天或更长,并在入住ICU 后 24 小时内进行了腹部CT 检查的成年患者。年龄小于18 岁的患者、腹部CT 不适合测量肌肉和脂肪的患者、患有严重基础性衰弱(即临床衰弱量表评分≥7)的患者、患有神经肌肉疾病或中风的患者、双侧股骨损伤导致无法进行肌肉超声检查的患者,以及主治医生认为不适合参与研究的其他患者均被排除在外。
数据收集
我们收集了以下基线数据:年龄、性别、身高、体重、体重指数(BMI)、临床衰弱量表评分、入院前日常生活活动能力(ADL)评分(通过巴氏指数和功能独立性评定量表(FIM)评估)、入住重症监护病房(ICU)的原因、APACHE II 评分以及入院时SOFA评分。巴氏指数和FIM 通过与患者、家属或其护理人员的访谈进行评估。SOFA 评分也在第3 天和第7 天进行评估。在第1 天、第3 天和第7 天,采集血液样本以检测酮体(即β-羟基丁酸[BHB]和乙酰乙酸[AA])、血脂(即游离脂肪酸[FFAs]、甘油三酯、低/高密度脂蛋白胆固醇[LDL/HDL-C])和脂肪因子(即脂联素和瘦素)。脂联素和瘦素通过市售的酶联免疫吸附测定试剂盒进行分析。计算了截至第7 天的平均热量和蛋白质摄入量,以及某些药物(胰岛素、儿茶酚胺、神经肌肉阻滞剂和全身性类固醇)的使用量。在重症监护病房(ICU)住院期间,机械通气和肾脏替代治疗的使用情况均有记录。在本研究中,我们采用腹部CT 来估算脂肪组织或骨骼肌的量。利用患者入住重症监护病房(ICU)后24 小时内进行的腹部CT,我们根据先前的研究计算了脂肪面积和腹部肌肉面积(AMA)。测量了第三腰椎水平的脂肪面积和腹部肌肉面积。脂肪面积被定义为Hounsfield 单位(HU)范围在-190 至 30 之间的区域,并通过工作站预装的程序半自动地将其分为内脏脂肪面积(VFA)和皮下脂肪面积(SFA)。总脂肪面积(TFA)定义为VFA 和 SFA 的总和。AMA 被定义为在手动勾勒出的骨骼肌(包括腰大肌、竖脊肌、腰方肌、腹横肌、腹外斜肌、腹内斜肌和腹直肌)内HU范围在-29 至 +150 之间的区域。此外,还以同样的方式测量了双侧股骨小转子下方的股四头肌面积(QMA),并取其平均值用于分析。如果可行,这些身体成分分析也会在第4 天至第10 天之间进行的后续腹部CT 扫描中进行。
评估方法
为评估ICU住院期间的肌肉萎缩情况,我们依照先前的研究8,在第1、3和7天通过超声测量了股直肌的横截面积(CSARF)。肌肉超声检查由经验丰富的ICU医生进行,且医生对患者分组情况不知情。测量时CSARF,患者取仰卧位,肢体伸直并放松。在髂前上棘和髌骨近端边缘的中点处进行测量CSARF,并在首次测量时做好标记,以便后续测量。测量时,将线阵探头垂直于股直肌放置,施加最小的压力并使用充足的耦合剂,以避免组织变形。除单侧肢体受伤无法进行肌肉超声检查的患者外,每侧均测量3次,取平均值作为结果CSARF。我们将本研究的主要结局定义为严重肌肉萎缩,即在第1 天至第7 - 8 天期间体重下降CSARF 超过10%,因为其他直接反映肌肉无力的参数(如握力和医学研究委员会[MRC] 总分)在非计划入院的病例中,其患病前和患病后的状态很少能进行比较。我们还评估了以下次要结局:从第1 天到第3 天和第7 天的体重变化CSARF;基线和随访CT 之间身体成分(即脂肪面积、四肢肌肉面积和四肢肌肉质量)的变化;ICU 出院时的握力和MRC 总分;出院时的生存情况;以及患病前和出院时的Barthel 指数和FIM的变化。两个CT 之间身体成分的变化以每天变化的百分比来评估,计算方法为从入院CT 到随访CT 的差值除以基线值和两个CT 之间的天数。生存情况、Barthel 指数和FIM 也通过电话访谈患者进行评估。在6 个月和12 个月时对患者家庭或其护理人员进行了调查。通过邮寄36 项简明健康调查问卷(SF-36)第2 版对患者报告的生活质量(QOL)进行了评估。
三、结果
在研究期间,筛选了395 名有腹部CT 数据的成年患者,其中134 名患者(33.9%)被纳入研究。在这些患者中,26 名患者(19.4%)的主要结局无法评估,主要是由于重症监护病房(ICU)住院时间少于7 天,其中包括3 名在6 天内死亡的患者;这些患者被排除在分析之外。分析患者的背景特征和治疗情况见表1。在分析的患者中,62 名(57%)为男性,年龄和急性生理与慢性健康状况评分系统II(APACHE II)评分分别为73(59 - 80)岁和19(13 -28)。分析患者的体重指数(BMI)为22.9(19.6 - 25.8)kg/m²,根据亚太地区分类标准,15 名(14%)、20 名(19%)和34 名(31%)患者分别被归类为体重过轻(< 18.5 kg/m²)、超重(23 -24.9 kg/m²)或肥胖(> 25 kg/m²)。尽管两组患者在虚弱程度或病前日常生活活动能力方面没有显著差异,但脂肪组患者的肌肉面积、BMI 和脂肪面积均显著大于消瘦组。在分析的患者中,39 名(36%)和12 名(11%)患者分别接受了机械通气和肾脏替代治疗。64 名(59%)患者在入院后48 小时内开始肠内营养,平均每日摄入量为在第一周,脂肪组的热量和蛋白质摄入量分别为650(438 - 827)千卡/天和24.5(16.1 - 33.3)克/天。按照目前指南的建议15,对于BMI ≤ 25 的患者,根据实际体重计算营养剂量;对于BMI > 25 的患者,根据理想体重计算营养剂量。脂肪组的热量(10.2 [8.3 - 14.6] 千卡/千克/天对比13.0 [9.2 - 17.1] 千卡/千克/天,p = 0.062)和蛋白质(0.40 [0.27 - 0.61] 克/千克/天对比0.52 [0.32 - 0.68] 克/千克/天,p = 0.093)摄入量有偏低的趋势,但这些差异无统计学意义(表1)。除脂肪组的胰岛素剂量较高外,两组在其他治疗方面无显著差异。
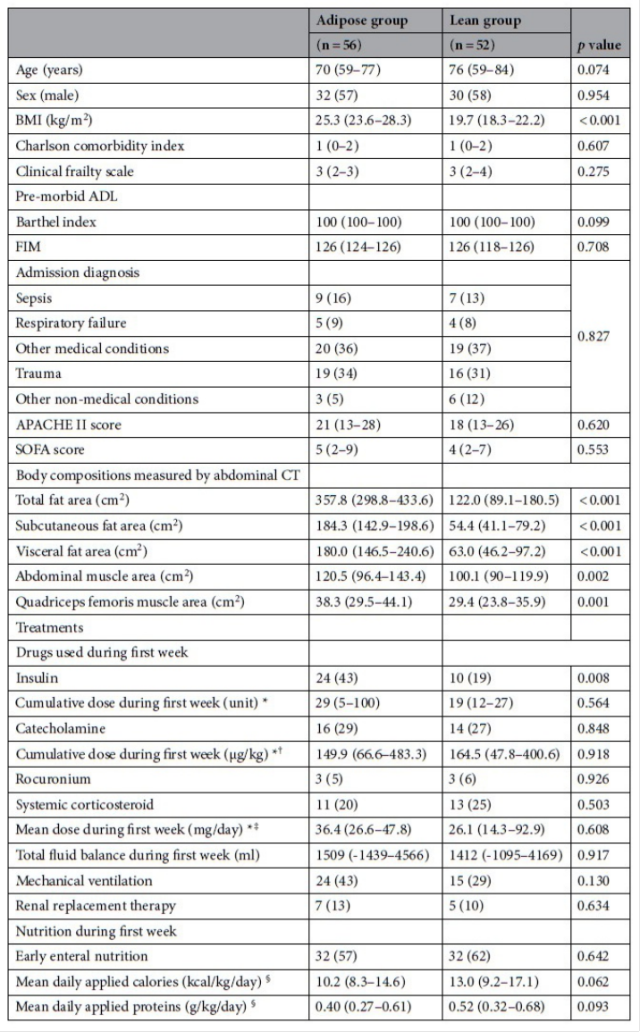
表 1.背景特征及治疗。* 仅对使用该药物的患者进行了分析。† 以去甲肾上腺素剂量表示,剂量换算依据等效剂量计算。‡ 以泼尼松龙剂量表示,剂量换算依据等效剂量计算。§ 营养剂量根据体重指数(BMI)≤ 25 的患者的实际体重和BMI > 25 的患者的理想体重计算,遵循当前指南的建议15。ADL,日常生活活动;APACHE,急性生理与慢性健康状况评估;BMI,体重指数;FIM,功能独立性评定;SOFA,序贯器官衰竭评估。
主要和次要结局指标见表2 和图1。如图2A 所示,尽管在第一周内,肥胖组的CSARF 显著高于消瘦组,但到第7 天时,肥胖组的CSARF 减少量显著大于消瘦组(-9.3 [-14.8–-4.5] % 对比-4.5 [-10.4–1.3] %,p = 0.014;图2B)。到第7 天时,体重变化与TFA、SFA 和 VFA 之间存在微弱但具有统计学意义的负相关(补充图2)。肥胖组严重肌肉萎缩的发生率显著高于消瘦组(27 例 [48%] 对比14例 [27%],p = 0.023)。在63 名(58%)有随访CT 数据可供测量的患者中,肥胖组的QMA 减少量也显著大于消瘦组(-1.2 [-1.9–-0.8] %/天对比-0.8 [-1.3–0.6] %/天,p = 0.005),AMA 的减少量也倾向于更大(-0.44 [-0.89–0.20] %/天对比-0.17 [-0.73–1.18] %/天,p = 0.063)。两组的SFAs 和 VFAs 变化无显著差异。肥胖组的ICU 住院时间显著长于消瘦组。在重症监护病房(ICU)出院时,分别有97名患者和100 名患者的握力和MRC 总分可评估,且肥胖组的这两项指标显著更高。肥胖组患者在ICU 出院时MRC 总分低于48 分的比例(13%)低于消瘦组(25%),但差异无统计学意义。尤其是第7 天测量的指标,与ICU出院时的握力和MRC 总分显著相关。两组患者的生存率、住院时间和出院时的日常生活活动能力(即Barthel 指数、FIM 评分及其与患病前状态的变化)均无显著差异。此外,两组患者的长期生存率、生活质量(QOL)和日常生活活动能力(ADL)也无显著差异。
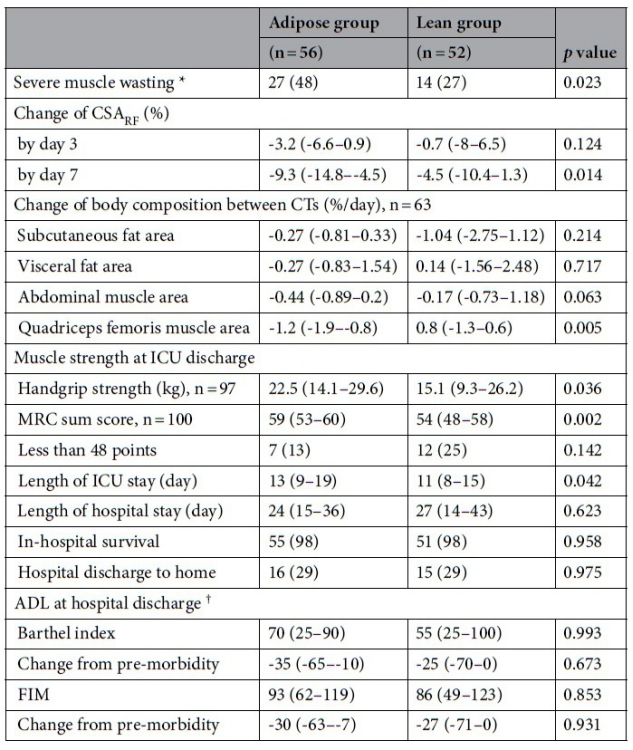
表 2.主要和次要结局指标。* 定义为第7 天肌力较基线下降超过10%。† 非存活者的Barthel 指数和FIM 评分均为0 分。ADL,日常生活活动;CSARF,股直肌横截面积;FIM,功能独立性评定量表;MRC,医学研究委员会。
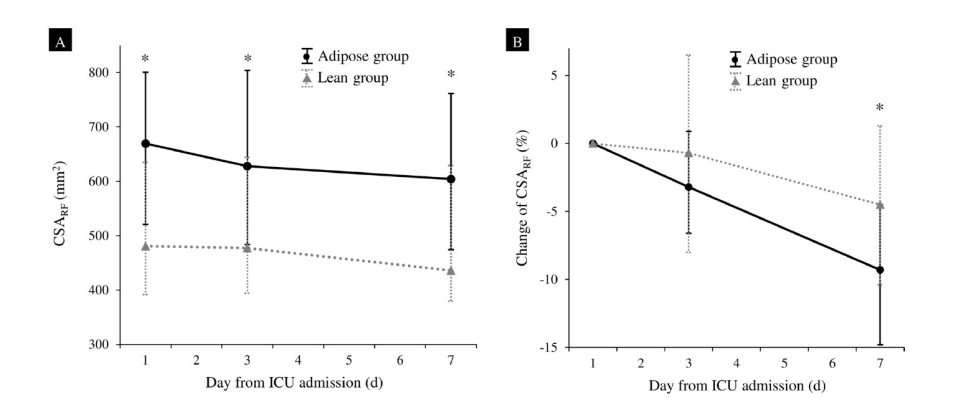
图1.CSARF 及其在脂肪组和瘦组第一周的变化情况,绝对值CSARF(A)及其相对于基线的变化(B)显示至第7 天。数据以中位数和四分位间距表示。黑色圆点和灰色三角形分别表示脂肪组和瘦组。CSARF,股直肌的横截面积,* p < 0.05。
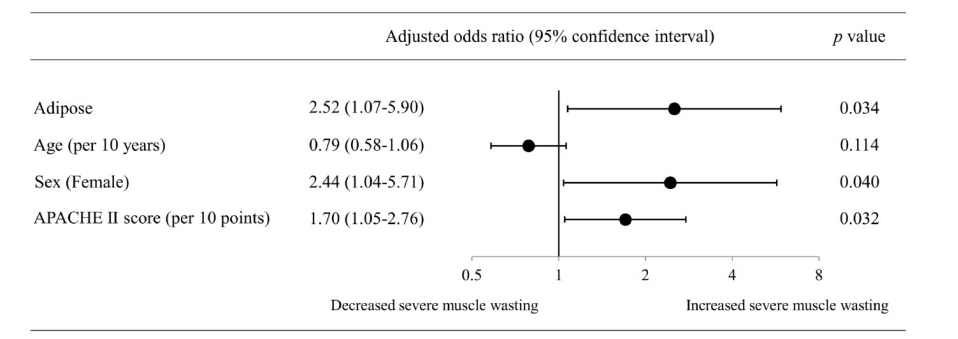
图3.脂肪组织分组与严重肌肉萎缩风险的关联,模型已根据入院时的年龄、性别和急性生理与慢性健康状况评估II 评分进行了校正。
图3 显示了肥胖与严重肌肉萎缩的校正比值比。肥胖组与严重肌肉萎缩风险增加独立相关(校正比值比2.52;95% 置信区间[CI] 1.07 - 5.90,p = 0.034)。当模型中用皮下脂肪组或内脏脂肪组替代总体脂肪组时,皮下脂肪组仍与严重肌肉萎缩风险增加显著相关(校正比值比:3.02;95% CI:1.27 -7.18;p = 0.013),而内脏脂肪组则无此相关性(校正比值比:2.01;95% CI:0.86 - 4.70;p = 0.106)。在敏感性分析中,除了机械通气外,将其他变量(例如CSARF 第 1 天情况、第1 周平均每日摄入的热量或蛋白质)添加到模型中,均未影响这些结果。当加入机械通气这一因素时,尽管总体脂肪量与严重肌肉萎缩之间的关联不再显著,但皮下脂肪量仍与严重肌肉萎缩的增加风险独立相关。
生化分析结果。第1 天的BHB 在脂肪组织组中略低(156 [76–313] μmol/L 对比252 [109–569] μmol/L,p = 0.081),且第1 天的BHB 与 TFA 呈弱但显著的负相关(r = -0.221,p = 0.021)。尽管第1 天的BHB 与 APACHE II 评分所指示的疾病严重程度呈正相关,但第1 天的BHB 与第7 天的体重变化(r = -0.262,p = 0.006)呈显著负相关。在多变量逻辑回归分析中,第1 天升高的BHB 与严重肌肉萎缩风险降低独立相关(每100 μmol/L 调整后的OR 为 0.91;95% CI 0.83–0.99,p = 0.036)。第3 天和第7 天的BHB 以及第1 周的FFAs 在两组之间无显著差异。尽管在第1 周内脂肪组织组的瘦素水平显著较高,而脂联素水平显著较低,但这些脂肪因子与严重肌肉萎缩的风险无独立关联。第3 天的C 反应蛋白(CRP)水平和第7 天的白细胞计数在脂肪组中显著更高。第3 天的CRP 水平也与TFA 显著相关。并且在第7 天时CSARF 的水平下降,这与严重肌肉萎缩的风险相关(每1 毫克/分升的校正比值比为1.07;95% 置信区间1.02 - 1.13,p = 0.007)。
四、讨论
在本研究中,我们评估了重症监护病房(ICU)住院第一周的肌肉萎缩情况,并对肥胖患者和消瘦患者进行了比较。与我们的假设相反,严重肌肉萎缩在肥胖患者中显著更常见,尤其是那些皮下脂肪堆积较多的患者,而非消瘦患者。据我们所知,这是首次前瞻性研究评估ICU 住院期间肌肉萎缩与腹部CT 估计的脂肪组织量之间的关联。肥胖的保护作用这一悖论现象,通常被称为“肥胖悖论”,在肌肉萎缩和ICU 获得性肌无力等几种情况下均有报道。然而,以往大多数评估“肥胖悖论”的研究都是基于体重指数(BMI)来定义肥胖的。尽管BMI 是诊断肥胖的标准指标,但它可能并不总是能准确反映脂肪堆积的程度,因为BMI受脂肪量和瘦体重(包括骨骼肌)的影响。此前的一项研究显示,通过生物电阻抗光谱法测量的高脂肪堆积,BMI 的敏感性较低(仅为39.6%),且骨骼肌体积较小的患者被误判为非肥胖的情况更为常见。因此,应基于某些方法评估的脂肪堆积程度来定义肥胖,以确定脂肪堆积增加本身是否会影响临床结局。此前针对危重症患者肌肉萎缩中的“肥胖悖论”所开展的研究结果并不一致,等人报告称,与健康对照组相比,消瘦的危重症患者肌纤维更小,但在肥胖危重症患者与肥胖健康对照组之间未观察到这种现象。然而,由于这是对其随机对照研究的事后分析,无法评估个体肌肉参数的变化。等人开展的一项前瞻性研究显示,通过超声测量的肌肉深度变化在消瘦患者和超重/肥胖患者之间没有显著差异,但该研究纳入的患者数量非常少。此外,另一项前瞻性研究在调查严重肌肉萎缩的风险因素时发现,体重指数并非独立风险因素。然而,这些研究均未评估肌肉萎缩与脂肪堆积本身之间的关系。仅有一项针对新冠肺炎患者的回顾性研究根据胸部CT 估计的脂肪堆积程度对肥胖患者和消瘦患者进行了比较。在本研究中,观察到肥胖患者的竖脊肌横截面积减少程度比非肥胖患者更为严重,这与我们的研究结果一致。然而,由于该研究的回顾性,用于肌肉评估的CT 扫描时间在不同患者之间存在差异,这种差异可能会影响对肌肉萎缩程度的评估。与之前的报告不同,我们基于脂肪体积来定义肥胖,并在预先设定的时间点前瞻性地评估肌肉质量的变化。
在规划本研究时,我们假设由于脂肪组的β-羟基丁酸(BHB)水平较高,其严重肌肉萎缩的风险会降低。已有报道表明,BHB 具有多种保护作用(例如抗炎、抗氧化、线粒体保护和神经保护作用,它可能通过减少危重症患者中假设的肌肉萎缩机制来改善肌肉萎缩。。在本研究中,第1 天 BHB 水平升高也与严重肌肉萎缩风险降低独立相关,正如我们所预期的那样。由于内源性BHB 主要由脂肪分解提供的乙酰辅酶A 合成,肥胖患者BHB 水平升高是预料之中的,正如在小鼠模型中所显示的那样。然而,脂肪组患者在急性期的BHB 水平反而较低,并且与脂肪体积呈负相关,这与我们的假设相悖。脂肪组患者在急性期BHB 水平的意外降低可能解释了他们严重肌肉萎缩风险增加的原因。两组间血清游离脂肪酸水平相当,表明两组的脂肪分解程度相同,而肥胖组的生酮作用可能受到更多抑制,原因可能包括胰岛素水平较高。
在本研究中,我们还假设了其他几种导致肥胖组严重肌肉萎缩风险增加的机制。首先,肥胖组更强的急性炎症反应可能会增加严重肌肉萎缩的风险。尽管慢性炎症及其在肥胖患者代谢综合征发病中的作用已有大量文献记载,但肥胖对危重症患者急性炎症反应的影响仍存在争议。在本研究中,肥胖组在第3 天的C 反应蛋白(CRP)水平较高,提示其急性炎症反应更强。第3 天 CRP 水平升高也与严重肌肉萎缩风险增加有关。由于早期全身性炎症是导致肌肉萎缩的主要危险因素之一,因此这种更强的炎症反应被认为是肥胖组严重肌肉萎缩风险增加的一个可能原因。其次,病前的肌肉萎缩可能会减轻重症监护病房(ICU)住院期间的进一步肌肉萎缩,这可能是消瘦组严重肌肉萎缩发生率较低的机制之一。然而,即使在对第1 天的CSARF 进行了调整之后,肥胖与严重肌肉萎缩风险增加之间的显著关联仍然存在。第三,各组之间所应用的热量和蛋白质剂量的差异可能会影响肌肉萎缩。
在本研究中,由于各组所应用的营养物质总量没有差异,肥胖组的实际体重较高,导致该组的营养剂量较低。这些较低的营养剂量可能会导致更严重的肌肉萎缩。然而,对于危重症急性期应给予多少热量或蛋白质,尤其是对于体重过轻或肥胖的患者,目前仍不确定,而且在最近的干预研究中,较高的营养剂量并未改善肌肉力量或生活质量。在本研究中,对所应用的热量或蛋白质剂量进行调整,并未影响肥胖与严重肌肉萎缩风险增加之间的关联。
在本研究中,肥胖患者在入住重症监护病房(ICU)的早期阶段出现严重肌肉萎缩的风险高于消瘦患者。肥胖患者早期酮体生成减少可能是导致这一风险增加的原因。这些结果表明,有必要进一步研究评估酮体补充剂对预防肌肉萎缩和ICU 获得性肌无力(ICU-AW)的效果,尤其是在脂肪堆积较多的患者中。
话险危夷·述评
这篇论文挑战了危重症领域长期存在的“肥胖悖论”假说,具有重要的理论突破意义。与传统认知相反,该前瞻性研究发现,经腹部CT确认的脂肪堆积增加,尤其是皮下脂肪,反而与更严重的肌肉萎缩独立相关(校正比值比2.52),而肥胖患者早期酮体(β-羟基丁酸)水平意外降低可能是其机制之一。这一结果有力地质疑了仅凭体重指数定义肥胖并得出“保护作用”的既往研究,揭示了体重指数无法区分脂肪与瘦组织的根本缺陷。研究在方法学上较为严谨,采用CT精确量化脂肪分布、超声动态监测肌肉变化,并控制了多个混杂因素。但需注意,单中心设计、仅108例的可分析样本量、以及两组间营养摄入偏低且存在差异趋势,均可能影响结论的稳健性。此外,主要结局为肌肉横截面积下降,而肥胖组出院时医学研究委员会评分低于48分的比例(13% vs. 25%)并无统计学差异,提示肌肉量的减少未必同步转化为功能丧失。总体而言,这项研究打破了“脂肪越多越保护”的简单化认知,强调在危重症管理中应警惕肥胖患者的早期肌肉萎缩风险,并为探索补充酮体等代谢干预策略提供了有价值的方向。


