中科院宁波材料所Biomaterials:综述多维靶向探针用于乳腺癌精准医学
时间:2026-05-05 13:05:19 热度:37.1℃ 作者:网络
背景介绍
乳腺癌是全球女性发病率最高、癌症相关死亡率第二的恶性肿瘤,约占所有新发癌症病例的11.6%。尽管乳腺X线摄影、超声和磁共振成像等传统影像学手段在乳腺癌筛查和诊断中发挥了重要作用,但它们主要提供形态学信息,在早期微小病灶检出、分子分型精准判定、转移灶定位以及疗效动态监测等方面存在明显局限。核医学成像(PET/CT、SPECT/CT)能够无创、定量、全身性地评估肿瘤代谢活性和功能状态,弥补了传统结构影像的不足。然而,现有PET探针(如[¹⁸F]‑FDG)在特异性、肿瘤背景比和标准化方面仍面临挑战。因此,开发能够从多维度解析肿瘤生物学特征的分子成像探针,实现从细胞内代谢到细胞表面受体再到肿瘤微环境的系统靶向,已成为乳腺癌精准诊疗的重要方向。
研究思路
针对上述挑战,中国科学院宁波材料技术与工程研究所吴爱国教授、陈天翔研究员与浙江中医药大学李强教授合作,系统综述了乳腺癌多维靶向PET探针的最新进展。文章创新性地提出了一个三维空间分类框架:第一维聚焦肿瘤细胞内代谢过程(葡萄糖、氨基酸、胆碱、核酸代谢等),第二维靶向肿瘤细胞表面特异性受体(ER、PR、HER2、EGFR、TROP‑2、CD146、Nectin‑4、整合素、GPCRs等),第三维覆盖肿瘤微环境(CAFs、TAMs、血管生成、缺氧、ECM重塑等)。通过这一空间维度导向的分类体系,文章将分子成像信号转化为可解释的病理生理信息,建立了影像靶标与临床可操作治疗策略之间的一一对应关系。此外,文章还讨论了探针设计的化学策略(放射性核素选择、螯合剂、连接子、载体工程等),并展望了从诊断向治疗一体化(theranostics)的转化前景。相关内容以Advances in Multi-Dimensional Targeting Probes for Precision Medicine of Breast Cancer为题,发表在Biomaterials!
图片解析
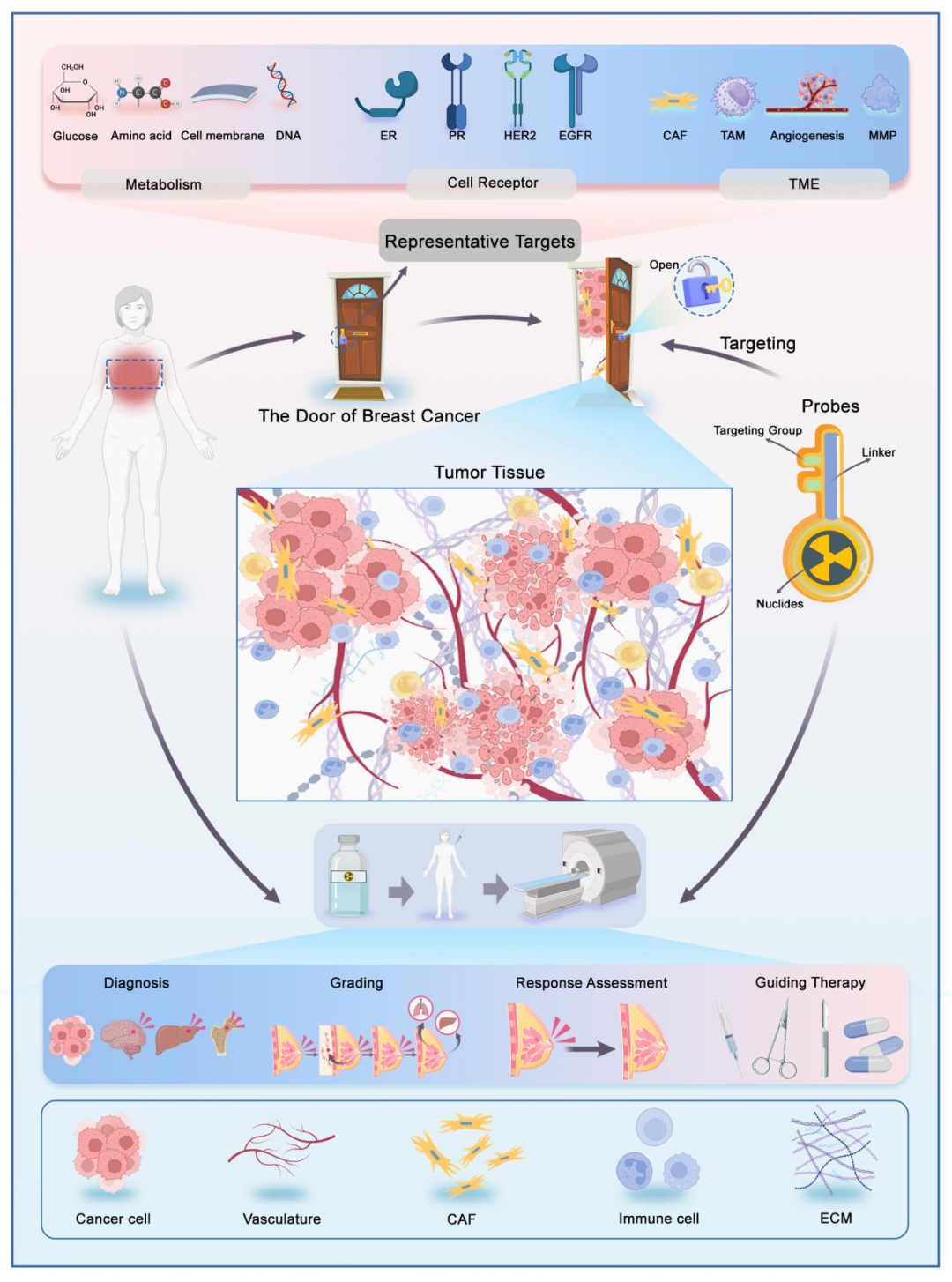
图1. 用于乳腺癌多维成像的探针示意图: 从左至右分别靶向肿瘤细胞内代谢、肿瘤细胞表面受体和肿瘤微环境。图中列出了代表性的PET探针,如[¹⁸F]‑FDG(葡萄糖代谢)、[¹⁸F]‑FES(ER受体)、[⁶⁸Ga]‑FAPI(成纤维细胞活化蛋白)等,突出显示了从细胞内到细胞外空间的多层次靶向策略。
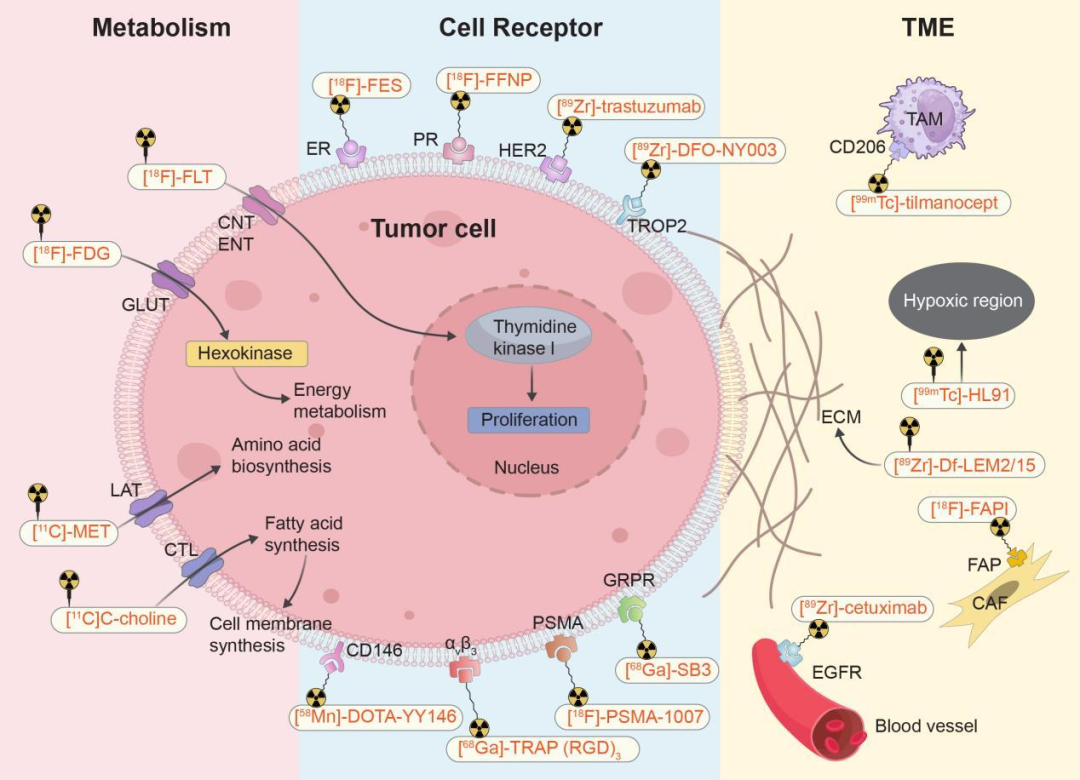
图2. 临床已建立和正在开发的下一代PET探针: 以乳腺癌细胞为中心,展示了靶向代谢(糖酵解、氨基酸、胆碱、DNA合成)、细胞表面受体(激素受体、RTKs、细胞黏附分子、GPCRs等)和微环境(CAFs、TAMs、血管生成、缺氧、ECM)的探针化学结构及其对应的放射性核素。该图直观体现了探针从广谱代谢剂向高特异性分子工具的演变。
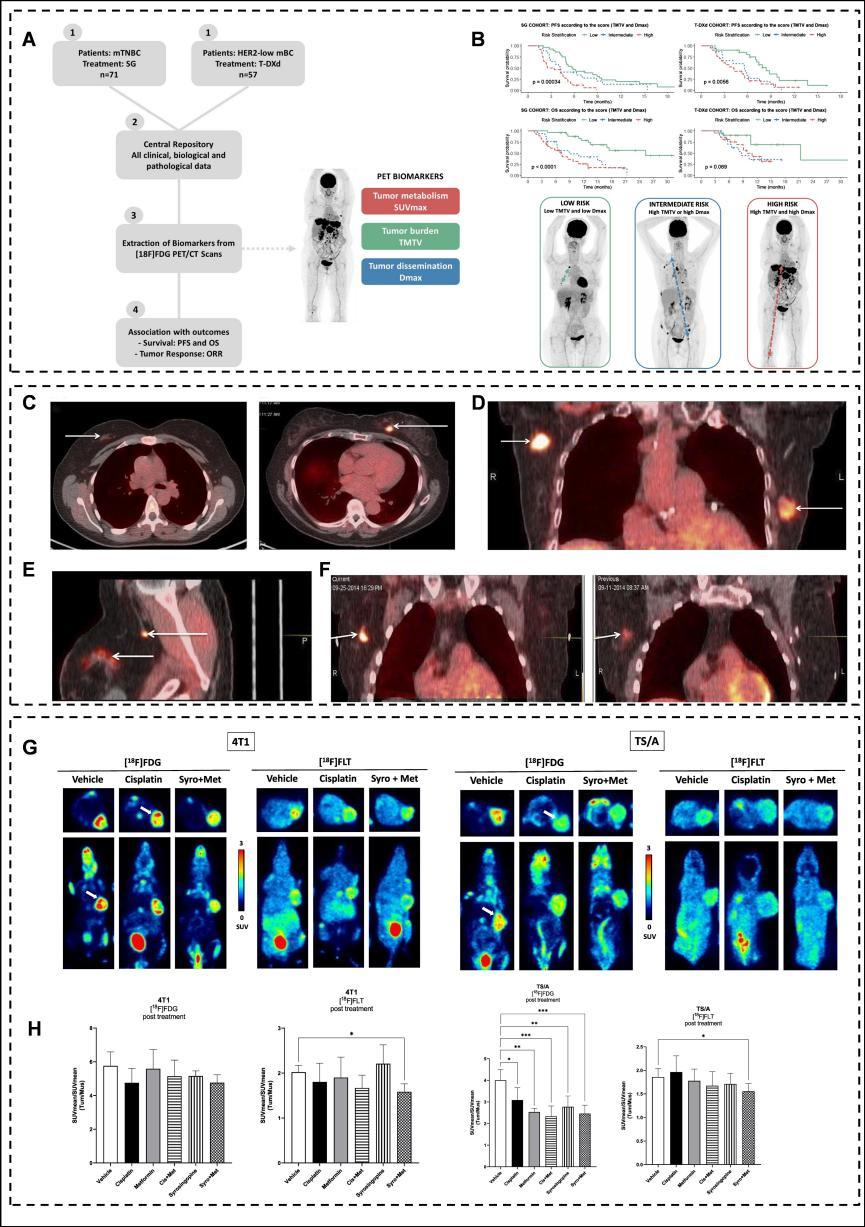
图3. 肿瘤代谢类探针在乳腺癌成像中的应用: (A) 患者选择流程图。(B) 利用全身代谢肿瘤体积(TMTV)和最大肿瘤播散(Dmax)进行风险分层。(C) [¹⁸F]‑氟西洛维(fluociclovine)PET/CT在良性导管增生(左)和浸润性导管癌(右)中的高摄取。(D) 双侧乳腺癌中右侧三阴性IDC摄取高于左侧ER⁺/HER2⁻ IDC。(E) 左侧浸润性小叶癌(ILC)的[¹⁸F]‑氟西洛维图像。(F) ILC转移至乳内淋巴结中,[¹⁸F]‑氟西洛维摄取高于[¹⁸F]‑FDG。(G-H) 4T1和TS/A荷瘤小鼠治疗后[¹⁸F]‑FLT和[¹⁸F]‑FDG PET图像及肿瘤/肌肉比值。
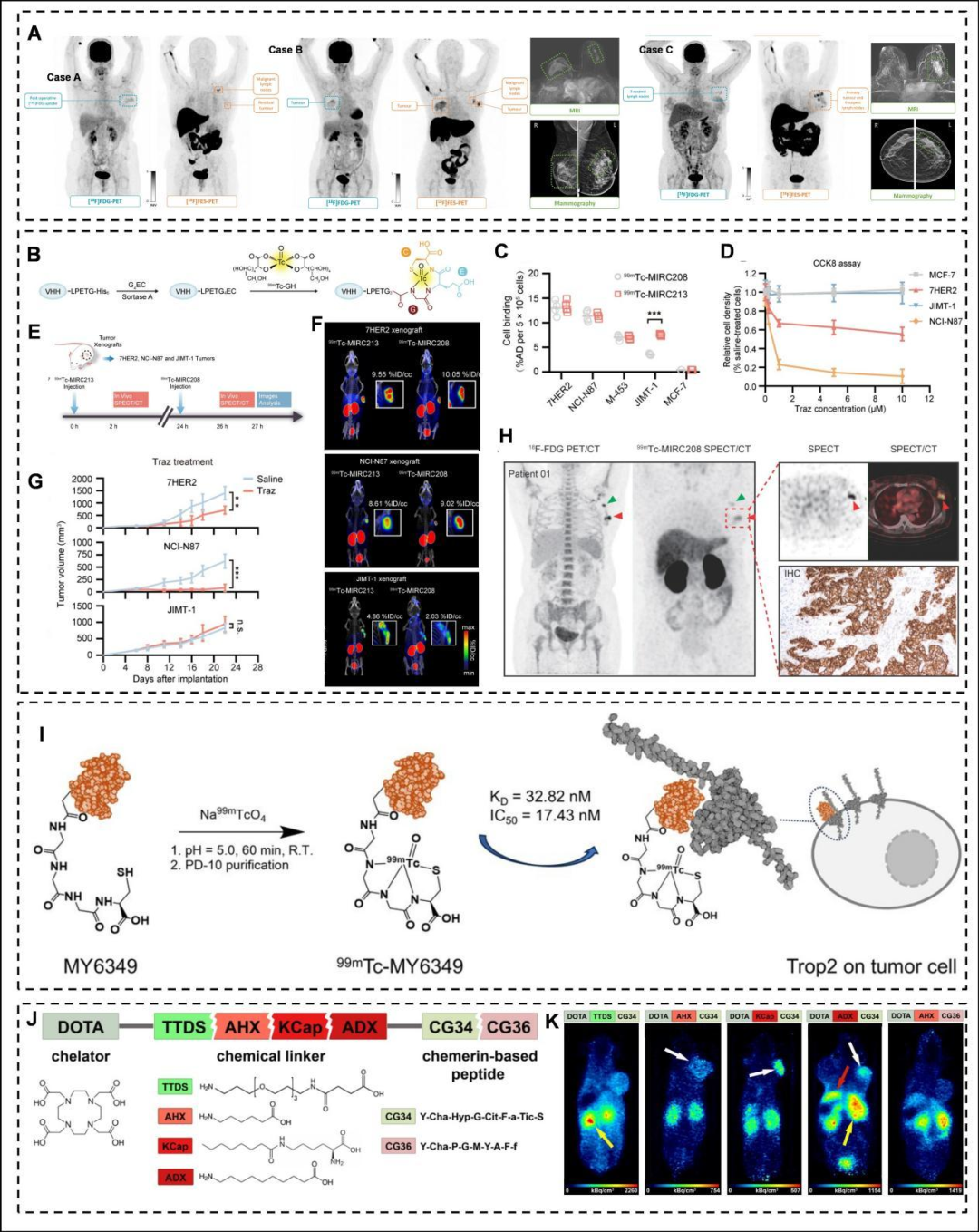
图4. 细胞受体类探针在乳腺癌成像中的应用: (A) 三例乳腺癌患者的[¹⁸F]‑FDG PET、[¹⁸F]‑FES PET、乳腺MRI和钼靶对比,显示FES在ER⁺病变中的特异性。(B) 新型HER2特异性⁹⁹ᵐTc探针的构建。(C) 不同HER2表达水平细胞系中两种探针的摄取差异。(D) 曲妥珠单抗(Traz)对不同细胞系的体外疗效。(E) SPECT/CT成像策略示意图。(F) 同一小鼠中两种探针的不同摄取模式。(G) 不同异种移植瘤在Traz治疗下的生长曲线。(H) 患者SPECT/CT融合图像及HER2 IHC染色。(I) [⁹⁹ᵐTc]Tc‑MY6349 Trop2靶向SPECT探针的制备流程图。(J) 五种CMKLR1靶向肽‑DOTA偶联物的结构。(K) 五种探针在荷瘤小鼠中的PET静态图像。
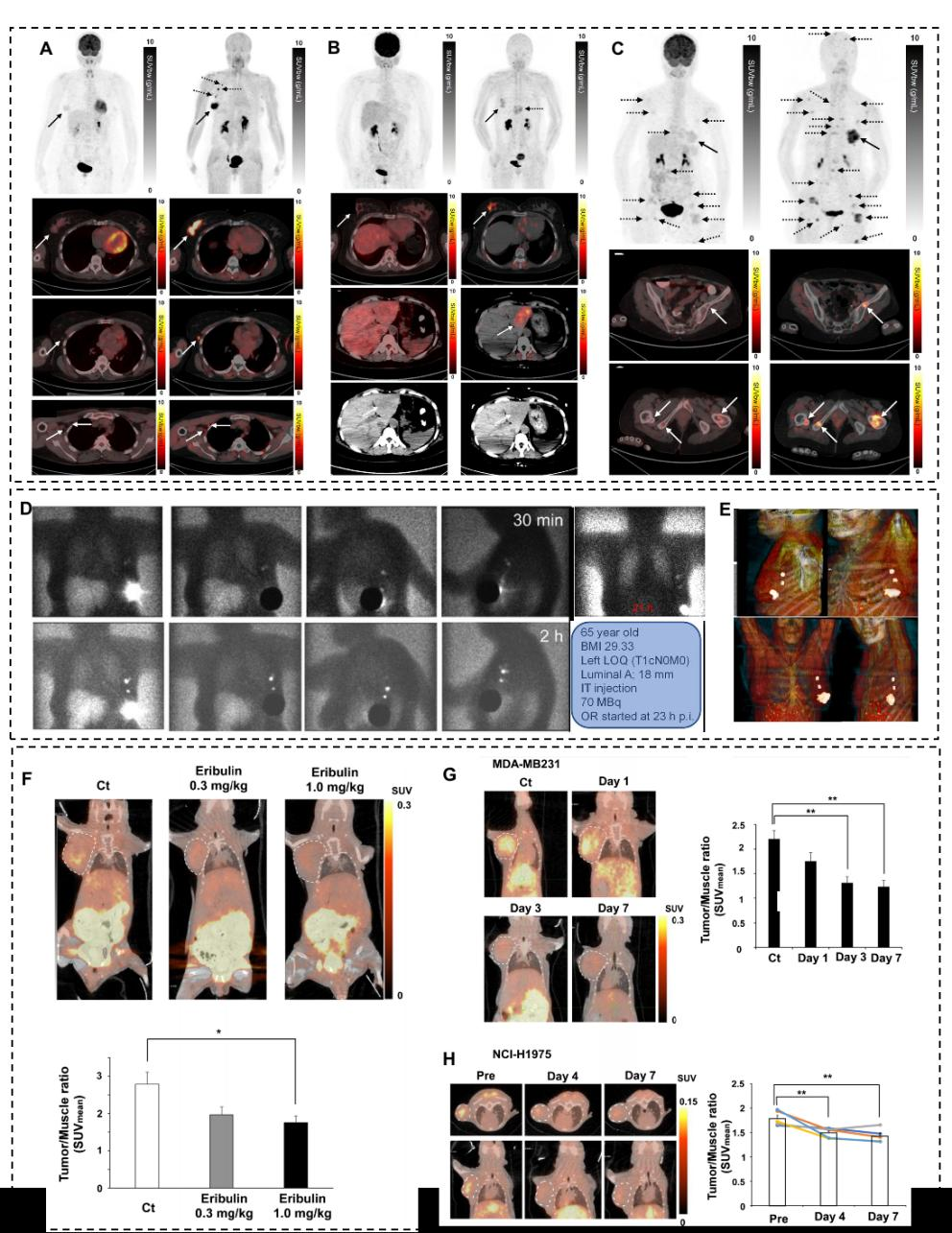
图5. 肿瘤微环境类探针在乳腺癌成像中的应用: (A-C) 三例浸润性小叶癌(ILC)患者的[¹⁸F]‑FDG PET(左)与[⁶⁸Ga]‑FAPI PET(右)最大强度投影及轴位融合图像,显示FAPI在ILC中具有更高的肿瘤背景比。(D-E) 乳腺癌患者瘤内注射[⁹⁹ᵐTc]‑替马诺塞普(tilmanoccept)后不同时间的SPECT/CT图像及三维重建,显示前哨淋巴结清晰显像。(F) [¹⁸F]‑DiFA PET/CT用于监测艾日布林治疗后肿瘤缺氧改善情况。(G-H) MDA‑MB‑231和NCI‑p975模型中艾日布林对瘤内[¹⁸F]‑DiFA积聚的时间依赖性影响。
结论
本综述创新性地将乳腺癌PET探针按照三维空间生物学框架进行分类:细胞内代谢、细胞表面受体和细胞外肿瘤微环境。这一分类体系不仅有助于将影像信号转化为可解释的病理生理信息,还建立了影像靶点与临床治疗策略之间的直接联系(如HER2靶向探针指导抗HER2治疗、FAPI探针指导基质干预等)。文章系统总结了从第一代广谱代谢探针(如[¹⁸F]‑FDG)到新一代高特异性分子探针(如[¹⁸F]‑FES、[⁸⁹Zr]‑曲妥珠单抗、[⁶⁸Ga]‑FAPI、[¹⁸F]‑DiFA等)的演进,并强调了探针化学设计(核素选择、螯合剂、连接子、多价策略)对药代动力学和成像对比度的关键影响。最后,文章展望了多功能诊疗一体化探针(如[¹⁷⁷Lu]标记的靶向载体)与人工智能增强多组学分析相结合的未来方向,有望推动乳腺癌从形态学指导向功能驱动的精准治疗范式转变。
原文链接:
https://doi.org/10.1016/j.biomaterials.2026.124247


