综述:脑部恶性肿瘤的脑脊液免疫特征(胶质瘤、原发CNS淋巴瘤、脑转移瘤和软脑膜转移瘤)
时间:2026-05-05 13:05:22 热度:37.1℃ 作者:网络
脑脊液是中枢神经系统内的一个活跃免疫界面,能够反映并塑造通常在血液中不可见的肿瘤-免疫相互作用。越来越多的证据表明,脑脊液的免疫重塑具有高度的恶性肿瘤特异性,而非在所有脑癌中呈现统一模式。
《Neuro-Oncology Advances》近日发表综述,整合了近期关于胶质瘤、原发性中枢神经系统淋巴瘤、脑转移瘤和软脑膜转移瘤中脑脊液免疫谱的研究进展,重点阐述了每种疾病如何构建独特的细胞和细胞因子回路。胶质瘤的特征为髓系偏移和IL-6相关炎症;原发性中枢神经系统淋巴瘤表现为IL-10/CXCL13驱动的B细胞支持性微环境;脑转移瘤呈现原发肿瘤印记的炎症特征;而软脑膜转移瘤则以显著的巨噬细胞主导和补体介导的免疫重编程为特征。重要的是,脑脊液的这些变化不仅具有相关性,而且与免疫逃逸、疾病进展和治疗响应性存在机制性联系。作者进一步讨论了脑脊液分析在分子分层、免疫监测和治疗反应评估中的转化应用价值,并批判性地评估了脑脊液导向治疗策略的新兴作用。
综上,本综述将脑脊液定位为一个生物学和临床整合的组成,其在精准神经肿瘤学中的重要性日益增加。

本文要点
脑恶性肿瘤以疾病特异性模式重塑脑脊液免疫微环境,而非通过统一的免疫抑制程序。
每种恶性肿瘤具有独特的脑脊液免疫程序,包括:胶质瘤中的IL-6相关髓系炎症,中枢神经系统淋巴瘤中的IL-10/CXCL13介导的B细胞支持,脑转移瘤中的原发肿瘤特异性炎症特征,以及软脑膜转移瘤中的巨噬细胞主导的重编程。
脑脊液分析在捕捉中枢神经系统特有的分子和免疫特征方面通常优于血浆,支持其在分层、监测和治疗开发中的应用。
引言
中枢神经系统长期以来被视为免疫豁免器官,主要归因于其独特的解剖屏障,包括血脑屏障、血-脑脊液屏障以及常规淋巴引流系统的缺乏。然而,脑膜淋巴管的发现以及中枢神经系统内活跃免疫细胞进出的证据,已将其概念修正为“免疫特化”(immune specialization)而非绝对豁免。与此同时,单细胞RNA测序和液体活检等先进分子技术的发展,使研究人员能够更精细地研究中枢神经系统的免疫微环境。
在中枢神经系统免疫调控的各个组成部分中,脑脊液扮演着核心角色。脑脊液充满脑室系统、蛛网膜下腔和血管周围间隙,不仅提供机械保护,还作为免疫细胞和细胞因子的载体。脑脊液中检测到的免疫细胞来源于多个相互连接的部位,包括外周血、脑膜间隙和脉络丛。这些细胞通过不断进出脑脊液,监测中枢神经系统边界区域,并在脑-脑脊液界面参与免疫通讯。因此,分析脑脊液可以为脑恶性肿瘤相关的免疫学和分子变化提供宝贵信息。虽然脑脊液在软脑膜转移瘤中直接反映肿瘤微环境,但在脑实质肿瘤(如胶质瘤、中枢神经系统淋巴瘤和脑转移瘤)中,脑脊液的变化可能受到中枢神经系统解剖屏障的间接影响。尽管如此,多种中枢神经系统恶性肿瘤会主动重塑脑脊液免疫景观,以促进肿瘤生存和逃避免疫反应。每种肿瘤类型采用不同但重叠的免疫调控机制。这些脑脊液中的免疫重塑事件凸显了脑脊液液体活检在诊断和疾病监测中的价值。
本综述全面概述了多种中枢神经系统恶性肿瘤脑脊液中的免疫细胞群和细胞因子谱,重点阐述了每种肿瘤类型如何构建其独特的免疫抑制或促炎微环境。还讨论了这些见解如何有助于开发更有效的免疫治疗策略,专门针对中枢神经系统内复杂的免疫屏障。通过对脑脊液免疫景观的深入理解,旨在为精准医学方法照亮新路径,将诊断、预后和治疗维度整合到针对个体患者中枢神经系统肿瘤独特特征的定制策略中。
脑脊液:窥视大脑的窗口
功能
脑脊液在中枢神经系统内发挥多种关键功能。首先,它提供机械保护,通过围绕大脑形成液体缓冲垫,防止其直接接触颅骨并抵御物理冲击。这种浮力效应使大脑的表观重量减轻10-15倍。虽然人脑重约1.2-1.4公斤,但在颅腔内的负荷仅相当于其质量的约4%。脑脊液还通过调节电解质水平和运输维持中枢神经系统稳定性所需激素和神经递质,有助于化学稳态。此外,脑脊液支持营养运输,输送中枢神经系统所需的必需物质,同时通过清除毒素和代谢副产物促进废物清除。进一步地,脑脊液作为一个调控的双向运输通道,支持中枢神经系统和外周腔室之间的分子和细胞交换。这种运输包括中枢神经系统来源的代谢物和抗原,以及循环中的免疫介质和细胞,包括β-淀粉样蛋白、tau蛋白、细胞因子、趋化因子、免疫球蛋白、细胞外囊泡和免疫细胞。通过这些持续且协调的交换,脑脊液将代谢清除与免疫监视联系起来,并提供中枢神经系统生理和病理状态的复合读数。由于这些特性,脑脊液具有重要的诊断和治疗意义。它作为诊断中枢神经系统疾病的可及介质,并允许药物直接输送至脑脊液,这对于软脑膜转移瘤的治疗尤为重要,尽管其通常难以渗透到脑实质中。
产生与循环
脑脊液主要由位于脑室内的脉络丛产生。该结构过滤血液浆液,在成人中以每天400-600 mL的速率产生脑脊液,但由于持续的循环和引流,成人中枢神经系统内任何给定时间的总体积约为150 mL。大约70%的脑脊液来源于脉络丛,其余部分来自其他来源,如脑毛细血管和室管膜细胞。脑脊液最初通过脉络膜毛细血管的被动血浆过滤产生,随后通过脉络膜上皮细胞的主动转运,其中离子泵和水通道蛋白调节其组成和流动。脑脊液循环始于侧脑室,经过第三和第四脑室,随后进入蛛网膜下腔,包围大脑和脊髓。这种循环由动脉搏动和呼吸运动驱动。传统上认为脑脊液引流主要通过蛛网膜颗粒进入硬脑膜静脉系统。然而,来自动物模型和人体研究的越来越多的证据表明,仅凭这一途径并不能完全解释脑脊液的总流出量。相反,位于硬脑膜内的脑膜淋巴管在脑脊液引流中发挥主要作用,促进脑脊液来源的大分子运输到颈部淋巴结。其他清除途径包括神经周围淋巴管和鼻咽淋巴丛的连接,突显了脑脊液循环与外周淋巴系统之间的紧密整合。除了经典的脑脊液循环外,胶状淋巴系统已成为调节脑脊液-间质液交换的关键机制。该系统由动脉搏动和水通道蛋白-4依赖的星形胶质细胞通路驱动,促进代谢废物和免疫相关分子的清除。胶状淋巴流动的失调与神经炎症和神经退行性疾病有关,进一步突显了其在健康和疾病状态下对脑脊液动态的相关性。
细胞成分
在正常生理条件下,脑脊液的细胞含量极少,并受到严格调控以维持中枢神经系统稳态。在健康成人中,脑脊液基本无细胞,通常每微升含0至5个白细胞。脑脊液中红细胞的存在通常提示病理状况,如出血或创伤性腰椎穿刺,而非正常发现。脑脊液的细胞组成以淋巴细胞为主,成人正常的淋巴细胞与单核细胞比例约为2:1至3:1,但在婴儿中这种平衡可能发生改变,单核细胞更为普遍。如此低的细胞计数对于预防中枢神经系统内不必要的免疫激活至关重要,因为即使是轻微的细胞增加也可能提示炎症或病理状况,包括感染、自身免疫性疾病或脑脊液间隙的恶性肿瘤相关炎症。尽管脑脊液在稳态下细胞数量很少,但该腔室内的免疫细胞并非静止不动,而是在外周血、脑膜界面和脉络丛之间动态运输。特别是,越来越多的证据表明,脑脊液免疫细胞中有相当一部分来源于脑膜,包括硬脑膜和软脑膜,这些部位含有能够监视中枢神经系统邻近区域的组织驻留和循环免疫细胞群。这些脑膜免疫细胞可以进入脑脊液并在脑脊液间隙内动态再分布,有助于对中枢神经系统边界区域的免疫监测。与此同时,脉络丛作为一个特化的免疫门户,通过血-脑脊液屏障允许外周免疫细胞受调控地进入脑脊液。
在免疫细胞中,T淋巴细胞在正常脑脊液中占主导地位,其中CD4+ T细胞占大多数。这些细胞具有既往抗原接触史,并在再次刺激时具有快速回忆反应的能力,在中枢神经系统免疫监视中发挥关键作用。CD4+ T细胞计数通常为每微升0.08至1.43个。其他细胞类型的小群体包括:CD8+ T细胞(每微升0.04-0.40个),其贡献于细胞毒性免疫反应;B淋巴细胞(每微升0.00-0.03个),负责抗体产生;以及自然杀伤细胞(每微升0.00-0.05个),介导先天细胞毒性,偶尔出现但仅占总细胞数的极小部分。树突状细胞(DC)包括髓样和浆细胞样类型,是关键的抗原呈递细胞,以低频率(每微升0.01-0.18个)可检测到,提示其在中枢神经系统免疫监视中的潜在作用,尽管它们在健康脑脊液中的具体功能仍在研究之中。偶尔,操作过程中的污染物可能会将非天然细胞类型引入脑脊液。软骨细胞和成纤维细胞可能在腰椎穿刺后出现,而脉络丛或室管膜细胞的小簇有时在脑室脑脊液样本中发现,特别是在幼儿或脑积水患者中。值得注意的是,脑脊液的细胞组成和可溶性因子浓度可能因采样部位而异,腰椎脑脊液通常在数量上不同于脑室或Ommaya储液囊来源的脑脊液,这一点在解释临床和转化研究时尤为重要。
非细胞成分
除了有限的细胞成分外,正常脑脊液还含有多种维持中枢神经系统稳态所必需的非细胞成分。正常脑脊液中的主要非细胞成分包括蛋白质、葡萄糖、电解质和各种可溶性分子。成人正常脑脊液中的总蛋白水平通常较低,范围在15至45 mg/dL。存在的主要蛋白质包括来源于血浆的白蛋白,以及少量免疫球蛋白,主要为IgG。脑脊液中免疫球蛋白的低浓度可能部分反映了中枢神经系统内有限的免疫活性,但它也受到中枢神经系统屏障限制性的强烈影响。在这种情况下,脑脊液IgG可能来源于有限的血浆外渗和脑膜处的局部免疫球蛋白产生,而非表示缺乏免疫过程。其他蛋白质,如β-痕迹蛋白和β-2微球蛋白,分别作为脑脊液来源和更新的标志物。脑脊液葡萄糖水平通常为血糖水平的三分之二,范围在50至80 mg/dL之间。虽然脑脊液葡萄糖水平升高通常诊断意义不大,但脑脊液葡萄糖水平降低可能提示细菌或真菌感染等状况,因为病原体通常消耗葡萄糖。关键的电解质如钠、钾、钙、氯和镁在脑脊液中受到严格调控,维持渗透平衡和神经元兴奋性。钠和氯浓度与血浆水平相似,而脑脊液中钾较低,有助于控制神经元动作电位。
正常脑脊液还含有少量神经递质、细胞因子和代谢副产物。神经递质如谷氨酸、γ-氨基丁酸和多巴胺以痕量存在,而细胞因子水平非常低,反映了生理条件下中枢神经系统内严格调控的免疫活性。正常脑脊液中的乳酸水平通常低于3 mmol/L,但在中枢神经系统缺氧或炎症情况下可能升高。尽管脂质含量极少,但它们有助于细胞膜完整性和神经元功能。脑脊液脂质含量的异常增加可能与髓鞘分解有关,如脱髓鞘疾病所见。
胶质瘤:重塑中枢神经系统免疫环境
胶质瘤是起源于胶质细胞的原发性脑肿瘤,胶质细胞在中枢神经系统中支持和绝缘神经元方面发挥着关键作用。胶质瘤具有高度异质性,包括多种亚型,如星形细胞瘤、少突胶质细胞瘤和胶质母细胞瘤,其中胶质母细胞瘤是最具侵袭性的。胶质瘤的一个标志性特征是它们能够重塑中枢神经系统的免疫环境,从而抑制免疫监视并促进肿瘤的生存、侵袭和进展。这种免疫重塑不是被动的副产物,而是胶质瘤建立支持性微环境的主动机制。
胶质瘤脑脊液中的免疫细胞群
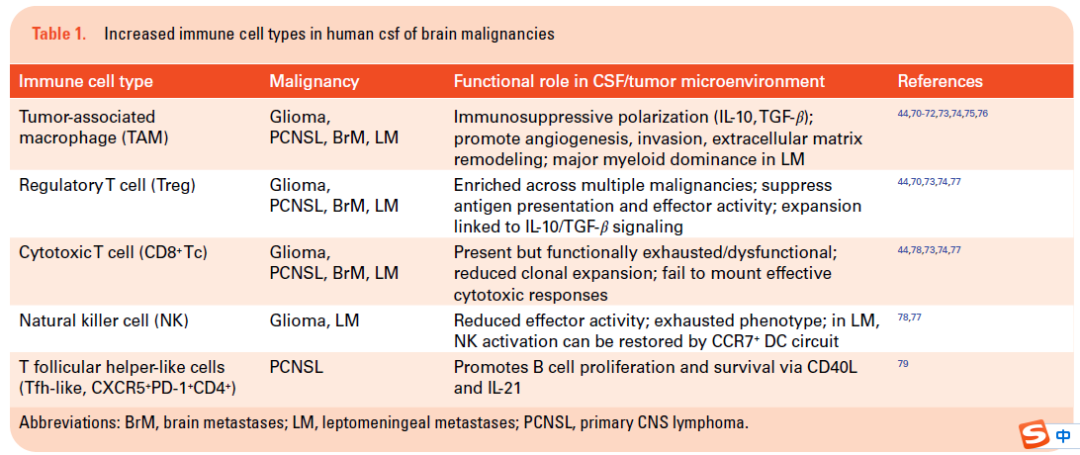
与健康中枢神经系统相对免疫稳定的环境相比,胶质瘤与脑脊液免疫的显著重塑相关(图1和表1)。
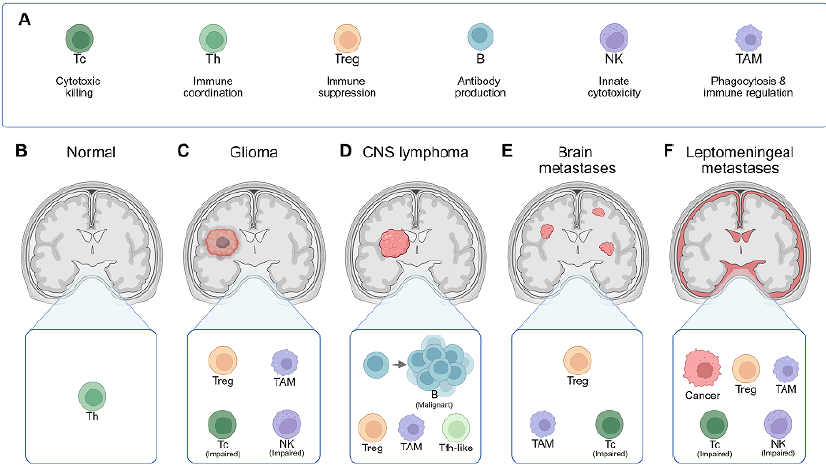
图1. 脑恶性肿瘤脑脊液中免疫细胞群的改变 (A) 脑脊液中主要免疫细胞群的经典免疫功能,包括细胞毒性T细胞、辅助T细胞、调节性T细胞、B细胞、自然杀伤细胞和巨噬细胞(肿瘤相关巨噬细胞)。 (B) 正常脑脊液中含有极少且受到严格调控的免疫细胞库,以Th细胞为主。 (C) 在胶质瘤中,脑脊液表现为Treg和TAM富集,伴有T细胞和NK细胞功能受损。 (D) 在原发性中枢神经系统淋巴瘤中,脑脊液以恶性B细胞为主,同时伴有Treg、支持性髓系细胞群以及滤泡辅助T样细胞。 (E) 在脑实质转移瘤中,脑脊液呈现髓系偏移的免疫格局,伴有T细胞和NK细胞区室功能受损。 (F) 在软脑膜转移瘤中,肿瘤细胞直接占据脑脊液空间,表现为显著的髓系主导、Treg富集以及T/NK细胞活性受损。
对胶质母细胞瘤患者脑脊液的单细胞分析一致显示出一个髓系偏移的景观,并伴有显著的巨噬细胞富集。髓系主导地位进一步得到肿瘤相关巨噬细胞相关标志物(包括CD163)水平升高的支持,以及巨噬细胞相关细胞因子特征与高级别胶质瘤疾病侵袭性和临床预后的相关性。在这种髓系主导的环境中,胶质瘤脑脊液中调节性T细胞经常增加,与抑制性免疫环境一致。与此同时,对IDH野生型胶质瘤鞘内淋巴细胞的流式细胞术分析显示,适应性免疫发生改变,其特征为T细胞耗竭,并且在NK细胞群上也检测到耗竭标志物的表达增加。总之,胶质瘤脑脊液表现出一种趋同的免疫表型,其特征为肿瘤相关髓系细胞富集、Treg扩增以及Tc和NK细胞的功能障碍。
胶质瘤脑脊液中的细胞因子谱
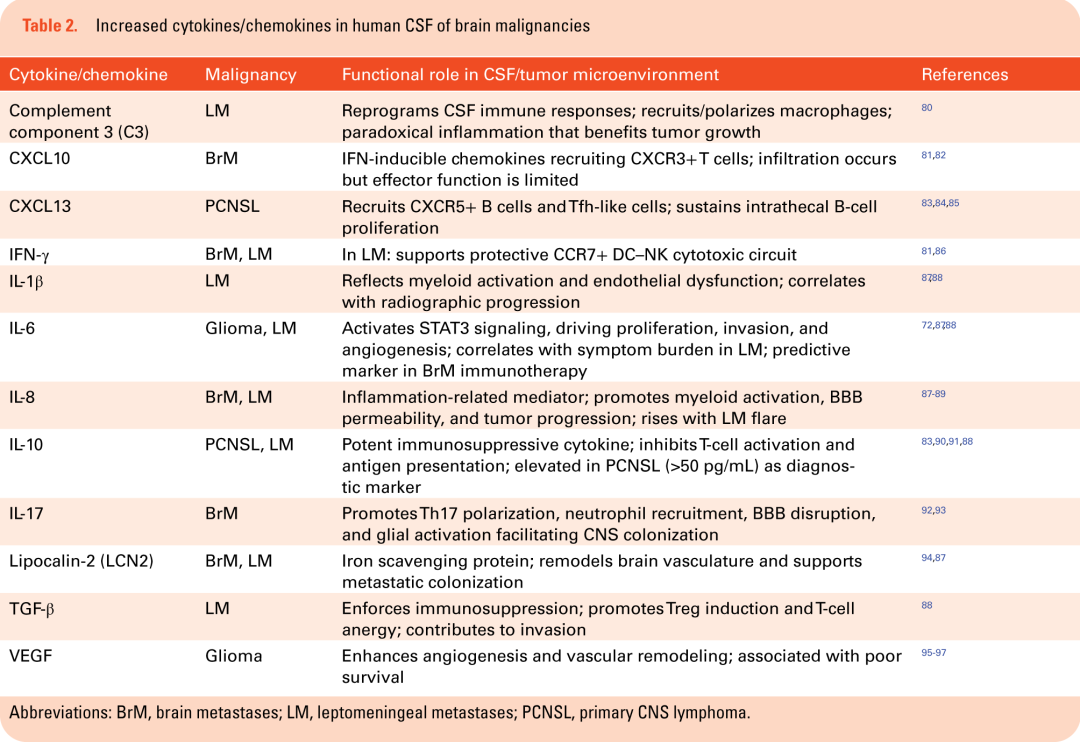
胶质瘤脑脊液的细胞因子环境与该区室观察到的髓系富集免疫景观密切相关(表2)。
其中最一致检测到的改变之一是白介素-6在胶质瘤患者脑脊液中升高,并且与不良临床结局相关。值得注意的是,脑脊液IL-6浓度与肿瘤相关巨噬细胞浸润相关,支持髓系激活与脑脊液细胞因子重塑之间的生物学联系。血管生成相关信号也是胶质瘤脑脊液的一个显著特征。脑脊液中的血管内皮生长因子水平和血管生成能力与胶质瘤分级和预后相关,表明脑脊液蛋白可能捕捉到临床相关的血管重塑程序。除了这些因素外,稳态和免疫调节细胞因子的改变进一步反映了脑脊液区室内的免疫失调。胶质母细胞瘤患者中脑脊液IL-7水平降低已被报道,与T细胞稳态受损一致。此外,瘤内巨噬细胞浸润已被证明与多种脑脊液细胞因子相关,包括eotaxin、IFN-γ、IL-1β、IL-2、IL-10、IL-13、IL-16和VEGF,突显了胶质瘤微环境与脑脊液免疫环境之间的协调串扰。总之,目前的脑脊液研究最一致地支持胶质瘤中存在IL-6和VEGF相关的细胞因子谱,与髓系驱动的炎症和血管重塑一致,而更广泛的免疫抑制细胞因子主张应基于可获得的脑脊液特异性原始证据。
胶质瘤脑脊液分析的治疗意义
胶质瘤表现出显著的空间和时间异质性,重复的组织活检意义可能有限。在这方面,脑脊液提供了对瘤周生物学的可重复获取,能够整合读取肿瘤核酸、免疫细胞状态和细胞因子程序。目前,脑脊液分析尚未基于免疫谱分析用于指导常规治疗决策,但它代表了一个有价值的研究窗口,用于观察难以纵向捕捉的肿瘤-免疫动态。
最近的研究表明,脑脊液液体活检在检测胶质瘤特异性改变方面优于血浆,包括MGMT启动子甲基化以及IDH1/2和TERT启动子中的可靶向突变。除基因组学外,脑脊液中的细胞因子谱分析已显示出预后意义,并可能为生物学上可行的治疗假设提供信息。升高的脑脊液IL-6水平和IL-6/IL-10比值与胶质瘤患者不良临床预后相关,支持其作为潜在预后标志物的效用。重要的是,临床前证据表明,IL-6驱动的信号传导不仅仅是相关的,而是可治疗的。例如,在胶质母细胞瘤模型中,同时靶向IL-6信号和CD40产生了协同的抗肿瘤免疫反应和生存获益,将IL-6/STAT3相关通路确立为免疫调节干预的可行靶点。在这种情况下,脑脊液分析可以通过将细胞因子定义的免疫状态与治疗脆弱性联系起来,作为转化研究的桥梁。值得注意的是,新兴证据表明,脑脊液构成了一个活跃的功能背景,可以调节治疗反应,而不仅仅是作为相关生物标志物的来源。将患者来源的胶质母细胞瘤细胞暴露于自体脑脊液已被证明可以调节对放化疗的敏感性,表明脑脊液携带的因素功能性地影响治疗反应,并加强了脑脊液分析作为机制和治疗背景的相关性。
基于微透析的框架已经证明了在检查点阻断期间进行实时局部免疫监测的可行性,表明连续的脑脊液采样可以作为早期药效学读数,尽管这些方法仍处于研究阶段,尚未临床验证。展望未来,将脑脊液细胞因子特征与脑脊液基于突变的追踪相结合,可能实现生物学知情的患者分层和适应性试验设计,包括评估靶向IL-6/STAT3信号、巨噬细胞极化或血管生成通路(如VEGF)的策略。因此,虽然脑脊液免疫谱分析目前尚未指导常规治疗决策,但它代表了一个机制上信息丰富的平台,具有明确的支持胶质瘤精准免疫疗法开发的潜力。
中枢神经系统淋巴瘤:B细胞恶性肿瘤与免疫失调
原发性中枢神经系统淋巴瘤是一种侵袭性弥漫性大B细胞淋巴瘤亚型,局限于大脑、脊髓、眼睛和软脑膜,诊断时无全身受累。通过适应中枢神经系统独特的免疫环境,原发性中枢神经系统淋巴瘤重编程血管周围和脑膜微环境,削弱细胞毒性监视,并驱动侵袭性行为和高复发风险,尽管初始对化疗敏感。在这方面,原发性中枢神经系统淋巴瘤提供了一个模型,展示了恶性B细胞如何通过规避中枢神经系统免疫监视机制实现长期持久存在。
中枢神经系统淋巴瘤脑脊液中的免疫细胞群
在部分原发性中枢神经系统淋巴瘤患者中可检测到软脑膜或脑脊液受累,报告频率约为7-42%,具体取决于诊断方法学标准。无实质病变的原发软脑膜原发性中枢神经系统淋巴瘤很少见,大多数脑脊液受累病例发生在实质淋巴瘤的背景下。重要的是,脑脊液分析的价值超出了明显的软脑膜疾病。神经影像学研究表明,约97%的实质原发性中枢神经系统淋巴瘤病变直接接触脑脊液表面,突显了肿瘤细胞与脑脊液区室之间密切的解剖学关系。这种近乎普遍的邻近性为基于脑脊液的肿瘤和免疫特征检测提供了强有力的生物学依据,即使在没有细胞学可检测的脑脊液播散的情况下也是如此。
当存在脑脊液受累时,其特征是检测到恶性或克隆性扩增的B细胞,这些细胞被认为来源于占据血管周围和脑膜界面的肿瘤细胞群,并通过Virchow-Robin间隙进入脑脊液。除恶性成分外,脑脊液免疫景观通常表现为效应细胞低表达、调节和髓系偏移状态(图1和表1)。虽然Treg细胞和TAM样群相对富集,但Tc细胞存在但表现出耗竭和减弱的细胞毒性程序,反映了瘤内微环境并与不良临床结局相关。除了这些典型转变外,CXCR5+PD-1+CD4+ T滤泡辅助样细胞在原发性中枢神经系统淋巴瘤脑脊液中的富集是一个显著特征。已知这些细胞通过CD40L和IL-21信号支持B细胞增殖和存活,促进生发中心程序如BCL6。在原发性中枢神经系统淋巴瘤的背景下,Tfh样细胞的存在可能因此有助于恶性B细胞的持续存在和免疫逃逸,表明肿瘤利用适应性免疫成分来维持肿瘤生存。
中枢神经系统淋巴瘤脑脊液中的细胞因子谱
原发性中枢神经系统淋巴瘤脑脊液中的细胞因子特征进一步强调了其免疫抑制环境(表2)。其中IL-10是最持续升高的细胞因子,通常超过50 pg/mL,而正常脑脊液中检测不到。功能上,IL-10是一种强效免疫调节细胞因子,抑制T细胞活化和抗原呈递,从而减弱抗肿瘤免疫反应。除了免疫调节作用外,B细胞淋巴瘤中的IL-10信号已被证明与JAK/STAT3通路的激活和增强的肿瘤细胞存活有关。因此,原发性中枢神经系统淋巴瘤脑脊液中IL-10的显著升高表明,该细胞因子不仅可能促进免疫抑制,还可能有助于鞘内恶性B细胞的持久存在。CXCL13是原发性中枢神经系统淋巴瘤脑脊液中的另一个定义性细胞因子。作为一种关键的B细胞趋化因子,它有助于CXCR5+ B细胞和Tfh样细胞的招募和滞留。升高的脑脊液CXCL13水平与活动性疾病状态相关,并在治疗反应后趋于下降。总之,这些细胞因子模式反映了脑脊液环境的特点:由IL-10介导的免疫调节和趋化因子依赖的B细胞招募,两者都有助于中枢神经系统淋巴瘤的维持和进展。
中枢神经系统淋巴瘤脑脊液组分的治疗意义
从转化角度来看,脑脊液分析已成为原发性中枢神经系统淋巴瘤中强大的诊断和监测工具。脑脊液中IL-10的测量显著改善了原发性中枢神经系统淋巴瘤与炎症或其他恶性疾病之间的术前鉴别。更重要的是,脑脊液中的IL-10/IL-6比值提供了更优的诊断准确性,敏感性和特异性分别高达95.5%和96.1%,优于单独使用IL-10。除诊断外,脑脊液细胞因子也为治疗监测提供了可操作的标志物。连续的IL-10测量反映了治疗反应:在大剂量甲氨蝶呤基础治疗期间早期下降与放射学/临床反应相关,而持续存在或反弹则预示早期复发和较短的无进展生存期。在这方面,脑脊液细胞因子监测可以整合到适应性治疗方案中,允许近实时地升级或修改治疗。此外,脑脊液谱分析也可能指导新的治疗策略。例如,可以探索IL-10阻断或CXCL13/CXCR5信号调节来破坏肿瘤在脑脊液微环境中的生长。此外,随着免疫检查点抑制剂越来越多地被考虑用于原发性中枢神经系统淋巴瘤,基线脑脊液细胞因子状态(如IL-10/IL-6比值、Tfh样细胞富集)可以作为对免疫检查点抑制剂治疗反应或耐药性的预测因子。因此,将脑脊液分析纳入临床试验设计至关重要,不仅用于患者选择,也用于药效学读数。
脑转移瘤:适应中枢神经系统的全身肿瘤
脑转移瘤是当来自颅外原发肿瘤的癌细胞迁移至并在中枢神经系统定植时产生的继发性肿瘤。这些转移是成人中最常见的颅内肿瘤,显著增加发病率和死亡率。与原发性中枢神经系统肿瘤不同,实质脑转移瘤必须首先突破中枢神经系统屏障,然后适应非天然的微环境。在这一适应过程中,转移细胞主动调节局部免疫,以在中枢神经系统微环境内确保生存和生长。尽管由于空间限制,脑脊液不能完全反映这些实质变化,但它仍然提供了一个微创窗口来了解潜在的生物学。
脑转移瘤脑脊液中的免疫细胞群
实质脑转移瘤在解剖上与脑脊液间隙不同,因此脑脊液中可检测到的免疫信号取决于病变的大小和邻近程度。因此,脑转移瘤脑脊液部分反映了颅内病变的免疫状态,但仍提供了一个具有临床意义的颅内免疫窗口。事实上,单细胞谱分析和TCR基因分型证明,脑转移瘤组织和脑脊液之间存在共享的克隆型,强调了脑脊液可以捕捉正在进行的T细胞反应。在免疫活性水平上,脑转移瘤脑脊液表现出一般的免疫调节谱,与匹配的肿瘤组织和非恶性脑脊液相比,细胞毒性效应程序的表达减少,炎症转录特征减弱(图1和表1)。尽管存在这种共享的免疫调节背景,脑转移瘤脑脊液仍保留了反映原发肿瘤生物学的免疫特征。例如,黑色素瘤来源的脑转移瘤的脑脊液显示出大量的T细胞浸润,但效应功能有限。此外,在乳腺癌脑转移瘤中,脑脊液特征性地呈髓系为主,具有显著的单核细胞/TAM特征和可变的中性粒细胞参与。这些模式表明,尽管脑转移瘤脑脊液中的免疫信号可能相对于肿瘤组织有所减弱,但它们仍然捕捉到了中枢神经系统内肿瘤相关的免疫细胞组成和功能极化转变。
脑转移瘤脑脊液中的细胞因子谱
脑转移瘤的脑脊液细胞因子谱不同于原发性中枢神经系统淋巴瘤典型的IL-10富集的免疫抑制,而是以IFN/趋化因子驱动的信号和炎症相关介质为主(表2)。在非小细胞肺癌脑转移瘤脑脊液中,IFN-γ诱导的CXCL10和CXCL11升高,已知它们能招募CXCR3+ T细胞。此外,在非小细胞肺癌脑转移瘤脑脊液中已报道IL-17相关的炎症信号升高,根据已建立的机制研究,这已被证明与中性粒细胞招募、血脑屏障破坏和促进癌细胞脑定植的胶质细胞激活有关。在黑色素瘤脑转移瘤中,脑脊液显示出向CXCL10/CXCL4/CXCL17/IL-8的转变,伴随着IL-1α/IL-4/IL-5/CXCL22的减少,这与一种招募T细胞但功能受限的炎症一致,这种炎症支持肿瘤的持续存在。除了肿瘤特异性细胞因子特征外,最近的转化研究已确定脂质运载蛋白-2是多种脑转移瘤背景下的一个共享介质。LCN2是一种分泌蛋白,由肿瘤细胞和脑微环境中的反应性成分(包括星形胶质细胞和髓系细胞)产生,而不是脑脊液特异性因子。在黑色素瘤和乳腺癌来源的脑转移瘤实验模型中,LCN2已在脑脊液中被检测到,并被证明与转移负荷相关,表明脑脊液LCN2水平可能反映肿瘤-脑界面的病理重塑。虽然这些发现支持LCN2与中枢神经系统转移生物学相关,但仍需要在人类脑脊液队列中进行进一步验证,以确立其作为脑脊液生物标志物的实用性。
脑转移瘤脑脊液组分的治疗意义
对于实质脑转移瘤,脑脊液中癌细胞的检测是可行的,尽管取决于肿瘤的位置。随着脑脊液活检的产率随肿瘤大小和位置增加,这些特征可用于构建预测患者结局的回归模型。有趣的是,脑脊液的ctDNA比血浆更准确地捕捉脑肿瘤特有的突变和耐药机制。此外,细胞因子谱分析也提供预后和药效学价值。在非小细胞肺癌脑转移瘤中,多重脑脊液细胞因子谱分析已被证明可以预测基于PD-1的免疫疗法的颅内反应,较高的基线脑脊液LAMP3区分有反应者,而选定的炎症细胞因子(如CXCL10和IL-18)在基线时较低并在治疗期间进一步下降。这些发现强调了脑脊液免疫谱分析作为一种非侵入性方法的潜力,用于捕捉肿瘤组织生物标志物无法反映的中枢神经系统特异性免疫状态。在黑色素瘤脑转移瘤中,脑脊液中升高的CXCL10/IL-6/IL-8/CCL2可以在全身和放疗期间提供炎症重编程或播散风险的早期读数。
软脑膜转移瘤:癌细胞直接定植于脑脊液
当癌细胞浸润脑脊液和软脑膜时发生软脑膜转移,创造了一个独特的支持癌细胞存活和增殖的肿瘤微环境。软脑膜转移与乳腺癌、肺癌和黑色素瘤等晚期癌症相关。作为软脑膜转移瘤的直接环境,脑脊液经历显著的免疫和分子变化,这些变化既可反映也可促进疾病进展。
软脑膜转移瘤脑脊液中的免疫细胞群
软脑膜转移将脑脊液重构为一个髓系主导、免疫抑制的微环境(图1和表1)。最一致的细胞转变是TAM样巨噬细胞的扩增,伴随单核细胞和粒细胞MDSC亚群。跨脑脊液屏障的硬脑膜巨噬细胞浸润进一步增加了软脑膜微环境中的髓系主导地位。它们可以通过SPP1-MMP14程序进入脑脊液,获得与软脑膜转移负荷紧密相关的免疫抑制表型。这种髓系亚群的主导地位与Treg富集以及T细胞和NK细胞的功能障碍相结合,有效沉默了适应性免疫监视。相反,CCR7+迁移性树突状细胞进入脑脊液,在那里它们激活NK细胞并部分恢复细胞毒性活性。因此,软脑膜转移瘤代表了一种“拉锯战”,其中促肿瘤的髓系回路通常压倒抗肿瘤的DC/NK相互作用,解释了软脑膜转移瘤的快速进展和不良预后。
软脑膜转移瘤脑脊液中的细胞因子谱
软脑膜转移瘤的细胞因子环境反映了这种二元性(表2)。一方面,促炎细胞因子如IL-6、IL-8和IL-1β持续升高,表明强烈的髓系激活、内皮/血脑屏障通透性和症状负担。另一方面,免疫抑制介质包括TGF-β和IL-10也经常升高,迫使T细胞无反应、抗原呈递减少和Treg扩增。一个特别值得注意的因素是补体成分3,它通过招募/极化巨噬细胞和放大有利于肿瘤生长的矛盾性炎症,重编程脑脊液免疫以利于肿瘤进展。一个相反方向、软脑膜转移瘤特异性的保护回路涉及IFN-γ驱动的CCR7+树突状细胞,它们在脑脊液内激活NK细胞。当这一轴完整时,细胞因子模式向着增加IFN信号和细胞毒性读数转变。重要的是,可以检测到原发肿瘤特异性印记。黑色素瘤软脑膜转移瘤的脑脊液通常显示补体/炎症相关的激活。此外,乳腺癌软脑膜转移瘤突出了代谢适应信号,包括LCN2,它促进铁的清除。这些结果强调,软脑膜转移瘤中脑脊液的细胞因子景观并非统一,而是反映了叠加在脑脊液微环境上的原发肿瘤生物学。
软脑膜转移瘤脑脊液分析的治疗意义
由于软脑膜转移瘤直接位于蛛网膜下腔,相比于其他中枢神经系统恶性肿瘤,脑脊液分析提供了一个异常直接和可操作的平台。基于脑脊液的ctDNA检测显示出优于传统细胞学的敏感性,并且在检测中枢神经系统特异性驱动因子和耐药突变方面优于血浆。这些能力使得靶向治疗得以实现,例如在非小细胞肺癌中使用EGFR/ALK抑制剂,在乳腺癌中使用HER2导向方案,以及在黑色素瘤中使用BRAF/MEK抑制剂。此外,脑脊液免疫谱分析增加了临床相关的价值。IL-6、IL-8和IL-1β的水平通常在放射学或临床进展期间升高,纵向脑脊液谱分析表明,炎症细胞因子信号可能随疾病控制而下降,提供了潜在的治疗反应动态读数。与这一概念一致,最近一项整合了乳腺癌来源软脑膜转移瘤中脑脊液循环肿瘤细胞检测、单细胞转录组学和蛋白质组学分析的多模式研究表明,肿瘤负荷和炎症信号的动态变化与治疗反应密切相关,强调了脑脊液作为实时监测区室的实用性。临床前证据进一步表明,在软脑膜转移瘤脑脊液中识别的免疫轴可作为治疗靶点加以利用。在乳腺癌来源的软脑膜转移瘤小鼠模型中,补体C3阻断已被证明可以逆转脉络丛条件化并限制软脑膜转移瘤生长。在黑色素瘤软脑膜转移瘤小鼠模型中,IFN-γ-CCR7+树突状细胞-NK细胞回路的扩增增加了鞘内细胞毒性并减少了肿瘤负荷。在肺癌软脑膜转移瘤小鼠模型中,中断硬脑膜来源的巨噬细胞运输也已被证明可以减少髓系积累并延长生存期。总之,这些发现确立了脑脊液不仅是诊断液体,更是肿瘤-免疫相互作用的机制性读数和潜在的治疗途径本身。
结论与未来方向
脑脊液已从一个被动的生物液体转变为理解中枢神经系统恶性肿瘤免疫生物学的动态整合窗口。脑脊液分析揭示,每种肿瘤类型驱动独特的免疫程序,而不是单一的免疫抑制特征。具体来说,胶质瘤产生一种髓系/Treg偏移、效应细胞贫乏的表型;原发性中枢神经系统淋巴瘤以恶性B细胞为主,伴随强烈的IL-10/CXCL13信号;实质脑转移瘤反映原发肿瘤特异性的炎症和损伤反应;而软脑膜转移瘤表现出深度髓系主导伴T/NK功能障碍。重要的是,脑脊液中的可溶性因子不仅仅是被动反映,而是与免疫重塑机制性相关,包括原发性中枢神经系统淋巴瘤中的IL-10、脑转移瘤中的CXCL10/IL-6/IL-8,以及软脑膜转移瘤中的补体C3/IL-6/IL-8/IL-1β(表2)。
除了细胞和细胞因子谱分析,脑脊液中的肿瘤来源核酸在检测中枢神经系统特有的突变和耐药机制方面通常优于血浆,强调了脑脊液作为神经肿瘤学中特权分子信息源的地位(图2)。
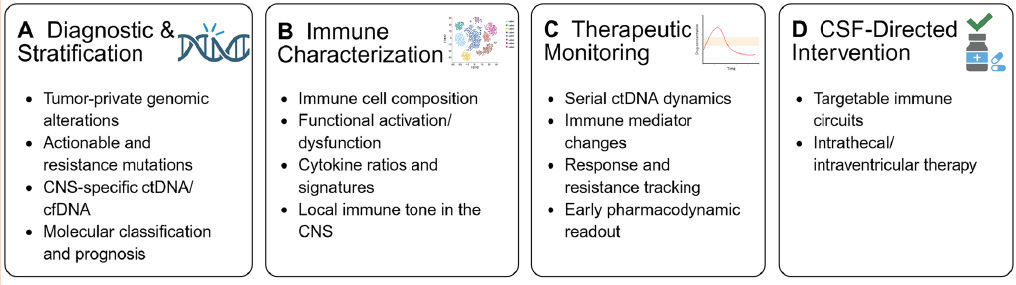
图2. 脑脊液分析在脑恶性肿瘤中的临床应用 脑脊液分析提供了一个可重复的窗口,用于观察颅内肿瘤生物学及免疫动态变化,这些变化在外周血中无法完全反映。 (A) 诊断与分子分层 基于脑脊液的液体活检能够检测肿瘤特有的基因组改变,包括可靶向突变和耐药相关突变。在特定情况下,脑脊液来源的ctDNA和cfDNA比血浆更准确地捕捉中枢神经系统特有的分子特征,支持分子分型和预后评估。 (B) 免疫谱分析与疾病特征刻画 脑脊液的免疫谱分析,包括免疫细胞组成和细胞因子图谱,可提供对中枢神经系统内局部免疫状态和疾病活性的深入了解。独特的免疫和细胞因子特征反映了肿瘤相关的免疫重塑。 (C) 治疗监测与药效学评估 连续脑脊液分析通过捕捉肿瘤来源核酸和免疫介质的动态变化,支持对疾病演变的纵向监测。这些变化可能与治疗反应、新发耐药或治疗过程中的免疫调节相关。 (D) 治疗开发与脑脊液导向干预 除了诊断和监测作用外,脑脊液本身也是一个生物学活跃的界面,肿瘤细胞、免疫细胞群和可溶性介质在此相互作用。脑脊液分析为脑脊液导向治疗策略(尤其是在软脑膜转移瘤中)的开发和评估提供依据,并支持局部干预与全身或免疫调节治疗的整合。
这些见解已经为当前的临床实践提供了信息——例如,胶质瘤中的MGMT甲基化和IDH1/2检测,原发性中枢神经系统淋巴瘤中的IL-10/IL-6比值,脑转移瘤中的PD-L1反应特征,以及软脑膜转移瘤中的ctDNA负荷(图2)。总之,这些发现支持了脑脊液分析可以从诊断辅助工具演变为能够指导治疗选择和纵向监测的动态生物标志物区室的概念。在这方面,连续的脑脊液谱分析可以作为颅内疾病活动的免疫和分子读数,特别是在接受免疫调节治疗的患者中。当与影像学和临床评估整合时,脑脊液来源的生物标志物有潜力指导适应性治疗策略,尽管这种方法仍处于研究阶段,需要前瞻性验证。
与其诊断和监测角色并行,脑脊液也作为一种治疗途径被探索,特别是在软脑膜转移瘤的情况下(图2)。然而,过去二十年的临床结果表明,脑脊液导向的治疗占据一个细微和选择性的角色,而不是一个广泛适用的治疗范式。结果因肿瘤类型、研究设计和患者人群而有很大差异,反映了软脑膜疾病固有的生物学异质性和实际限制。
在前瞻性研究中(表3),随机DEPOSEIN试验提供了最清晰的信号,即脑脊液内持续的药物暴露可以影响软脑膜疾病动力学。在这项研究中,在全身治疗基础上加入鞘内脂质体阿糖胞苷,与单独全身治疗相比,适度延长了软脑膜无进展生存期,而总生存期获益仍然有限。重要的是,研究者强调了患者选择和临床背景在解释这些结果时的重要性,强调鞘内化疗可能适用于特定情况,而非统一适用于所有软脑膜转移瘤患者。早期阶段的试验进一步说明了可行性和限制。在HER2阳性乳腺癌软脑膜转移瘤中,鞘内曲妥珠单抗(NCT01325207)显示出相对于历史预期的令人鼓舞的疾病控制和生存结局,支持了基于抗体的疗法可以在脑脊液区室内达到治疗相关暴露且全身毒性可接受的概念。同样,鞘内培美曲塞已在多项I/II期研究中进行评估,显示出可控的安全性和在选定患者(特别是在非小细胞肺癌中)的可测量活性。尽管如此,这些研究并非旨在定义比较疗效,报告的结果仍然存在异质性。
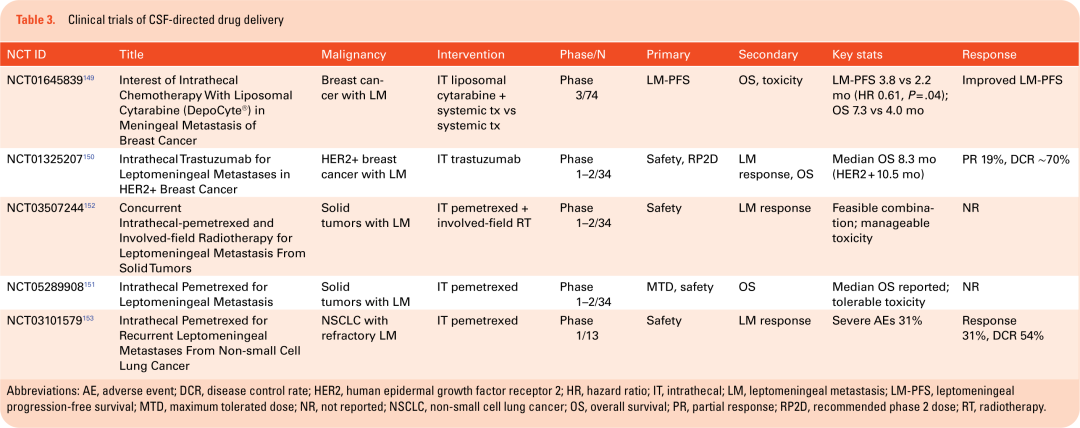
在这些试验中,一个反复出现的主题是,治疗获益与软脑膜疾病本身的生物学和物理特性密切相关。在晚期软脑膜转移瘤中经常观察到的脑脊液循环受损,可能限制药物分布并增加神经毒性风险,如化学性蛛网膜炎,这加强了治疗前评估和仔细监测的重要性。总之,现有数据表明,在选定患者中,脑脊液导向治疗可以有意义地改变局部疾病动态,但其影响既不统一,也不足以取代全身性方法。
这些临床观察与对脑脊液区室更广泛的概念转变相一致。脑脊液不仅仅是药物输送的管道,它代表了一个生物学上活跃的界面,其中肿瘤细胞、免疫群和可溶性介质相互作用。正如前面所强调的,这个环境由不同于外周血的独特免疫回路和细胞因子网络塑造。因此,当与并行的生物标志物分析相结合时,利用脑脊液作为治疗空间可能最为有效,从而实现局部治疗与全身或免疫调节策略的理性整合。
脑脊液导向方法的转化相关性可能较少依赖于传统鞘内化疗的扩展,而更多地依赖于生物学知情的干预措施。脑脊液区室越来越容易受到多种治疗模式的影响,包括小分子、抗体类药物、纳米颗粒制剂和细胞疗法,主要是在软脑膜疾病的背景下,并可能扩展到实质脑肿瘤。在这个框架下,脑脊液应被视为一个整合的生物区室——将分子监测与靶向干预联系起来——而非被动液体或独立的治疗途径。
参考文献
Neurooncol Adv . 2026 Feb 27;8(1):vdag058. doi: 10.1093/noajnl/vdag058.


