好文推荐 | 短期内行为学重复测定对3xTg-AD小鼠认知及焦虑状态评估效果的影响
时间:2026-05-05 17:16:12 热度:37.1℃ 作者:网络
摘要
目的 探讨短期内重复测试旷场、新物体识别、巴恩斯迷宫行为学实验对3xTg-AD小鼠认知及焦虑状态评估效果的影响。方法 通过前期不同方式处理获得4组12月龄3xTg-AD小鼠,其中实验组1~3为3种不同药物干预,对照组为生理盐水处理。依次对小鼠进行旷场实验、新物体识别实验、巴恩斯迷宫实验。采用行为学视频分析系统记录小鼠的活动轨迹并分析小鼠在中心区域停留的时间、探索新旧物体的时间和到达目标孔的潜伏期。待完成1次完整的测试后,随即开展3次重复测试,所有测试在1个月内完成。结果 随着重复次数增加,旷场实验中小鼠在中心区域停留的时间减少(P<0.05);新物体识别实验中新物体识别指数变异系数变大,对新环境和新物体的探索行为减少;巴恩斯迷宫实验中,4次测试小鼠到达目标孔的潜伏期之间无显著差异,具有较好的重复性。结论 短期重复测试会干扰3xTg-AD小鼠在旷场实验中焦虑状态的评价以及在新物体识别实验中对新物体的偏好,但对小鼠在巴恩斯迷宫实验中找到目标孔的潜伏期无明显影响。3xTg-AD小鼠行为学能否进行重复测定,应根据不同实验而确定。
关键词:重复测定;3xTg-AD小鼠;认知评估;行为学实验;焦虑状态
Key words:Repeated measurement;3xTg-AD mice;Cognitive assessment;Behavioral tests;Anxiety status
行为学实验是神经行为研究领域中评估动物行为的重要途径,以此可以评估实验动物的学习记忆能力、协调运动能力、焦虑状态、社交行为以及各种身体和神经系统疾病[1],在现代神经科学研究中占有十分重要的地位[2]。
动物行为学实验通常包括评估学习及记忆能力的Morris水迷宫实验、穿梭实验;检测运动行为的跑台实验、负重游泳实验以及评估情绪活动强迫游泳实验、悬尾实验、糖水偏好实验等,其中旷场实验、新物体识别实验、巴恩斯迷宫实验较为常见。旷场实验是一种用于评估啮齿类动物自主运动活性和焦虑状态的行为学实验[3]。它通过将动物放置在陌生的开放场地中激发探索行为从而获取有关自主运动行为和焦虑相关情绪的信息,被广泛用于焦虑的神经生物学基础研究以及药物的镇静作用评价[4-7]。新物体识别实验是一种常见的认知测试,旨在评估动物对新奇事物的兴趣和识别能力、对重复出现物体的记忆能力[1,8]。它采用识别指数(recognition index,RI)作为主要测量指标量化实验动物对新奇事物的探索行为,从而反映动物对新奇事物的偏好,被广泛用于阿尔茨海默病(Alzheimer disease,AD)、后天性脑积水和缺血性脑卒中等损伤模型动物的认知能力评估[9]。巴恩斯迷宫实验是一项成熟的用于评估啮齿动物空间学习和记忆能力的实验[10,11]。空间学习能力评估是行为神经科学的核心,研究小鼠的空间学习能力对于了解AD等神经系统变性疾病的潜在机制以及潜在的治疗方法至关重要[12-14]。
AD是以进行性认知障碍和行为障碍为特征的中枢神经系统变性疾病,其患病率随年龄的增长而增加,是最常见的痴呆类型[15,16]。随着我国老龄化程度的加剧,我国AD患者数量将不断增加[17,18]。预计到2050年,我国AD及其他痴呆症患者的人数将上升至6 630万[19]。在AD发病机制及其防治药物开发研究中,通常用动物模型开展AD病理机制研究、药物筛选和评价以及临床前研究。3xTg-AD小鼠因携带人源APP、MAPT和PSEN1基因,因此表现出Aβ沉积、tau蛋白过度磷酸化、年龄相关的认知缺陷等[20-22]病理学特征,是一种用于AD研究的典型转基因模型鼠。AD模型小鼠焦虑抑郁状态以及认知和记忆功能通常采用旷场实验、新物体识别、水迷宫和巴恩斯迷宫等行为学实验来评估[23-26]。然而,行为学实验易受到操作人员、外环境条件、具体操作细节及小鼠状态等诸多因素的影响而导致初次实验效果不佳,从而不能真正反映小鼠的焦虑状态或认知能力。对于短期内行为学测试能否重复进行的问题,尽管国内外有一定的研究,但研究采用的皆是C57BL/6 J、ICR、昆明小鼠等正常鼠,尚未有模型鼠重复测试结果报道。
本研究采用3xTg-AD小鼠,短期内对小鼠在旷场中心区域停留时间、新物体的偏好以及在迷宫中找到目标孔的潜伏期进行重复测定,进而分析短期内多次重复测定对小鼠行为学评估效果的影响,旨在为AD模型小鼠认知及焦虑状态研究提供借鉴与参考。
1 材料与方法
1.1 实验动物
3xTg-AD小鼠30只(SPF级,购于南京大学模式动物研究所),每组7~8只,雌雄数量比趋于1∶1。所有小鼠饲养条件相同,水食自由。小鼠动物房温度保持在23~25 ℃,相对湿度(55%±10%),维持12/12 h的昼夜节律。
1.2 实验仪器
小鼠行为学分析系统(Smart 3.0,西班牙Panlab)。
1.3 实验设计
将30只3xTg-AD小鼠随机分为4组(记为实验组1~3和对照组),其中实验组1~3采用3种不同药物干预,对照组注射相同剂量的生理盐水。随后饲养至12月龄,开展首次行为学检测(时间点记为t0),依次完成旷场实验、新物体识别实验、巴恩斯迷宫实验后进行3次重复测试(时间点分别记为t1~t3),所有测试在1个月内完成。
1.4 行为学检测
1.4.1 旷场实验
将边长为40 cm的顶部开口的正方体的底面用九宫格九等分,居中的方格定义为中心区域,其余为周边区域。实验时,将小鼠背对实验者置于中心区域,利用摄像头和运动跟踪软件记录5 min内小鼠的自主活动情况。每次实验结束后将小鼠安全放回笼中,用75%乙醇清洁并消毒旷场区域。
1.4.2 新物体识别实验
将两个边长为3 cm的蓝色正方体木块(旧物体)放在旷场实验箱侧壁的左右两端,以物体为圆心,将半径5 cm的区域定义为物体探索区域。实验时,将小鼠背对两物体从另一侧壁中央放入场地内自由探索。5 min后将小鼠放回原来饲养的鼠笼内,用酒精清理实验场地。待小鼠休息1小时后,将其中一个旧物体更换为新物体(直径为3 cm,高度为4 cm材质与旧物体相同的绿色圆柱体木块),以相同方式将小鼠放入实验场地,用视频采集系统记录5 min内小鼠对新、旧物体的探索时间。计算RI量化小鼠的记忆能力。RI=探索新物体时间/(探索新物体时间+探索旧物体时间)。
1.4.3 巴恩斯迷宫实验
实验装置是一个环形围绕20个小圆洞(直径5 cm)的圆形平台(直径100 cm,高度100 cm),平台四周设置不同的参照物。实验开始前选择一个小圆洞作为目标孔,在其底部放置一个暗盒供小鼠隐藏。实验分为适应期、训练期、测试期三个阶段。适应期:将小鼠置于平台中央,开启噪声和灯光刺激,任其自由探索3 min。探索时间结束后,将未找到暗盒的小鼠引导进入暗盒并适应1 min。每次实验结束后用75%乙醇清洁平台和暗盒。训练期:与适应过程相同,每天训练3次,每次训练间隔30 min,连续训练3 d。测试期:将暗盒移除,用行为学软件追踪系统记录小鼠的运动轨迹和到达目标孔的潜伏时间。
1.5 统计学分析
使用Microsoft Excel 2019和SPSS 27.0软件对行为学实验数据进行汇总和统计学分析。实验数据采用中位数(四分位数间距)[M(P25,P75)]进行描述。同一时间点不同组别的实验数据采用多个独立样本的非参数Kruskal-Wallis检验进行单因素分析,同一组别不同时间点的实验数据采用多个相关样本的非参数Friedman检验进行差异性比较,然后对具有统计学差异的组间进行两两比较,并使用GraphPad Prism 9.1.0软件对分析结果作图,P<0.05为差异具有统计学意义。
2 结果
2.1 旷场实验
小鼠在旷场中的活动轨迹如图1所示。t0~t3时间点,实验组1~3和对照组3xTg-AD小鼠在中心区域停留时间的Kruskal-Wallis检验统计量H值分别为9.91、1.43、1.90、1.67,对应的P值分别为0.019、0.700、0.594、0.644(见表1)。因t0时间点的P<0.05显著水平,对t0时间点进行不同组别3xTg-AD小鼠在中心区域停留时间两两比较,如表2所示,可以看出t0时间点,实验组1和对照组之间小鼠在中心区域停留时间存在显著性差异(P<0.05)(见图2),实验组1小鼠在中心区域停留时间显著高于对照组,焦虑抑郁程度较轻。
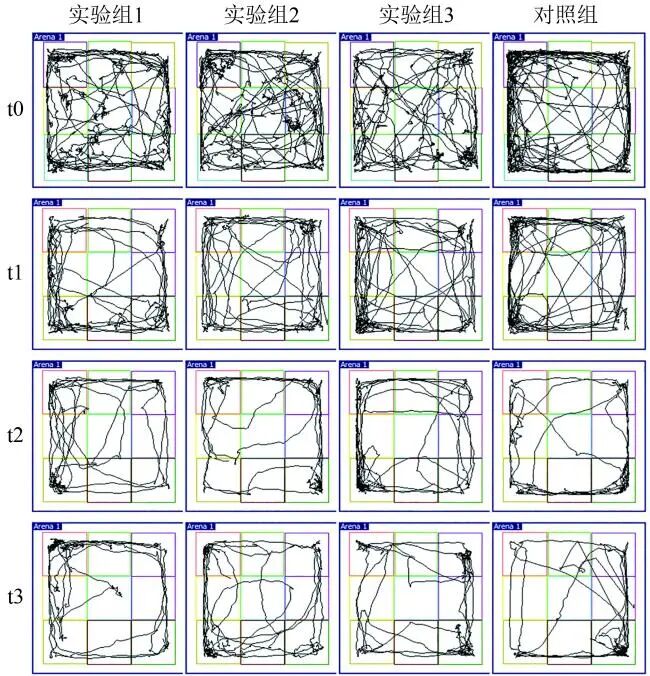
图1 旷场实验小鼠活动轨迹图
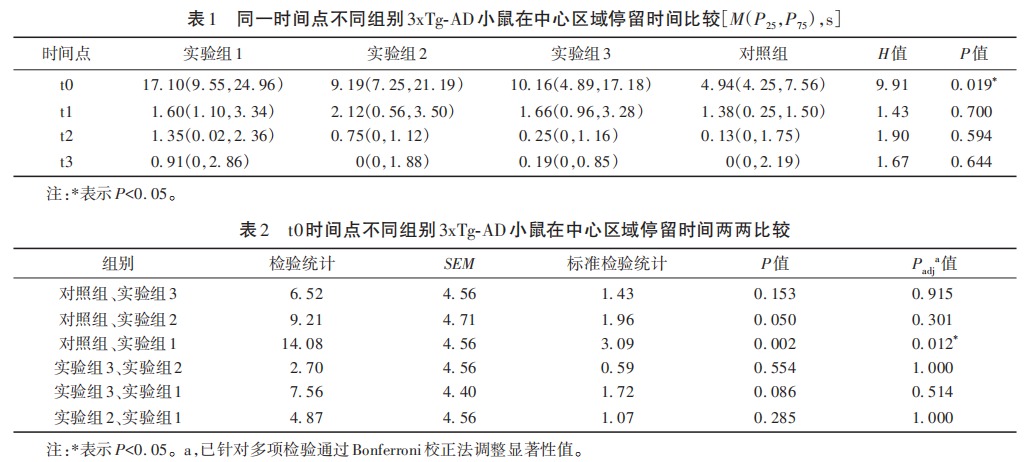
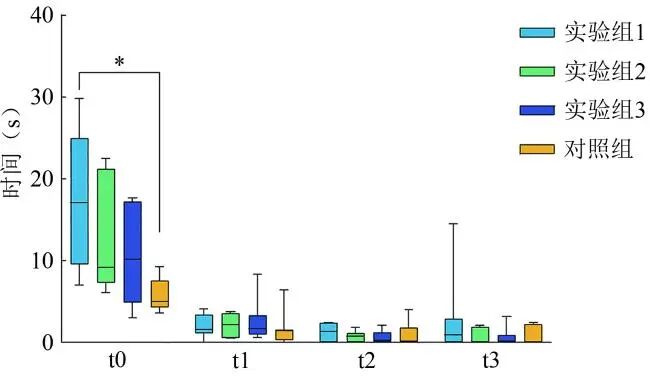
注:*表示P<0.05。
图2 同一时间点不同组别3xTg-AD小鼠在中心区域停留时间比较
实验组1~3和对照组,t0~t3时间点3xTg-AD小鼠在中心区域停留时间的Friedman检验χ2值分别为13.11、19.50、16.62、14.02,对应的P值均<0.01,如表3所示,说明同一组别不同时间点小鼠在中心区域停留时间存在显著性差异。
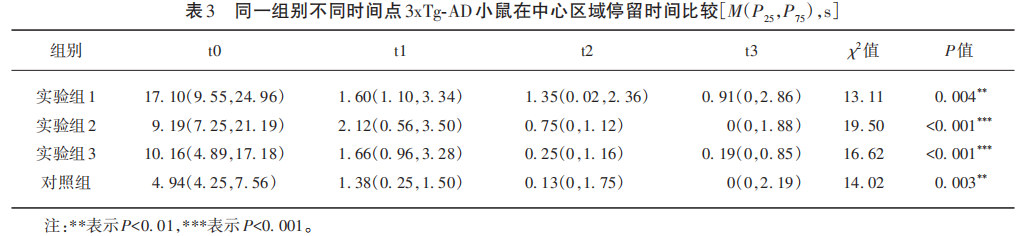
对同一组别不同时间点3xTg-AD小鼠在中心区域停留时间进行两两比较(见表4),发现每个组别t0时间点3xTg-AD小鼠在中心区域停留时间均多于t2、t3时间点,其差异具有统计学意义(P<0.05)(见图3)。
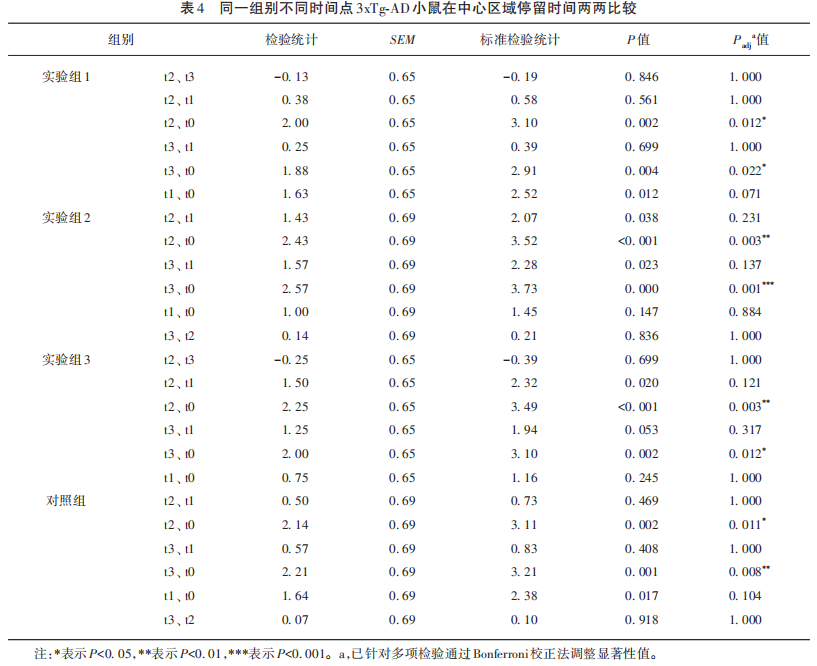
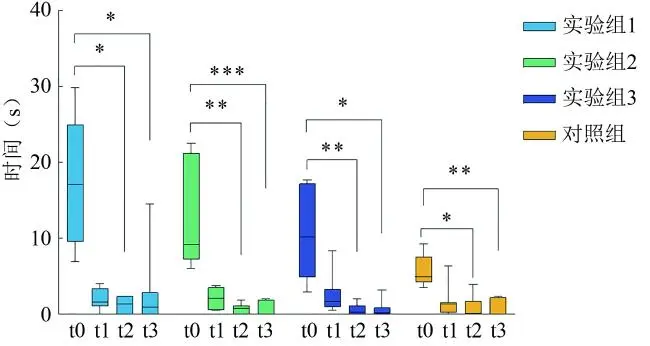
注:*表示P<0.05,**表示P<0.01,***表示P<0.001。
图3 同一组别不同时间点3xTg-AD小鼠在中心区域停留时间比较
2.2 新物体识别实验
新物体识别实验中小鼠探索新旧物体的活动轨迹如图4所示。t0~t3时间点,实验组1~3和对照组3xTg-AD小鼠新物体识别指数的Kruskal-Wallis检验统计量H值分别为5.57、2.28、3.05、1.93,对应的P值分别为0.135、0.517、0.385、0.587(见表5),均>0.05,说明同一时间点不同组别3xTg-AD小鼠新物体识别指数差异无统计学意义(见图5)。
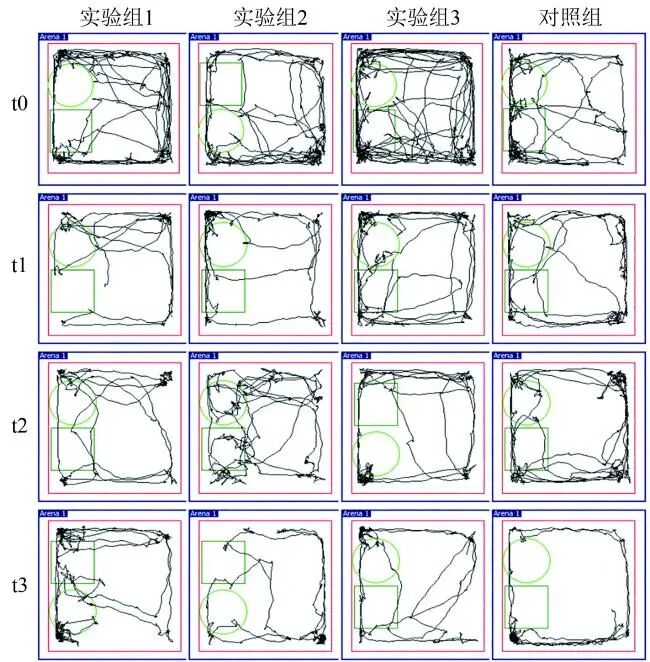
图4 新物体识别实验小鼠活动轨迹图
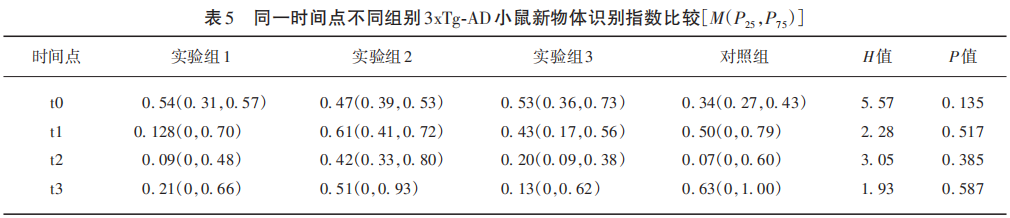
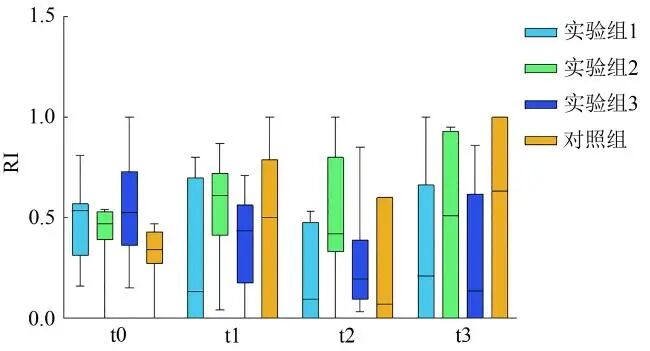
图5 同一时间点不同组别3xTg-AD小鼠新物体识别指数比较
实验组1~3和对照组,在t0~t3时间点3xTg-AD小鼠新物体识别指数的Friedman检验χ2值分别为6.21、0.39、1.41、1.53,对应的P值分别为0.102、0.942、0.704、0.677(见表6),均>0.05,说明同一组别不同时间点3xTg-AD小鼠新物体识别指数差异无统计学意义(见图6)。然而,实验组1~3和对照组,在t0~t3时间点3xTg-AD小鼠新物体识别指数的变异系数明显增大(见表7)。特别是实验组2和实验组3中3xTg-AD小鼠新物体识别指数的变异系数呈明显随重复测定次数递增的趋势(见图7),表明随着重复测定次数的增加,所获得的新物体识别指数的数据的离散程度和波动程度递增,出现极端值的概率增加,实验数据的可靠性下降。
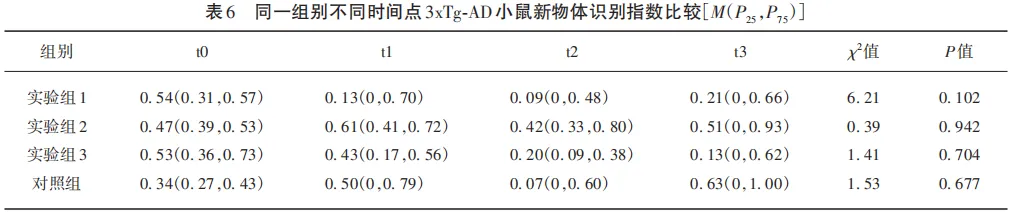
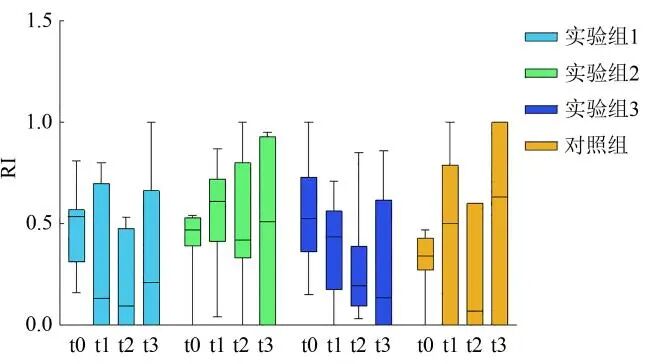
图6 同一组别不同时间点3xTg-AD小鼠新物体识别指数比较
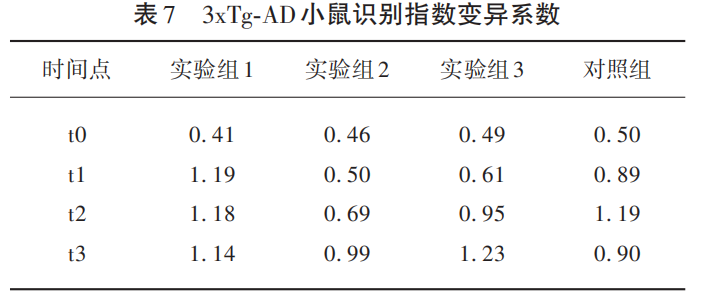
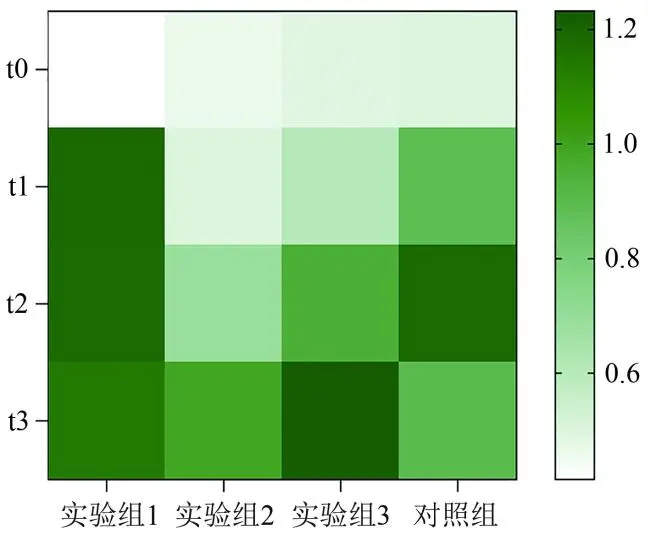
图7 3xTg-AD小鼠识别指数变异系数
2.3 巴恩斯迷宫实验
小鼠在迷宫中的活动轨迹如图8所示。t0~t3时间点,实验组1~3和对照组3xTg-AD小鼠到达目标孔的潜伏时间的Kruskal-Wallis检验统计量H值分别为0.09、1.22、9.61、3.83,对应的P值分别为0.993、0.748、0.022、0.280(见表8)。
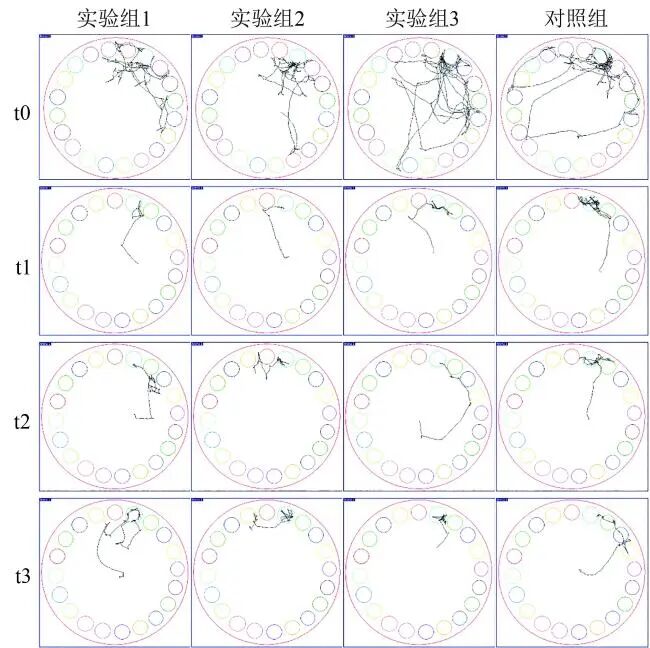
图8 巴恩斯迷宫实验小鼠活动轨迹图
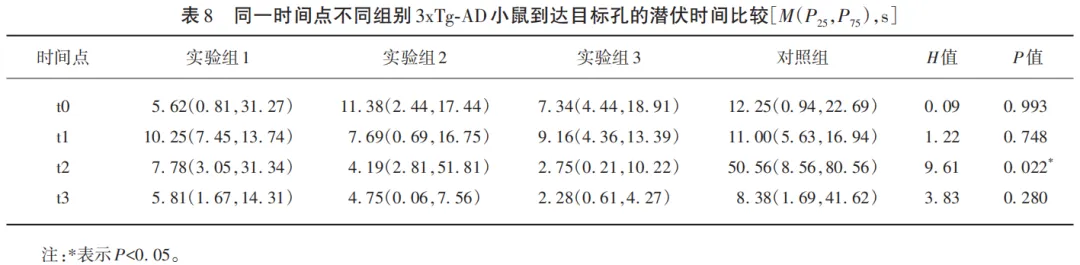
因t2时间点的P<0.05,对t2时间点进行不同组别3xTg-AD小鼠到达目标孔的潜伏时间两两比较,如表9所示,可以看出t2时间点,实验组3和对照组之间小鼠到达目标孔的潜伏时间差异具有统计学意义(P<0.05)(见图9),实验组3的3xTg-AD小鼠到达目标孔的潜伏时间显著高于对照组,表明实验组3中3xTg-AD小鼠的空间学习和记忆能力较对照组好。
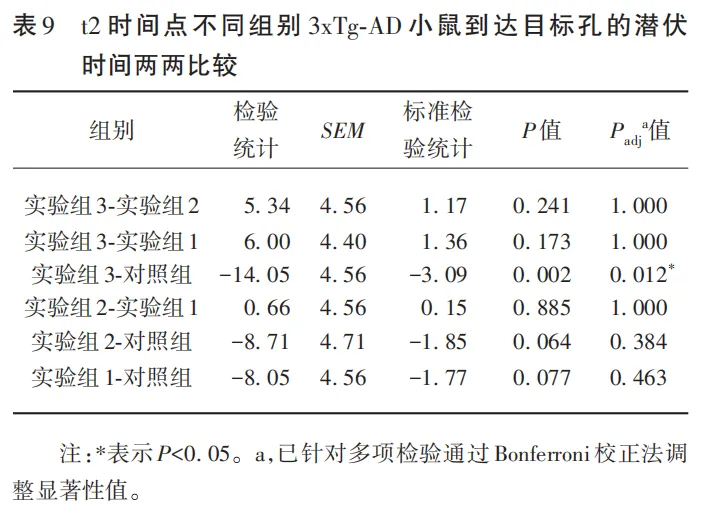
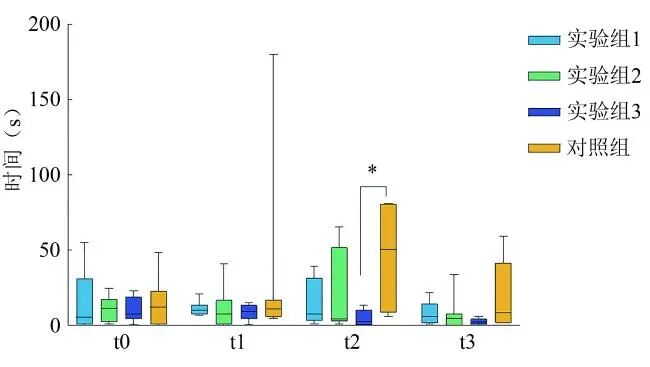
注:*表示P<0.05。
图9 同一时间点不同组别3xTg-AD小鼠到达目标孔的潜伏时间比较
实验组1~3和对照组,在t0~t3时间点3xTg-AD小鼠到达目标孔的潜伏时间的Friedman检验χ2值分别为1.95、0.43、7.35、5.91,对应的P值分别为0.583、0.934、0.062、0.116(见表10),均>0.05,说明同一组别不同时间点3xTg-AD小鼠到达目标孔的潜伏时间差异无统计学意义(见图10)。
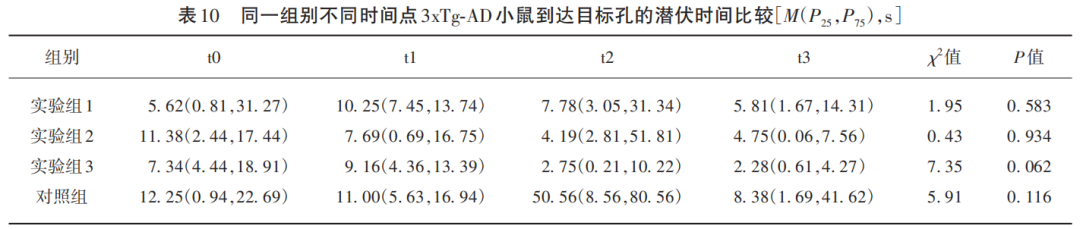
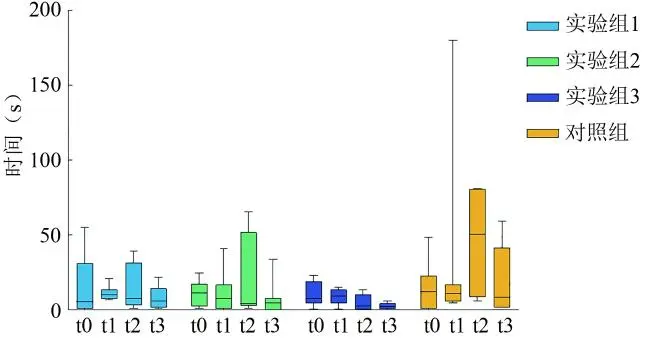
图10 同一组别不同时间点3xTg-AD小鼠到达目标孔的潜伏时间比较
3 讨论
行为学实验为揭示动物内在的行为机制提供了重要依据,推动了动物行为及其背后神经生物学基础的研究。但行为学实验能否用于重复测试,目前的研究更多地关注于重复数据能否用于疾病发展的纵向研究或能否正确反映干预前后小鼠认知功能、情绪状态等的变化[27,28]。本研究利用3xTg-AD小鼠短期内的行为学重复数据,对其重复性进行了分析,旨在探讨短期内行为学重复测定对3xTg-AD小鼠认知及焦虑状态评估效果与初次检测结果是否一致。
3.1 关于旷场实验
在旷场实验中,我们发现随着重复测试的进行,小鼠在中央区域停留的时间减少。有趣的是,与最初的测试时间点t0相比,4个组别的小鼠在中心区域停留的时间在第一次重复时虽出现了明显减少,但没有显示出差异,而在第二、第三次重复中均显示出了明显差异。这表明随着3xTg-AD小鼠对旷场环境的熟悉,它们对中央区域进行探索的好奇心减弱,且这种情况在第一次重复时就有所体现,并在随后的测试中更加明显。此时,以在中心区域停留的时间作为评估小鼠焦虑状态的指标已不再合适。最初测试中出现的实验组1和对照组间在中心区域停留时间的差异也在后续的连续重复测试中消失,说明小鼠对周围环境的记忆不仅减少了小鼠的探索行为还影响了组间比较的结果。由此可以看出,采用旷场实验评价3xTg-AD小鼠焦虑状态的方法是不适宜在同一对象上重复进行的。
陈超杰等[29]用同一批ICR小鼠进行了3次测试,也得到了一致的结果。有研究认为,这一结果是因小鼠只在首次暴露于旷场环境时引起主要由焦虑介导的行为导致的[30]。因此,只有首次暴露于旷场的情况下,才可用小鼠进入中央区域的次数或在中央区域停留的时间等指标评估各种药物对焦虑水平的影响。此外,一项基于C57BL/6 J小鼠的研究认为重复测试似乎对小鼠在旷场实验中的表现影响不大,甚至重复测试对小鼠在旷场中自主运动情况的影响可以通过适当的测试前安抚得到一定的缓解[31]。本研究认为重复检测的差异性可能和小鼠的品系、年龄、状态以及重复测试的间隔时间有关。无论如何,在采用旷场实验评价小鼠的焦虑状态时应避免在同一环境对同一对象进行重复测试,更换场地能否保持小鼠对新环境的探究兴趣,有待进一步的研究。
3.2 关于新物体识别实验
新物体识别实验,通过对识别指数的分析发现重复测试似乎对小鼠在新物体识别实验中的表现没有明显影响,但小鼠识别指数的变异系数随重复测试次数的增加而增大,表明随着重复测试的进行,每组小鼠识别指数的波动程度加大,数据变得紊乱,难以用于评估小鼠对新物体的识别能力。这说明不更换新旧物体的新物体识别实验的重复测试是行不通的,尽管保持相同的测试程序,小鼠对先前测试的记忆会干扰后续测试中对“新物体”的识别。
以往实验表明,只要每次实验同时更换新旧物体,新物体识别实验可以在同一批小鼠中重复测试,小鼠对新物体的探索时间总是长于旧物体[32]。因此在新物体识别实验中,应尽量避免对单一对象进行重复测试。如果在实验设计中要对整体进行重复测试,也应在每次测试时同时更换新旧物体,这样可以更好地保持小鼠对新物体的探究兴趣。另一项研究表明,用不同粒度的砂纸为新旧物体提供不同的纹理也可以在重复测试中保持小鼠对新物体的探究兴趣[33]。提示不一定要对新旧物体进行完全的替换,只要在每次测试中对新旧物体的颜色、纹理、形状等外在因素进行调整,新物体识别实验便可以重复检测。最近一项研究表明,腹侧被盖区多巴胺神经元在出现新物体时会增加放电,而在反复接触过程中会减少放电,并且多次熟悉过程能增强小鼠对随后出现的新奇事物的辨别力[34,35]。这提示我们如果新物体识别实验中发现小鼠对新物体的辨别力较弱,可以通过更换新旧物体并在实验设计中增加熟悉旧物体的时间或次数来增强小鼠对新物体的辨别能力。
3.3 关于巴恩斯迷宫实验
巴恩斯迷宫实验重复测试,小鼠到达目标孔的潜伏期没有差异,表明巴恩斯迷宫实验具备较好的重复性。此外,本研究进行了4次检测,虽然小鼠对迷宫环境已足够熟悉,但噪声和灯光刺激依然可以使小鼠积极寻找目标孔。当然,可重复次数的阈值目前尚不清楚。
Koopmans等对巴恩斯迷宫实验训练阶段小鼠到达目标孔的潜伏期进行了重复数据的分析[36,37]。不同于本次实验,他们采用的是实验设计中训练阶段的重复数据进行分析;而本次实验是在完成了一次完整的测试之后,又经历了短期训练,随后才进行下一次测试,并且是利用每次测试期的结果来进行分析的。Koopmans等发现训练阶段的重复测试会对小鼠到达目标孔的潜伏期产生影响,随着训练的推进,小鼠到达目标孔的潜伏期变短,能更快找到目标孔。而在完成完整测试后,以测试阶段的重复数据进行分析,其结果并无差异,说明小鼠在经过完整的适应、训练、测试阶段后,到达目标孔的潜伏期达到稳定状态,对目标孔的空间记忆已然完成。当然,更换目标孔的位置后能否重新建立小鼠对目标孔的记忆以及这个记忆是否受到先前实验的影响仍需进一步研究。
此外,不同于其他3个时间点,t2时间点实验组3和对照组到达目标孔的潜伏期表现出了差异,原因可能是,实验组3小鼠到达目标孔的潜伏期一致且稳定,甚至随着重复测试的进行,能越来越快地找到目标孔;而对照组到达目标孔的潜伏期长且波动较大。不管怎样,在4次测试中实验组3小鼠到达目标孔的潜伏期均短于对照组,差异趋势始终是一致的。
综上所述,重复测试会干扰3xTg-AD小鼠在旷场实验中焦虑状态的评价以及在新物体识别实验中对新物体的偏好,但对其在巴恩斯迷宫实验中到达目标孔的潜伏期无明显影响。因此,采用旷场实验评价小鼠焦虑状态时应避免重复测试;不更换新旧物体的前提下,对同一对象开展新物体识别实验的重复测试也不可取;用小鼠到达目标孔的潜伏期评价小鼠对目标孔的空间记忆时,巴恩斯迷宫实验在短期内可以进行一定的重复,其重复数据对小鼠空间学习和记忆能力的评价效果与初次测试结果无显著差异。
参考文献
[1] Kishi T, Kobayashi K, Sasagawa K, et al. Automated analysis of a novel object recognition test in mice using image processing and machine learning[J]. Behav Brain Res, 2025, 476: 115278.
[2] 任多多, 向晨瑶, 赵永康, 等. 元宝枫籽油对阿尔茨海默病模型小鼠的神经保护作用及机制研究[J]. 阿尔茨海默病及相关病杂志, 2025, 8(1): 36-46.
[3] Schulz M, Zieglowski L, Kopaczka M, et al. The open field test as a tool for behaviour analysis in pigs: Recommendations for set-up standardization-A systematic review[J]. Eur Surg Res, 2023, 64(1): 7-26.
[4] Horka P, Langova V, Hubeny J, et al. Open field test for the assessment of anxiety-like behavior in gnathonemus petersii fish[J]. Front Behav Neurosci, 2024, 17: 1280608.
[5] 宋玉, 曾志安, 刘果, 等. 一种牛乳酪蛋白肽粉复合物对睡眠的改善作用[J]. 现代食品科技, 2024, 40(11): 12-20.
[6] 张认真, 叶钰娟, 魏玉婷, 等. 肝郁气滞型失眠实验动物模型复制方法及评价概述[J]. 中医杂志, 2024, 65(14): 1496-1503.
[7] 朱秋轶, 刘果, 龙明芳, 等. 羊乳酪蛋白酶解物的改善睡眠作用[J]. 现代食品科技, 2023, 39(11): 11-17.
[8] Sakai O, Yokohata D, Hotta T. Boldness affects novel object recognition in a gecko species[J]. Behav Process, 2024, 220: 105072.
[9] Golden RK, Dilger RN. Determining underlying influences of data variability in the novel object recognition paradigm as used with young pigs[J]. Front Behav Neurosci, 2024, 18: 1434489.
[10] Rodríguez Peris L, Scheuber MI, Shan H, et al. Barnes maze test for spatial memory: A new, sensitive scoring system for mouse search strategies[J]. Behav Brain Res, 2024, 458: 114730.
[11] Tachiki Y, Suzuki Y 2nd, Kurahashi M, et al. Scale space calibrates present and subsequent spatial learning in Barnes maze in mice[J]. eNeuro, 2023, 10(6): ENEURO.0505-22.2023.
[12] Illouz T, Ascher LAB, Madar R, et al. Unbiased analysis of spatial learning strategies in a modified Barnes maze using convolutional neural networks[J]. Sci Rep, 2024, 14: 15944.
[13] Laczó M, Martinkovic L, Lerch O, et al. Different profiles of spatial navigation deficits in Alzheimer’s disease biomarker-Positive versus biomarker-negative older adults with amnestic mild cognitive impairment[J]. Front Aging Neurosci, 2022, 14: 886778.
[14] Plácido J, de Almeida CAB, Ferreira JV, et al. Spatial navigation in older adults with mild cognitive impairment and dementia: A systematic review and meta-analysis[J]. Exp Gerontol, 2022, 165: 111852.
[15] Diomede L, Conz A, Mosconi M, et al. The AβA2V paradigm: From molecular insights to therapeutic strategies in Alzheimer’s disease and primary tauopathies[J]. Pharmacol Res, 2025, 211: 107563.
[16] Zhao G, Zhang H, Xu Y, et al. Research on magnetic resonance imaging in diagnosis of Alzheimer’s disease[J]. Eur J Med Res, 2024, 29(1): 632.
[17] 王刚, 齐金蕾, 刘馨雅, 等. 中国阿尔茨海默病报告2024[J]. 诊断学理论与实践, 2024, 23(3): 219-256.
[18] 首都医科大学宣武医院国家神经疾病医学中心, 中国疾病预防控制中心慢性非传染性疾病预防控制中心, 国家卫生健康委能力建设和继续教育中心, 等. 中国阿尔茨海默病蓝皮书(精简版)[J]. 中华医学杂志, 2024, 104(29):2701-2727.
[19] Liu Y, Wu Y, Chen Y, et al. Projection for dementia burden in China to 2050: a macro-simulation study by scenarios of dementia incidence trends[J]. Lancet Reg Health West Pac, 2024, 50: 101158.
[20] Carvalho D, Diaz-Amarilla P, Smith MR, et al. Untargeted metabolomics of 3xTg-AD neurotoxic astrocytes[J]. J Proteomics, 2025, 310: 105336.
[21] Barber AJ, Del Genio CL, Swain AB, et al. Age, sex and Alzheimer’s disease: A longitudinal study of 3xTg-AD mice reveals sex-specific disease trajectories and inflammatory responses mirrored in postmortem brains from Alzheimer’s patients[J]. Alzheimers Res Ther, 2024, 16(1): 134.
[22] Jiao JJ, Hu Y, Cui YJ, et al. Anisomycin alleviates cognitive impairments and pathological features in 3xTg-AD mice[J]. Neuropharmacology, 2024, 261: 110159.
[23] Naeem A, Waseem A, Khan MA, et al. Therapeutic potential of MCC950 in restoring autophagy and cognitive function in STZ-induced rat model of Alzheimer’s disease[J]. Mol Neurobiol, 2025, 62(5): 6041-6058.
[24] Feng Y, Yu X, Han J. Quercetin regulates the polarization of microglia through the NRF2/HO1 pathway and mitigates Alzheimer’s disease[J]. Actas Esp Psiquiatr, 2024, 52(6): 786-799.
[25] Yuan L, Song G, Xu W, et al. Diethyl butylmalonate attenuates cognitive deficits and depression in 5 × FAD mice[J]. Front Neurosci, 2024, 18: 1480000.
[26] Heo JJ, Han YE, Kim MS, et al. Suffruticosol B from Paeonia lactiflora ameliorates Alzheimer’s disease pathology by inhibiting MAO-B activity[J]. Phytother Res, 2025, 39(2): 593-603.
[27] Menashe N, Salama Y, Steinauer ML, et al. Do behavioral test scores represent repeatable phenotypes of female mice?[J]. J Pharmacol Toxicol Methods, 2022, 115: 107170.
[28] You R, Liu Y, Chang RC. A behavioral test battery for the repeated assessment of motor skills, mood, and cognition in mice[J]. J Vis Exp, 2019(145): (145).
[29] 陈超杰, 钟志凤, 俞昌喜. 重复测试和不同性别对小鼠旷场行为的影响[J]. 海峡药学, 2014, 26(7): 49-51.
[30] Choleris E, Thomas AW, Kavaliers M, et al. A detailed ethological analysis of the mouse open field test: Effects of diazepam, chlordiazepoxide and an extremely low frequency pulsed magnetic field[J]. Neurosci Biobehav Rev, 2001, 25(3): 235-260.
[31] Sturman O, Germain PL, Bohacek J. Exploratory rearing: A context- and stress-sensitive behavior recorded in the open-field test[J]. Stress, 2018, 21(5): 443-452.
[32] 李盛建, 黄竹燕, 叶夷露, 等. 物体材质与检测间隔时间对小鼠新物体识别实验结果的影响[J]. 浙江大学学报(医学版), 2014, 43(3): 346-352.
[33] Hayashi Y, Alamir N, Sun G, et al. An effective textured Novel Object Recognition Test (tNORT) for repeated measure of whisker sensitivity of rodents[J]. Behav Brain Res, 2024, 472: 115153.
[34] Fleury S, Kolaric R, Espera J, et al. Role of dopamine neurons in familiarity[J]. Eur J Neurosci, 2024, 59(10): 2522-2534.
[35] Gunaydin LA, Grosenick L, Finkelstein JC, et al. Natural neural projection dynamics underlying social behavior[J]. Cell, 2014, 157(7): 1535-1551.
[36] Fierros-Campuzano J, Ballesteros-Zebadúa P, Manjarrez-Marmolejo J, et al. Irreversible hippocampal changes induced by high fructose diet in rats[J]. Nutr Neurosci, 2022, 25(6): 1325-1337.
[37] Koopmans G, Blokland A, van Nieuwenhuijzen P, et al. Assessment of spatial learning abilities of mice in a new circular maze[J]. Physiol Behav, 2003, 79(4-5): 683-693.
引证本文
黎小月 , 王彩贤 , 尹湧华 , 陈金慧 , 赵韩 , 林方昭 , 曹海军. 短期内行为学重复测定对3xTg-AD小鼠认知及焦虑状态评估效果的影响[J]. 中风与神经疾病杂志, 2025, 42(8): 727-735.


