Cancer Discovery | 夏铮团队开发单细胞生存分析新工具scSurvival,可精准预测患者结局并识别相关风险细胞亚群
时间:2026-05-05 17:16:09 热度:37.1℃ 作者:网络
生存分析是临床肿瘤学研究的核心方法,可用于评估总生存期(OS)、无进展生存期(PFS)等。传统批量RNA测序(RNA-seq)利用生存分析建模基因表达、构建多基因风险评分,可将患者分层以进行预后及治疗反应评估;单细胞RNA测序(scRNA-seq)则提供了前所未有的分辨率,能够解析肿瘤微环境的细胞异质性,结合大规模癌症队列临床生存数据,为揭示不同细胞亚群对肿瘤进展及患者预后的影响提供了新方向。
但当前单细胞生存分析存在明显局限,早期研究通过整合单细胞和批量数据筛选预后相关细胞亚群,未能充分利用单细胞数据真实生存信息;现有适配单细胞的生存分析两种策略如伪批量整合、细胞占比分析,易丢失细胞亚群关键信息。此外,但目前尚无有效方法可基于单细胞数据直接构建生存结局模型。
近日,美国俄勒冈健康与科学大学夏铮团队及其合作者开发了一种基于注意力机制的多实例Cox回归框架scSurvival,其将每个肿瘤样本建模为细胞的集合,能够同时在患者和单细胞水平预测生存结局。针对单细胞数据高维度、稀疏性及批次效应等问题,scSurvival整合了基于变分自编码器(VAE)的特征提取模块与生成式建模,以提升特征稳定性与跨批次泛化能力。模拟实验及黑色素瘤、肝癌真实队列证实,该框架具备优异分析性能和可拓展性,不仅能精准预测患者预后,还能识别影响生存的关键细胞亚群。总之,scSurvival能够稳健预测患者生存状态,同时解析生存相关细胞亚群,为癌症领域单细胞生存分析技术提供了有力工具。相关内容以”“scSurvival: Single-Cell Survival Analysis of Clinical Cancer Cohort Data at Cellular Resolution为题发表在Cancer Discovery。

scSurvival的核心原理是将每个患者的单细胞数据压缩为低维特征,再通过注意力权重聚合为患者水平的表示,随后利用Cox回归分析在患者层面构建生存模型。该框架包含两大模块:一是基于VAE特征提取模块,可处理数据稀疏、高维与批次效应等问题,完成跨批次单细胞特征提取;二是基于多头注意力的多实例Cox回归(AMICR)模块,将单细胞特征聚合为患者水平表征,结合风险评分器完成风险评估与回归分析建模,还可纳入临床协变量以提升模型准确度。此外,模型采用多组分损失函数与双阶段训练策略,保障特征提取稳定性与生存回归拟合效果。
scSurvival不仅输出细胞风险调整评分(hazard_adj)和患者水平风险评分,还能揭示肿瘤内部细胞水平的风险异质性,支持后续下游分析与新增患者的预后风险预测。
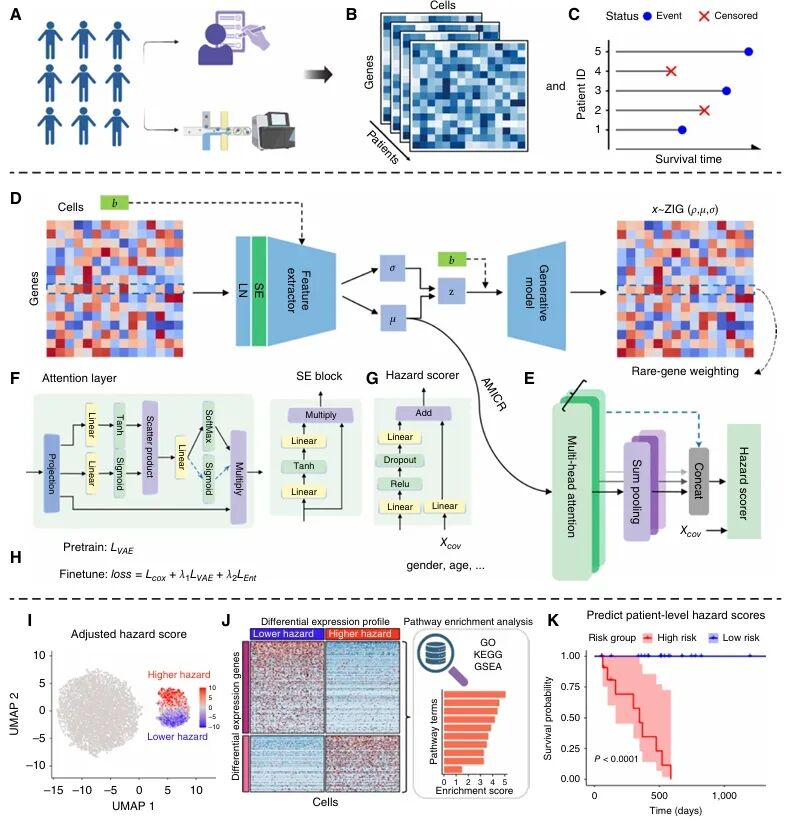
图1. scSurvival概述
为系统评估scSurvival性能,研究团队构建了多组模拟数据集。基础模拟(Sim.0)显示,scSurvival可精准识别真实风险驱动细胞亚群,准确率达98.7%,F1评分为0.989;患者水平五折交叉验证显示,该框架预测的风险分数显著区分了具有不同生存结局的患者,平均一致性指数(C-index)达0.942。双批次模拟显示,scSurvival有效校正了批次差异。
研究团队进一步设计了六种复杂场景(Sim.1–Sim.6)。在大多数场景下,scSurvival能识别真实风险驱动细胞亚群,平均F1评分通常高于0.8,患者水平C-index高于0.8;在最具挑战性的场景中,其能精准识别稀有及嵌套分布的风险细胞,维持稳定的预后预测效能。基准对比表明,相较于PCA、HVG2000、NMF及传统Cox生存分析方法,scSurvival在特征提取、细胞亚群识别与患者风险预测上优势显著,在保留单细胞分辨率的同时,兼具优异的分析性能与泛化能力。
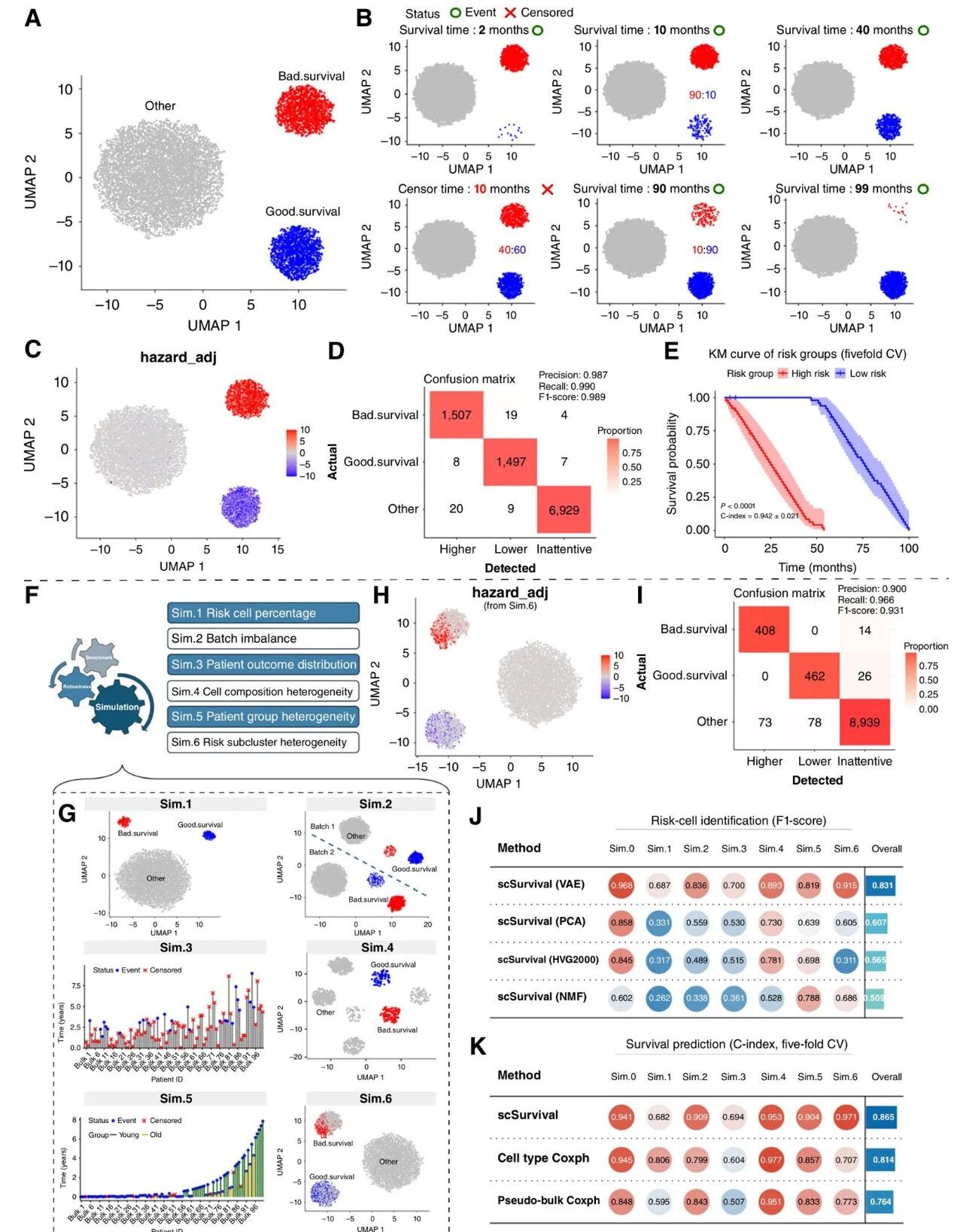
图2. scSurvival在模拟数据集上的性能评估
大规模癌症单细胞队列分析算力需求高,借助高性能GPU加速运算,scSurvival具备优异的可扩展性。在固定100名患者的情况下,分析100万个细胞约需17.5分钟,内存/显存消耗约30GB/50GB,scSurvival运行时间和内存使用与细胞数量呈线性增长;在固定10万个细胞情况下,分析500名患者约33分钟,内存/显存约3 GB/6 GB,运行时间同样线性增长,而内存使用几乎保持不变。
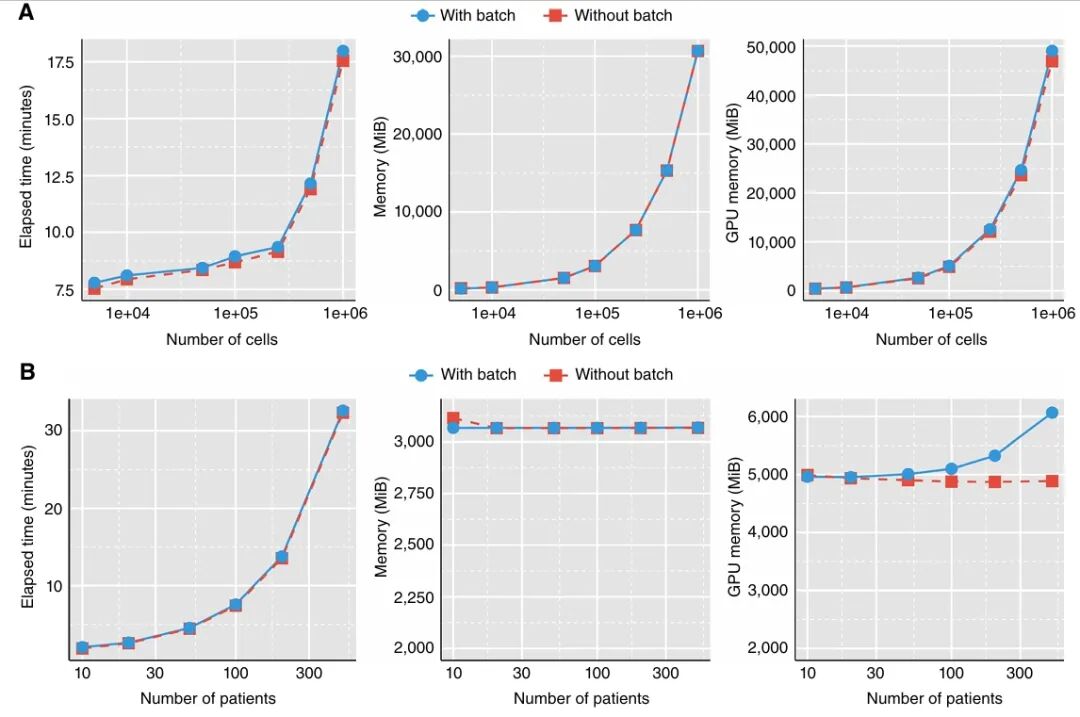
图 3. scSurvival运行效率
为开展真实场景验证,研究团队将scSurvival应用于一个接受免疫治疗的黑色素瘤队列数据集中,包含32例患者的48份样本,共计16,291个已注释免疫细胞。结果显示,B细胞和浆细胞整体呈现低风险评分,这与三级淋巴结构的形成相关;单核细胞/巨噬细胞呈现明显的风险双峰分布,高风险亚群高表达 SPP1,低表达CXCL9,富集中性粒细胞迁移、趋化和脂质代谢通路,呈现典型M2促肿瘤特征;低风险亚群高表达CXCL9,低表达SPP1,富集淋巴细胞分化、II型干扰素应答和抗原呈递通路,符合M1抗肿瘤特征。
此外,scSurvival还能解析患者内部细胞风险异质性,其界定的关键细胞风险评分与治疗应答高度相关:应答组风险评分更低,低风险细胞占比更高。单变量Cox分析证实,scSurvival预测的风险评分与OS显著相关,预测效能优于传统方法。
进一步,研究团队从上述黑色素瘤数据集中分离出T细胞,使用scSurvival进行单独分析。结果显示,细胞毒性T细胞、耗竭性CD8+ T细胞和调节性T细胞与较长生存期相关,而记忆T细胞与较短生存期相关。低风险T细胞上调TCF7、CCR7等干性记忆相关基因,与良好免疫治疗反应相关;高风险T细胞上调TIM-3、LAG3等多种免疫抑制性受体和热休克应激基因,富集耗竭及功能障碍通路,与不良预后相关。基于T细胞构建的模型评分可有效区分免疫治疗应答与无应答患者。此外,多套独立外部队列验证证实,scSurvival能够跨数据集稳定预测患者生存结局,风险评分具有独立预后意义。
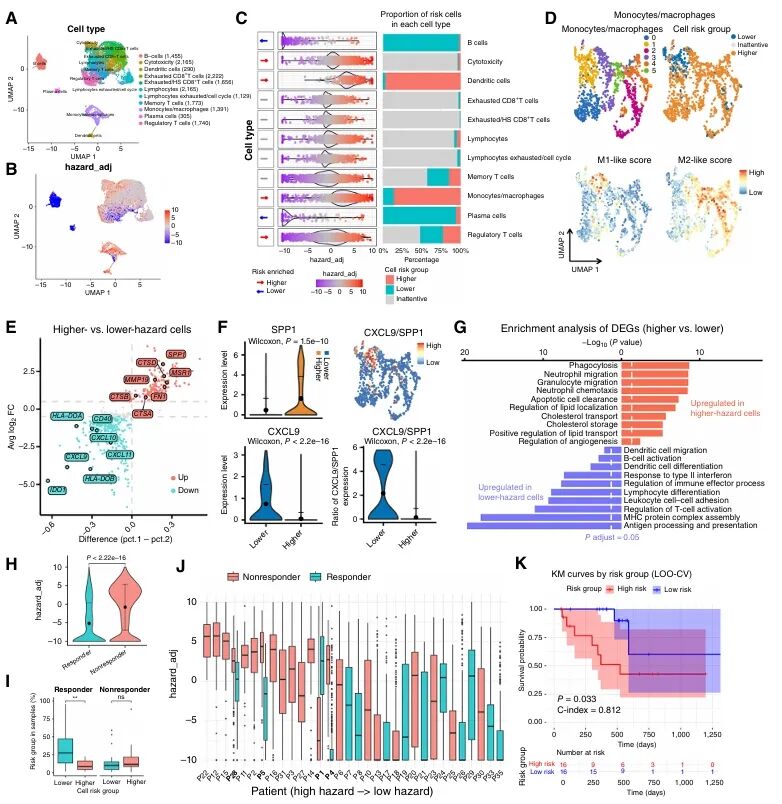
图4. 黑色素瘤队列的scSurvival分析
研究团队将scSurvival应用于包含189个样本、124名患者、总计1,092,172个细胞的肝癌单细胞图谱,计算了所有细胞的细胞水平风险分数。结果显示,肿瘤上皮细胞存在显著预后异质性,约三分之一为高风险,其余均为低风险。高风险细胞高表达缺氧(HIF1A)、干性(PSCA)、上皮间质转化(EMT)相关基因,富集EMT、TGFβ等信号通路;低风险细胞则高表达肝脏代谢基因ARG1和ALDOB,富集代谢相关通路。
基于高低风险肿瘤细胞的差异基因,研究团队构建了肝癌单细胞不良生存特征(scLCSS),该特征在四个独立批量肝癌队列中能显著区分肿瘤与正常组织,并随病理分期进展而升高,且scLCSS高表达患者的OS、PFS均显著劣于低表达患者。患者水平的五折交叉验证显示,scSurvival预测风险评分的平均C-index为0.719,优于基于细胞类型比例等的基准模型。
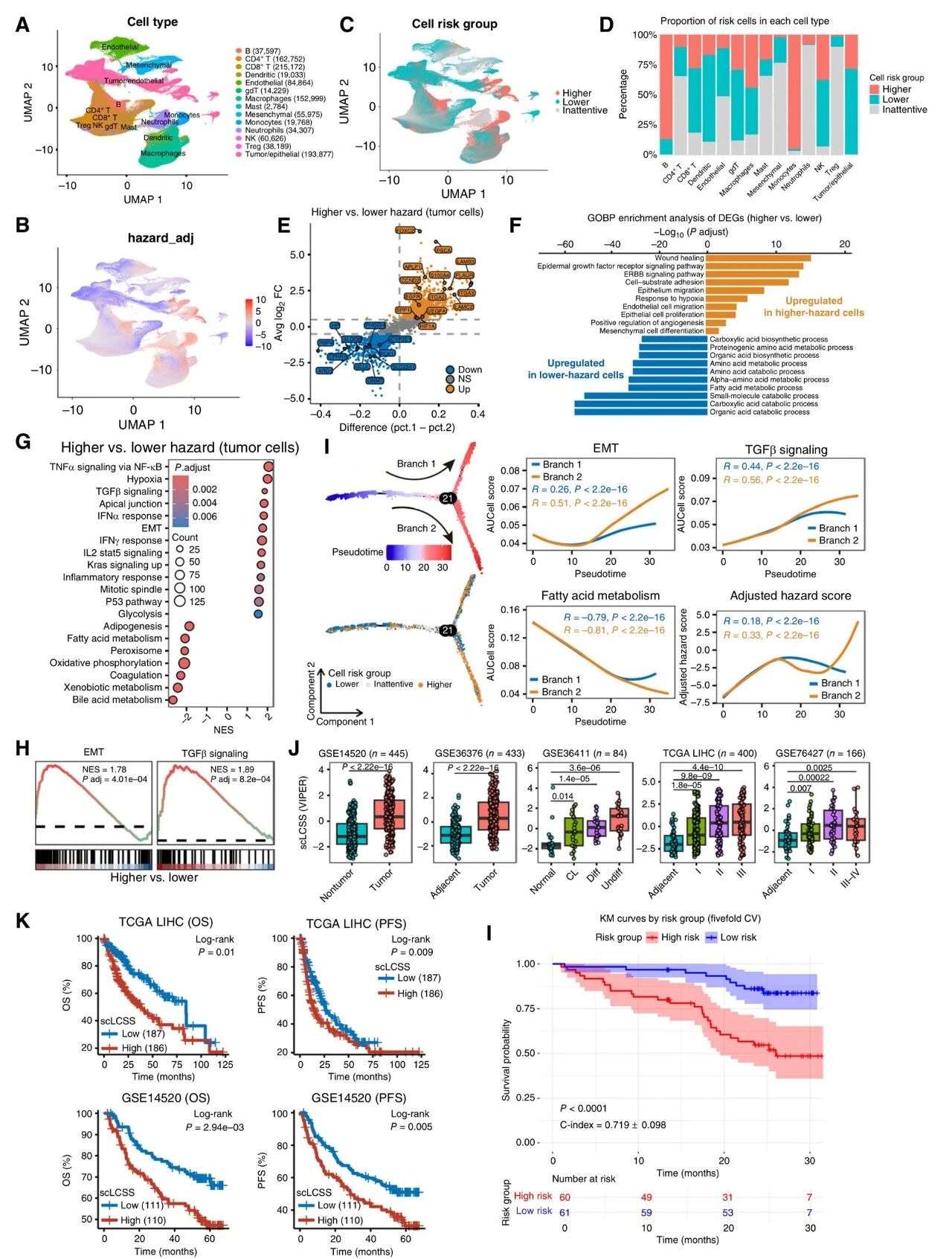
图5. 肝癌单细胞样本集的scSurvival分析
综上所述,scSurvival首次实现了直接从肿瘤单细胞数据进行细胞分辨率生存建模,最大程度保留了细胞异质性信息。该工具不仅能精准预测患者生存结局、构建高鲁棒性预后模型,还能系统性挖掘与预后相关的关键细胞亚群,解析肿瘤微环境中细胞状态与临床结局的关联机制。scSurvival不仅填补了临床肿瘤学中单细胞生存分析的工具空白,还推动了队列级单细胞分析在癌症研究中的广泛应用,加速肿瘤转化研究与临床实践的深度融合。
参考文献:
https://aacrjournals.org/cancerdiscovery/article/doi/10.1158/2159-8290.CD-25-0965/782647/scSurvival-Single-Cell-Survival-Analysis-of


