最新Nature子刊:高通量单囊泡成像平台——无需分离,直接分析人血浆细胞外囊泡,助力液体活检
时间:2026-05-05 17:16:14 热度:37.1℃ 作者:网络
背景介绍
细胞外囊泡(EVs)是细胞分泌的纳米级囊泡,携带来自母细胞的多种生物分子,在细胞间通讯中发挥关键作用,也是极具潜力的液体活检生物标志物。然而,EVs固有的高度异质性(即使同一细胞系分泌的EVs也包含多个分子和物理特征各异的亚群)给精准表征带来了巨大挑战。传统的EV分析方法多为批量测量,需要裂解EVs,破坏囊泡结构,并通过平均化掩盖了不同EV亚群之间的差异。近年来发展的单EV成像技术(如ExoView、超分辨显微镜)虽能解析单颗粒水平的异质性,但普遍存在通量低、依赖专用芯片/仪器、且通常需要先进行超速离心或尺寸排阻色谱等繁琐的EV分离步骤,限制了其在大规模临床样本分析中的应用。
研究思路
针对上述技术瓶颈,哈佛医学院布莱根妇女医院David R. Walt教授团队开发了一种高通量单EV成像平台,可直接从未经处理的人血浆样本中对单个EV进行蛋白表达分析。该平台的核心技术包括:(1)优化的一步法PEG-硅烷玻璃表面功能化策略,兼容96孔板和18腔室玻片等标准高通量格式,有效抑制非特异性吸附;(2)利用同一抗体(如抗CD9)同时作为捕获和检测抗体的“单抗策略”——由于单个EV表面表达多个CD9拷贝,可被同一抗体同时捕获和检测,而可溶性CD9蛋白无法同时结合两个相同抗体,从而实现EV特异性检测;(3)与液体处理机器人和电动显微镜集成,实现全自动化操作(96个样本约2小时完成,49个视野/孔<1小时成像);(4)基于Python和ImageJ的自动化图像分析流程。研究系统验证了该平台的检测灵敏度(LOD 2.8×10⁴颗粒/mL)、动态范围(约4个数量级)、捕获效率(60-80%)和重现性(板内CV<4%)。应用该平台分析了191例人血浆样本(96例正常、27例早期乳腺癌、46例晚期乳腺癌),发现晚期乳腺癌患者血浆中CD9⁺ EV水平显著升高(AUC=0.86),而CD81⁺ EV无显著变化。相关内容以“High-throughput single-vesicle imaging platform for direct extracellular vesicle profiling of human plasma”发表在《Nature Communications》!

图片解析
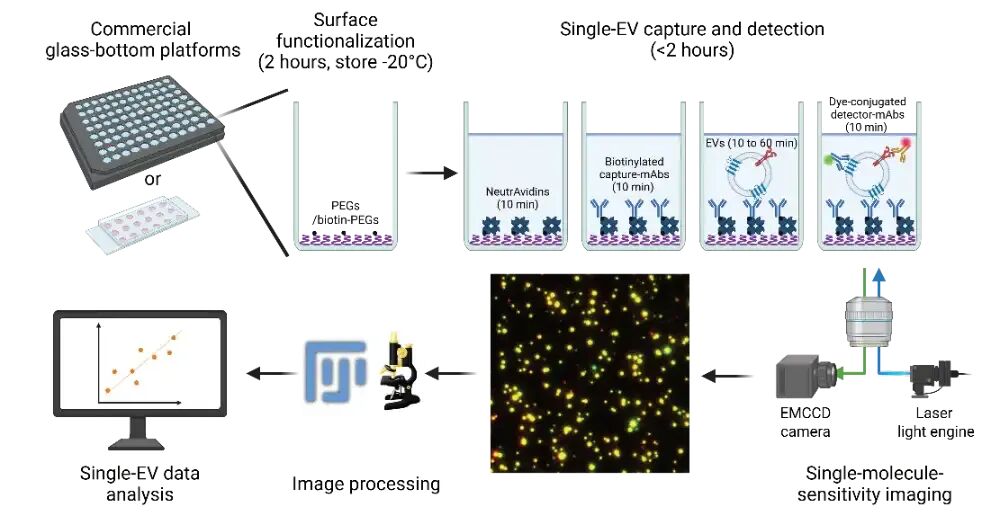
图1. 高通量单EV成像平台工作流程示意图:96孔玻璃底板或18腔室玻片经PEG功能化后,通过NeutrAvidin固定生物素化捕获抗体,直接加入稀释的血浆样本(无需EV预分离),孵育后加入荧光标记检测抗体,用配备EMCCD的荧光显微镜成像,通过ImageJ/Python自动提取单EV荧光信号。
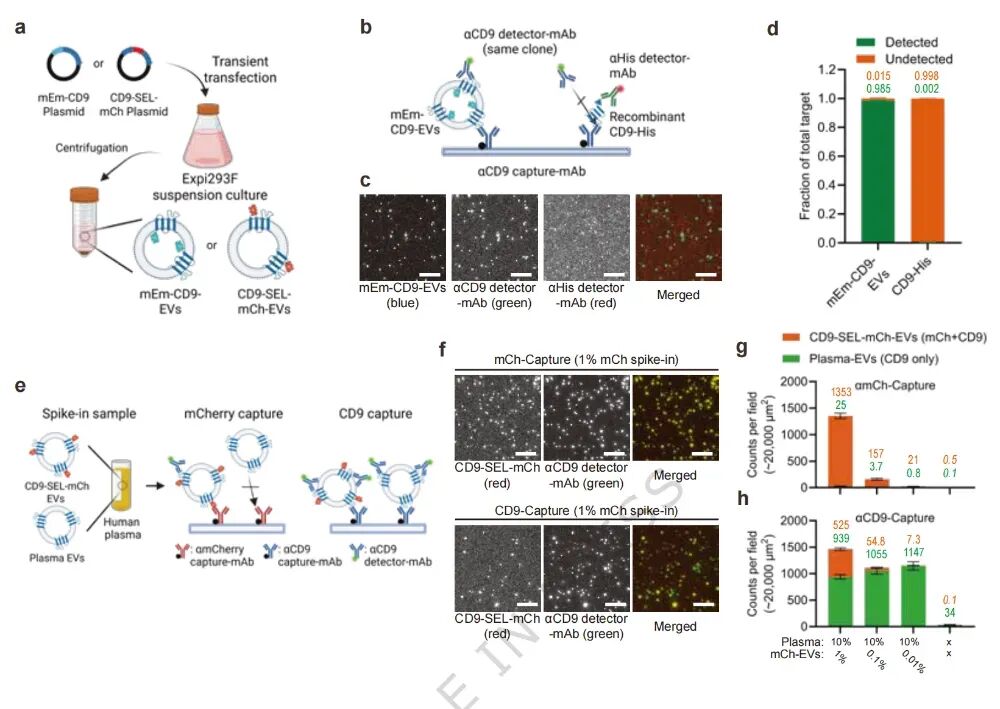
图2. 表面功能化优化与EV特异性检测验证:(a) 重组EV示意图(mEmerald-CD9-EVs和CD9-SEL-mCherry-EVs)。(b) 单抗策略示意图:同一抗CD9抗体同时用于捕获和检测,只有表面表达多个CD9拷贝的EV才能被检测到。(c-d) 混合物中mEm-CD9-EVs(蓝色)与可溶性CD9-His蛋白(红色)的检测:~99%的mEm-CD9-EVs被抗CD9检测抗体(绿色)检测到,而可溶性CD9-His几乎不被检测(<0.2%共定位)。(e) 血浆中掺入CD9-SEL-mCherry-EVs的特异性检测示意图。(f-h) 抗mCherry捕获表面(上)和抗CD9捕获表面(下)的成像与定量:抗mCherry表面特异性捕获掺入的mCherry⁺ EVs(黄色),血浆内源性CD9⁺ EVs仅显示绿色;抗CD9表面同时捕获两种EV。检测到的mCherry⁺ EV与血浆EV的比例与实际掺入比例高度一致(1%掺入时比值为56%,0.1%时为5.2%)。
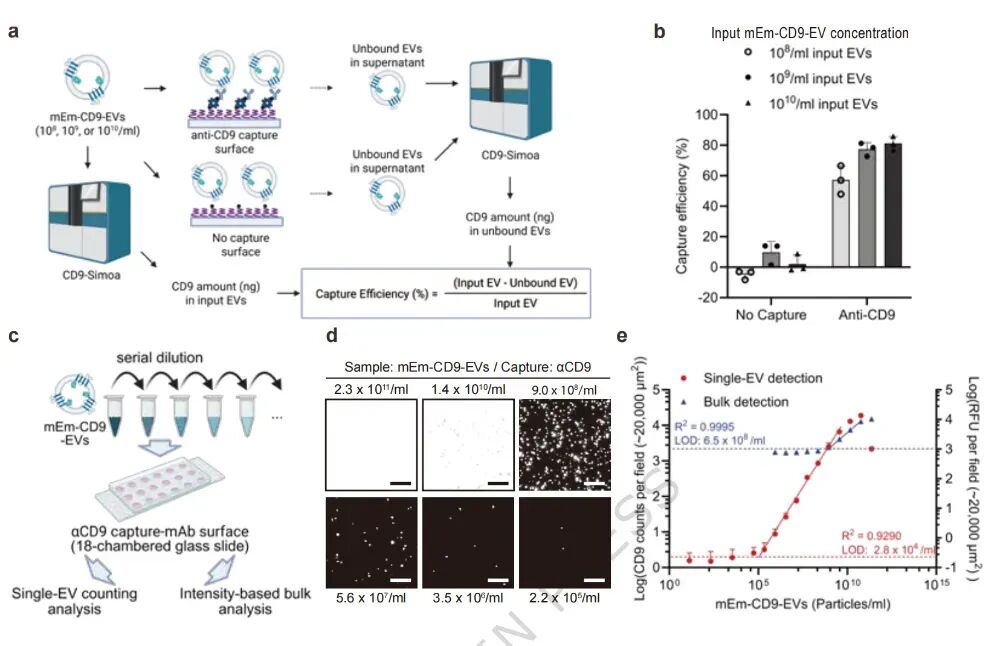
图3. 捕获效率与检测灵敏度表征:(a) 利用Simoa(单分子阵列)评估EV捕获效率的工作流程。(b) 抗CD9表面在10⁸-10¹⁰颗粒/mL输入范围内,扣除非特异性损失后捕获效率为60-80%。(c) 检测灵敏度与动态范围评估流程:mEm-CD9-EVs(2.3×10¹¹颗粒/mL)进行17次4倍梯度稀释。(d-e) 单EV计数(红色)与批量荧光强度(蓝色)对比:单EV计数动态范围约4个数量级(2.2×10⁵-3.6×10⁹颗粒/mL),LOD为2.8×10⁴颗粒/mL;批量测量动态范围<2个数量级,LOD为6.5×10⁸颗粒/mL(高约10,000倍)。
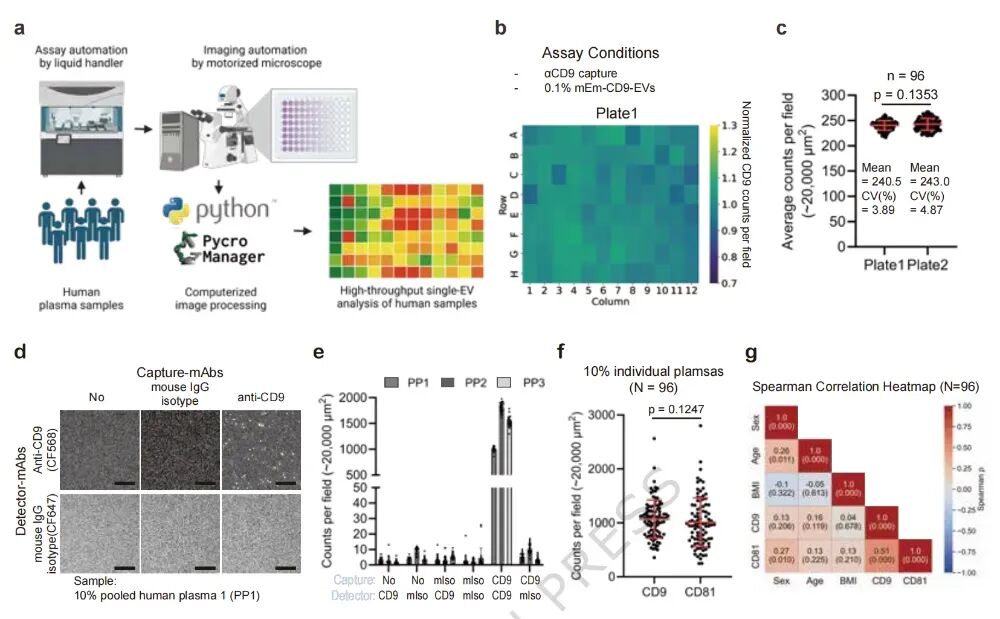
图4. 自动化工作流程重现性与正常人血浆基线分析:(a) 自动化工作流程集成Tecan液体处理机器人、HydroSpeed洗板机、BioShake摇床和Nikon Ti2E电动显微镜。(b-c) 96孔板内mEm-CD9-EVs检测:板内CV为3.89%,板间无显著差异(p=0.1353)。(d-e) 正常人血浆中CD9⁺ EV和CD81⁺ EV检测:无捕获抗体或同型对照表面有效抑制非特异性结合,抗CD9/CD81表面检测到明显信号。(f) 96例正常人血浆CD9⁺ EV(平均~1,070 counts/field)和CD81⁺ EV(~1,011 counts/field)计数,CV分别为34.5%和49.3%。(g) Spearman相关性热图:CD9⁺与CD81⁺ EV计数呈中等正相关(ρ=0.56,p<0.001),与年龄、性别、BMI无显著关联。
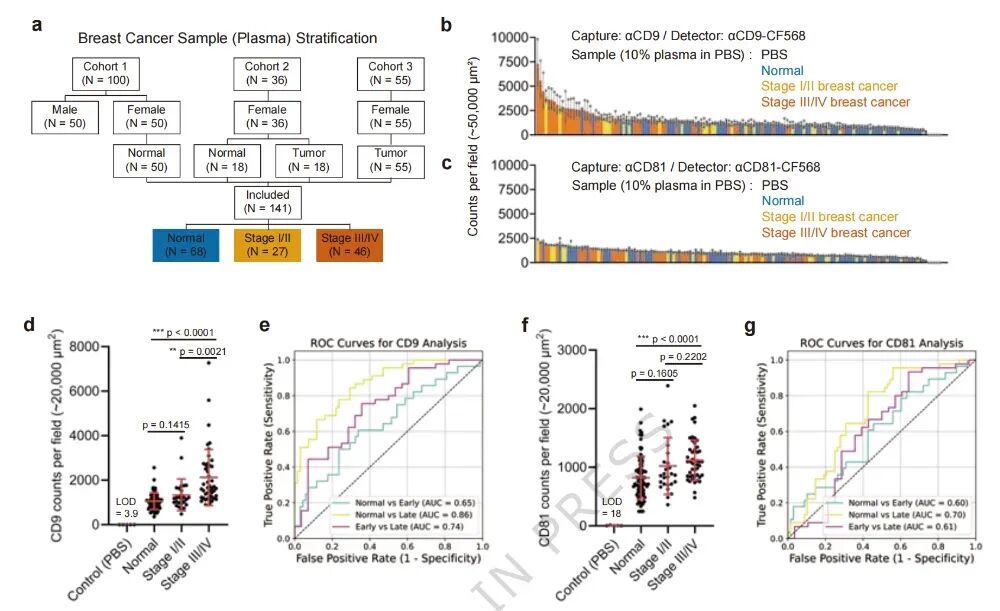
图5. 乳腺癌患者血浆EV水平分析:(a) 样本队列:68例正常、27例早期(I/II期)、46例晚期(III/IV期)乳腺癌血浆。(b-c) CD9⁺ EV(b)和CD81⁺ EV(c)计数排序:晚期乳腺癌CD9⁺ EV显著升高,CD81⁺ EV无明显变化。(d) Kruskal-Wallis检验显示CD9⁺ EV在三组间差异显著(p<0.001),Dunn事后检验显示晚期显著高于正常(adj. p<0.001)和早期(adj. p=0.002)。(e) ROC曲线分析:正常vs晚期的AUC为0.86(区分能力强),早期vs晚期为0.74,正常vs早期为0.65。(f-g) CD81⁺ EV虽在正常vs晚期有统计学差异(adj. p<0.001),但AUC仅0.70,区分能力显著低于CD9⁺ EV。
结论
本研究成功开发了一种高通量单EV成像平台,通过优化的PEG表面功能化和单抗检测策略,实现了直接从微量(10 μL)未处理血浆样本中对单个EV进行高灵敏度、高特异性、高重现性的蛋白表达分析。该平台与现有实验室自动化技术兼容,可在约2小时内完成96个样本的全自动处理,板内CV<4%,检测灵敏度达2.8×10⁴颗粒/mL,动态范围约4个数量级。应用该平台分析191例血浆样本,首次在大规模队列中证实晚期乳腺癌患者血浆CD9⁺ EV水平显著升高(AUC=0.86),而CD81⁺ EV无明显变化,且与年龄、性别、BMI等人口学因素无关。该平台解决了现有单EV技术通量低、依赖EV预分离的核心瓶颈,为基于EV的大规模临床生物标志物发现和转化研究提供了强有力的工具。
原文链接:
https://doi.org/10.1038/s41467-026-72179-0


