非霍奇金淋巴瘤中基于MRD指导的治疗:现状与未来
时间:2026-05-06 19:10:50 热度:37.1℃ 作者:网络
传统的影像学检查(包括PET)仍是非霍奇金淋巴瘤(NHL)反应评估的核心,但缺乏检测分子水平疾病的分析灵敏度。微小残留病(MRD)评估能够为B细胞NHL的各亚型提供高度肿瘤特异性和定量的治疗反应测量,特别是通过循环肿瘤DNA(ctDNA)。超灵敏的ctDNA能够检测到频率低至百万分之一的变异,并能在治疗过程中更精确地量化肿瘤负荷。例如在大B细胞淋巴瘤中,ctDNA动力学在一线治疗后预测临床结局方面比PET更准确,并且对靶向药物和CAR-T细胞治疗仍具有预后价值。在套细胞淋巴瘤中,诱导治疗后检测不到MRD可以识别出可以安全省略高剂量化疗巩固的患者。
目前涵盖NHL各亚型的前瞻性临床试验已经常规将MRD评估纳入其中,以评估其在临床决策(包括治疗时机和方案选择)中的实用性。但在NHL中广泛采用MRD的也存在障碍,包括缺乏标准化的样本采集和分析方法、检测的可及性,以及治疗仅分子水平疾病能改善结局的确切证据。正在进行的临床试验正在解决这一信息空白,并将指导如何将MRD整合到常规临床实践中。
《Seminars in Hematology》近日发表综述,阐述了非霍奇金淋巴瘤中基于MRD指导的治疗的现状与未来方向。

引言
B细胞非霍奇金淋巴瘤(NHL)涵盖广泛的临床谱系,从侵袭性亚型如大B细胞淋巴瘤(LBCL),这类肿瘤生长迅速但通常可治愈,到惰性类型如滤泡性淋巴瘤(FL),这类肿瘤进展缓慢但很少能治愈,因此它们的治疗目标也有所不同。侵袭性淋巴瘤患者通常接受旨在治愈的一线化学免疫治疗,而惰性淋巴瘤患者则接受诱导治疗,随后进行巩固和/或维持治疗以延长缓解期。NHL反应评估标准依赖于使用Deauville评分解读的¹⁸F-氟脱氧葡萄糖正电子发射断层扫描(PET),1至3分表示完全缓解,而4或5分提示存在残留淋巴瘤。然而PET的准确性有限。在LBCL中,PET在中期评估时早期检测复发的阳性预测值范围为30%至70%,在治疗结束时降至50%以下;阴性预测值较高,但仍有15%至20%的PET阴性患者会复发。这种不精确性可能是导致PET指导的治疗方法失败的原因之一。在惰性淋巴瘤中,定义PET的预测值本身就有局限性,因为无论PET反应如何,大多数患者最终都会复发。即便如此,PET也常常无法检测到具有临床意义的残留病变。在FL中,诱导治疗后达到PET阴性完全缓解的患者仍然能从利妥昔单抗维持治疗中获益,表明存在低于PET检测阈值的持续性疾病。
微小残留病(MRD)代表着在治疗期间和治疗后持续存在、但对影像学不可见的小群恶性肿瘤细胞。高度灵敏的分子检测方法现在能够对其进行量化,提供了超越单纯影像学的分辨率。因此,MRD提供了最精确的可用疾病负荷测量指标,可检测到MRD通常预示着NHL各亚型的复发和不良结局。NHL 的早期 MRD 研究采用基于聚合酶链反应 (PCR) 的循环肿瘤细胞检测(细胞MRD),靶向复发性易位,例如套细胞淋巴瘤 (MCL) 的免疫球蛋白重链 (IGH)-细胞周期蛋白D1(IGH–CCND1) 和 FL 的 IGH B 细胞淋巴瘤 2(IGH-BCL2)。MRD检测将疾病检测的范围扩展到了影像学之外,但灵敏度和适用范围有限,因为许多NHL亚型缺乏复发性易位或循环细胞。
随着能够检测循环肿瘤DNA(ctDNA)的方法的出现,振兴了淋巴瘤中的MRD评估。ctDNA由肿瘤细胞在增殖、凋亡和坏死过程中释放到外周血中的DNA片段组成。这些片段包含高度肿瘤特异性的信息,包括免疫球蛋白受体序列、单核苷酸变异、插入/缺失、拷贝数异常和染色体易位,这些信息可以通过高度复杂的二代测序(NGS)平台在大多数NHL患者中捕获(游离MRD)。ctDNA分析的不同方面为肿瘤生物学提供了互补的见解。定量ctDNA水平与PET衍生的肿瘤负荷相关,可以追踪MRD动力学,并预测LBCL、MCL和FL的结局。与此同时,ctDNA的基因组分析作为一种非侵入性的“液体活检”,显示出与组织基因分型的高度一致性,并提高了对空间异质性的检测能力。
淋巴瘤中最初的ctDNA平台侧重于使用NGS检测和连续追踪克隆性免疫球蛋白V(D)重排。这种免疫球蛋白基因NGS(IgNGS)方法具有高度肿瘤特异性,但其分析灵敏度受到血液样本中可用于扩增的投入DNA量的限制。在LBCL使用IgNGS的经验中,基线校准强烈依赖于样本。总体而言,83.7%的ID样本校准成功,福尔马林固定石蜡包埋或来自淋巴组织/结外肿块的基因组DNA成功率更高(91.3%),而外周血校准成功率则低得多(45.3%)。在MCL和FL中,克隆型鉴定失败同样归因于DNA投入不足,以及较少见的难以确定优势克隆型(序列独特性和背景库)。这些技术和生物学的限制在某些情况下降低了灵敏度。例如在LBCL治疗后的单个时间点,IgNGS仅识别出30%后续复发的患者(图1)。
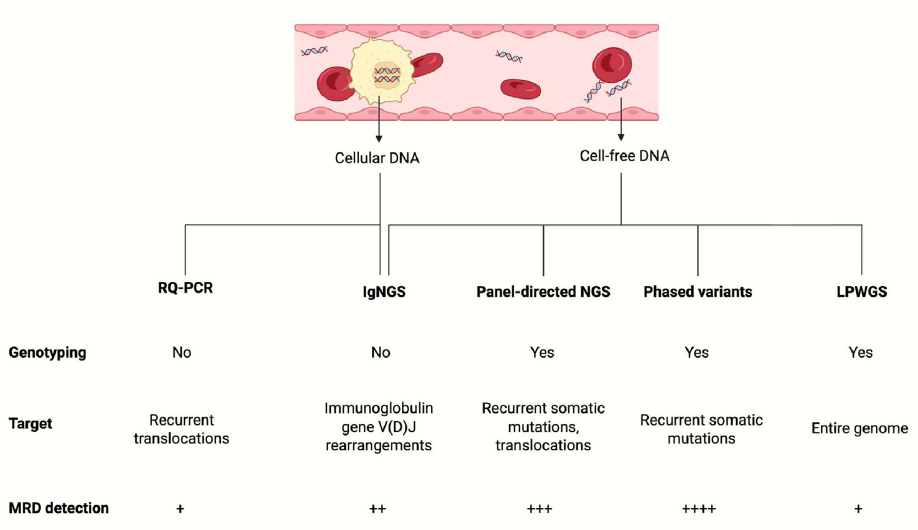
图1. 应用于淋巴瘤的MRD检测方法。检测淋巴瘤MRD的方法包括基于PCR和基于测序的方法。这些方法中的每一种都靶向肿瘤基因组的不同区域,并在疾病检测和肿瘤基因分型方面具有不同的性能特征。
基于Panel的NGS平台将检测范围扩展到免疫球蛋白位点之外,靶向数百个反复突变或易位的区域,从而增加了信息性ctDNA片段的数量,并提高了相对于IgNGS的灵敏度。Cancer Personalized Profiling by Deep Sequencing(CAPP-Seq)是最具验证性的例子。尽管CAPP-Seq不受总DNA投入量的限制,但在非常低的变异等位基因频率下,背景测序噪声会降低其在残留病灶负荷最低时的性能。这种局限性在治疗结束时(EOT)最为明显,在该时间点,它检测到的LBCL患者中随后复发的比例不到一半(图1)。
相位变异(phased variants)检测通可过利用位于同一ctDNA片段上的多个单核苷酸变异来克服这一障碍,能有效区分真正的肿瘤衍生变异与背景噪声。最成熟的平台是Phased Variant Enrichment and Detection by Sequencing(PhasED-Seq),其分析灵敏度可达每百万正常DNA片段中检测到1个癌症DNA分子,并且可以检测超过90%后来出现复发的LBCL患者的治疗后MRD(图1)。
Low-pass whole genome sequencing是一种新兴的ctDNA检测补充策略,其可捕获大规模的基因组特征,包括可能被靶向NGS panel遗漏的拷贝数异常和结构变异。它可以识别具有预后相关性的基因组改变,并在治疗前对LBCL患者进行风险分层。其实验室工作流程更简单,但与目前NHL中最广泛使用的靶向基于突变的NGS检测相比,其MRD检测灵敏度较低(图1)。
现代ctDNA检测方法,特别是相位变异检测,可以在百万分之一的范围内发现肿瘤成分,从而扩展了NHL中残留病灶检测的边界。ctDNA具有广泛的适用性和高度的肿瘤特异性,有潜力准确地为治疗决策提供信息,但需要在介入性试验中进行严格测试。
在这篇综述中,作者总结了早期ctDNA研究的关键见解,并重点介绍了正在进行的、使用ctDNA识别不同临床环境中的高危患者,以及根据分子反应调整治疗持续时间和强度的试验。
LBCL中基于MRD决策的挽救治疗——“早期挽救”
LBCL是一组具有不同生物学和临床亚型的侵袭性B细胞肿瘤,最常见的形式是弥漫性LBCL,非特指型,此外还有预后良好的原发性纵隔LBCL以及与较差结局相关的高级别B细胞淋巴瘤等亚型。利妥昔单抗联合环磷酰胺、多柔比星、长春新碱和泼尼松(R-CHOP)或相关方案是前线治疗的基础,将抗体药物偶联物维泊妥珠单抗加入R-CHP(Pola-R-CHP)方案可改善无进展生存期,效果优于R-CHOP。这些方案可治愈约70%的患者(图2)。
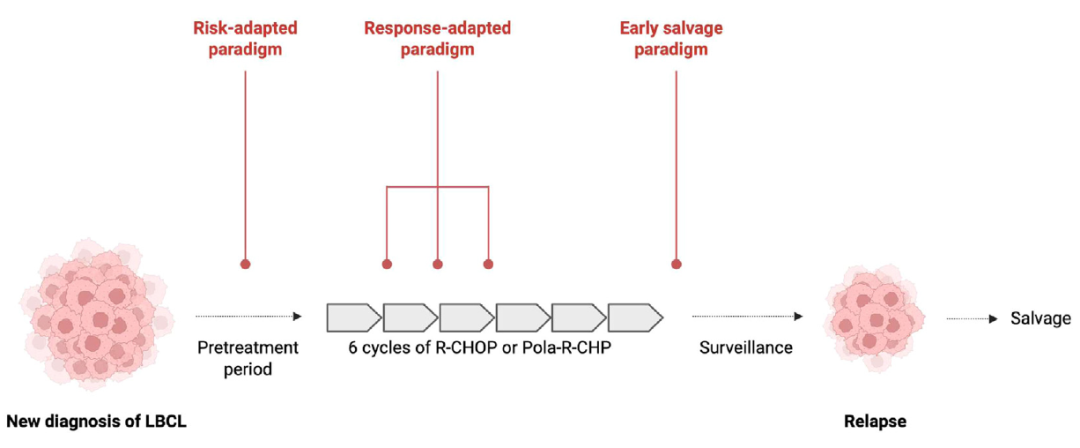
图2. LBCL临床试验中ctDNA驱动的治疗模式。新诊断LBCL的标准一线治疗包括6个周期的R-CHOP或R-CHP联合维泊妥珠单抗,对于12个月内复发的患者,首选抗CD19嵌合抗原受体T细胞作为挽救治疗。ctDNA能够在这条治疗轨迹的多个时间点实现风险分层。在治疗前阶段,ctDNA基因分型正在被评估,以识别高危分子亚群并指导风险适应性治疗选择。在治疗期间,定量ctDNA动力学作为反应适应性工具正在研究之中,用于调整治疗持续时间和强度。治疗结束后,基于ctDNA的微小残留病评估正被测试作为在临床或影像学进展前启动抢先性挽救治疗的早期触发因素。
对于一线治疗难治或1年内早期复发的LBCL患者,两项随机试验已证实二线CAR-T细胞治疗优于挽救性化疗和自体干细胞移植(ASCT)巩固,其持久缓解率可达40%。然而,早期识别对一线治疗的耐药性对于改善结局至关重要。CAR-T细胞治疗是一个多步骤过程,包括宿主T细胞的白细胞分离术、将编码CAR的基因转移到T细胞基因组、体外扩增以及淋巴细胞清除化疗后回输CAR-T细胞。由于制备需要数周时间,肿瘤负荷大或疾病快速进展的患者可能不符合条件或需要桥接治疗。更高的肿瘤负荷也会导致T细胞耗竭并降低CAR-T细胞的疗效。
在肿瘤负荷仍然较低时早期准确地识别对一线化疗的耐药性,可能使更多患者能够接受二线CAR-T细胞治疗并提高其疗效。然而如前所述,仅依赖影像学的反应评估在诊断残留病变方面准确性有限。这种不确定性反映在NCCN指南建议,对于EOT PET阳性患者,在开始挽救治疗前,应进行组织活检或重复间歇性PET扫描以确认活动性疾病(图3A)。EOT PET阴性的患者则接受为期长达2年的、伴或不伴影像学检查的门诊随访监测。这些额外的程序延误了治疗,增加了医疗资源利用,并可能使PET假阳性的患者暴露于不必要且有潜在危害的治疗中。
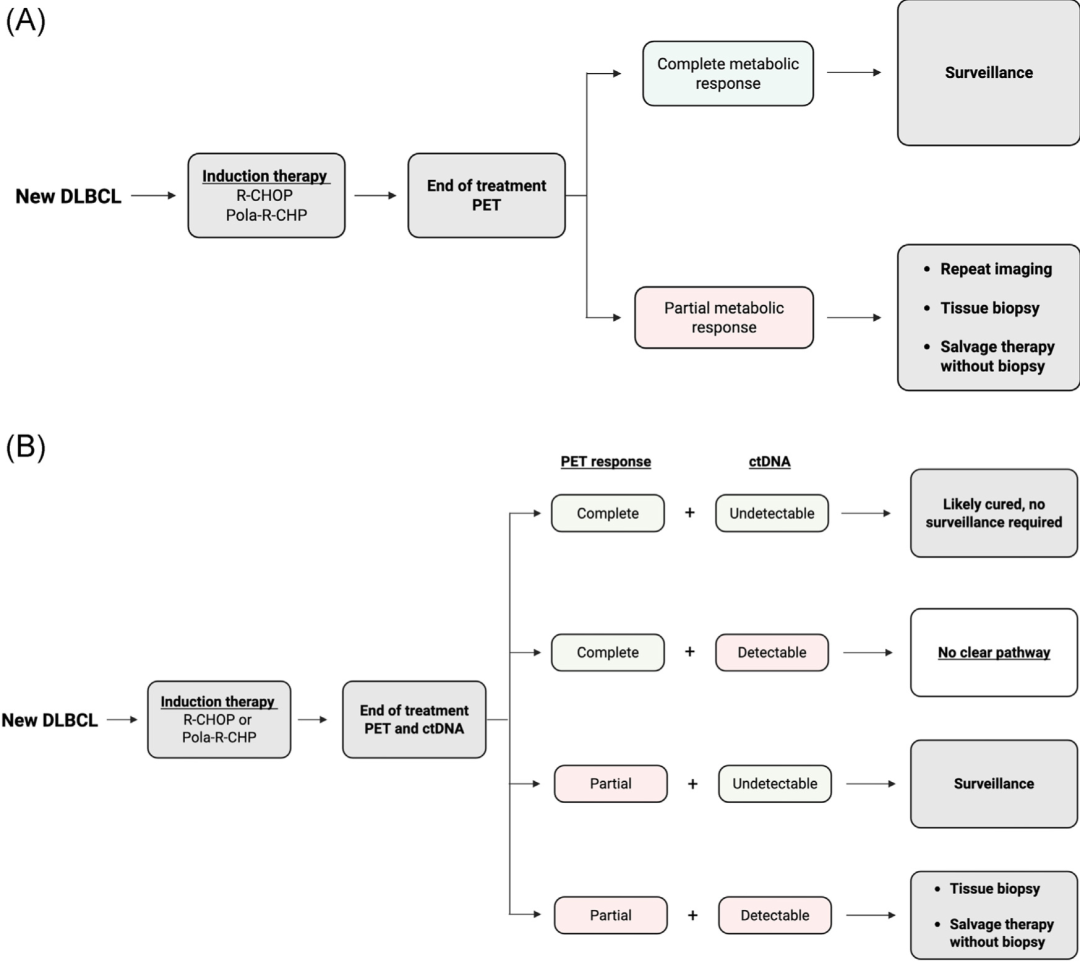
图3. LBCL完成一线治疗后的反应评估路径。(A) 传统反应评估依赖于使用Deauville标准的¹⁸F-氟脱氧葡萄糖PET,将患者分类为完全缓解或残留病变。(B) 整合反应评估路径将ctDNA与PET相结合,能够实现残留病变的分子水平检测并细化风险分层。
使用ctDNA中的相位变异进行MRD评估,比单独使用PET能更准确地确定缓解状态,并可能更好地指导启动挽救治疗的决策(图3B)。一项汇总分析报告了5项前瞻性一线蒽环类化疗的临床试验,其中4项纳入了新药,包括阿可替尼、来那度胺、奥妥珠单抗、维泊妥珠单抗和/或坦昔妥单抗。在治疗结束时(EOT)可获得126名患者的血浆样本,其中98名(78%)检测不到MRD。检测不到MRD的患者2年无进展生存期(PFS)为97%,而检测到MRD的患者为29%(风险比[HR] 29,P<0.001)。在98名EOT MRD检测不到的患者中,95名(97%)在中位随访37个月后仍维持无进展状态。3名复发的患者中有1名在治疗结束后8个月出现孤立性中枢神经系统复发。相反,28名EOT MRD检测到的患者中有19名(68%)随后复发。在EOT进行的单次MRD检测识别出了22个总进展事件中的19个(90%),其中包括一个发生在治疗结束后30个月的进展事件。此外,治疗后的MRD状态独立于PET反应对患者进行风险分层。在EOT PET阴性的患者中,检测到MRD与2年PFS为31%相关,而检测不到MRD的患者为98%(P<0.001)。在EOT PET阳性患者中,检测到MRD与2年PFS为30%相关,而检测不到MRD的患者为93%(P=0.009)。
在另一项针对188名接受R-CHOP治疗患者的多中心独立研究中观察到了类似结果。在170份可评估的EOT样本中,126份(74%)检测不到MRD,其2年疾病进展时间为95%,而检测到MRD的患者为39%(P<0.001);仅5名(4%)MRD阴性患者复发。无法检测的 EOT MRD 可识别出低复发风险患者,无论 EOT PET 为阴性 (3%) 还是阳性 (8%),而可检测的 EOT MRD 与38%的 PET 阴性患者和61%的 PET 阳性患者的复发相关。第三项研究使用分阶段变异的156例患者证实了这些结果。在 EOT 时,76%的患者检测不到MRD,其2年 PFS 为88%,而可检测到 MRD 的患者为28%(HR 10,P<0.0001)。EOT PET 和 MRD 阴性患者的2年 PFS 为91%,而 EOT PET 和 MRD 阳性患者均复发。
总的来说,这些研究确立了EOT MRD检测不到的阴性预测值 > 90%。它可以识别出可能已治愈、不需要监测、进一步检查或挽救治疗的患者,即使在PET阳性时也是如此(图3B)。考虑到CAR-T细胞治疗相关的大量毒性,包括细胞因子释放综合征、免疫效应细胞相关神经毒性综合征、噬血细胞性淋巴组织细胞增生症样综合征、血细胞减少、感染以及继发性淋巴和髓系恶性肿瘤,这一发现尤其重要。NCCN指南现在纳入了对一线治疗后PET显示部分反应的LBCL患者进行灵敏度约为1×10⁻⁶的ctDNA MRD评估,以替代组织活检或重复影像学检查(图3B)。
虽然EOT MRD的阴性预测值已明确,但对检测到MRD的患者的最佳处理仍不确定。这些患者并非总是会复发,正在进行的临床试验正在测试在影像学进展前对分子水平疾病患者进行更早的挽救治疗是否能改善结局(图2)。ALPHA-3研究(NCT06500273)将EOT PET阴性但EOT MRD检测到的患者随机分配接受异基因CD19 CAR-T细胞疗法temcabaptene ansegedleucel治疗或观察。该试验计划在50个中心入组240名患者,主要终点是无事件生存期(EFS)。另一种非随机化方法正在NCT06828991中进行测试,该研究将入组40名年龄超过70岁、在一线维泊妥珠单抗、利妥昔单抗和减剂量CHP治疗后EOT PET阴性但MRD检测到的患者,并使用CD3xCD20双特异性抗体莫妥珠单抗治疗6个周期,主要终点是MRD清除。
总之,使用相位变异ctDNA进行EOT MRD评估比PET准确得多,并能识别出可能已治愈、可以免于进一步监测或毒性挽救治疗的患者。正在进行的试验将确定在EOT MRD检测到但无影像学证据的患者中更早地干预是否能改善结局。
LBCL中基于MRD决策的诱导持续时间——“反应适应性(Response-adapted)”
LBCL一线治疗的持续时间传统上是经验性的,而非反应驱动的。大多数患者接受6个周期的化学免疫治疗,这是基于利妥昔单抗时代关键试验中使用的固定治疗周期。这种方法可能导致过度治疗和可避免的伤害,尤其是在那些本身对化疗毒性更敏感的患者中。老年人、有明显合并症的患者以及有潜在免疫缺陷(如HIV)的患者特别容易受到治疗相关毒性的影响,并且不成比例地受到经验性、固定持续时间治疗方法的影响。
在经过选择的侵袭性淋巴瘤患者中,较短的治疗持续时间可以是治愈性的。在一项2期研究中,55名HIV感染且新诊断LBCL的患者接受了剂量调整的依托泊苷、泼尼松、长春新碱、环磷酰胺、多柔比星和利妥昔单抗(DA-EPOCH-R)治疗。从第2个周期开始,在每个周期前使用CT和PET评估治疗反应。与之前的中期扫描相比,PET标准摄取值较基线下降 > 50%且CT测量结果稳定的患者仅接受额外1个周期的治疗。中位随访12.6年后,5年PFS和总生存期(OS)分别为64.3%和71.8%。在有中期PET扫描的47名患者中,30名(64%)转为PET阴性并提前停止治疗。值得注意的是,他们的5年PFS与中期PET阳性并接受延长治疗的患者相似(73.4% vs 62.7%,P=0.14)。在另一项研究中,低危伯基特淋巴瘤患者接受反应适应性疗程的DA-EPOCH-R治疗。2个周期后中期PET阴性的患者仅接受额外1个周期的DA-EPOCH-R治疗,并达到100%的4年EFS。虽然这些结果不能确定缩短治疗持续时间具有相同的疗效,且研究设计也不能确定如果中期PET阴性的患者完成了标准治疗其PFS会是多少,但它们表明,在精心挑选的一部分患者中,缩短治疗疗程可能足以治愈。
通过ctDNA进行的MRD评估可提供早期且生物学精确的治疗反应指标,并可能指导个体化的治疗持续时间。在一项包含217名接受根治性一线或挽救性化学免疫治疗患者的研究中,使用基于Panel的测序在第1和第2个周期后对ctDNA进行定量。第1周期后ctDNA下降≥2-log(早期分子反应,EMR)和第2周期后下降≥2.5-log(主要分子反应,MMR)均能预测最终的完全缓解。在92%的患者中,EMR和MMR是一致的。在一个验证队列中,EMR和MMR均与显著更优的2年EFS相关(EMR:83% vs 50%,P = .0015;MMR:82% vs 46%,P < .001)。重要的是,分子反应完善了中期PET的评估。两种方法均显示有利结果的患者具有极佳的结局,而中期PET阳性但无分子反应的患者治疗失败的风险显著增加(均P<0.001)。
额外的证据来自DA-EPOCH-R治疗期间基于IgNGS的MRD追踪。在2个周期后,检测到ctDNA的患者5年疾病进展时间为41.7%(95% CI, 22.2-60.1),而ctDNA检测不到的患者为80.2%(95% CI, 69.6-87.3)(P<0.0001)。在24名中期ctDNA检测到的患者中,15名(63%)出现临床进展,而84名中期ctDNA检测不到的患者中仅有17名(20%)出现进展。
通过提供对LBCL一线治疗反应的早期准确评估,ctDNA可能实现治疗过程中的调整(图2)。正在进行的NCT06693830试验正在测试这一概念,其使用中期ctDNA来确定治疗持续时间。在这项试验中,最多32名新诊断LBCL患者接受R-CHOP或Pola-R-CHP治疗,并在3个周期后使用相位变异进行中期PET和ctDNA评估。中期PET阴性和中期ctDNA检测不到的患者在4个周期后停止治疗,而中期PET阳性或ctDNA检测到的患者则完成6个周期。
另一项正在进行的研究为NCT04604067,根据整合的中期PET和ctDNA结果评估治疗缩短和强化。Non MCD基因亚型DLBCL患者接受2个周期的R-CHOP,然后进行反应评估。中期PET阴性和中期ctDNA检测不到的患者接受总共4个周期的R-CHOP短期疗程。Er Deauville评分为4分且中期ctDNA检测到的患者,通过加入布鲁顿酪氨酸激酶(BTK)抑制剂阿可替尼来强化治疗。中期PET Deauville评分为4分或中期ctDNA检测到的患者继续接受标准的6个周期R-CHOP。
这些ctDNA反应适应性研究的结果将提供初步证据,证明基于MRD驱动的方法能否将LBCL的一线治疗从固定持续时间的模式转变为生物学告知的、患者特异性的策略。大多数具有EMR、MMR或中期ctDNA检测不到的患者很可能被治愈,如果在更大规模的临床试验中,缩短治疗在这些群体中能维持极好的结局,那么中期ctDNA指导的降阶梯治疗可能成为最早期和最实用的MRD应用,以个体化一线治疗并减少毒性。
LBCL中基于MRD决策的治疗类型选择——“风险适应性(Risk-adapted)”
虽然中期和治疗结束时的MRD评估为研究基于反应的治疗调整提供了强大的工具,但ctDNA在治疗开始时也提供了有意义的信息。治疗前的ctDNA水平和基因分型为风险分层提供了补充信息,可以在任何治疗实施前识别具有侵袭性疾病生物学的患者,并促进风险适应性治疗方法的研究(图2)。
治疗前ctDNA水平可预测LBCL的临床结局,并与既定的预后因素密切相关。在一项包含217名接受一线或挽救治疗患者的研究中,通过基于Panel的测序在213名(98%)患者中检测到治疗前ctDNA,且较高的水平与较差的EFS呈连续相关性。治疗前ctDNA浓度 > 2.5 log单倍体基因组当量/mL的患者在一线(HR 2.6;95% CI, 1.3-5.2,P=0.007)和挽救(HR 2.9;95% CI, 1.3-6.4,P=0.01)治疗中的2年EFS均较差。在多变量分析中,无论国际预后指数(IPI)评分、分子亚型和代谢肿瘤体积如何,治疗前ctDNA仍然是EFS的独立预后因素。
在另一项包含267名患者的研究中,较高的ctDNA水平与较短的诊断到治疗间隔相关。诊断到治疗间隔是指从病理诊断到开始化学免疫治疗的时间,可作为需要立即治疗的侵袭性疾病生物学患者的替代指标。较短的诊断到治疗间隔与晚期、较高的IPI和较差的EFS相关(均P<0.001)。通过基于Panel的测序测量的较高ctDNA水平预示较短的诊断到治疗间隔,且独立于IPI。在多变量分析中,无论诊断到治疗间隔如何,ctDNA仍然是EFS的独立预后因素。
除了治疗前定量水平的预后价值外,ctDNA基因分型作为一种非侵入性的“液体活检”,还能够准确识别LBCL基因亚型,且与组织分析的一致性很高。这种分子分层支持选择与潜在生物学相匹配的治疗。例如,MCD或cluster 5基因亚型的特征是复发性MYD88 L265P和CD79B功能获得性突变以及慢性活跃的B细胞受体(BCR)信号传导。在一项比较Pola-R-CHP与R-CHOP的3期研究中,MCD疾病患者接受Pola-R-CHP治疗获得了更优的5年PFS(70.4% vs 42%,P=0.005)。该亚型对BTK抑制剂介导的BCR通路抑制也特别敏感。基于此生物学原理,试验NCT04604067通过基于Panel的测序在治疗前进行ctDNA基因分型,以识别MCD疾病患者,然后这些患者接受在标准R-CHOP基础上加入阿可替尼的风险适应性治疗。
总而言之,治疗前ctDNA将MRD在风险评估中的效用扩展到LBCL的整个治疗连续过程中。目前尚无完成的试验评估在治疗前、治疗中和治疗后根据ctDNA定义的高危亚组修改治疗是否能改善结局,但几项正在进行的研究正在直接测试这些模式。
MCL中基于MRD决策的巩固治疗
MCL的治疗策略与LBCL根本不同。由于MCL大多不可治愈,治疗的目标是在最小化累积毒性的同时实现持久缓解。老年患者或有合并症的患者接受强度较低的化疗,如苯达莫司汀加利妥昔单抗联合或不联合BTK抑制剂,随后进行利妥昔单抗维持治疗。较年轻、体能状态良好的患者通常接受含阿糖胞苷的诱导治疗,随后进行ASCT巩固和利妥昔单抗维持治疗。
尽管随着伊布替尼等靶向药物的出现,标准治疗有所发展,但MCL的一线治疗仍然是经验性的,并不根据治疗反应的深度进行调整。大多数患者无论其风险状况或对诱导治疗的反应性质如何,都会接受巩固和/或维持治疗。一项3期试验挑战了ASCT巩固的传统作用。在这项研究中,870名年龄≤65岁的患者被随机分配到3个组。A组接受含阿糖胞苷的诱导治疗后进行ASCT。A+I组接受相同的诱导和ASCT,但在诱导期间和作为固定持续时间的维持治疗中添加了伊布替尼。I组接受相同的诱导和伊布替尼维持治疗,但省略了ASCT。A+I组达到了88%(95% CI, 84-92)的优异3年无失败生存期,而A组为72%(95% CI, 67-79)(P=0.0008)。重要的是,A组并不优于I组,两组的3年无失败生存期分别为72%(95% CI, 67-79)和86%(95% CI, 82-91)(P=0.9979),表明当BTK抑制剂被纳入诱导和维持治疗时,可以安全地省略ASCT。
诱导后的MRD具有预后意义,并可能有助于个体化治疗。对两项欧洲MCL联盟试验(MCL Younger和Elderly)的汇总分析使用基于实时定量(RQ)-PCR的方法对406名患者进行了细胞MRD评估。在MCL Younger试验中,年龄<65岁的患者被随机分配接受R-CHOP与R-DHAP(利妥昔单抗、高剂量阿糖胞苷和顺铂)交替方案,而MCL Elderly试验入组>60岁的患者,接受R-CHOP对比利妥昔单抗、氟达拉滨和环磷酰胺,随后随机分配接受利妥昔单抗或干扰素维持治疗。在两项研究中,诱导后MRD阴性预示着更好的2年缓解率(MCL Younger:94% vs 74%,P=0.022;MCL Elderly:77% vs 34%,P=0.021),并且独立于临床反应和MIPI评分(P=0.028)。
MCL中诱导后MRD的第一个实际应用在于识别可以安全省略ASCT的患者(图4)。
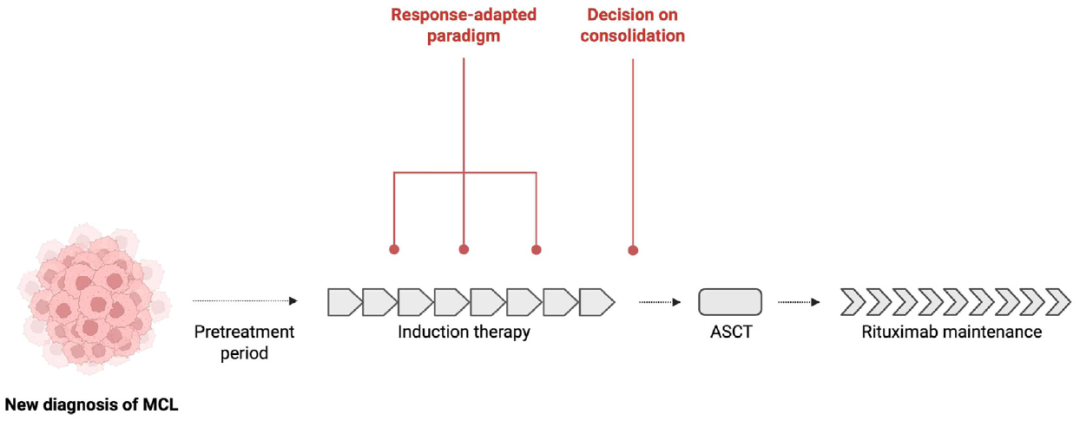
图4. MCL临床试验中MRD驱动的治疗模式。新诊断MCL的一线治疗通常包括诱导化学免疫治疗,随后进行ASCT巩固和/或利妥昔单抗维持治疗。MRD评估正被整合到该治疗路径的多个时间点。在诱导治疗期间,早期MRD清除正作为一种反应适应性策略被评估,以支持提前停止治疗。在诱导治疗结束后,MRD阴性正被测试作为安全省略ASCT巩固治疗且不损害临床结局的标准。
在一项包含650名年龄18至70岁、根据MIPI和诱导强度分层患者的研究中,使用IgNGS检测的细胞MRD被用来指导第一次缓解期的ASCT决策。检测不到MRD的患者被随机分配接受ASCT加利妥昔单抗维持治疗或仅接受利妥昔单抗维持治疗。两组的3年PFS相似,分别为76.6%和77.4%(P=0.79),3年OS也相似,分别为82.1%和82.7%(P=0.66),表明MRD阴性的患者可以放弃ASCT而不影响结局。在诱导后30名检测到MRD的患者中,17名(57%)在ASCT后转为检测不到MRD,并且结局极好,3年PFS和OS均为100%。相比之下,MRD持续阳性的患者3年PFS和OS显著较差,分别为48.8%和63.6%,表明持续MRD阳性的患者可能从ASCT中获益。
MCL中基于MRD决策的治疗持续时间
即使在诱导期间和使用新型靶向药物时,MRD评估也能提供对治疗反应的早期洞察,并有助于指导治疗持续时间的决策。在一项包含53名接受基于硼替佐米的化学免疫治疗患者的研究中,通过IgNGS检测的持续性ctDNA在1个周期后预示较差的PFS(中位1.7 vs 7.3年;P=0.002),在2个周期后以及诱导结束时均预示较差的PFS和OS(2个周期后中位PFS:1.8 vs 2.7年,P=0.005;中位OS:7.4 vs 13.8年,P=0.03;诱导结束时中位PFS:1.5 vs 2.6年,P=0.003;中位OS:3.9 vs 12.4年,P=0.02)。
靶向治疗联合方案目前正在MCL的一线治疗中得到广泛评估,通常无限期或按任意持续时间给药,MRD提供了一种实用的策略来个体化治疗长度并避免不必要的暴露(图4)。在一项包含25名TP53突变MCL患者的研究中,患者接受泽布替尼、奥妥珠单抗和维奈克拉治疗,并根据MRD指导停药。对于达到完全缓解且MRD检测不到的患者,可在2年后停止治疗。15名MRD阴性患者中的13名(87%)在停止治疗后仍保持无进展。在另一项包含24名未经治疗、接受阿可替尼、来那度胺和利妥昔单抗治疗的患者的研究中,类似的方法是可行的。7名通过IgNGS检测达到完全缓解且MRD检测不到的患者在24个周期后停止治疗,并维持缓解状态直至随访结束。在另一项包含59名接受维奈克拉、来那度胺和利妥昔单抗治疗的患者的研究中,对于达到完全缓解、通过RQ-PCR检测MRD检测不到且该状态维持3个月的患者,停止治疗。在停止治疗的28名患者中,有3名经历了分子复发,所有这些患者在接受再治疗后均重新获得了检测不到的MRD。
两项正在进行的研究正在未经治疗和复发的MCL患者中更正式地测试这种反应适应性框架。NCT04855695正在评估阿可替尼、维奈克拉和奥妥珠单抗在53名患者中的应用。将使用IgNGS监测MRD,对于那些达到并维持MRD检测不到状态3个月的患者,将停止治疗,并可以选择在分子复发时重新开始治疗。NCT05951959将入组108名患者接受阿可替尼、维奈克拉和利妥昔单抗治疗。通过IgNGS检测达到完全缓解且MRD检测不到的患者将被随机分配继续接受阿可替尼治疗或观察,如果MRD变为可检测,可以选择重新开始阿可替尼治疗。
MRD正成为在MCL多个治疗阶段个体化治疗的核心工具,可以可靠地识别可以安全省略ASCT的患者,同时引导持续性疾病患者接受更密集的巩固治疗。在分子复发时基于MRD指导的停药和再治疗已被证明是可行的,强化了MRD将MCL管理从固定持续时间的方案转变为真正反应适应性治疗的潜力。此外,MCL为MRD评估提供了一个独特的机会,因为肿瘤细胞(细胞MRD)和ctDNA(游离MRD)通常都可检测到。首选的方式仍未确定,但细胞性和游离MRD都提供了有意义的临床信息。
FL中基于MRD决策的治疗持续时间
FL是最常见的惰性淋巴瘤,其临床病程以反复复发为特征,且复发频率倾向于随时间增加。由于患者接受多线治疗,限制治疗持续时间和累积毒性是一个核心目标。一线选择包括抗CD20抗体联合苯达莫司汀或CHOP的化学免疫治疗,以及来那度胺加利妥昔单抗。利妥昔单抗维持治疗可延长PFS,但不能改善OS。尽管约80%的患者的总生存期与普通人群相当,但近20%的患者属于高危亚组,在一线治疗后24个月内出现疾病进展(POD24),其5年生存率仅为50%。POD24状态的定义本身是在治疗后才知道的,而现有的其他预后工具复杂、依赖治疗方案,且阳性预测值低于50%,限制了它们在风险适应性决策中的价值。
诱导期间和刚结束后的MRD对POD24有很强的预测价值,并且与PET联合使用时,可以标记出早期进展风险增加的患者。在一项包含141名患者的3期试验(比较来那度胺-利妥昔单抗与化疗)的研究中,使用相位变异在140名(99.3%)患者中检测到ctDNA。诱导后ctDNA检测不到的患者与检测到ctDNA的患者相比,具有更长的PFS(中位未达到 vs 17.7个月)(P=0.0038)。将ctDNA与PET结合可准确预测POD24,阳性预测值为86%,阴性预测值为94%。在另一项包含1202名患者、比较奥妥珠单抗与利妥昔单抗联合化疗的3期试验中,使用RQ-PCR评估的MRD显示出相似的预后价值。诱导治疗期间和结束后持续检测到MRD与较差的PFS相关(HR 3.03,95% CI 2.1-4.5,P<0.001,和2.25,95% CI 1.5-3.3,P<0.001)。
由于关键目标之一是避免过度治疗,第一个合乎逻辑的MRD指导的治疗为确定治疗持续时间,允许在低风险患者中缩短治疗(图5)。NCT06557330研究通过评估一线苯达莫司汀加利妥昔单抗治疗3个周期后的PET反应和基于IgNGS的MRD来应用这种方法。MRD检测不到且达到完全缓解的患者在4个周期后早期停止苯达莫司汀,而MRD检测到或部分缓解的患者则完成计划的6个周期。
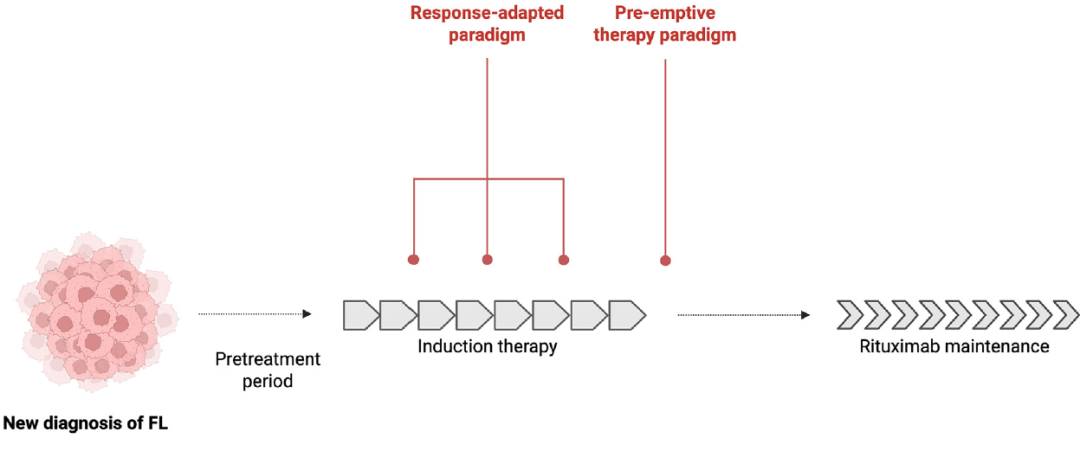
图5. FL临床试验中MRD驱动的治疗模式。FL的一线治疗通常包括诱导化学免疫治疗或来那度胺联合利妥昔单抗,随后进行抗CD20维持治疗。MRD评估正被整合到该治疗轨迹的多个时间点。在诱导治疗期间,早期MRD清除正作为一种反应适应性方法被研究,以支持治疗降级或提前停止治疗。在诱导治疗结束时,MRD阴性正被评估作为安全省略维持治疗的标准。诱导治疗后,连续的MRD监测正被探索作为一种检测分子复发并在临床进展前启动抢先性干预的工具。
另一种限制治疗的方法是了解哪些患者可以安全地省略维持治疗而不影响结局(图5)。MRD能否指导维持治疗的患者选择仍不确定。在一项包含807名高肿瘤负荷患者的研究中,标准的经验性维持治疗优于使用PET和诱导结束时基于RQ-PCR的MRD来分配诱导后治疗的反应适应性方法(3年PFS 86% vs 72%,P<0.001)。实验组包括3条路径:MRD阴性完全缓解的患者接受观察,如果在随访期间MRD变为可检测则进行抢先性利妥昔单抗治疗;MRD阳性完全缓解的患者接受4周每周一次的利妥昔单抗治疗;未达到完全缓解的患者接受1剂ibritumomab治疗,随后进行标准的利妥昔单抗维持治疗。由于约40%的患者无法进行MRD评估并仅根据PET进行管理,因此对结果的解读受到检测覆盖范围的限制。该试验没有追踪诱导期间的连续MRD,而连续MRD可能比单个时间点提供更好的风险分层。总体而言,该试验确立了反应适应性管理的可行性,但MRD在指导维持治疗决策中的作用需要使用更灵敏和广泛适用的ctDNA检测方法进行进一步评估。
将MRD整合到常规治疗中的障碍
MRD,特别是ctDNA,正在成为一种有临床意义的工具,它补充了影像学检查,能够捕获早期耐药性,并可能实现在NHL中的个体化护理。尽管取得了这些进展,但在ctDNA被广泛应用于临床实践之前,必须解决几个程序性、临床和实践性障碍(表格)。
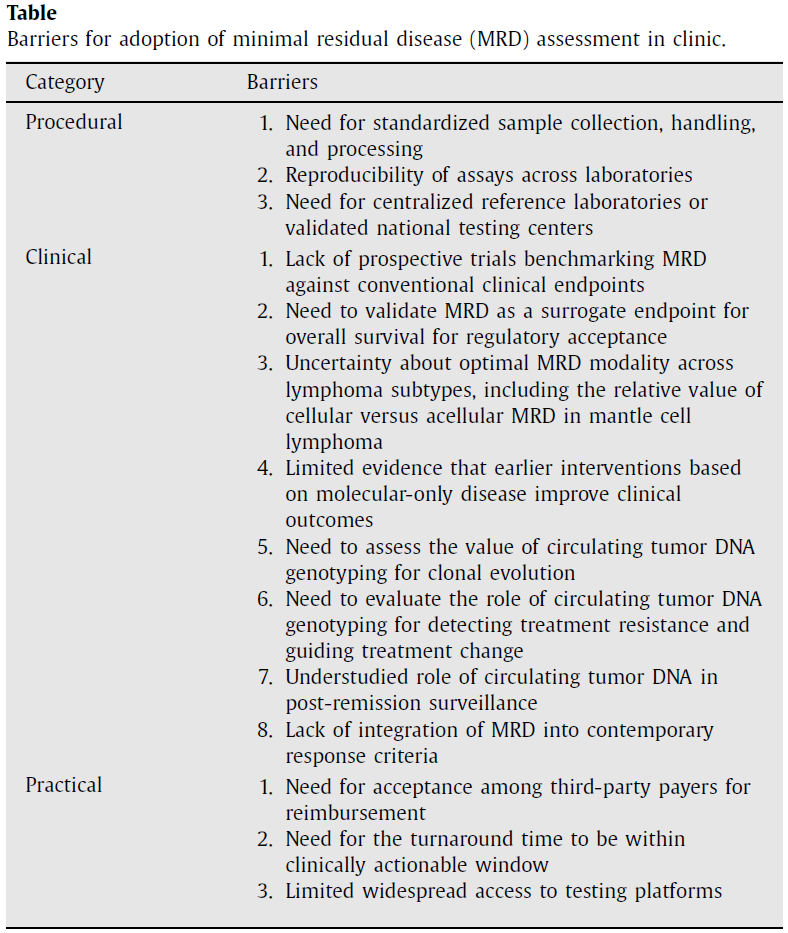
程序性障碍源于缺乏标准化的分析前工作流程。样本收集、处理和分析在不同中心之间仍然存在差异,任何步骤的偏差都可能损害检测性能。检测方法也必须在不同实验室之间具有可重复性,或者在具有经过验证的工作流程和可靠周转时间的参考设施中进行集中化。此外,尚不清楚哪些ctDNA平台对于特定的NHL亚型最具临床信息价值。ctDNA的脱落在不同淋巴瘤亚型之间差异很大,直接影响检测灵敏度。相位变异检测是检测LBCL治疗后MRD最灵敏的技术,但在不同的NHL亚型中,不同的MRD方式可能是最优的。例如,MCL中的细胞性与游离MRD都提供有用的临床信息,但它们的相对价值仍然未知。
临床障碍反映了支持广泛实施所需证据的不足。大多数可用的ctDNA数据都是回顾性的,并且在淋巴瘤各亚型中进行前瞻性验证至关重要,这包括将MRD与传统临床和影像学终点进行对比的试验。由于MRD提供了高度精确的治疗反应测量指标,将MRD纳入正式的反应评估标准将扩大其临床应用,并为其作为替代终点获得监管机构认可提供必要证据。MRD检测方法的开发可以直接借鉴在多发性骨髓瘤中确立的监管路线图,在该路线图中,平行的学术团体与行业数据贡献者合作,对来自2期和3期试验的MRD数据进行了两项协调一致的荟萃分析,其统计计划是在与美国食品药品监督管理局(FDA)协商后制定的[72,73]。该证据包包括一致的分析灵敏度阈值、具有预先规定样本采集窗口的标准化评估时间点,以及对缺失或无法评估样本的透明处理(其中缺失的MRD在意向治疗分析中被计为MRD阳性),以及将MRD与PFS和OS联系起来的试验层面和患者层面的荟萃分析[74]。通过一系列公开研讨会,FDA的参与逐步推进,并于2024年4月达到高潮,肿瘤药物咨询委员会一致支持将MRD阴性完全缓解作为合理可能预测临床获益的中间终点。对于淋巴瘤,基于协调一致的检测性能标准、对缺失样本的透明核算以及与FDA前瞻性统计协调的类似协同策略,对于获得监管机构的认可至关重要。同时,一个关键的未解问题是,MRD指导的干预措施是否能在特定的临床环境中改善结局,以及此类策略是否能广泛应用于不同亚型。此外,ctDNA的非定量应用,如基因分型,仍处于探索阶段,需要在特定场景下进行评估,例如为靶向治疗选择患者,或检测惰性淋巴瘤中的克隆演变和组织学转化。
实践障碍包括当前ctDNA检测的高成本,通常每次测试在2000至3000美元之间,这强调了对成本效益研究的需求以及获得第三方付款人广泛接受以确保公平可及性的必要性。检测周转时间也至关重要。在大多数情况下,特别是在侵袭性淋巴瘤中,结果必须在大约7天内可用,以便为实时临床决策提供信息。
总结
通过定量ctDNA进行MRD评估,可提供淋巴瘤各亚型中最精确的治疗反应测量指标。它完善了基于PET的反应评估,且PET-ctDNA联合评估在LBCL和FL中具有很高的阳性和阴性预测值。在LBCL中,诱导治疗后检测不到ctDNA,可识别出复发风险极低、无需监测影像学检查的患者。在MCL中,诱导治疗后检测不到MRD,可筛选出能够安全省略ASCT且不影响疗效的患者。相反,LBCL患者在诱导治疗后检测到ctDNA但无影像学可见病灶,则代表了一个生物学上有利的干预时机,此时疾病负荷最低,正在开展的研究将揭示早期使用CAR-T细胞等新策略进行挽救治疗能否改善结局。中期ctDNA的预后价值推动了根据MRD反应调整治疗强度或持续时间的临床试验。如果在诱导治疗早期就清除ctDNA的患者接受较少周期治疗也能同样获益,则可避免有害的过度治疗。
目前有多项合作努力正在制定样本处理、基因组合设计和检测性能的标准,包括美国血液学会ctDNA工作组和第15届国际恶性淋巴瘤会议ctDNA研讨会的相关倡议。随着检测平台的技术进步与ctDNA指导的试验设计相结合,基于ctDNA的MRD有望演变为一个有用的替代终点,并成为淋巴瘤个体化治疗的基石。
参考文献
Semin Hematol . 2026 Feb 27:S0037-1963(26)00012-0. doi: 10.1053/j.seminhematol.2026.02.003.


