论文解读 | Hu Z/Guo Z/Yang L教授团队揭示抑制APE1可诱导细胞焦亡并增强NSCLC抗肿瘤免疫
时间:2026-05-06 19:10:46 热度:37.1℃ 作者:网络
非小细胞肺癌(NSCLC)的治疗仍面临诸多挑战。细胞焦亡是一种促炎性程序性死亡方式,其激活依赖于NLRP3炎症小体对胞质线粒体DNA(mtDNA)的识别。南京师范大学的Zhigang Hu/Zhigang Guo教授团队与南京大学的Lindong Yang教授团队合作,在本刊发表了题为“APE1 inhibition-promoted pyroptosis triggers T-cell infiltration and enhances anti-tumor immunity in NSCLC”的研究快讯。该团队此前发现,DNA修复蛋白APE1缺失可诱导NSCLC细胞焦亡,但具体机制尚不清楚。该研究发现,APE1抑制引起胞质mtDNA积聚,进而激活NLRP3-caspase-3-GSDME通路,诱导NSCLC细胞焦亡,促进T细胞浸润并增强抗肿瘤免疫应答。
1. 研究方法
研究团队利用shRNA在A549、NCI-H460和小鼠LLC细胞中敲低APE1,构建APE1-KD模型。通过形态学观察、Hoechst/PI染色和LDH释放实验评估细胞死亡情况;ELISA检测炎症因子水平;Western blot分析焦亡相关蛋白表达;RNA测序结合GSEA解析信号通路变化;qPCR和免疫荧光分别用于定量及定位胞质dsDNA与mtDNA;EtBr处理耗竭mtDNA以进行功能验证。在体内实验中,采用C57BL/6同种移植瘤模型和B-NDG人源化小鼠模型,评估肿瘤生长、细胞因子分泌及免疫细胞浸润情况。
2. 研究结果
首先,APE1-KD细胞表现出典型的焦亡形态,如细胞肿胀和膜泡形成;培养上清中IL-18、IFN-γ、IL-2等促炎细胞因子及CCL5、CXCL10等趋化因子水平显著升高,LDH释放增加。Hoechst/PI染色进一步证实细胞膜完整性破坏(图1A–C)。Western blot显示,APE1缺失特异性激活caspase-3并促进GSDME剪切,但不影响GSDMA、GSDMB、GSDMC、GSDMD或caspase-1的表达与活化(图1D)。
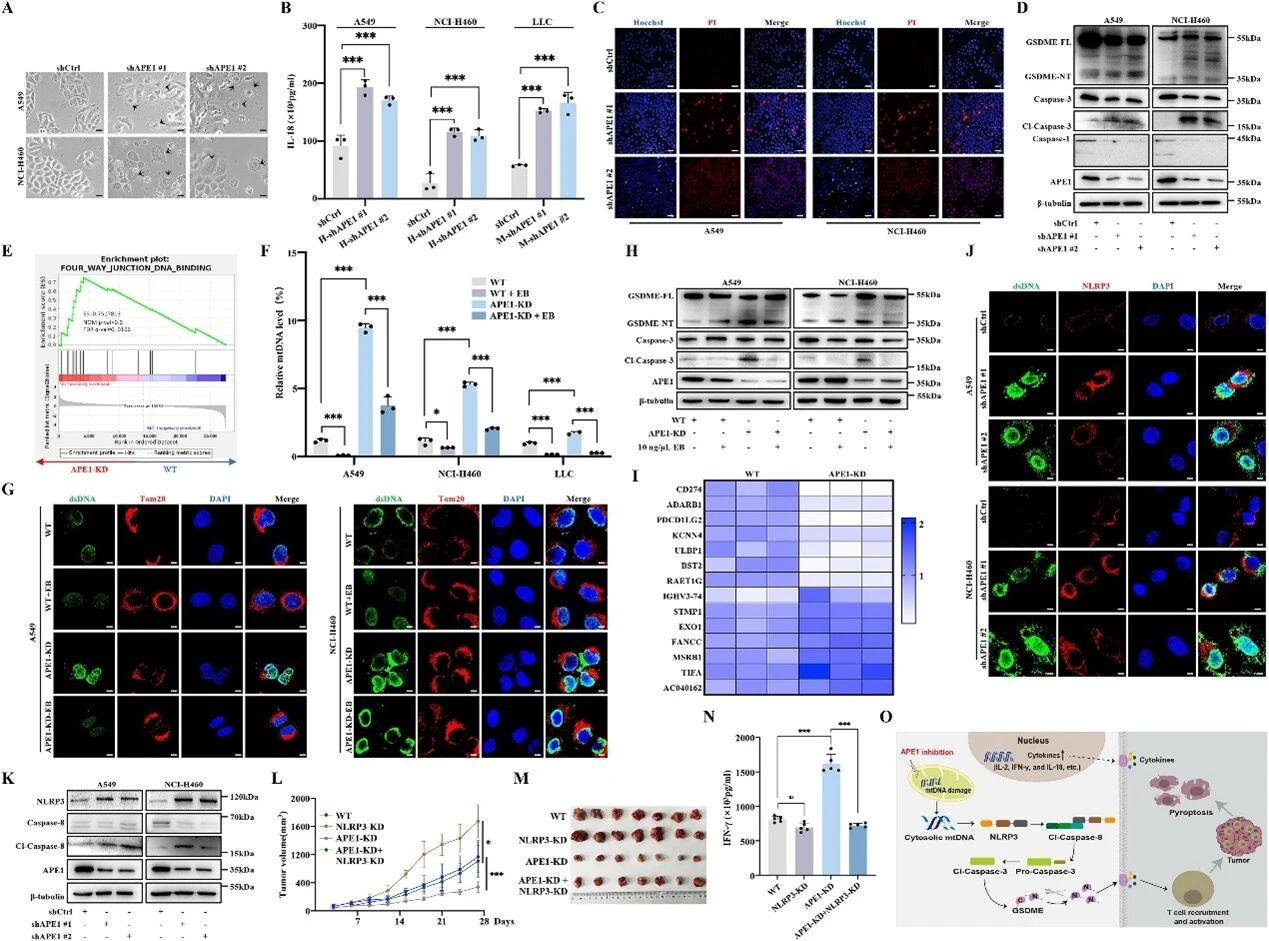
图1靶向APE1通过激活NLRP3–caspase-3–GSDME通路促进细胞焦亡
在机制探索中,RNA测序的GSEA分析提示APE1-KD细胞富集DNA结合相关通路;后续实验证实,这些细胞胞质dsDNA及mtDNA水平均上升(图1E–G)。EtBr耗竭mtDNA后,caspase-3活化及GSDME剪切均明显减弱,表明mtDNA积聚是APE1抑制诱导焦亡的关键环节(图1F–H)。
信号通路分析显示,APE1-KD细胞中免疫激活相关基因上调而免疫抑制基因下调;RNA测序热图中,STMP1等NLRP3通路相关基因表达改变。共聚焦显微镜观察证实,NLRP3与胞质dsDNA在APE1-KD细胞中共定位,而AIM2及cGAS-STING通路未见明显改变。Western blot结果显示,NLRP3、caspase-8和IL-1α的蛋白表达均上调(图1I–K)。功能验证实验显示:耗竭mtDNA可逆转NLRP3及caspase-8活化;单独敲低NLRP3、caspase-8或caspase-3后,GSDME剪切水平降低;NLRP3抑制剂MCC950处理也能抑制上述蛋白活化。此外,TNF-α或阿霉素(doxorubicin)处理APE1-KD细胞后,焦亡水平进一步升高;小分子化合物CRT处理也支持上述发现。
体内实验中,C57BL/6小鼠同种移植瘤模型显示:APE1-KD组肿瘤生长速率及终末体积均明显低于野生型组,而NLRP3敲低可逆转该抑制效应。血清ELISA检测显示,APE1-KD组小鼠IFN-γ水平升高,而NLRP3敲低后此效应消失;肿瘤组织中免疫细胞浸润增加(图1L–N)。B-NDG人源化小鼠模型中,APE1-KD联合人PBMC组呈现最小肿瘤体积、最高血清细胞因子水平及最显著的免疫细胞浸润;肿瘤组织中NLRP3、GSDME、cleaved caspase-3和cleaved caspase-8表达均上调。
3. 研究结论
本研究提示,APE1抑制可引起mtDNA损伤修复障碍,导致氧化型mtDNA释放入胞质,进而激活NLRP3-caspase-8-caspase-3-GSDME通路,最终诱导NSCLC细胞焦亡。焦亡过程中释放的炎症因子与趋化因子可促进T细胞浸润,增强抗肿瘤免疫应答。因此,APE1可作为NSCLC免疫治疗的潜在靶点,为联合免疫治疗策略提供理论依据。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304225003022
引用这篇文章:
Yang F, Long K, Qi Y, et al. APE1 inhibition-promoted pyroptosis triggers T-cell infiltration and enhances anti-tumor immunity in NSCLC. Genes Dis. 2026;13(4):101813.


