PD-L1高表达/TMB-H局部复发、化疗难治性骨未分化多形性肉瘤获益新辅助放疗联合帕博利珠单抗,获得完全缓解
时间:2026-05-05 13:05:14 热度:37.1℃ 作者:网络
骨未分化多形性肉瘤(UPS-B)是一种罕见的侵袭性癌症,在骨肉瘤中仅占很小的比例。与软组织未分化多形性肉瘤(UPS-ST)和骨肉瘤相比,骨未分化多形性肉瘤的化疗敏感性更低,预后也更差,据报道其五年生存率仅为 7.3%。尽管最佳治疗方案尚未明确,但标准治疗方案总体上参照了骨肉瘤的治疗方案,即手术、多药化疗和放疗。相比之下,靶向PD-1/PD-L1的免疫检查点抑制剂(ICIs)在软组织未分化多形性肉瘤中显示出了良好的活性,但在骨肉瘤中的疗效甚微,因此免疫检查点抑制剂在骨未分化多形性肉瘤中的作用在很大程度上仍不明确。本文报告一例 61 岁男性患者的病例,患有左侧髂骨复发性、化疗难治性骨未分化多形性肉瘤,在接受新辅助帕博利珠单抗联合放疗后再行手术切除,获得了完全且持久的缓解。该患者于2021年首次就诊时发现髂骨破坏性肿块,接受了多柔比星/顺铂诱导治疗,治疗期间并发急性肾损伤和血栓栓塞事件,随后接受了半骨盆切除术。术后四个月,患者出现局部复发,经活检证实。使用大剂量异环磷酰胺治疗未能实现持久的疾病控制,影像学检查显示肿瘤仍在进行性生长。分子检测显示其PD-L1表达率为 90%,存在包括SMARCA4和POLE在内的多种致癌突变,且突变特征符合高肿瘤突变负荷(TMB),提示其具有潜在的免疫原性。基于这些特征以及疾病进展情况,患者在术前接受了大分割放疗(15 次分割,总剂量 42.75 Gy),同时联合帕博利珠单抗治疗 3 个周期。2022 年 6 月手术切除的标本中未发现存活肿瘤,符合完全病理缓解的标准。患者随后完成了为期一年的帕博利珠单抗辅助治疗,目前仍在接受治疗,24个月随访时未发现复发迹象。
背 景
未分化多形性肉瘤(UPS)是一种高侵袭性癌症,可发生于软组织或骨骼,但骨未分化多形性肉瘤(UPS-B)远比软组织未分化多形性肉瘤(UPS-S)罕见,且预后更差。UPS-S与UPS-B之间的差异具有重要意义,这凸显了针对UPS具体类型制定个体化治疗方案的必要性。传统上,UPS-B的治疗方式与骨肉瘤等原发性骨肿瘤类似,采用手术联合包含甲氨蝶呤、顺铂和多柔比星的联合化疗方案,但UPS-B的最佳化疗方案仍不明确。需要注意的是,已有研究也指出UPS-B的化疗敏感性低于骨肉瘤。UPS-B患者的5年生存率约为 7.3%,远低于骨肉瘤的 77%。
免疫检查点抑制剂(ICIs)通过靶向PD-1/PD-L1通路增强机体对癌细胞的免疫应答,已经革新了多种癌症的治疗模式,但遗憾的是其在骨肉瘤中的疗效十分有限。不过,已有研究证实ICIs对晚期UPS-S有效:一项评估帕博利珠单抗在晚期肉瘤中安全性与疗效的研究显示,UPS-S对免疫治疗尤其敏感,客观缓解率达 23%,提示这类药物在该肉瘤亚型中具备应用潜力。有两项研究评估了新辅助免疫检查点抑制剂联合放疗(RT)治疗可手术切除UPS-S的效果:第一项是纳武利尤单抗(PD-1抑制剂)±伊匹木单抗(CTLA4抑制剂)的2期随机试验,在 10 例UPS-S患者中实现了 89% 的病理缓解率;第二项是SARC032随机试验,探索在3期软组织肉瘤(85% 的患者为UPS-S)的标准治疗(SOC)放疗基础上加用帕博利珠单抗的效果,结果显示2年无病生存率从 53% 显著提升至 70%。综上,这些研究结果表明免疫检查点抑制剂联合放疗治疗UPS-S的效果可能优于单药治疗,但该策略对UPS-B的疗效在很大程度上仍不明确。尤为值得关注的是,目前尚不清楚UPS-B对免疫检查点抑制剂的应答是与骨肉瘤相似,还是与UPS-S相似。本文报告一例局部复发性UPS-B患者,术前接受免疫检查点抑制剂联合放疗后获得了完全持久的缓解(图1)。
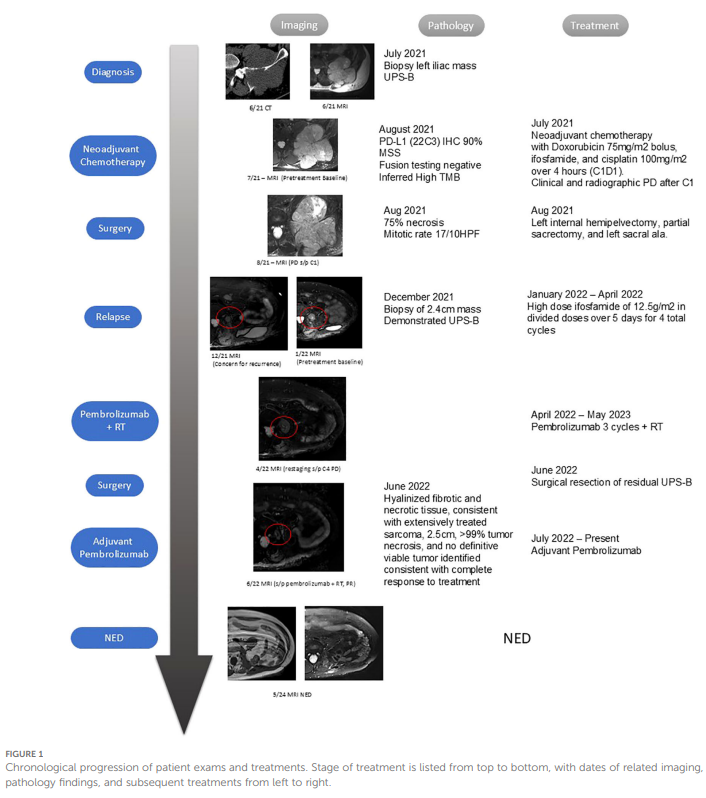
▲图1 患者检查和治疗的先后顺序
病 例
患者男,61 岁,既往病史包括骨关节炎、良性前列腺增生、已修补的食管裂孔疝、高血压、神经病变,以及存在 10 年的稳定肺结节,于 2021 年 2 月出现进行性左髋疼痛,随后在 2021 年 6 月很快发现左髋部可触及肿块。2021 年 6 月对该肿块进行影像学检查,显示左髂骨上部存在一巨大破坏性肿瘤,伴皮质破坏,软组织侵犯左侧腰大肌,肿瘤大小为 11.0×12.0×10 cm。2021 年 7 月对肿瘤进行活检,证实为骨未分化多形性肉瘤(UPS-B),镜下可见核分裂象为每高倍视野7个,且存在坏死灶(图2A)。
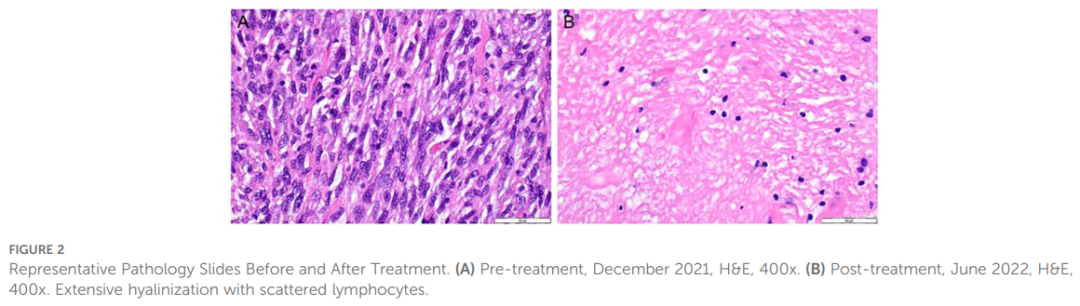
▲图2 治疗前后的代表性病理切片
通过下一代测序(NGS)对实体瘤进行基因检测,以GRCh37/hg19作为参考基因组进行变异识别。研究人员根据等位基因频率、预测致病性、癌症相关性注释以及是否存在于致癌通路中对变异进行优先级排序。拷贝数变异通过基于NGS的计算性CNV算法进行评估。活检标本的DNA检测报告显示,多个致癌基因和抑癌基因存在错义突变,包括ARID1A、ATR、AXL、BRAF、CDKN2A、CHEK1、ERBB2、EZH2、FANCA、FBXW7、FGFR2、NBN、NF1、NTRK3、POLE、RAC1、ROS1、SMARCA4、STK11、TERT、TP53和TSC1。由于缺乏胚系DNA用于比对,因此这些检出的变异被定义为肿瘤特异性变异,而非明确的体细胞变异。基于NGS检测结果,致癌通路上存在大量肿瘤特异性变异,提示肿瘤突变负荷相对较高,这可能与肿瘤免疫原性增强相关(表1)。免疫组化结果显示,错配修复蛋白MLH1、MSH2、MSH6和PMS2均保留核表达,符合错配修复功能完整的特征(图3)。使用22C3单抗克隆进行PD-L1免疫组化检测,结果显示肿瘤比例评分为 90%,即 90% 的存活肿瘤细胞存在膜染色。NY-ESO-1免疫组化结果为阴性,未观察到肿瘤细胞标记(0%)(数据未展示)。
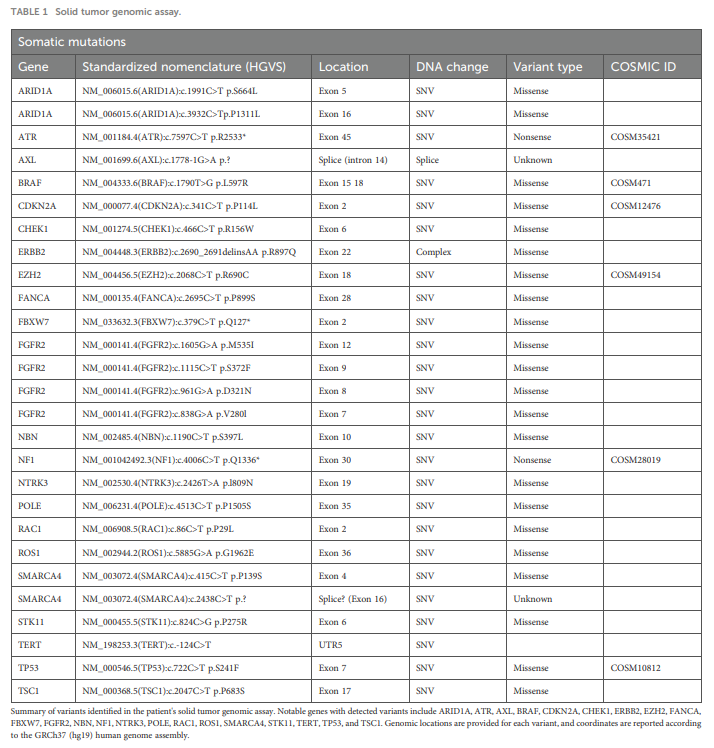
▲表1 实体瘤基因检测
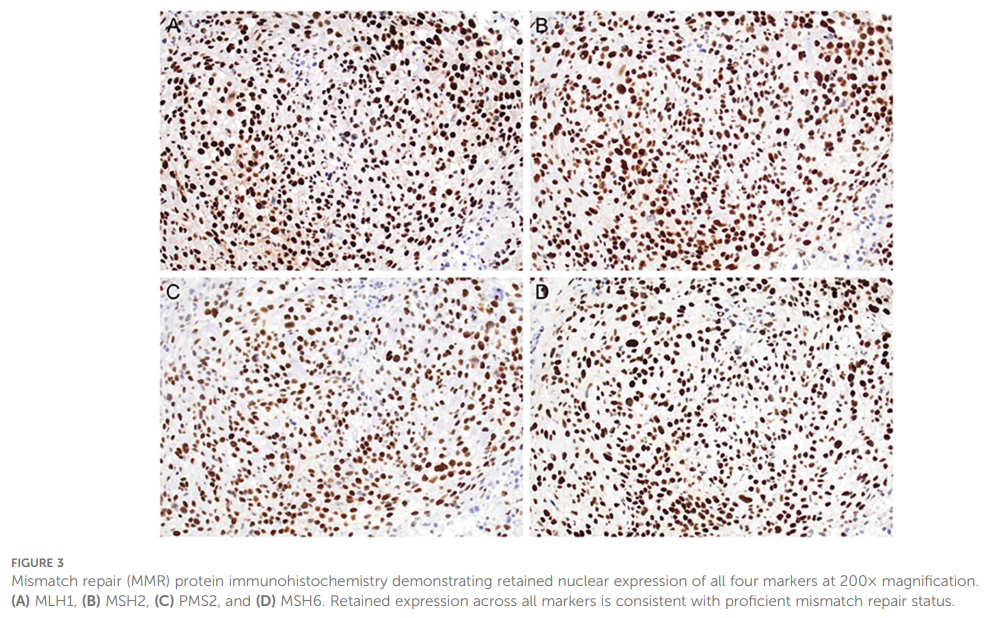
▲图3 错配修复(MMR)蛋白免疫组化染色显示,在 200 倍放大倍率下,所有四种标记物均保留了核表达
多学科团队建议该患者参照骨肉瘤方案接受新辅助化疗。2021 年 7 月(第 1 周期第 1 天),患者住院接受多柔比星 75 mg/m²注射、右丙亚胺治疗,同时输注顺铂 100 mg/m²,输注时长 4 小时。但初始治疗方案受急性肾损伤影响而复杂化,患者肌酐从 0.91 mg/dl升至 2.91 mg/dl。2021 年 8 月,患者出现右锁骨下静脉多发血栓栓塞及肺栓塞。第 1 周期治疗后,患者自述肿块增大,2021 年 8 月的MRI检查证实了这一点,显示肿块大小为 15.5×14.3×12 cm。因此化疗于 2021 年 8 月终止,患者于 2021 年 8 月接受手术切除,术式为左内侧半骨盆切除术、部分骶骨切除术及左侧骶骨翼切除术。术后并发症包括上肢无力(短暂性脑缺血发作)和手术部位感染,需对左侧盆腔及腹部胁腹进行清创和冲洗。此外,针对手术部位感染,患者接受了长期抗生素治疗,以处理作为盆腔脓肿来源的甲氧西林敏感金黄色葡萄球菌(MSSA)菌血症。2021 年 12 月,即术后 4 个月,盆腔MRI显示切除部位内侧边缘、右侧骶骨翼上外侧截骨术相邻区域存在一处 1.8×1.6 cm的软组织病变,高度提示疾病复发(图1标注为UPS-B复发)。2021 年 12 月行活检,证实为UPS复发。2022 年 1 月的再分期影像学检查显示肿瘤体积较前增大,现为 2.4×2 cm。2022 年 1 月至 2 月,参照骨肉瘤治疗方案,患者接受了大剂量异环磷酰胺治疗,总剂量 12.5 g/m²,分 5 天给药。第 2 周期治疗后,MRI影像学评估显示肿瘤大小稳定,因此继续该治疗方案。但第 4 周期治疗后的影像学检查显示肿瘤从之前的 2.7 cm增大至 3.4 cm。由于疾病进展,该治疗方案于 2022 年 4 月终止,建议患者术前行放疗后再接受手术。鉴于该患者的分子生物学特征提示治疗获益可能性较高(高TMB、PD-L1表达90%、存在SMARCA4和POLE基因突变)、此前全身化疗后出现疾病进展,同时结合显示帕博利珠单抗对UPS-S有效的SARC028研究数据,以及纳武利尤单抗联合伊匹木单抗同步放疗治疗UPS-S有效的既往经验,建议患者于 2022 年 4 月至 5 月期间接受放疗,同步联合帕博利珠单抗治疗 3 个周期。患者对该治疗方案耐受性良好,未出现任何不良反应。2022 年 6 月,患者接受了最终手术切除。最终病理显示存在透明样变的纤维化和坏死组织,符合经充分治疗的肉瘤表现,病灶大小 2.5 cm,肿瘤坏死率 >99%,未发现明确存活肿瘤,符合治疗后完全缓解的判定标准(图2B)。患者继续接受帕博利珠单抗辅助治疗,完成了为期 1 年的治疗。在此期间,2023 年 1 月患者左上背部出现轻度皮疹,使用外用类固醇乳膏治疗(1 级不良反应)。2023 年 5 月,患者开始术后帕博利珠单抗治疗。截至 2024 年 5 月最后一次随访,患者仍在接受帕博利珠单抗治疗,无疾病复发迹象。
讨 论
本文患者的预期之外反应对UPS-B的常规治疗方法提出了一个问题:是否应该开始将UPS-B视为像UPS-S一样的免疫敏感型肿瘤?这种显著的病理缓解可能源于免疫检查点抑制剂(ICI)与放疗的联合应用,此前一项评估新辅助ICI联合放疗治疗UPS和去分化脂肪肉瘤(DDLPS)患者的研究显示,UPS-S患者的中位病理缓解率(89%)远高于DDLPS患者(22.5%),且无病生存率有所提升。近期SARC032研究证实了放疗与ICI在局限性UPS-S患者中的协同作用,显示出无病生存率的明确获益。然而,尽管UPS-S患者中观察到了良好应答,但仍有部分UPS-S患者对ICI耐药,且目前缺乏可靠的疗效预测生物标志物。在本病例中,鉴于患者的组织学类型为UPS,且其他参照骨肉瘤的标准治疗化疗方案均失败,因此选择了放疗同步帕博利珠单抗治疗。
具体而言,该患者的肿瘤携带SMARCA4、POLE和STK11致癌突变,这些突变已被证实与ICI应答相关。此外,通过有限的NGS靶向面板检测发现该肿瘤存在大量突变,提示高TMB,而高TMB在多种癌症类型中均与ICI应答相关。但目前肉瘤中ICI应答的生物标志物尚未明确,由于缺乏能够准确预测ICI应答的明确指标,患者选择存在普遍不确定性,导致治疗疗效有限。
尽管骨肉瘤存在炎症性肿瘤微环境,但矛盾的是其对ICI应答不佳,这提示骨肉瘤亚型之间的免疫敏感性存在差异,也凸显了需要进一步研究来理解这些差异。生物标志物对于靶向并克服肉瘤的低免疫原性和治疗耐药性至关重要。近期肉瘤领域的研究表明,肿瘤中三级淋巴结构(TLS)的存在与ICI治疗的更佳应答相关。在一项评估帕博利珠单抗联合低剂量环磷酰胺治疗晚期肉瘤的2期试验(PEMBROSARC试验)中,通过专门筛选存在TLS的患者,试验达到了 6 个月无进展率(NPR)的主要终点(NPR为 40%),客观缓解率整体提升(从 2.4% 升至 30%),中位无进展生存期为 4.1 个月。这些发现与本病例的关联在于,提示存在TLS或高度炎症表型的UPS-B肿瘤可能表现出更佳的ICI应答性。
本研究的局限性包括其仅为单病例报告,且未直接评估TLS或免疫浸润情况。未来的研究应纳入UPS-B的免疫谱分析和多组学分析,以识别ICI应答的预测生物标志物。此外,有必要开展前瞻性研究评估放疗联合ICI治疗UPS-B的疗效。
参考文献:
Patel BA, Smith JT, Wangsiricharoen S, Wang W-L, Lin PP, Farooqi A, Nassif Haddad EF, Ummed K, Mericli AF, Adelman DM, Livingston JA and Conley AP (2026) Case Report: Complete response to the concurrent neoadjuvant radiation therapy and pembrolizumab in a locally recurrent, chemotherapy-refractory undifferentiated pleomorphic sarcoma of bone. Front. Oncol. 16:1645629. doi: 10.3389/fonc.2026.1645629


