Cell:颠覆性发现,阿尔茨海默病竟是“大脑癌症”?
时间:2026-05-05 13:05:16 热度:37.1℃ 作者:网络
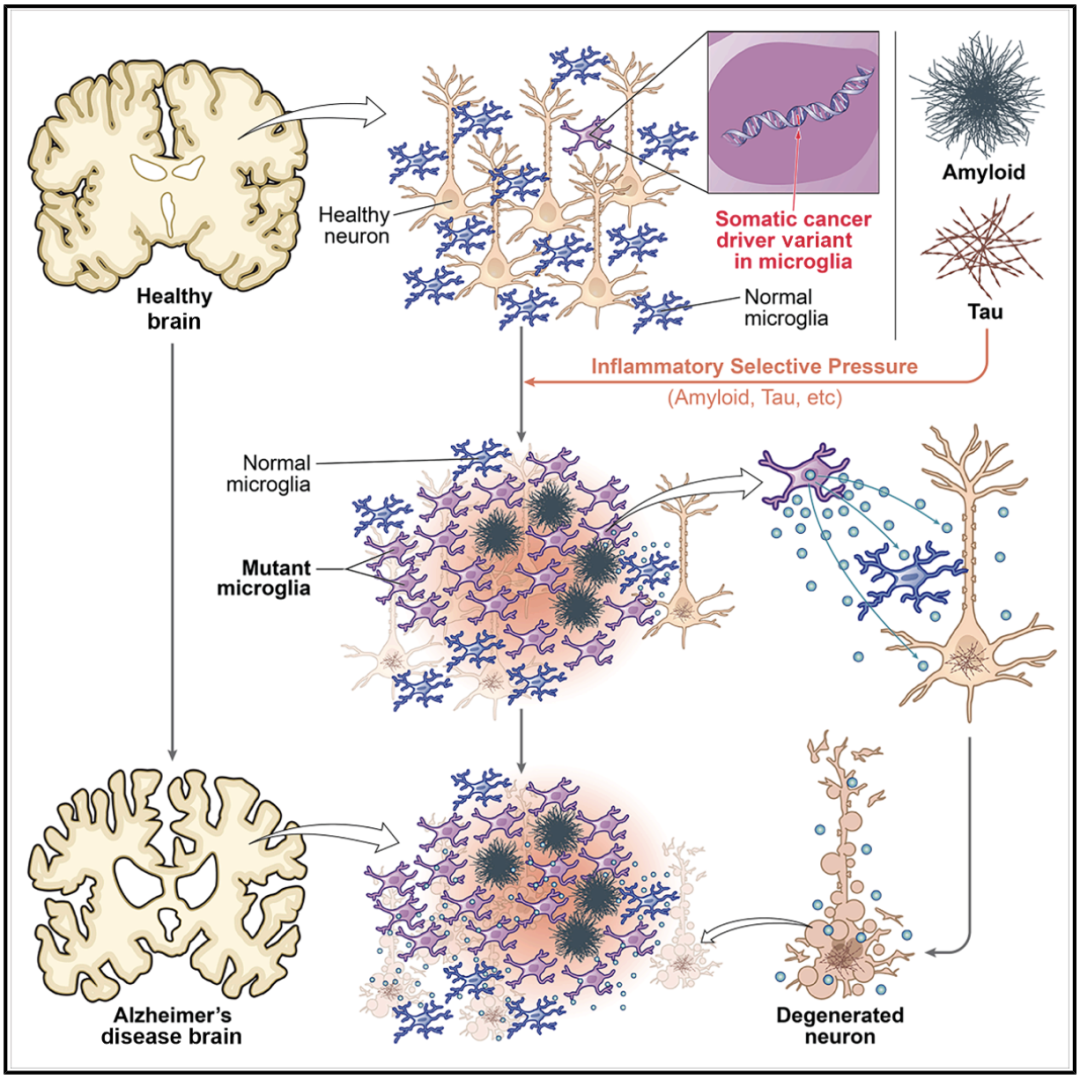
想象一下,大脑的免疫卫士——小胶质细胞,在巡逻时发生了“叛变”。它们不再保护神经元,反而开始释放炎症因子,攻击自己本该守护的“家园”。更令人惊讶的是,驱动这场“叛变”的基因突变,竟与白血病等癌症中发现的驱动突变高度相似。
2026年4月,国际顶级期刊《细胞》发表了一项由哈佛医学院波士顿儿童医院黄岳教授团队领衔的突破性研究。这项研究揭示,在阿尔茨海默病患者的大脑中,一类特殊的免疫细胞里富集了典型的癌症驱动基因突变。这些突变像“开关”一样,激活了细胞的炎症和增殖程序,可能加速了神经元的死亡和认知功能的衰退。这为理解阿尔茨海默病的复杂机制,打开了一扇全新的窗口。

02 研究背景
阿尔茨海默病,这种最常见的神经退行性疾病,传统上被认为主要由大脑中β-淀粉样蛋白的异常沉积和tau蛋白的神经纤维缠结所驱动。数十年来,全球绝大多数药物研发都聚焦于清除这些异常蛋白。然而,临床结果令人沮丧:绝大多数针对这些靶点的药物试验均告失败,少数获批的药物也只能带来非常有限的症状改善,且常伴有明显的副作用。
这迫使科学家们思考:除了淀粉样蛋白和tau蛋白,是否还有其他被忽略的关键“推手”?
近年来,大脑的固有免疫细胞——小胶质细胞,在阿尔茨海默病中的作用日益受到重视。在健康大脑中,小胶质细胞负责清除代谢废物、修剪多余的神经连接、抵御病原体入侵。但在阿尔茨海默病患者的大脑中,它们变得异常活跃,呈现出一种“疾病相关”的状态。这种过度激活的免疫反应,非但无益,反而可能“误伤”健康的神经元和突触,加剧病理进程。
与此同时,另一个领域的发现引起了神经科学家的注意:在衰老过程中,人体造血干细胞会积累一些体细胞突变。其中一些突变会赋予细胞生长优势,导致携带该突变的血细胞克隆性扩增,这种现象被称为“克隆性造血”。它不仅是血液肿瘤的前兆,其产生的突变免疫细胞所释放的炎症因子,还与心血管疾病等全身性衰老疾病风险增加相关。
一个大胆的猜想由此产生:这些在血液中发生的、与癌症相关的克隆性突变,是否会“潜入”大脑,影响那里的免疫细胞,从而参与阿尔茨海默病的发生?黄岳团队的研究,正是为了验证这一假说。
03 研究设计
要在大脑数以百亿计的细胞中,找到那些可能只存在于极少数细胞中的低频基因突变,无异于大海捞针。传统测序技术的深度有限,难以捕捉这些“暗藏”的变异。
为此,研究团队采用了革命性的技术组合。他们对311例阿尔茨海默病患者和健康对照者捐献的前额叶皮层脑组织样本,进行了平均深度超过1000倍的超深度靶向测序。这项技术结合了“唯一分子标识符”,能够极大降低测序错误,精准识别出突变频率低至0.1%的体细胞单核苷酸变异。这就像为研究者配备了一台“超高清数字显微镜”。
锁定突变后,下一个关键问题是:这些突变藏在哪种细胞里?研究团队利用荧光激活核分选技术,将大脑组织中的不同细胞类型(如神经元、小胶质细胞等)精确地分离开来,然后分别检测它们的基因突变情况。
为了在单细胞水平上同时看清“基因型”(细胞携带什么突变)和“表型”(细胞处于什么状态),团队采用了前沿的单细胞多组学技术。最后,他们使用基因编辑技术在实验室培养的诱导多能干细胞来源的小胶质样细胞中,引入特定的癌症驱动突变,以直接验证这些突变是否足以驱动细胞的病理改变。
04 研究结果
通过这一系列精密的设计,研究得到了几个层层递进的核心发现。
突变显著富集于患者大脑
分析显示,与年龄匹配的健康对照者相比,阿尔茨海默病患者大脑组织中,在TET2、ASXL1、DNMT3A等关键基因上携带的体细胞突变负担显著更高。这些基因都是著名的“肿瘤抑制基因”,它们的失活突变在白血病等血液肿瘤和克隆性造血中非常常见。特别值得注意的是,在AD患者中,TET2基因的突变集中发生在对其功能至关重要的催化结构域,这种模式与克隆性造血中观察到的完全一致。
突变高度集中于特定免疫细胞
这些突变并非随机分布,而是高度集中在特定的免疫细胞中。 细胞分选的结果指向了一类被称为“小胶质细胞样脑巨噬细胞”的细胞。与同一大脑样本中的神经元相比,突变在这些免疫细胞中的富集程度高出2到438倍。进一步的区域分析发现,这些突变细胞遍布大脑皮层和小脑。一个更关键的线索是:所有在大脑这些免疫细胞中发现的突变,都能在同一个体匹配的血液DNA样本中检测到。这强烈暗示,这些细胞很可能并非大脑“原住民”,而是来源于血液中的单核细胞。它们通过可能受损的血脑屏障进入大脑,并“伪装”成了小胶质细胞的样子。
突变细胞发生克隆性扩张
这些突变细胞获得了生长优势,并在大脑中“克隆性扩张”。 进化生物学分析显示,这些突变在阿尔茨海默病患者大脑中经历了比对照组更强的“正向选择”。这意味着,在AD大脑的特殊微环境下,携带这些突变的免疫细胞比正常细胞活得更好、增殖得更快,像肿瘤细胞一样形成了优势克隆。
突变直接驱动病理状态
最后,也是最重要的一点,这些突变直接驱动了细胞的病理状态。 单细胞多组学分析显示,携带突变的小胶质样细胞,其基因表达谱显著富集于“疾病相关小胶质细胞”状态。这是一种已知与神经退行密切相关的促炎、有害状态。为了证明是突变本身导致了这种变化,研究团队在实验室中,用基因编辑技术让人工培育的小胶质样细胞携带了TET2或ASXL1突变。结果,这些突变细胞自发地转向了促炎状态,其代谢模式也从正常的有氧呼吸转向了类似癌细胞的“糖酵解”模式,并持续分泌白细胞介素-1β等促炎因子。
05 连接血液与大脑,为阿尔茨海默病防治开辟新路
这项研究的意义,远不止于报告一个新现象。它在阿尔茨海默病和血液系统疾病这两个看似遥远的领域之间,架起了一座分子桥梁。
提供全新的疾病机制解释
研究首次在单细胞水平证明,来源于外周血液的、携带癌症驱动突变的免疫细胞,可以浸润大脑,并通过克隆性扩张和促炎转化,直接加剧阿尔茨海默病的神经炎症和损伤。这一机制独立于APOE4等传统遗传风险因素,为那些没有家族史的患者提供了新的病因学解释。
带来全新的诊疗可能性
首先,血液中这些突变的检测,未来或许能成为一种预警或辅助诊断阿尔茨海默病的生物标志物。其次,也是最令人期待的,是治疗策略的启示。既然驱动病变的是一群发生了“类癌变”的免疫细胞克隆,那么,借鉴癌症或克隆性造血的治疗思路,开发能够特异性清除这些突变细胞克隆,或阻断其促炎通路的药物,就可能成为遏制阿尔茨海默病神经炎症的全新疗法。
当然,这项研究也留下了许多有待解答的问题。例如,这些突变细胞是如何精确促进神经元死亡的?它们与淀粉样蛋白、tau蛋白病理之间如何相互作用?针对这一通路的干预,在疾病哪个阶段最有效?
无论如何,这项研究深刻地提醒我们,大脑并非一个与世隔绝的“孤岛”。全身性的衰老和病变,特别是免疫系统的异常,会以我们意想不到的方式影响大脑健康。对抗阿尔茨海默病这场漫长的战役,或许需要我们将目光从大脑内的蛋白质沉积,更多地投向血液与大脑之间动态的免疫对话。
参考文献:
Huang AY, Zhou Z, Talukdar M, et al. Somatic cancer variants enriched in Alzheimer's disease microglia-like cells drive inflammatory and proliferative states. Cell. 2026. DOI: 10.1016/j.cell.2026.03.040.
Huang AY, Zhou Z, Talukdar M, et al. Somatic cancer variants enriched in Alzheimer's disease microglia-like cells drive inflammatory and proliferative states. Cell . 2026. DOI: 10.1016/j.cell.2026.03.040.


