四川大学ACS Nano综述:靶向蛋白降解与递送策略在神经系统疾病中的应用
时间:2026-05-05 17:04:26 热度:37.1℃ 作者:网络
背景介绍
神经系统疾病已成为全球范围内导致死亡和残疾的首要原因。根据2021年全球疾病负担研究,这些疾病影响了34亿人,造成4.43亿伤残调整寿命年(DALYs)和1110万例死亡。从阿尔茨海默病、帕金森病到胶质母细胞瘤,神经疾病的共同病理特征包括毒性蛋白聚集、错误折叠蛋白的异常积累以及致病蛋白的功能获得性突变。传统小分子抑制剂依赖于“占位驱动”机制,往往受限于靶点缺乏可药性口袋、药物耐受和脱靶毒性。因此,迫切需要能够从根本上清除致病蛋白的全新治疗策略。
研究思路
针对上述挑战,四川大学华西药学院高会乐教授和童凡研究员团队系统梳理了靶向蛋白降解(TPD)技术在神经系统疾病中的最新进展。TPD利用细胞内泛素-蛋白酶体系统、内体-溶酶体途径或自噬-溶酶体途径,实现“事件驱动”的不可逆蛋白清除。文章详细论述了PROTACs、分子胶、双机制降解剂、LYTACs、双特异性适配体嵌合体、AbTACs、GlueTACs、AUTACs、ATTECs、AUTOTACs以及基于分子伴侣介导自噬的降解剂等多种TPD策略及其在脑疾病中的应用。然而,TPD分子自身存在分子量大、极性表面积高、构象柔性大等药理学缺陷,而血脑屏障(BBB)、脑组织间隙的物理阻挡以及细胞内吞后分选障碍,严重限制了其脑内递送效率。为此,文章重点介绍了如何将TPD与脂质体、聚合物纳米粒、仿生膜囊泡、DNA纳米花等药物递送系统(DDS)相结合,通过合理的载体设计(如受体靶向修饰、刺激响应释放、仿生伪装等),显著改善TPD分子的药代动力学、BBB穿透能力和病灶区特异性,从而克服神经药物开发的瓶颈。相关内容以Targeted Protein Degradation and Delivery Strategies in the Context of Neurological Disorders为题,发表在ACS Nano!

图片解析
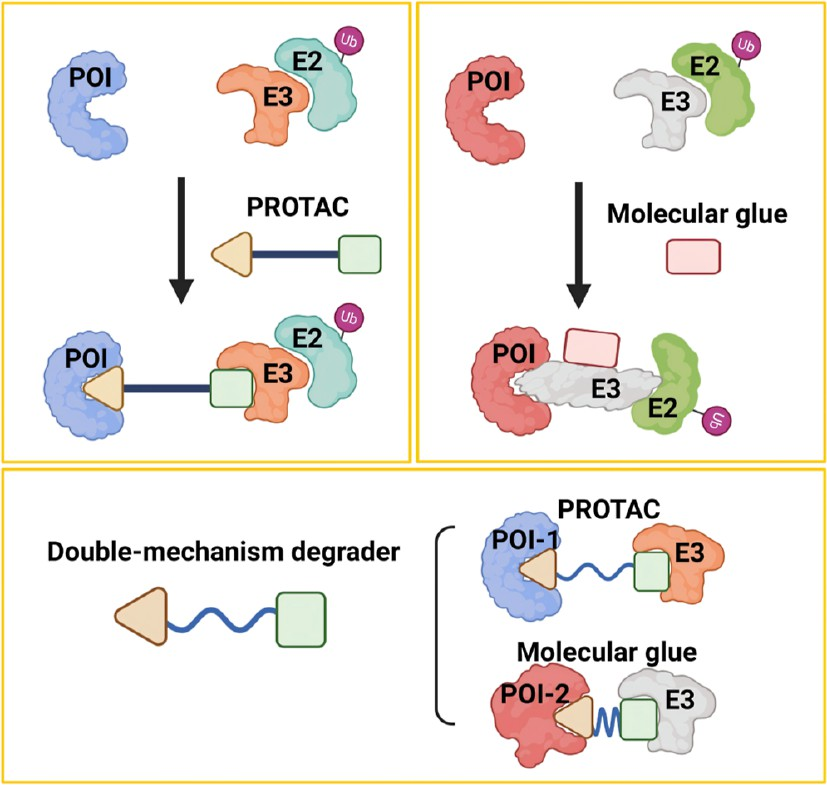
图1. PROTAC、分子胶和双机制降解剂的示意图: (A) PROTAC:双功能分子,一端结合靶蛋白,另一端结合E3泛素连接酶(如VHL、CRBN),诱导靶蛋白泛素化并被蛋白酶体降解。(B) 分子胶:单功能小分子,通过稳定E3连接酶与靶蛋白的相互作用,促进靶蛋白泛素化。(C) 双机制降解剂:同时具有酶抑制和靶蛋白降解功能,或协同利用蛋白酶体和自噬途径。
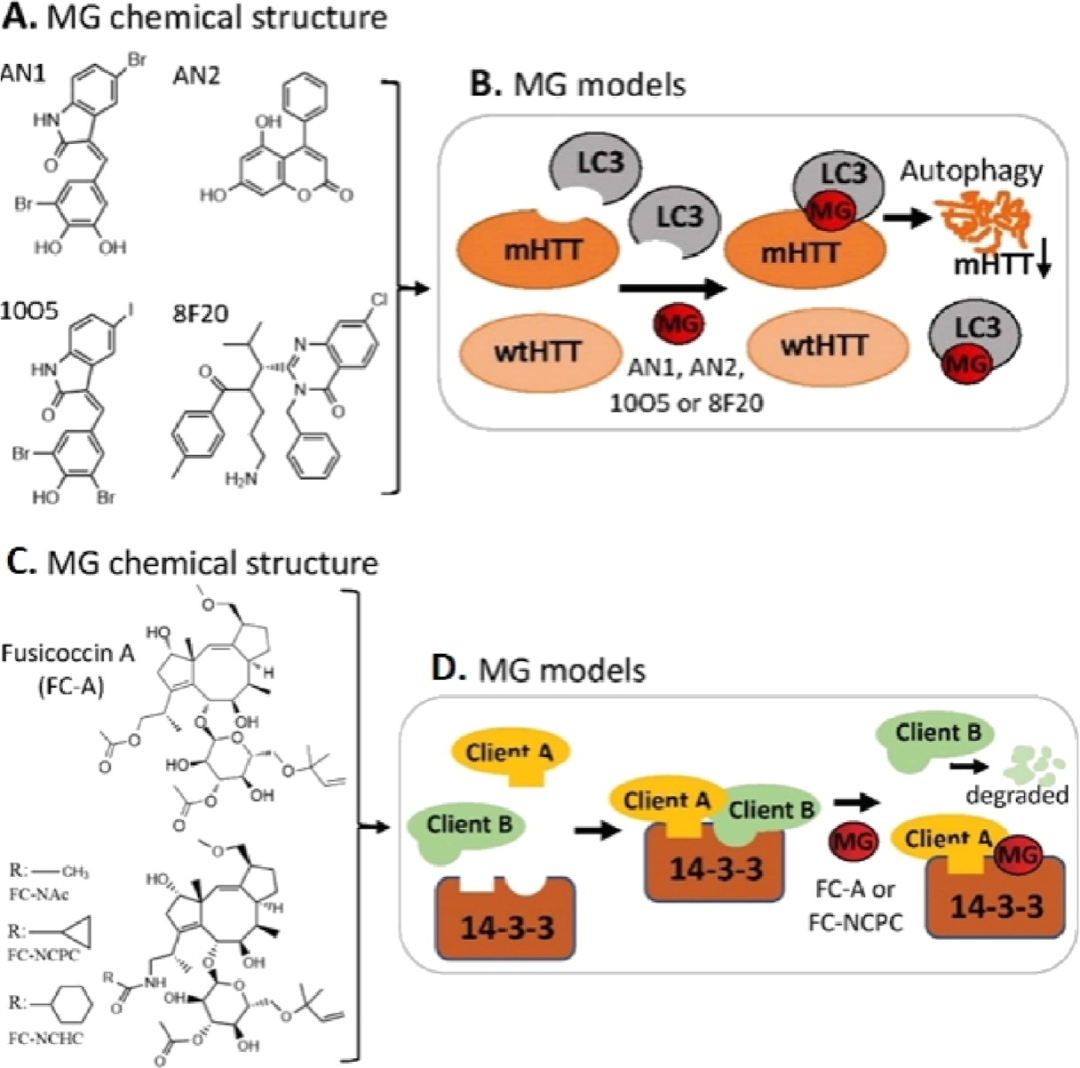
图2. 自噬靶向分子胶(ATTEC)的作用机制及代表性化合物: (A) AN1、AN2、100S、8F20等分子胶的化学结构。(B) 这些分子胶选择性促进LC3与突变型亨廷顿蛋白(mHTT)结合,而不影响野生型HTT,通过自噬-溶酶体途径降解mHTT。(C) 梭链孢酸A(FC-A)及其衍生物FC-NAC、FC-NCPC、FC-NCHC的化学结构。(D) 该类分子胶能够增强某些14-3-3客户蛋白的结合,同时破坏其他相互作用,调节神经突起生长。
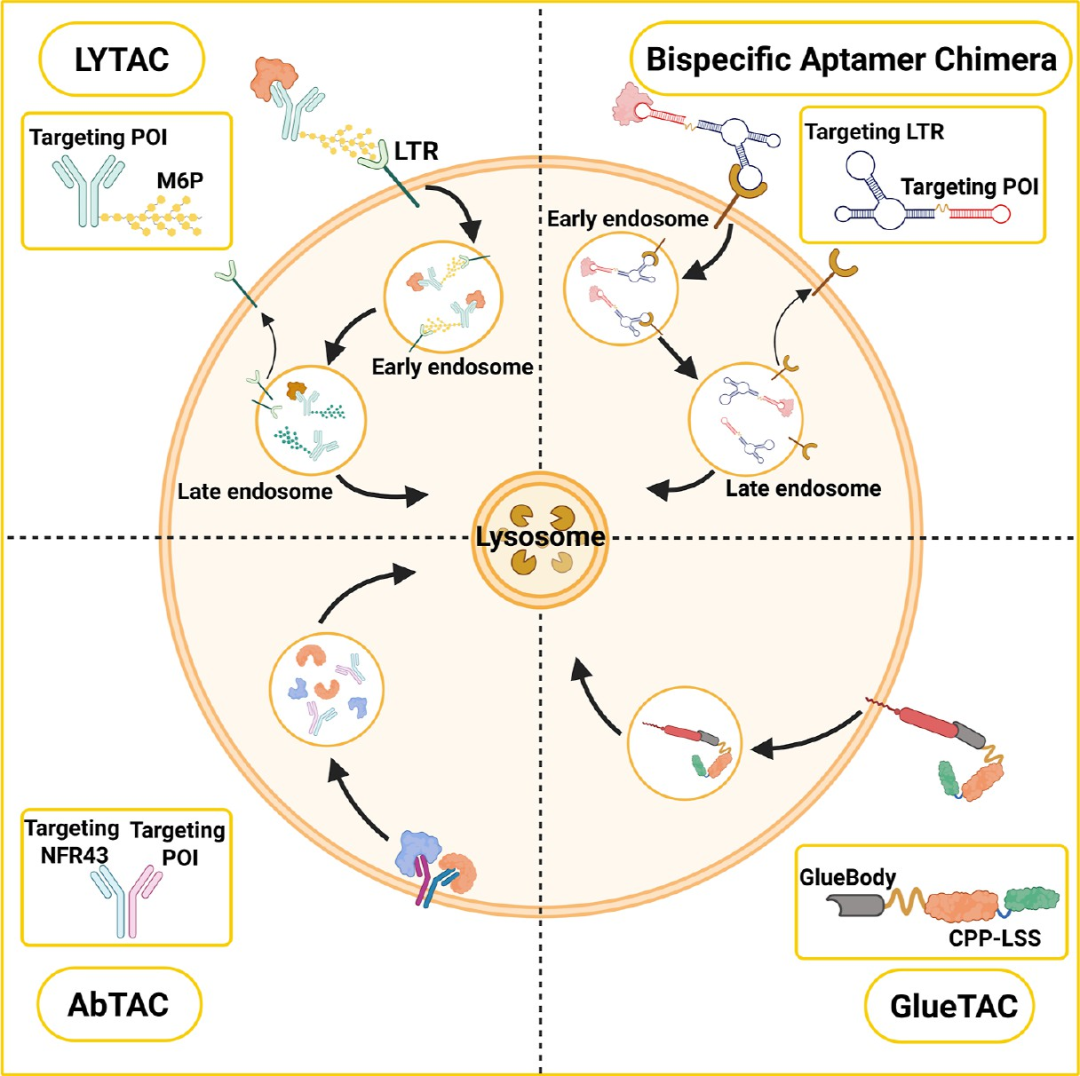
图3. 内体-溶酶体依赖性蛋白降解策略总结: 包括LYTACs(通过甘露糖-6-磷酸受体或去唾液酸糖蛋白受体介导内吞)、双特异性适配体嵌合体(核酸适配体靶向溶酶体穿梭受体和膜蛋白)、AbTACs(双特异性抗体同时靶向膜蛋白和跨膜E3连接酶RNF43/ZNRF3)以及GlueTACs(纳米抗体融合细胞穿膜肽和溶酶体分选信号肽),这些策略均将膜蛋白或胞外蛋白引导至溶酶体降解。
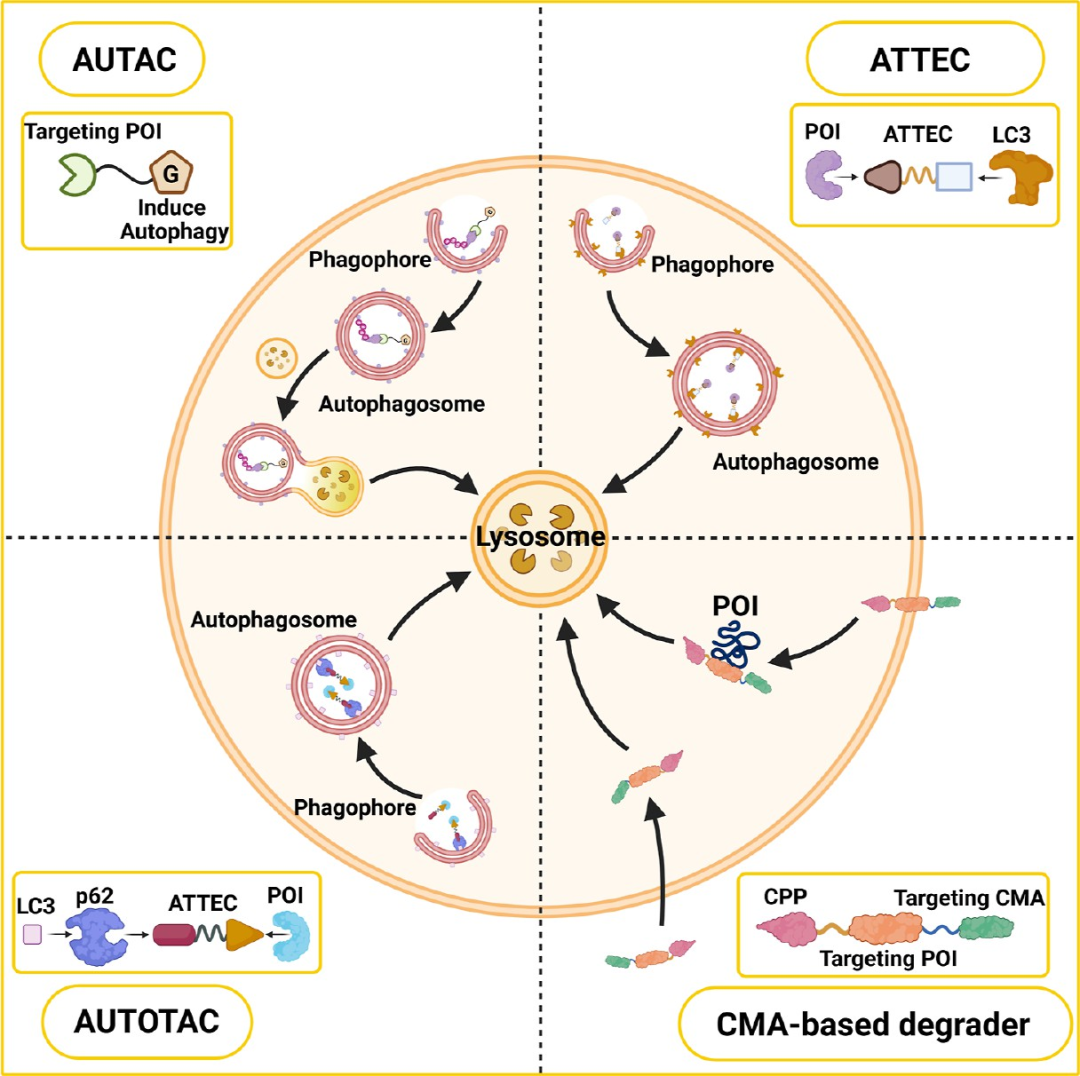
图4. 自噬-溶酶体依赖性蛋白降解策略总结: 包括AUTACs(通过S-鸟苷化引发K63-泛素链,被p62/LC3识别后进入自噬)、ATTECs(直接结合LC3和靶蛋白)、AUTOTACs(结合并激活p62,诱导靶蛋白-p62寡聚体形成)以及CMA基降解剂(利用HSC70识别KFERQ基序、LAMP2A介导的分子伴侣介导自噬)。这些策略能够清除蛋白聚集体、线粒体、脂滴等大尺度底物。
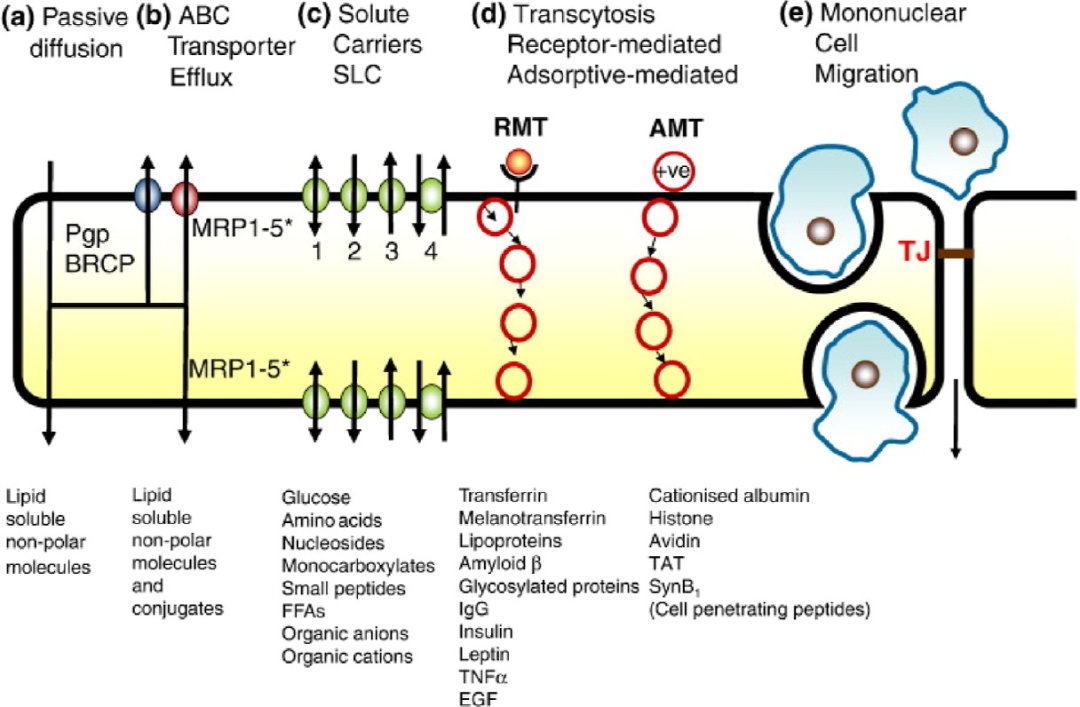
图5. 物质跨血脑屏障(BBB)的多种转运途径示意图: 包括被动扩散(小分子亲脂性药物)、载体介导转运(如葡萄糖、氨基酸转运体)、受体介导的胞吞(如转铁蛋白受体、LDL受体)、吸附介导的胞吞(阳离子蛋白)以及细胞旁路扩散(紧密连接)。大多数TPD分子因尺寸和极性过高,主要依赖受体介导的胞吞转运。
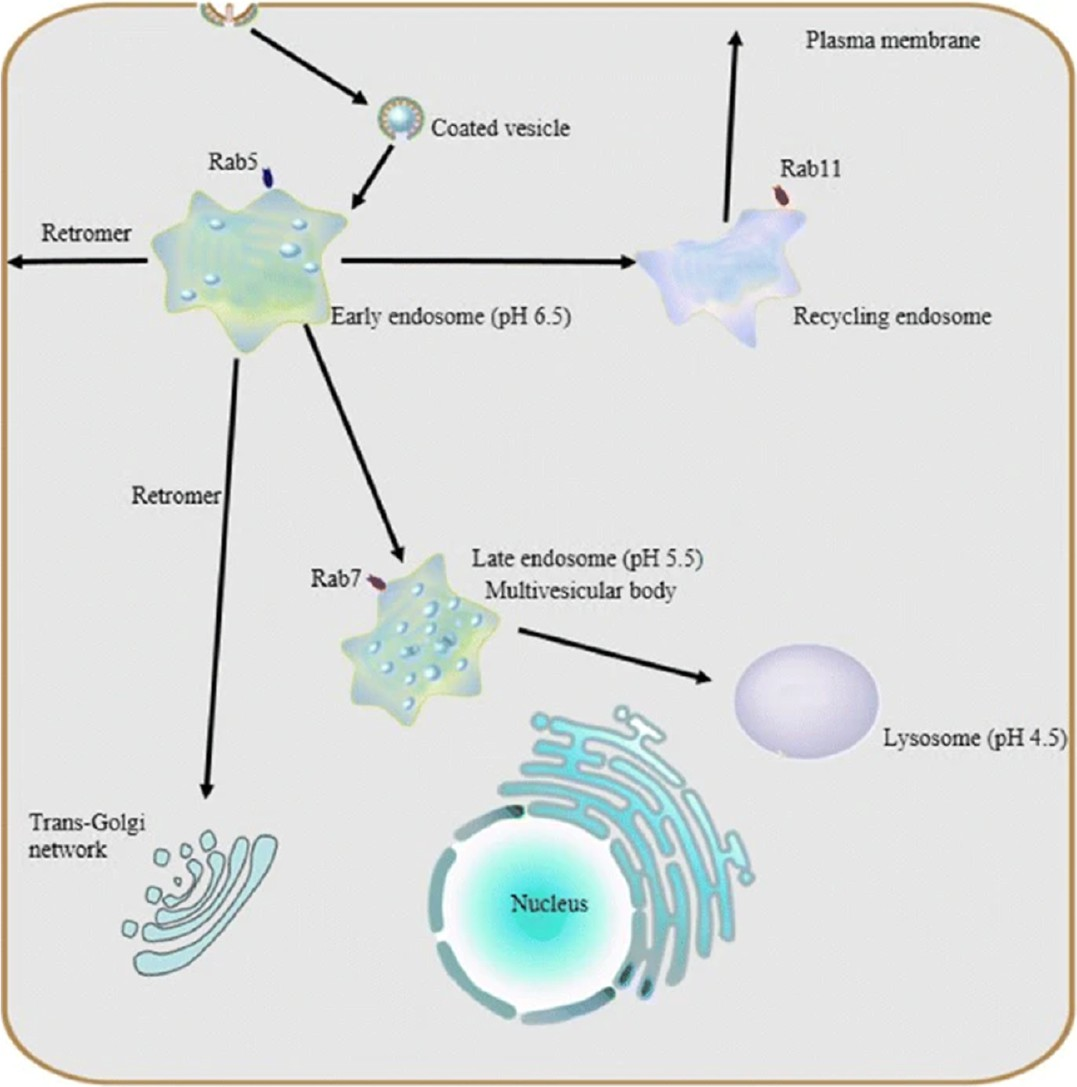
图6. 内吞运输途径及细胞器成熟过程示意图: 早期内体作为分选枢纽,可将内化物导向循环(回收至质膜)、逆行运输(至高尔基体)或降解途径(形成多泡体,最终与溶酶体融合)。TPD分子在内体中若被过早分选至循环途径将降低递送效率,若滞留在内体并被分选进入腔内囊泡则会进入溶酶体降解。
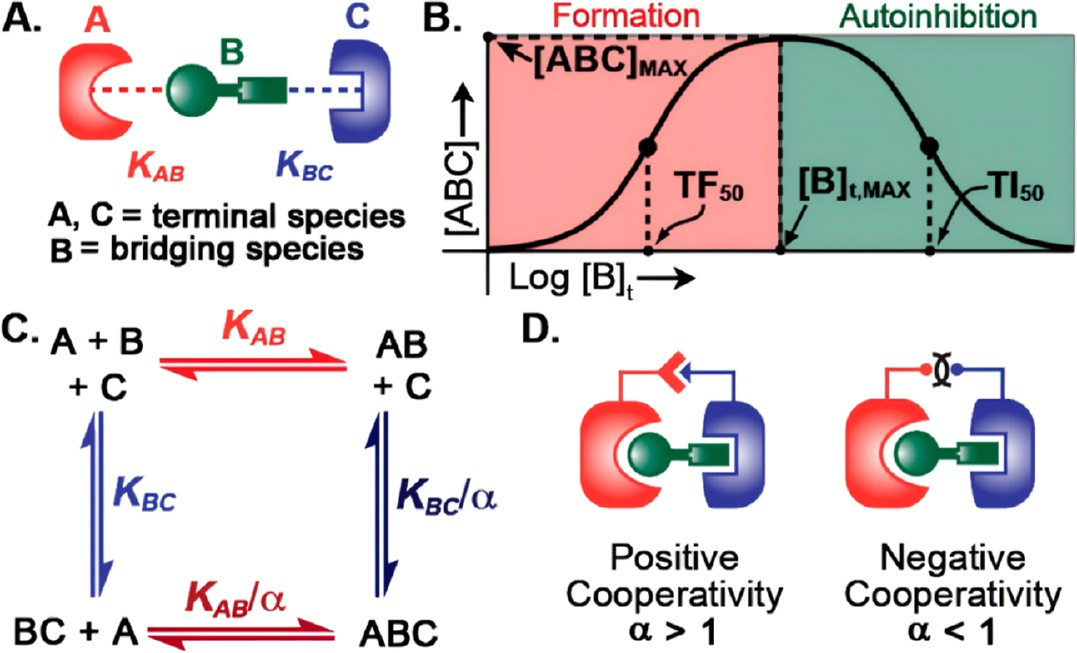
图7. 小分子诱导三元复合物形成的热力学循环和钩效应: 当降解剂浓度过高时,倾向于形成非功能的二元复合物(降解剂-靶蛋白或降解剂-E3连接酶),而非功能性的三元复合物(靶蛋白-降解剂-E3连接酶),导致降解效率随浓度升高而下降,呈现钟形浓度-响应曲线。纳米递送系统可通过控释将局部浓度维持在最佳窗口内。
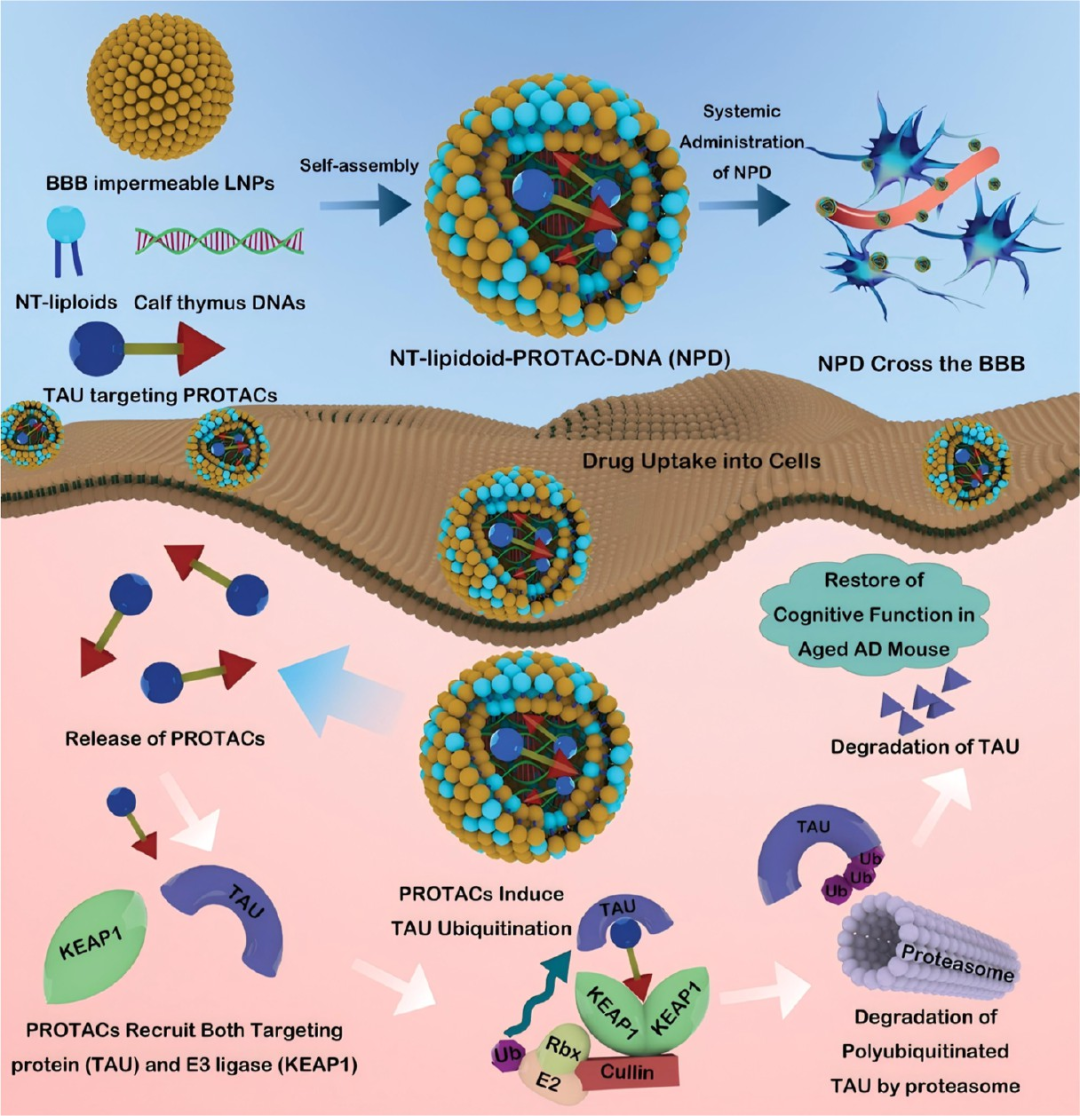
图8. 神经递质衍生脂质-PROTACs-DNA纳米复合物(NPD)的制备及其在AD治疗中的应用: (A) NPD的合成示意图:将阳离子PROTAC肽通过静电作用锚定在DNA上,再包裹以神经递质衍生脂质作为功能性载体。(B) NPD经静脉注射后主动穿越BBB,在脑内释放PROTAC,实现病理p-tau的有效清除(清除率达66%,而游离PROTAC仅23%)。
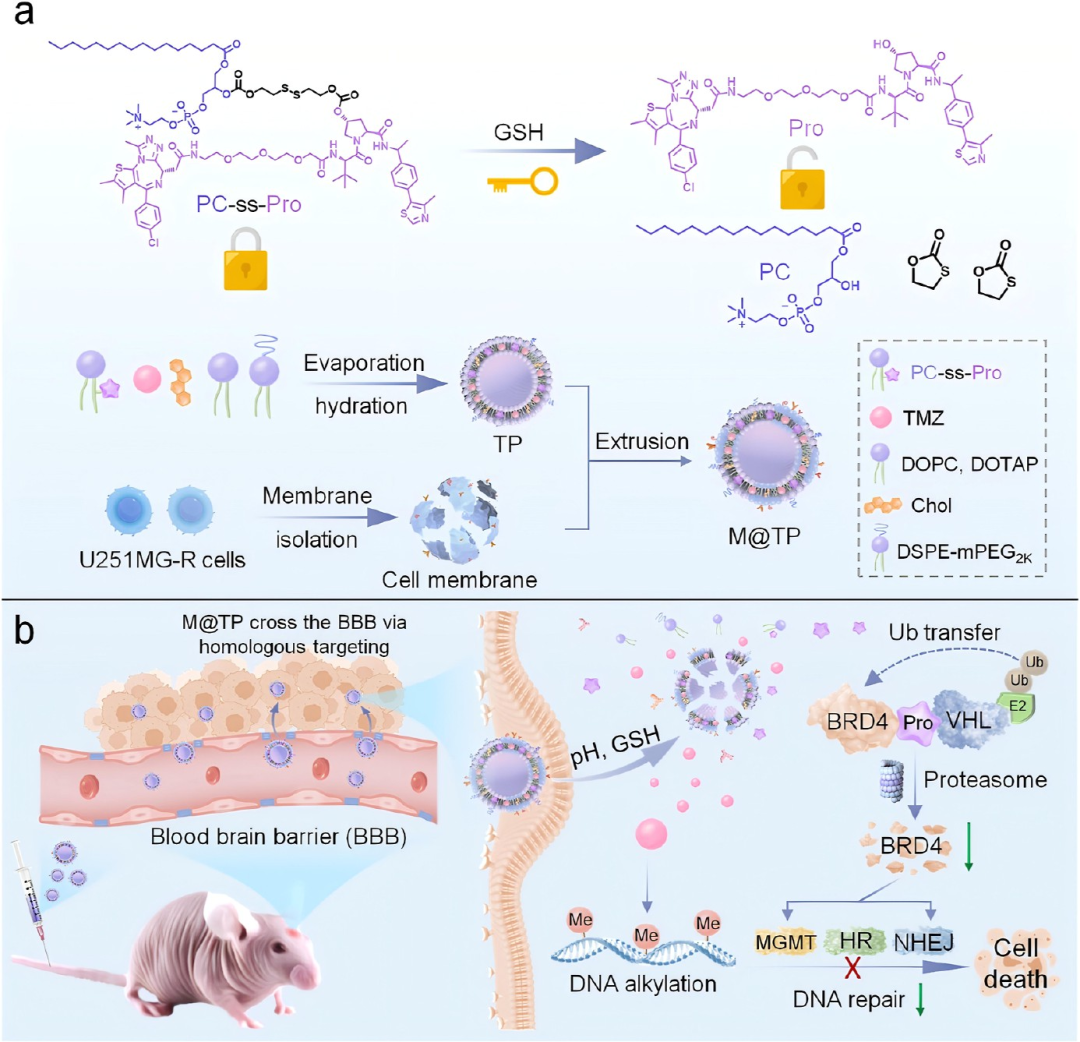
图9. 仿生杂化脂质体系统(M@TP)的设计与抗胶质母细胞瘤机制: (a) 二硫键连接的BRD4 PROTAC前药与替莫唑胺共包封于脂质核心,表面包被胶质母细胞瘤细胞膜,实现同型靶向和免疫逃逸。(b) M@TP通过BRD4降解阻断多种DNA修复通路,逆转替莫唑胺耐药。
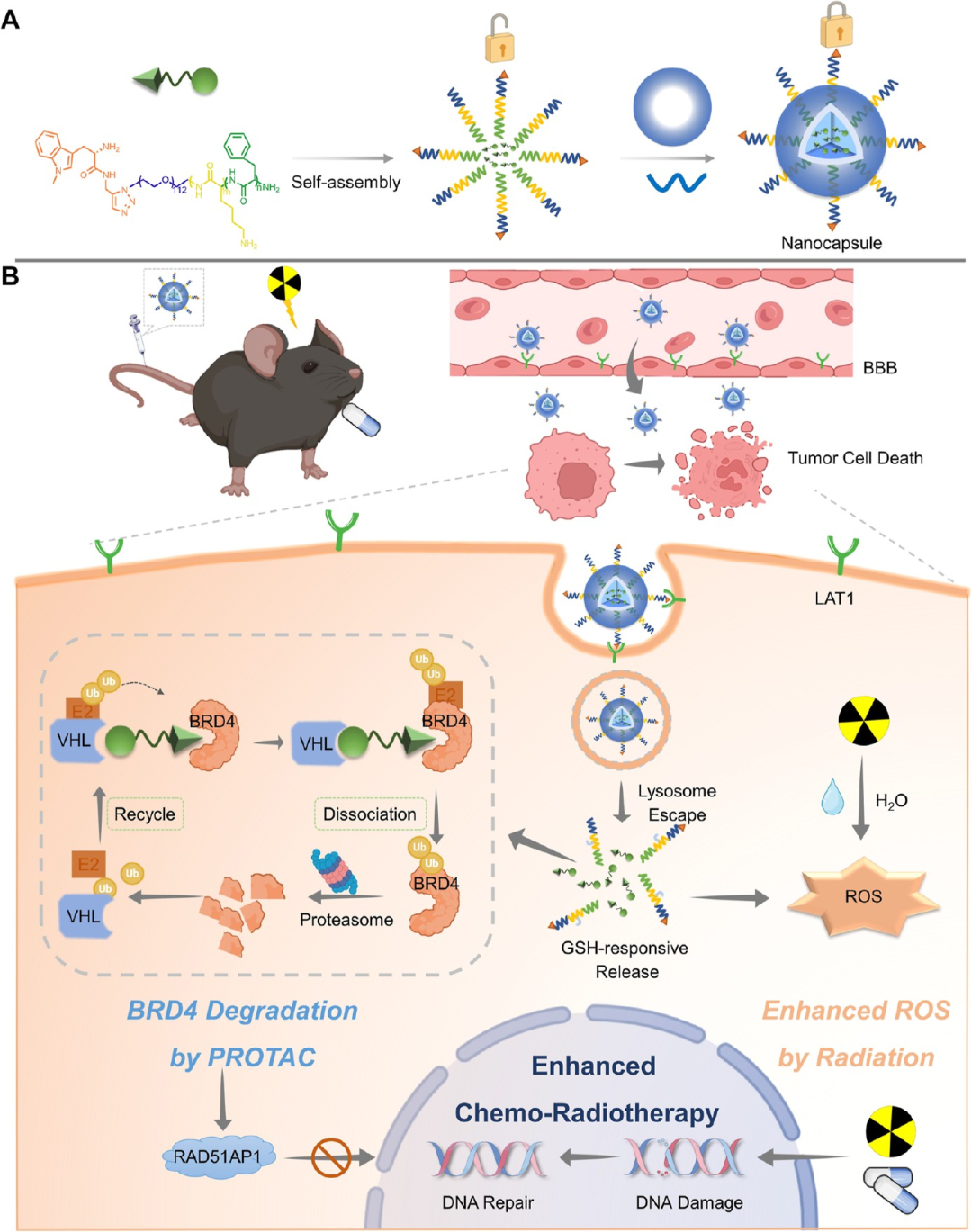
图10. 用于胶质母细胞瘤放化疗增敏的PROTAC纳米胶囊(MPL(SS)P@SIS): (A) 纳米胶囊的合成:将BRD4 PROTAC(SIS)封装于PEG-pLys-pPhe共聚物中,表面修饰L-型氨基酸转运体配体1-甲基-L-色氨酸(1-MT)。(B) 纳米胶囊通过LAT1主动跨越BBB并靶向GBM细胞,在GSH响应的肿瘤微环境中释放SIS,显著增强对放疗和化疗的敏感性。
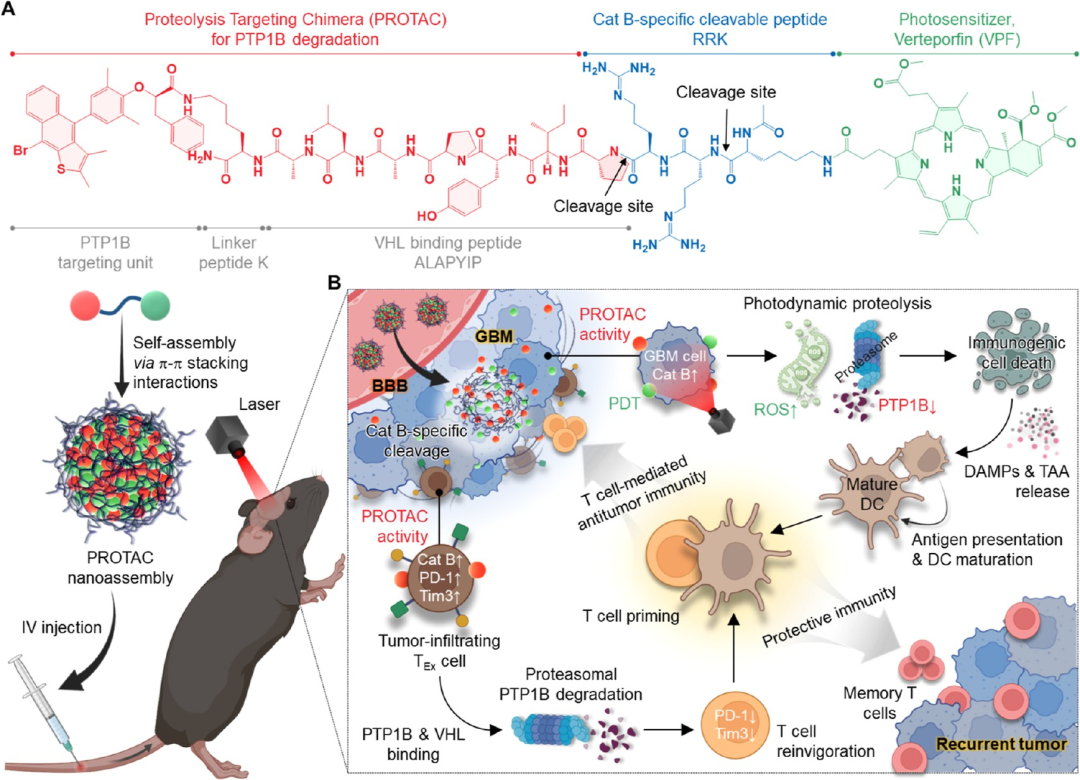
图11. 光动力PTP1B蛋白降解纳米组装体(PNPTP1B)的结构与作用模式: 将PTP1B靶向PROTAC与光敏剂维替泊芬(VPF)通过组织蛋白酶B敏感肽连接,利用VPF之间的π-π堆积自组装成纳米颗粒(载药量88.6%)。在激光照射下,PROTAC与光动力疗法协同,降解T细胞内PTP1B检查点,逆转免疫抑制。
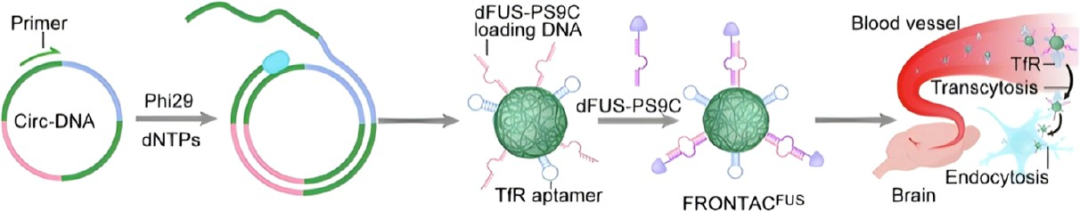
图12. 用于额颞叶痴呆和ALS治疗的DNA纳米花寡核苷酸PROTAC(FRONTACFUS)及TfR介导的BBB胞吞示意图: DNA纳米花表面功能化数百个转铁蛋白受体适配体和FUS蛋白结合适配体,通过受体介导的胞吞跨越BBB,单次静脉注射后2小时内脑实质中FUS蛋白降解约80%。
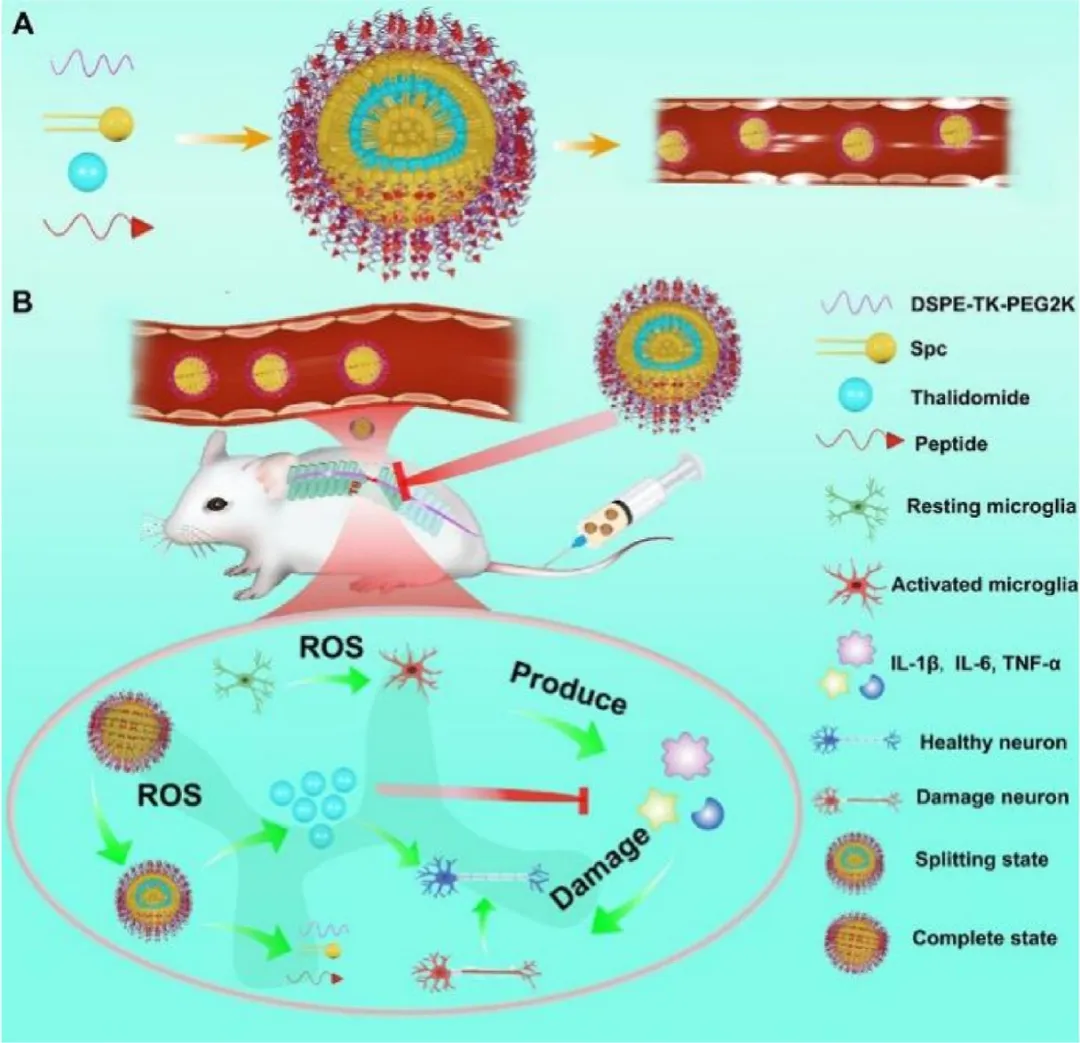
图13. 用于脊髓损伤治疗的活性氧响应型沙利度胺脂质体的设计与治疗机制: A6肽修饰的脂质体靶向炎症部位,硫代酮缩酮连接子赋予ROS响应性。在损伤微环境中(高pO2),12小时内药物释放达92%,通过调节小胶质细胞极化为M2表型,促进功能恢复。
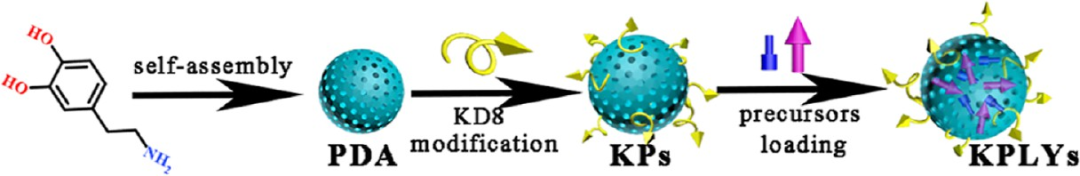
图14. 赖氨酸靶向嵌合体(KPLY)的理化结构表征: (A) KPLY的合成示意图:多巴胺表面修饰KD8肽(靶向RAGE受体),作为LYTAC前体。(B) 在Aβ-Cu²⁺复合物的催化下,KPLY原位自组装成具有降解活性的cli-LYTAC,并通过PDA载体清除ROS、重塑微环境。
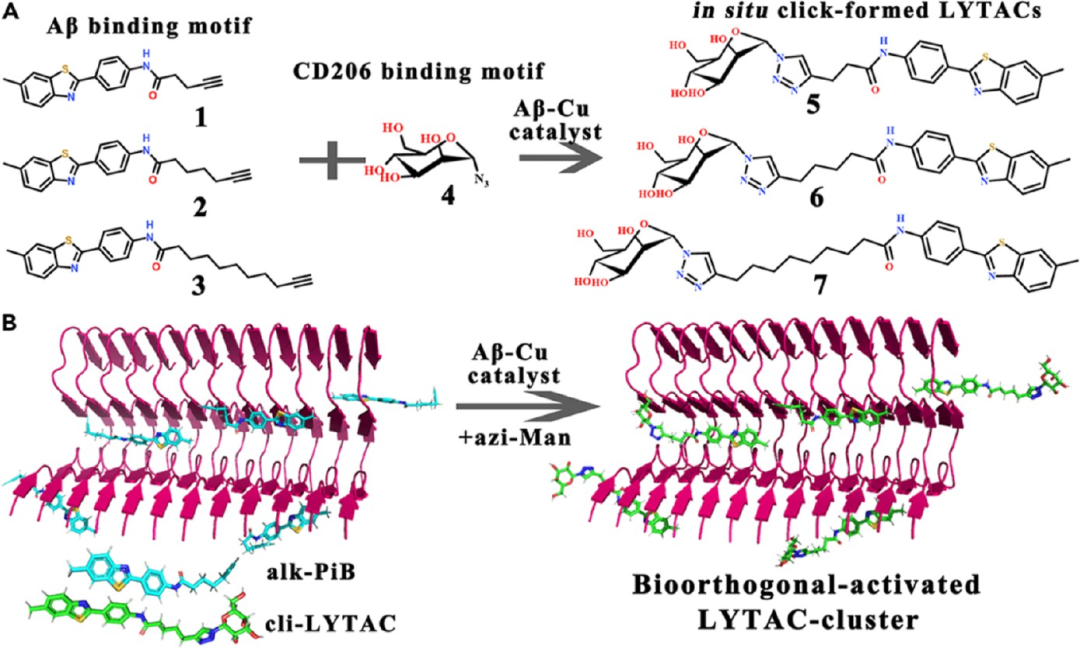
图15. 生物正交激活的LYTAC(cli-LYTAC)示意图: (A) 双功能分子cli-LYTAC的化学结构。(B) cli-LYTAC在Aβ纤维表面原位聚集形成团簇,通过与甘露糖受体(CD206)结合,引导Aβ进入溶酶体降解。PDA载体同时促进小胶质细胞向M2型极化。
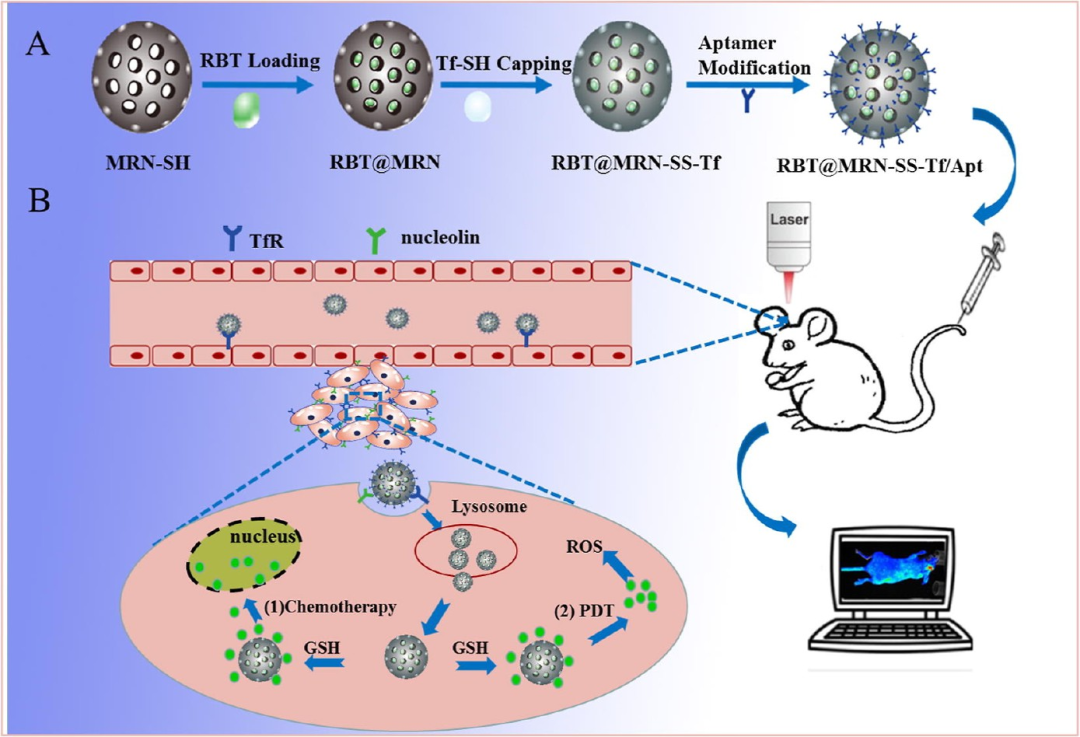
图16. 双靶向介孔钌纳米系统(RBT@MRN-SS-Tf/Apt)的设计: 表面共价接枝转铁蛋白(Tf)和AS1411适配体,通过氧化还原响应型二硫键连接。该平台能够跨越BBB、靶向胶质瘤,同时实现化学/光动力协同治疗。
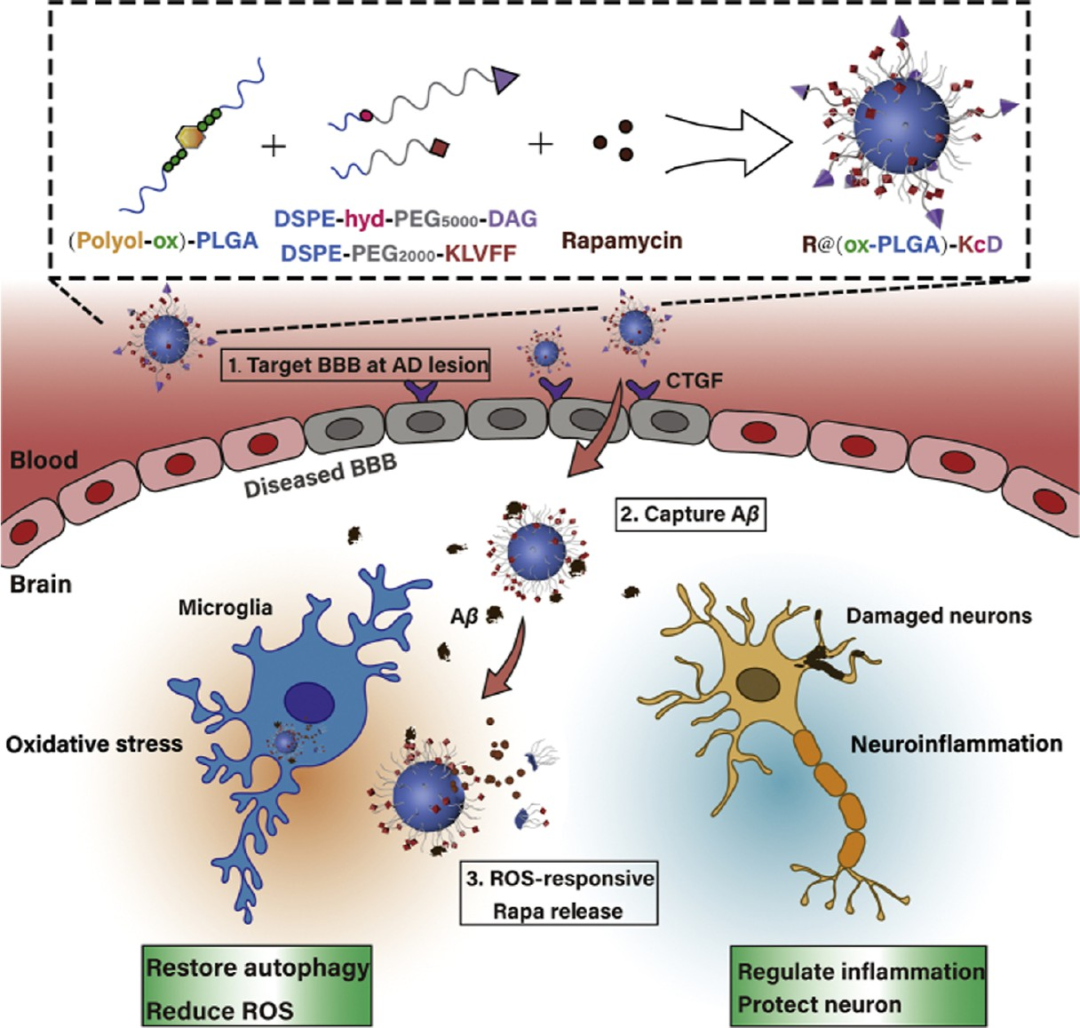
图17. 活性氧响应的特异性靶向纳米系统(Rβ(ox-PLGA)-KcD)示意图: PLGA纳米粒负载雷帕霉素,表面修饰Aβ捕获肽KLVFF和靶向肽DAG。通过CTGF介导的BBB穿透和Aβ捕获,在ROS触发下释放雷帕霉素,诱导自噬清除Aβ并抑制炎症。
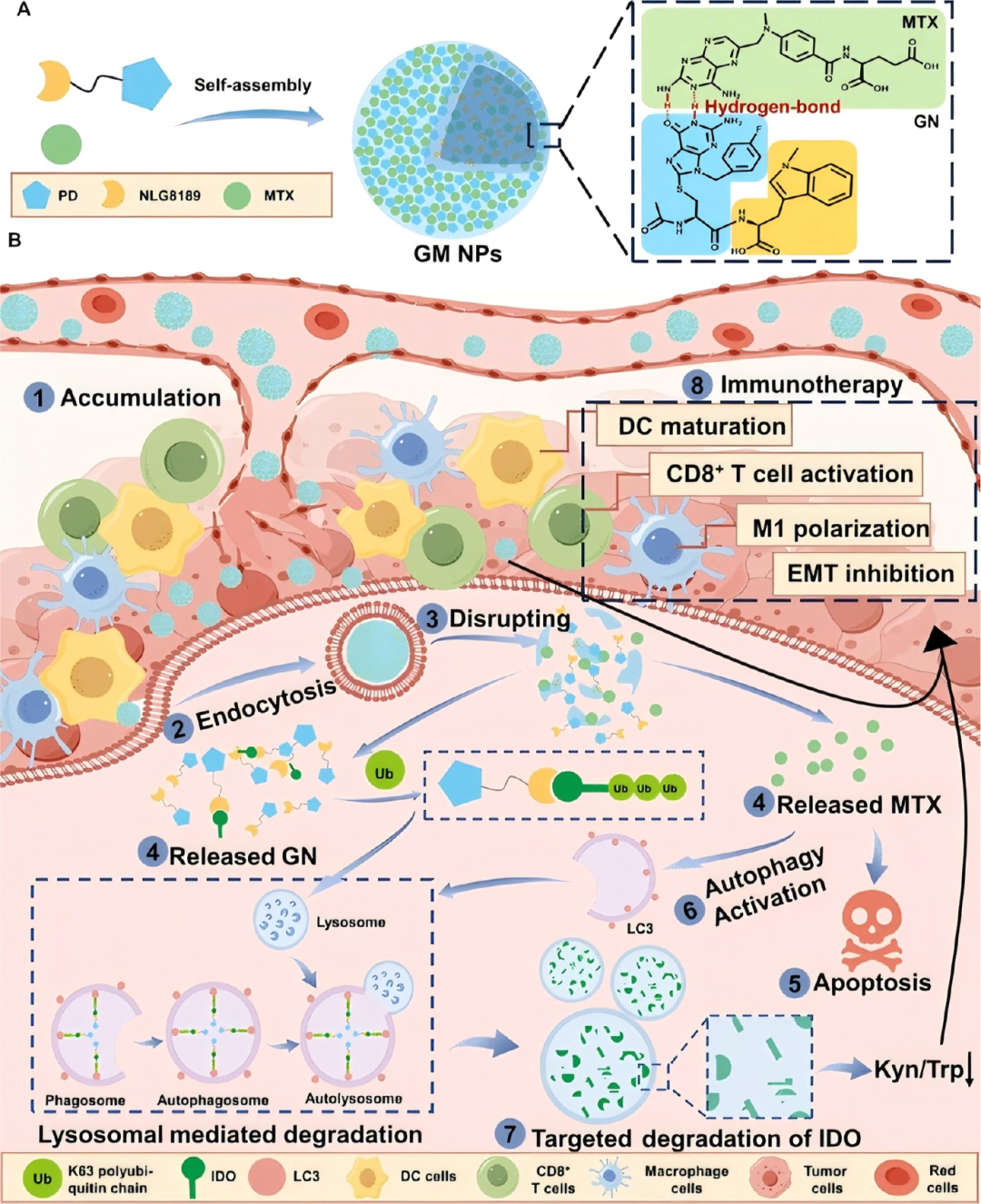
图18. 超分子人工纳米AUTAC(GM NPs)的设计与协同免疫治疗示意图: (A) 基于碱基配对的超分子组装过程。(B) 在肿瘤酸性微环境中纳米粒解体,释放甲氨蝶呤(MTX)和IDO降解物,通过调节免疫细胞代谢,增强效应T细胞应答。
结论
本综述全面总结了靶向蛋白降解(TPD)技术在神经系统疾病中的研究进展,系统分类了基于泛素-蛋白酶体、内体-溶酶体和自噬-溶酶体途径的各种降解策略及其代表性分子(PROTACs、分子胶、LYTACs、AUTACs、ATTEC、AUTOTAC等)。文章指出,TPD分子固有的药理学缺陷(高分子量、极性表面积大、代谢不稳定)以及中枢神经系统的多级屏障(血脑屏障、脑间质空间、细胞内分选瓶颈),严重限制了其在脑疾病中的转化。通过将TPD与先进的药物递送系统(脂质体、聚合物纳米粒、仿生膜囊泡、DNA纳米花等)相结合,可以实现药代动力学优化、BBB主动穿越、病灶特异性积累和可控释放,从而克服“钩效应”和脱靶毒性。未来研究应进一步关注载体本身的物理化学性质(刚度、形变能力、尺寸异质性)如何影响降解效率与途径选择性,以及如何利用人工智能构建更特异性的降解模块库。TPD与DDS的深度融合有望将原本“不可成药”的神经靶点转化为临床可行的治疗方案。
原文链接:
https://doi.org/10.1021/acsnano.6c04420


