四川大学Biomaterials:开发动态蛋白-多糖水凝胶,时空控释重塑脑微环境促进脑出血后神经再生
时间:2026-05-05 17:04:24 热度:37.1℃ 作者:网络
背景介绍
脑出血(ICH)是中风的一种亚型,具有高死亡率和致残率。脑出血后,病变部位形成以过量活性氧(ROS)、持续性炎症和胶质瘢痕形成为特征的恶劣微环境。更关键的是,这些病理特征动态演变且相互关联,形成“ROS-炎症-胶质瘢痕”的正反馈循环,加速损伤进展。同时,脑出血后脑内源性神经干细胞(NSCs)虽然被激活,但其再生能力极为有限,且受到恶劣微环境的进一步抑制。传统单靶点药物治疗因血脑屏障和毒副作用而受限,而现有水凝胶往往仅针对单一治疗窗口(早期神经保护或晚期神经再生),缺乏动态调控能力,难以精确匹配脑出血的多重动态病理变化。因此,亟需开发一种能够同步重塑微环境并促进内源性神经再生的智能水凝胶系统。
研究思路
针对上述挑战,四川大学华西医院神经外科、高分子科学与工程国家重点实验室的田猛教授团队,设计了一种动态蛋白-多糖水凝胶(GH),通过可见光诱导的巯基-二硫键交换反应作为通用策略构建,并整合了时空控释递送系统:软骨素酶ABC(ChABC)通过ROS响应性直接负载于水凝胶中,实现按需释放以动态自适应性减少胶质瘢痕;胰岛素样生长因子-1(IGF-1)则预载于介孔二氧化硅纳米颗粒(MSNs)中,实现持续缓释以调控内源性NSCs的行为和血管生成。水凝胶由巯基化明胶(TG)和巯基化透明质酸(TH)组成,模拟脑细胞外基质(ECM),提供细胞黏附、浸润和可调降解性,同时具有抗肿胀和促凝血能力。在脑出血小鼠模型中,该水凝胶有效清除组织ROS、抑制小胶质细胞/巨噬细胞活化并促使其向抗炎M2型极化、动态自适应性减少胶质瘢痕,同时促进内源性NSCs的增殖、迁移和分化以及血管生成,最终修复神经元和髓鞘,协同促进神经功能恢复。相关内容以Dynamic protein-polysaccharide hydrogels with spatiotemporal controlled delivery for brain microenvironment remodeling and neural regeneration of intracerebral hemorrhage stroke为题,发表在Biomaterials!
图片解析
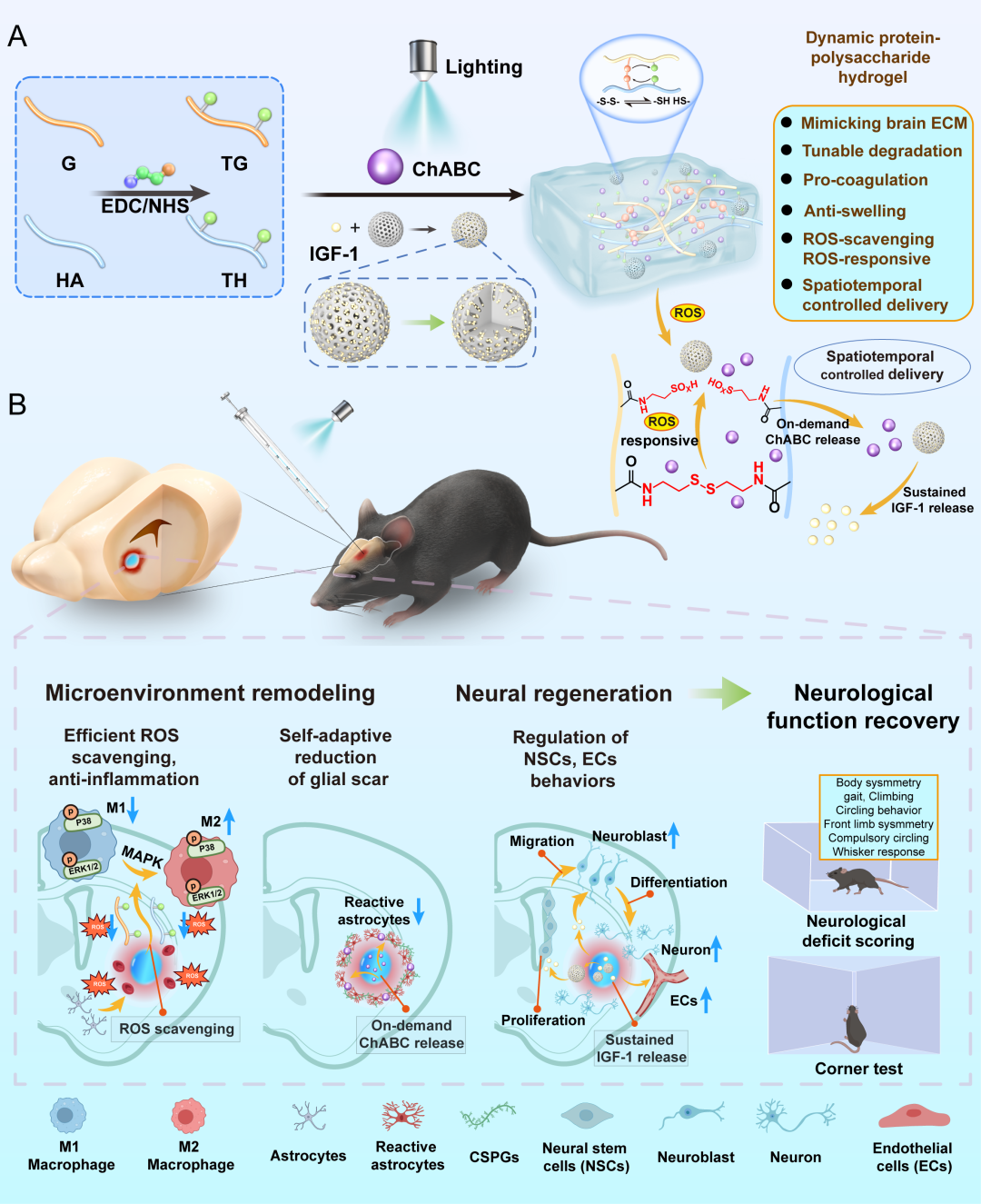
图1. 动态水凝胶构建及脑出血治疗机制示意图: (A) ChABC和IGF-1通过不同策略负载,实现ROS响应性和时空控释。(B) 水凝胶通过重塑微环境(清除ROS、抗炎、减少胶质瘢痕)和促进神经再生(NSCs调控、血管生成),协同促进脑出血小鼠神经功能恢复。
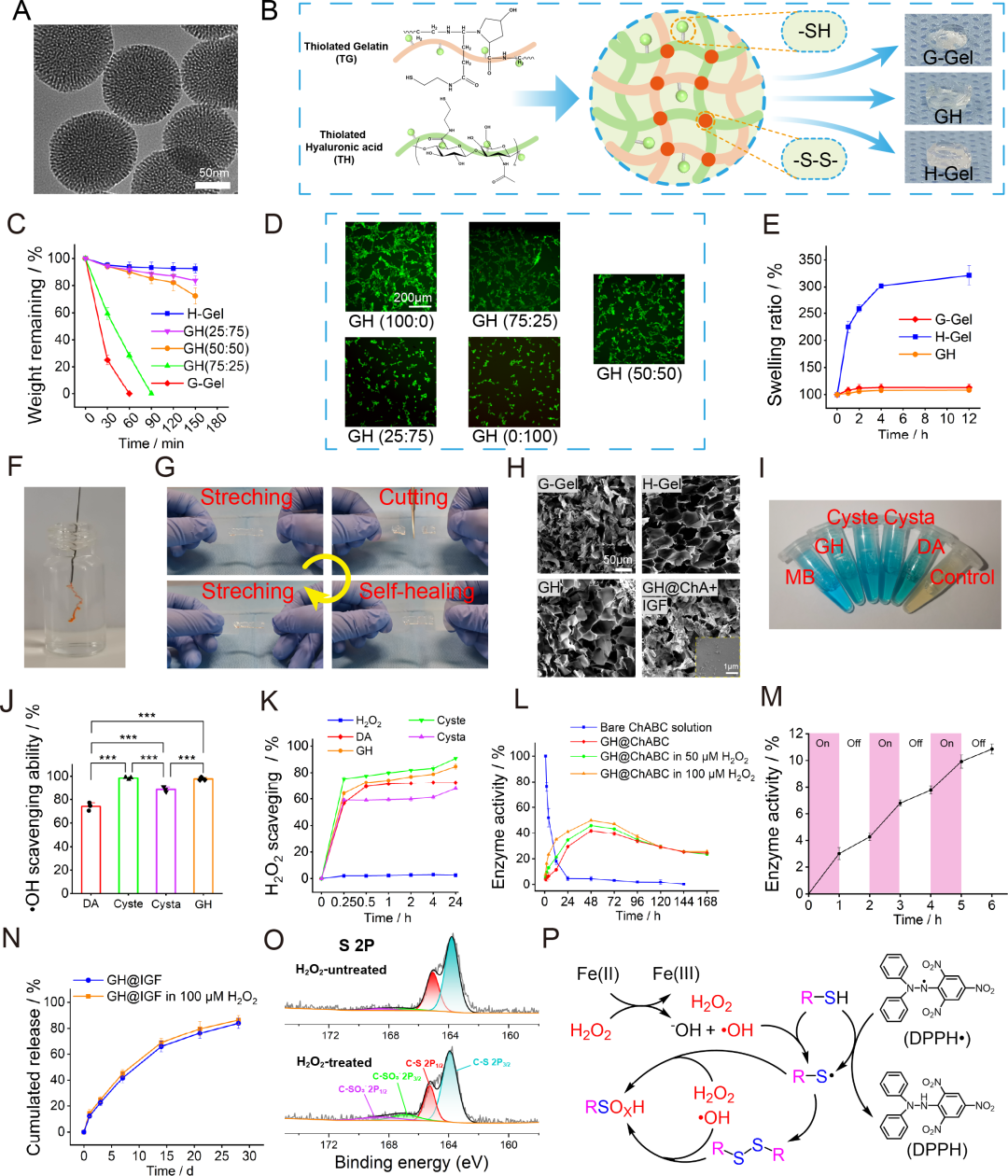
图2. 水凝胶的表征: (A) MSN的TEM图像,粒径约100 nm。(B) 通过巯基-二硫键交换反应形成GH水凝胶的示意图。(C) 不同TG/TH比例水凝胶的体外降解曲线:GH(50:50)在90分钟内稳定降解。(D) 细胞黏附代表性图像:G-凝胶和GH(75:25、50:50)组细胞铺展良好,H-凝胶组细胞呈圆形。(E) 水凝胶的溶胀性能:GH和G-凝胶溶胀约1.1倍(抗肿胀),H-凝胶溶胀超3倍。(F-G) 水凝胶的可注射性和自愈合性:可连续注射,切割后重新接触可反复拉伸。(H) SEM图像:水凝胶呈多孔结构(孔径30-80 μm),插图为MSNs。(I-J) MB溶液图像及羟基自由基清除定量:GH和Cyste组效率最高。(K) H₂O₂清除定量:GH和Cyste组24 h清除率显著高于Cysta和DA。(L) ChABC在不同H₂O₂浓度下的释放酶活性曲线:100 μM H₂O₂组释放最多。(M) ChABC在H₂O₂间歇暴露下的释放:暴露于H₂O₂时爆发释放,转回PBS后释放减慢。(N) IGF-1累积释放:28天释放83.8%。(O) GH水凝胶经H₂O₂处理前后硫元素的XPS分析:新出现-SO₃⁻峰(166.9、168.6 eV)。(P) 硫醇和二硫键清除ROS的机制示意图。
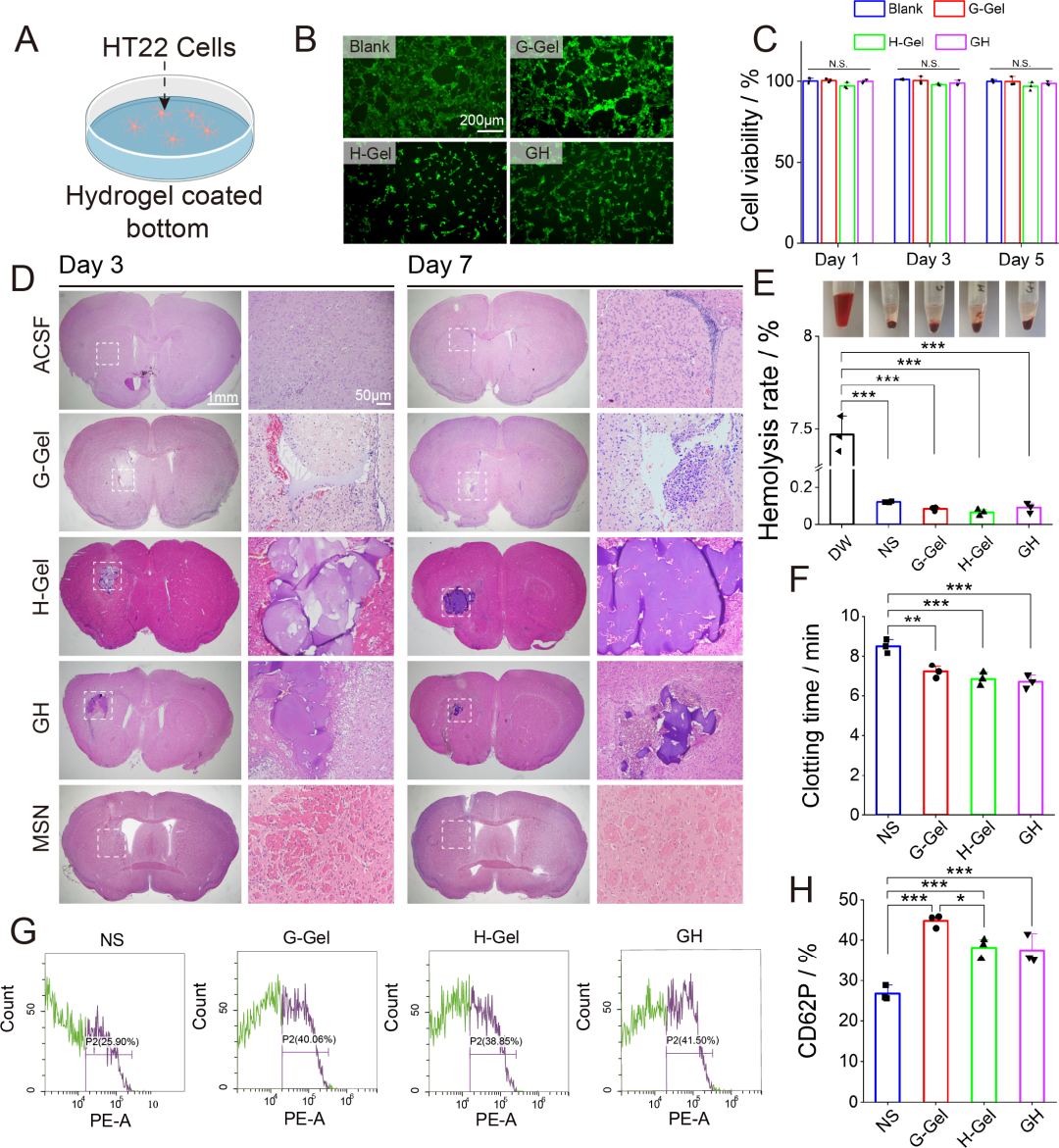
图3. 水凝胶的生物相容性评价: (A) HT-22细胞在水凝胶表面培养示意图。(B) Live/Dead染色:各组几乎无死细胞。(C) CCK-8细胞活力:各组无显著差异。(D) 正常小鼠脑组织H&E染色(3、7天):ACSF、MSNs和各水凝胶均引起轻微免疫反应,G-凝胶形成组织空洞,H-凝胶降解慢且细胞浸润少,GH水凝胶降解适中且细胞浸润明显。(E) 溶血活性:各组溶血率均<1%。(F) 全血凝固时间:GH和G-凝胶组显著短于NS和H-凝胶组。(G-H) 流式细胞术检测血小板活化(CD62P表达):GH和G-凝胶组与阳性对照(ADP+EPI)相当,促凝血能力良好。
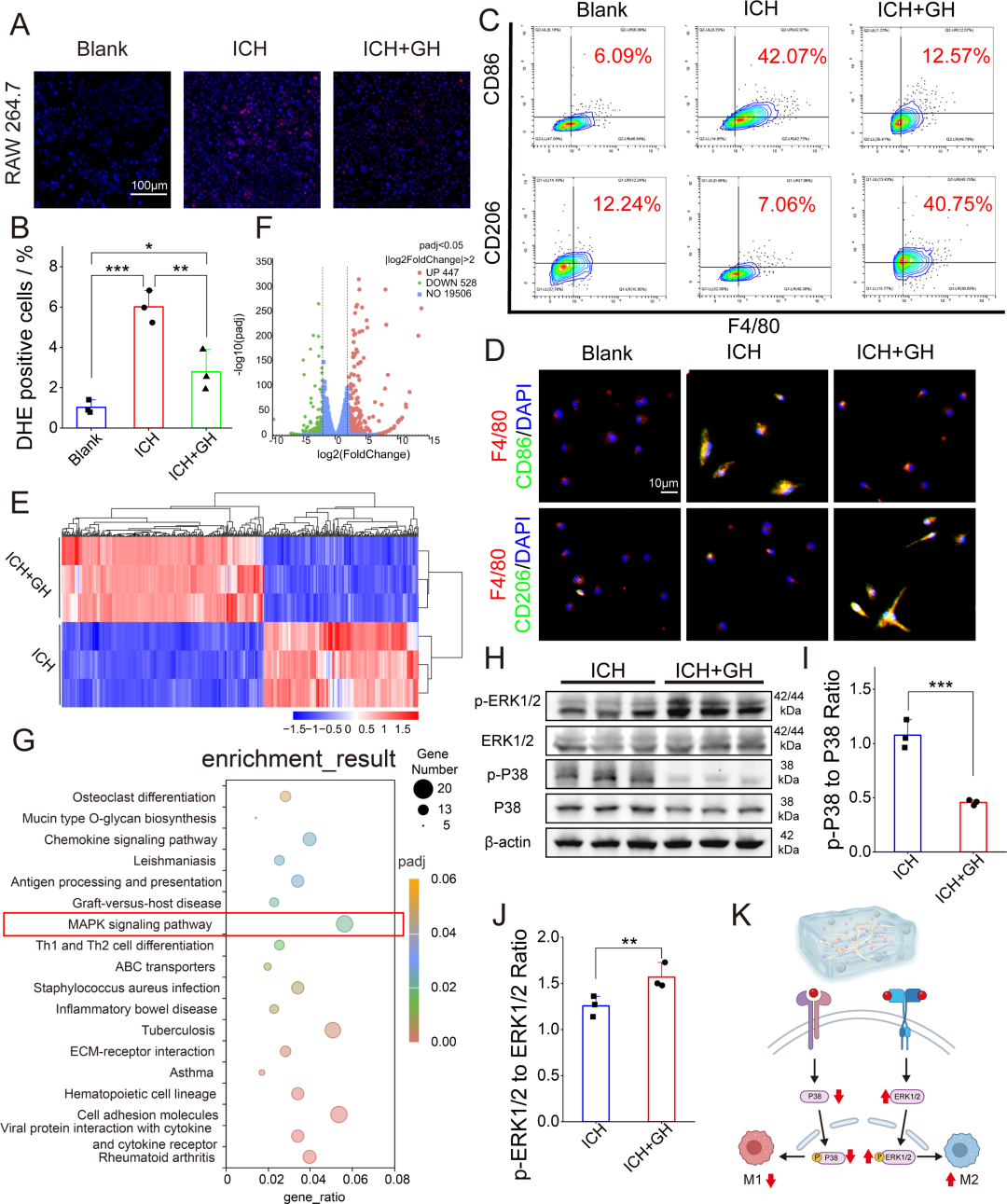
图4. GH水凝胶在体外降低细胞ROS水平并通过MAPK通路调节巨噬细胞向M2型极化: (A) DHE染色检测RAW 264.7细胞ROS水平:ICH组ROS升高,ICH+GH组降低。(B) DHE阳性细胞定量。(C) 流式细胞术:ICH组CD86⁺F4/80⁺(M1)比例升高,ICH+GH组CD206⁺F4/80⁺(M2)比例升高。(D) 免疫荧光:ICH组iNOS(M1)升高,ICH+GH组Arg-1(M2)升高。(E) ICH与ICH+GH组巨噬细胞差异表达基因热图。(F) 火山图:447个上调,528个下调。(G) KEGG富集分析:MAPK信号通路是显著富集通路之一。(H-J) Western blot及定量:ICH+GH组p-P38/P38比值降低,p-ERK1/2/ERK1/2比值升高。(K) MAPK通路调节巨噬细胞极化的机制示意图。
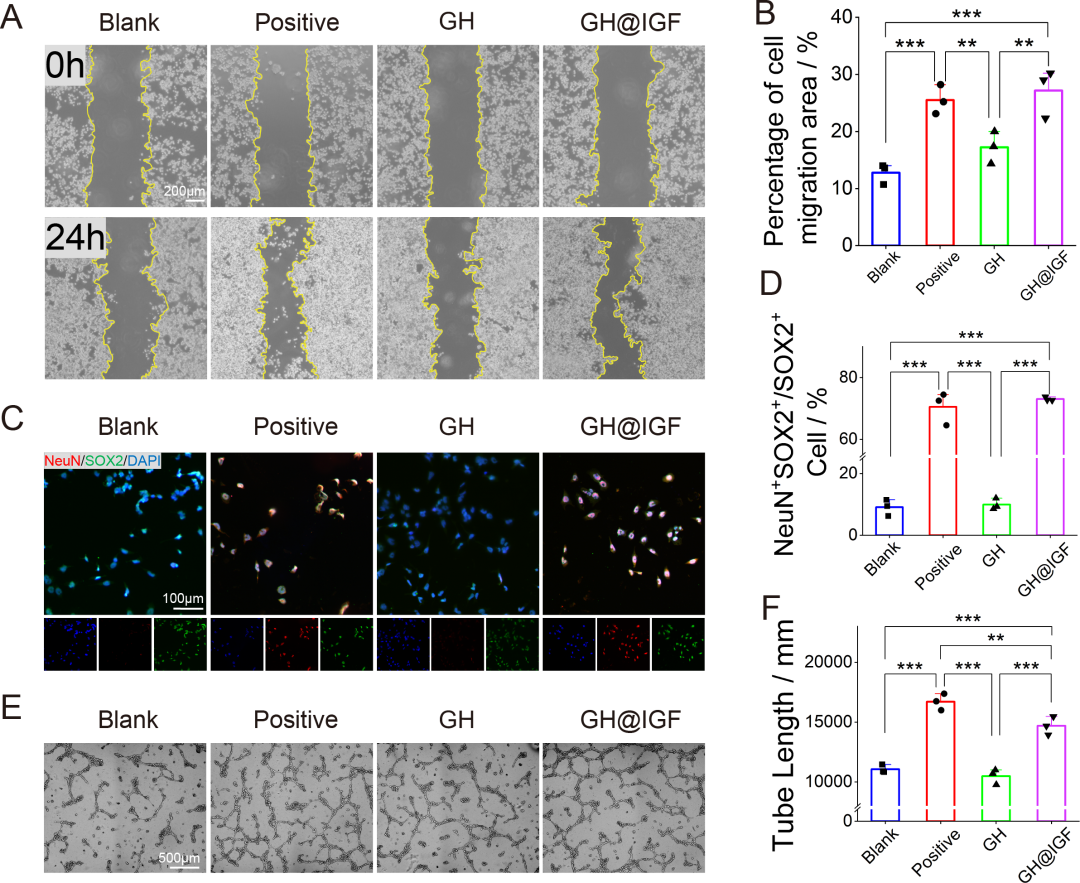
图5. GH@IGF在体外调节NSCs行为和内皮细胞血管生成: (A) 划痕实验代表性图像。(B) 细胞迁移面积定量:GH@IGF组和阳性对照组迁移率显著升高。(C) NE-4C细胞分化免疫荧光:NeuN(红)和SOX2(绿)。(D) NeuN⁺SOX2⁺/SOX2⁺细胞定量:GH@IGF和阳性组神经元分化比例升高。(E) HUVECs管形成实验。(F) 总管长度定量:GH@IGF和阳性组显著增加。
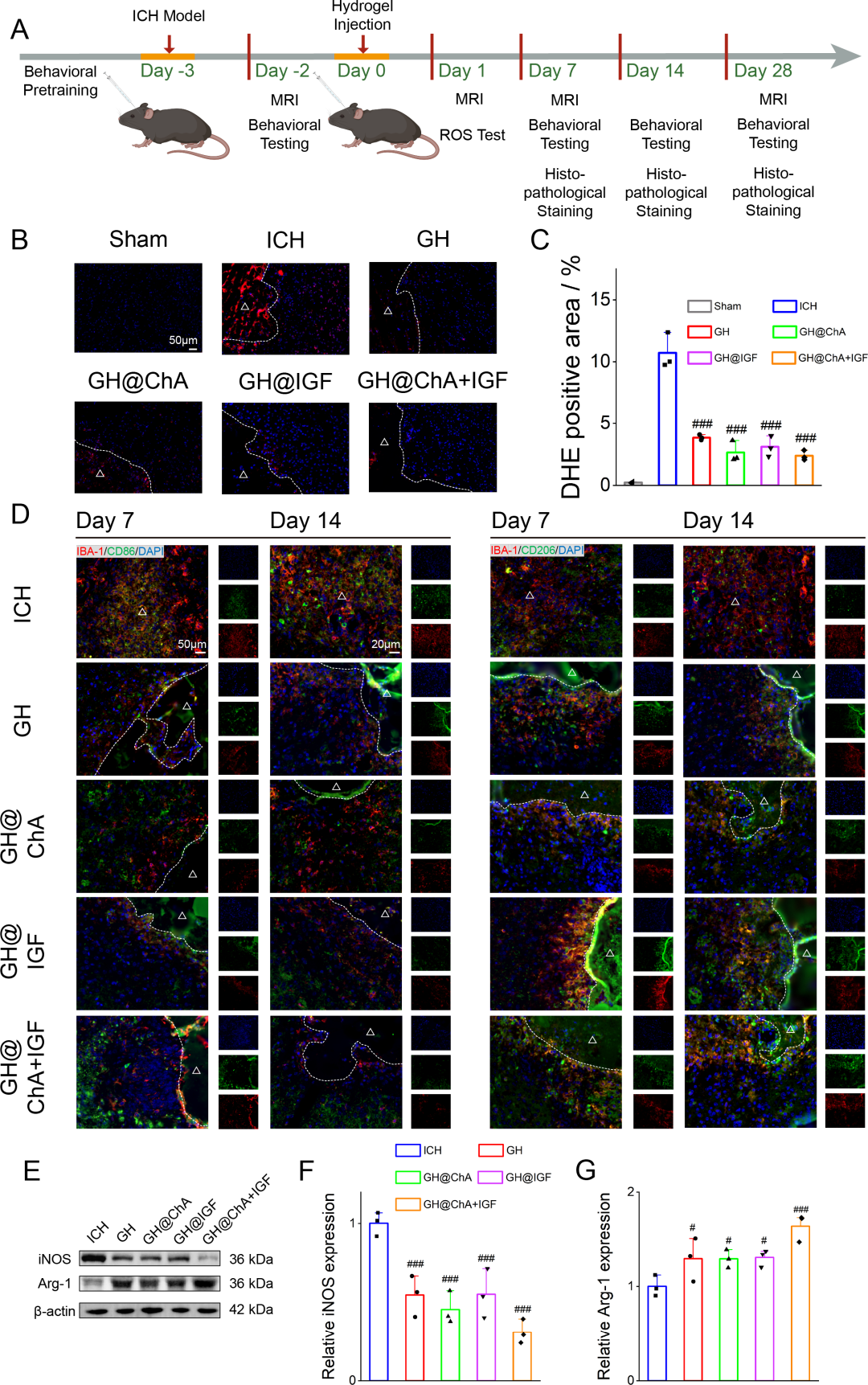
图6. 水凝胶在体内降低组织ROS水平、调节小胶质细胞/巨噬细胞活化和极化: (A) 实验流程图(脑出血建模、水凝胶注射、检测时间点)。(B-C) DHE染色及定量:ICH组ROS高表达,各治疗组均显著降低。(D) CD86/CD206(绿)和IBA-1(红)免疫荧光:第7、14天,治疗组CD86⁺IBA-1⁺减少,CD206⁺IBA-1⁺增加。(E-G) Western blot及定量:治疗组iNOS(M1)表达降低,Arg-1(M2)表达升高。
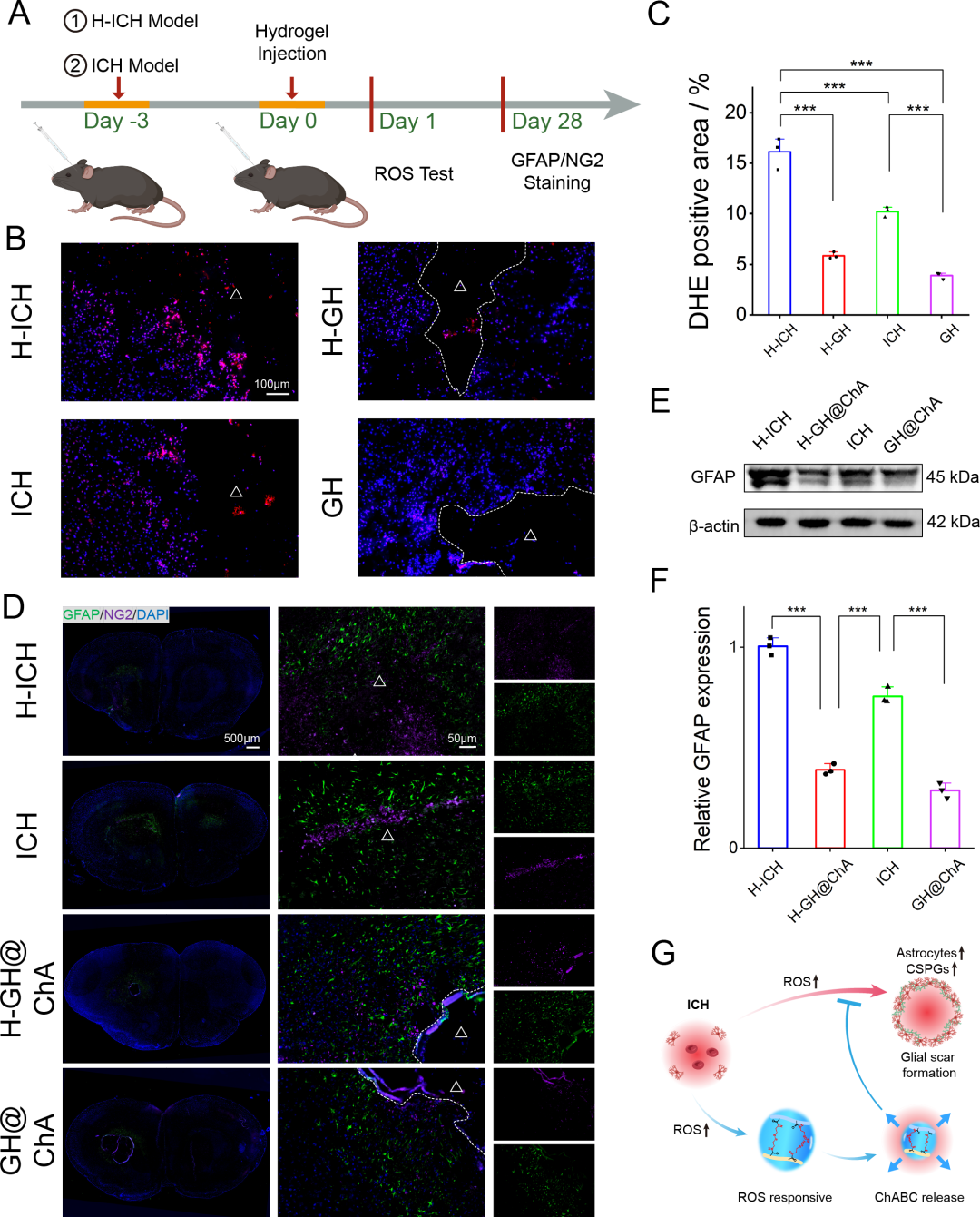
图7. 水凝胶减轻胶质瘢痕形成: (A) 重度脑出血(H-ICH)模型实验设计。(B-C) DHE染色及定量:H-ICH组ROS更高,GH组仍有效降低。(D) GFAP(绿)和NG2(远红)免疫荧光:第28天,治疗组GFAP和NG2表达降低,GH@ChA和GH@ChA+IGF组更显著。(E-F) Western blot及定量:治疗组GFAP表达降低。(G) 水凝胶通过ROS响应动态自适应性减少胶质瘢痕的机制示意图。
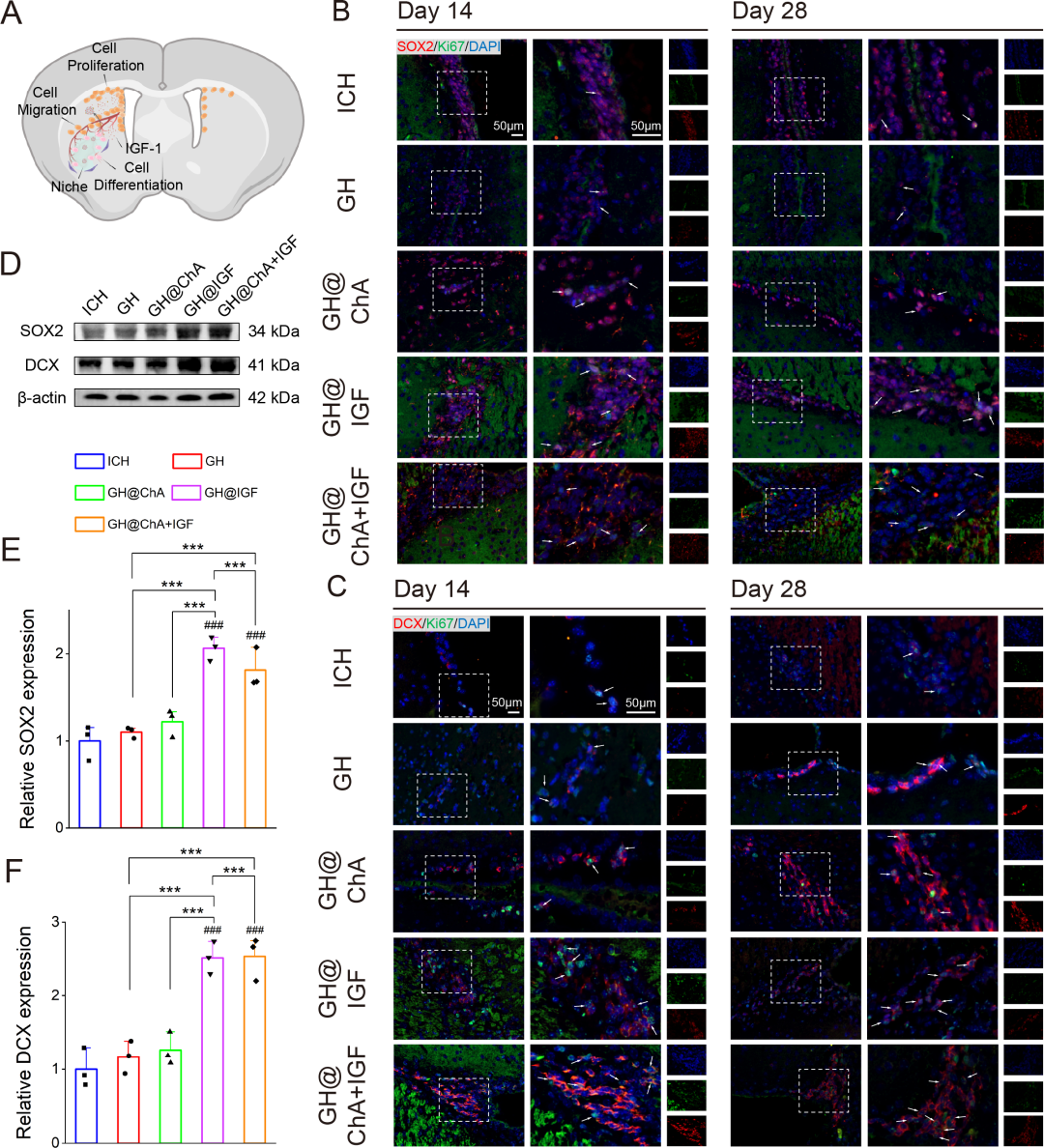
图8. 水凝胶在体内调节NSCs和神经母细胞行为: (A) 水凝胶调节内源性NSCs增殖、迁移和分化的示意图。(B) SOX2(红)和Ki67(绿)免疫荧光:GH@IGF和GH@ChA+IGF组SOX2⁺Ki67⁺比例显著升高。(C) SOX2⁺Ki67⁺/SOX2⁺细胞定量。(D-F) Western blot及定量:GH@IGF和GH@ChA+IGF组SOX2和DCX表达升高。
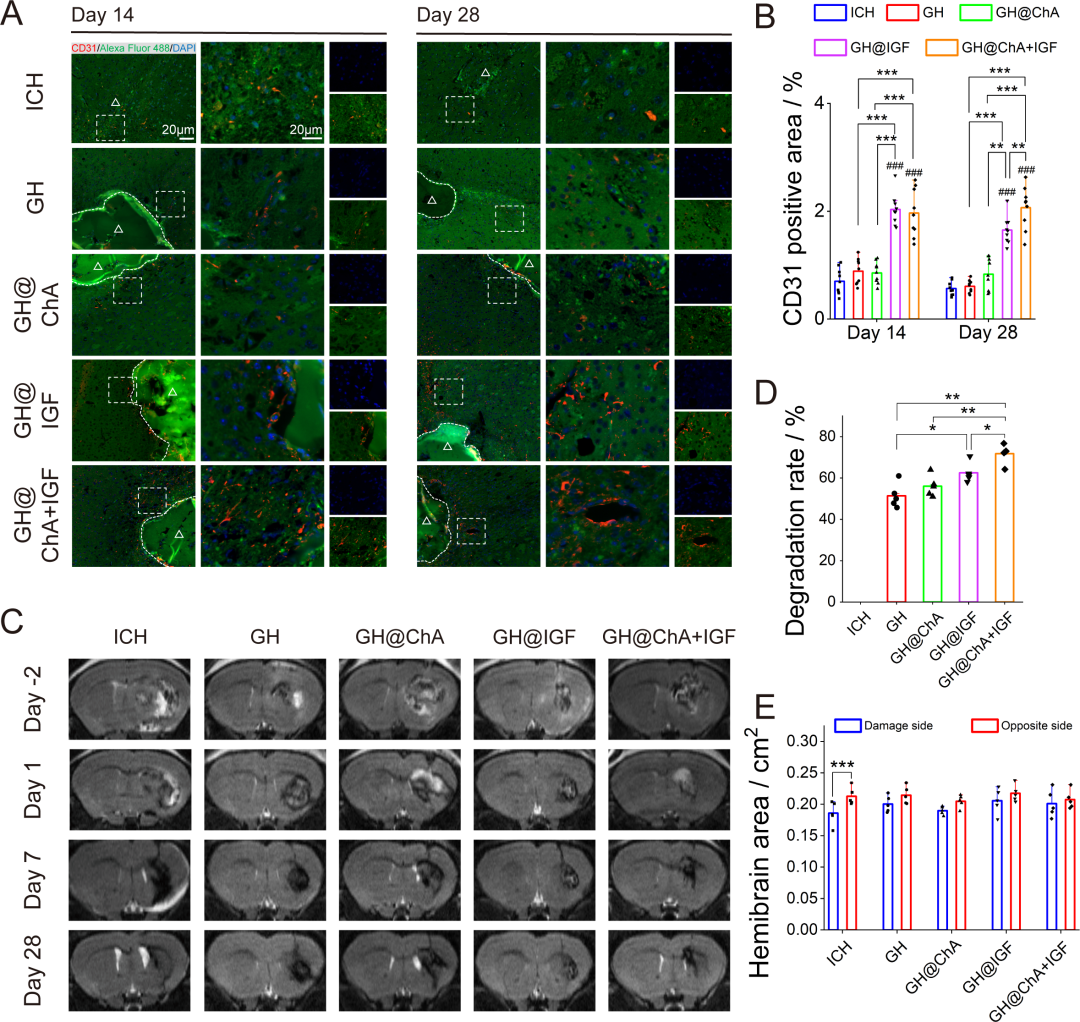
图9. 水凝胶促进血管生成并为受损组织提供结构支持: (A) CD31(红)免疫荧光:第14、28天,GH@IGF和GH@ChA+IGF组CD31表达最高。(B) CD31阳性面积定量。(C) MRI扫描:显示水凝胶定位及整合。(D) 第28天水凝胶降解程度:GH@ChA+IGF组几乎完全降解。(E) 第28天损伤侧与对侧半脑面积比:ICH组脑萎缩明显,水凝胶治疗组提供结构支持。
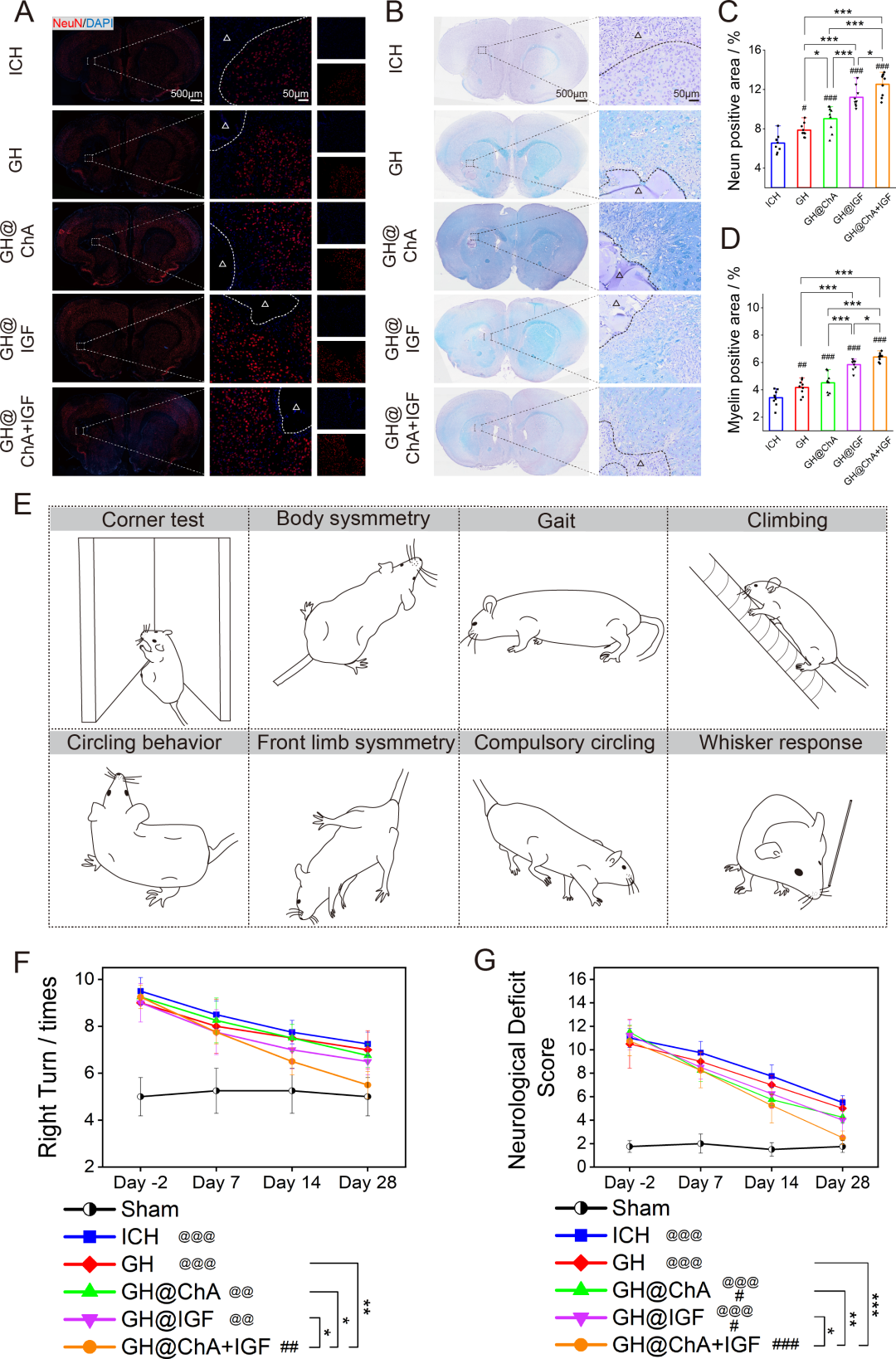
图10. 水凝胶促进神经元再生、髓鞘修复和神经功能恢复: (A) NeuN(红)免疫荧光:第28天,GH@ChA+IGF组神经元面积最大。(B) LFB髓鞘染色:GH@ChA+IGF组髓鞘完整性最佳。(C-D) NeuN阳性面积和LFB阳性面积定量。(E) 转角试验和神经功能缺损评分示意图。(F) 转角试验右转次数:第28天,GH@ChA+IGF组与Sham组无显著差异。(G) 神经功能缺损评分:随时间降低,GH@ChA+IGF组评分最低。
结论
本研究成功开发了一种动态蛋白-多糖水凝胶(GH),通过可见光诱导的巯基-二硫键交换反应构建,可模块化组合不同巯基化聚合物,具有通用性。水凝胶由巯基化明胶和巯基化透明质酸组成,模拟脑ECM,提供细胞黏附、浸润、可调降解性,同时具有抗肿胀和促凝血能力。基于巯基-二硫键化学特性,水凝胶具备高效ROS清除和ROS响应性按需释放ChABC的能力,结合MSNs介导的IGF-1持续缓释,实现了时空控释双药递送。在脑出血小鼠模型中,该水凝胶:1)清除组织ROS,抑制小胶质细胞/巨噬细胞活化并促使其向M2抗炎表型极化(通过MAPK通路);2)动态自适应性减少胶质瘢痕(GFAP、NG2、胶原沉积降低);3)促进内源性NSCs增殖、迁移和神经元分化,增强血管生成;4)最终修复神经元和髓鞘,协同促进神经功能恢复(转角试验和神经功能缺损评分显著改善)。该动态水凝胶系统为脑出血治疗提供了一种同时重塑微环境和促进神经再生的综合策略。原文链接:
https://doi.org/10.1016/j.biomaterials.2026.124274


