Cancer Discov:游离DNA和连续肿瘤测序可识别亚型特异性癌症进化和表观遗传状态
时间:2025-01-26 12:08:48 热度:37.1℃ 作者:网络
癌症仍是儿童疾病死亡的主要原因。近年来为了开发更有效的治疗,对患有难治性或复发性儿童癌症患者的肿瘤组织开展了许多精准医学检测,以期找到可靶向的基因改变,但人们对肿瘤在诊断和复发之间是如何演变的了解很有限,分层医学儿科是英国精准医学计划,希望提供快速周转的临床级测序,并为复发或难治性患者提供临床报告。
分层医学儿科的一个明确目标是识别可能出现以下情况的患者:对分子靶向治疗药物作出反应;期望在癌症复发样品中发现基因组和表观遗传的决定因素;除临床计划外,还为组织样本和与时间匹配的血浆样本归档。
最近,英国伦敦癌症研究所小儿肿瘤实验医学中心 (POEM)的 路易斯·切斯勒(Dr. Louis Chesler)团队在 Cancer Discovery 上发表题为 Stratified Medicine Paediatrics: Cell free DNA and serial tumour sequencing identifies subtype specific cancer evolution and epigenetic states 的论文,利用大型且注释良好的侵袭性儿童恶性肿瘤基因组数据库,确定了儿童癌症复发的基因组和表观遗传驱动因素,并强调了游离细胞DNA(cfDNA)分析在捕捉肿瘤内异质性和癌细胞表观遗传状态方面的效力和实用性。

1.与原发性匹对的复发性儿科肿瘤样本的基因组图谱
本文报告了与原发性匹对的复发样本中所发现的所有基因组改变的对比,41% 的序列改变同时存在于原发样本和复发样本中,而37% 仅在复发时发现(23% 仅在原发时发现)。所有参试人中,复发时最常改变的基因是 TP53(图 1a),在肉瘤患者中 TP53 突变的频率更高(图 1b)。在神经母细胞瘤中,复发时富集的最常见突变基因是ALK 和 NF1,应证了之前小型配对测序研究的结果 (图 1c)。除了复发时获得的ALK 突变外,ALK 也是诊断时最常见的突变基因,而ALK 突变仅在神经母细胞瘤中发现,显示了该基因在神经母细胞瘤发生和疾病进展中的突出作用。
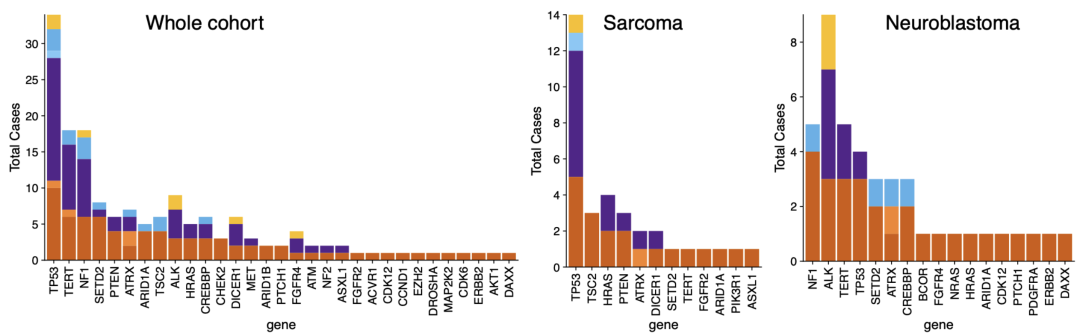
图1. 与原发性匹对的复发样本中所发现的所有基因组改变的对比
2.复发时的小儿癌症显示出富集的表观遗传修饰因子突变
使用二代测序(NGS) 板块测序数据,计算同义突变与非同义突变的比率 (dN/dS) 以识别非同义变异和截断变异,假设这些变异是复发的驱动因子,发现复发时 DNA 高度富集在负责表观遗传修饰的基因突变上,包括 ATRX、SETD2、ARID1B 和 CREBBP(图 2),与表观遗传重塑作为儿童癌症治疗耐药性驱动因子的推断一致。
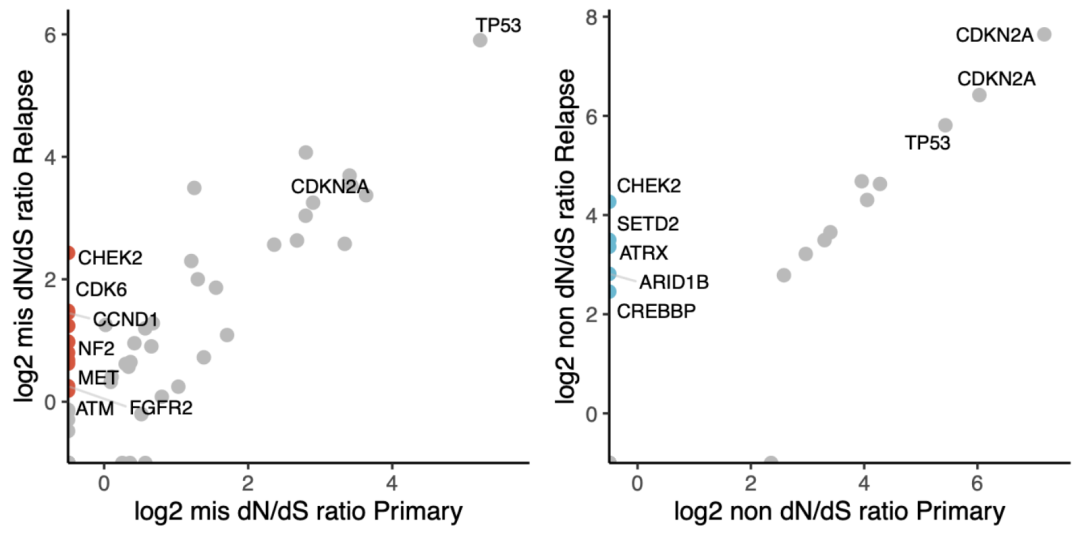
图2. 比较原发和复发时dN/dS 的比率,错义突变(红色)和截断突变(蓝色)
3.复发时高纯度 ctDNA 测序比组织测序能更好地反映肿瘤异质性
在所有测试人中(402 名患者),43% cfDNA 中检测到组织测序预期的改变,其中 89% 是预期的改变在高纯度样品中检测到,在低纯度样品中也检测到 25% 的预期变化。最常见的 cfDNA 独特变异是 ARID1A、NF1、PPM1D、TP53 和 CREBBP。在神经母细胞瘤中能检测到最高数量的 cfDNA 独特变异,与已知的神经母细胞瘤生物学中重要的表观遗传基因(ARID1A、ATRX、SMARCA4)和与超高危疾病相关的基因(ALK、NF1、PTPN11、FGFR1、TP53、ATM、CREBBP)一致。而且,当有足够的来自肿瘤的DNA(ctDNA)存在于循环系统(即cfDNA中ctDNA占比高)时,cfDNA测序比传统组织测序更好地反映了肿瘤异质性。
4.ctDNA能识别侵袭性亚克隆并可预测神经母细胞瘤的复发
例如,一名神经母细胞瘤患者的肾上腺肿瘤复发活检时未显示清晰的 CCND1 扩增,尽管确实显示了一些拷贝数变更(CNA) 表明肿瘤组织的存在,但复发时 cfDNA 的拷贝数谱有明显的CCND1 扩增,更符合与时间匹配时肝转移灶的活检(图3),这证明了 cfDNA 在检测神经母细胞瘤异质性方面的效用,包括检测出转移部位的遗传变化。另外,已知数据显示, TP53 和 RAS 通路突变在初诊和复发时与超高风险 (UHR) 神经母细胞瘤相关,但单次活检并不能完全捕获复发时肿瘤中存在的所有 UHR 突变,而这次大规摸试验表明了所有UHR 变异可以通过对肿瘤来源的游离 DNA 进行测序来检测。
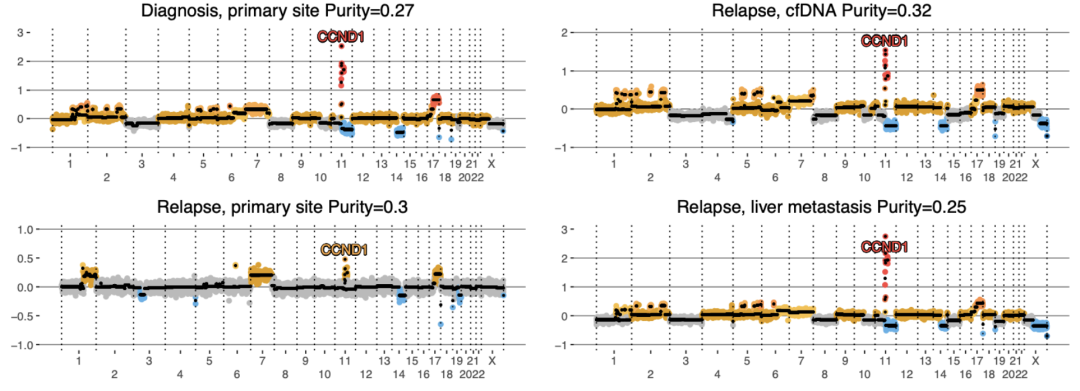
图3. 神经母细胞瘤患者的拷贝数概况:原发组织(左上)和复发组织原发胸部部位的活检样本(左下)、复发时的 cfDNA 样本(右上)以及从某个部位收集的其他复发组织活检样本肝脏转移性病变(右下)
5.cfDNA 片段组学分析揭示癌症和组织特异性特征
鉴于儿童癌症的总体突变频率较低,需要确定ctDNA分析能否推断与起源组织和癌症特异性相关的其他表观遗传表达特征。为建立儿科肿瘤来源的 ctDNA 片段组学模式,研究人员应用 Griffin 方法,对比包含共有结合位点的基因转录调控(GTRD )数据库,使用 Wilcoxon 测试和层次聚类来识别转录因子结合位点,与其他肿瘤类型相比,分析一种肿瘤类型的可及性与差异。这一方法明确得出癌症特异性转录因子表达特征簇。对4个主要集群的基因本体富集分析,发现与起源细胞相关的基因组,包括神经母细胞瘤中的神经嵴衍生途径、神经母细胞瘤中的肌肉发育横纹肌肉瘤、淋巴瘤的免疫途径和肝细胞分化肝母细胞瘤簇。
这一方法还得到了与非霍奇金淋巴瘤 (NHL) 相关的最大簇,包含大量已知在 NHL 发病机制中发挥作用的转录因子,例如 BCL6、IRF4、BATF3、FOXO1 和BCL11A。在肾母细胞瘤患者中,只有一种转录的结合位点因子被确定为高度特异性和高度易感性:SIX2 一种已知的预后较差生物标记物和干细胞/胚细胞亚型相关转录因子。在肝细胞簇中,三中之二的转录因子为已知的具有肝细胞特异性因子。在包含MYOD1 和 MYOG的泛横纹肌肉瘤核心调节线路(CRC)中,横纹肌肉瘤样品显示明显的覆盖面积损失。在神经母细胞瘤样本中,确立了非甲肾上腺素的核心调节线路与其关键组成的转录因子, HAND2、ISL1、TBX2、GATA3 和 MYCN。综上所述, ctDNA 片段组学模式可识别与细胞起源和表观遗传可塑性有关的不同肿瘤特异性簇,这一发现在分析抗药性和复发特征时,对鉴别转录特征具有很大的潜力。
尽管本研究证明了 cfDNA 测序的附加价值,但值得注意的是,对于在相当大比例的患者中,肿瘤组织活检或 ctDNA 中均未检测到遗传改变复发的时间。这与其他研究一致,更证明了寻找儿科肿瘤侵袭性疾病的非遗传生物标记物的重要性。复发是由多种遗传机制驱动的,同一肿瘤,每个肿瘤细胞都相对罕见,因此如果没有较大的参测群体就很难检测到。表观遗传失调越来越多的被认为是侵袭性儿童癌症的主要驱动因素,而且转录回路在驱动高侵袭性疾病中表现出了特定的依赖性,这对于开发新的药物具有很高的价值。
本研究展示了儿科肿瘤诊断和复发之间的特定演变模式,包括识别肿瘤特异性和泛队列复发驱动因素。此外,cfDNA 的核体物分析不仅有可能识别儿科癌症的疾病亚型,还可以识别与疾病相关的表观遗传变化生物学。最后,本研究表明,对于复发性和难治性癌症患者,cfDNA 的标准临床级 lcWGS 可以用于推断癌细胞与起源细胞相关的表观遗传状态,并且具有连续和大规模应用的潜力,在应用中包括支持诊断、提供预后信息、识别新型疗法的表观遗传目标,以及连续采样了解新型疗法在改变表观遗传程序中的作用。


