Nat Cardiovasc Res 华中科技大学同济医学院附属协和医院程翔团队系统阐述秋水仙碱在动脉粥样硬化性心血管疾病中的作用机制与治疗潜力
时间:2026-05-05 12:24:47 热度:37.1℃ 作者:网络
近日,华中科技大学同济医学院附属协和医院心内科程翔教授团队在心血管领域权威期刊Nature Cardiovascular Research在线发表综述“Mechanisms and therapeutic potential of colchicine in atherosclerotic cardiovascular disease”。该综述系统整合了秋水仙碱在动脉粥样硬化性心血管疾病(ASCVD)中的基础机制、细胞作用、蛋白组学证据及大型随机临床试验结果,全面阐述了其作为精准抗炎治疗药物的临床价值与未来方向。

秋水仙碱作为一种经典抗炎药物,已在家族性地中海热、痛风和心包炎中应用多年。近年来,COLCOT、LoDoCo2等大型临床研究显示,低剂量秋水仙碱可降低冠心病患者复发性心血管事件风险,使其重新成为ASCVD抗炎治疗领域的重要候选药物。秋水仙碱在微管动力学、炎症小体活化、氧化应激、胆固醇晶体调节、蛋白组重塑及多种细胞功能等多个层面发挥调控作用,体现了其广泛的药理功能。
秋水仙碱的药代动力学与细胞内富集特征
综述首先系统梳理了秋水仙碱在体内的吸收、分布、代谢和排泄特征(图1)。口服后,秋水仙碱主要在小肠吸收,并经肝脏和肠道CYP3A4酶代谢,同时受到P-糖蛋白(P-gp)外排转运系统调控。主要经胆汁/粪便和尿液排泄。值得注意的是,秋水仙碱的抗炎效应很大程度上依赖于细胞内富集。服药后,粒细胞和单核细胞中的秋水仙碱浓度可高于血浆浓度数倍,并在细胞内维持较长时间。中性粒细胞由于缺乏或低表达P-gp,更易蓄积秋水仙碱,这可能解释了秋水仙碱对中性粒细胞迁移、黏附、脱颗粒和NETs形成具有显著抑制作用。
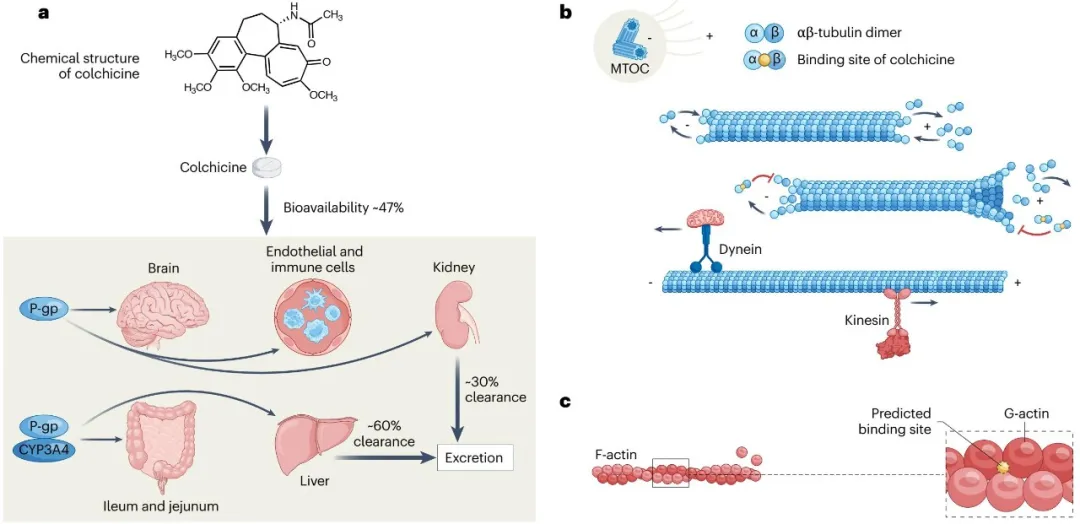
图1. 秋水仙碱的药代动力学与细胞骨架作用机制示意图。秋水仙碱经小肠吸收,受CYP3A4与P-gp共同调控,并主要通过肝胆和肾脏途径清除;其经典靶点为αβ-微管蛋白二聚体,同时可能影响肌动蛋白骨架。
秋水仙碱的经典机制:微管解聚与NLRP3炎症小体抑制
秋水仙碱最经典的作用机制是结合αβ-微管蛋白二聚体,抑制微管聚合并扰乱细胞内运输系统。微管不仅是细胞骨架结构,也是线粒体、囊泡、蛋白复合体和炎症信号分子运输的重要轨道。
在ASCVD中,胆固醇晶体、氧化低密度脂蛋白及细胞损伤信号可激活NLRP3炎症小体,促进caspase-1活化及IL-1β、IL-18成熟释放。综述指出,秋水仙碱可通过多重方式抑制NLRP3炎症小体:抑制NF-κB介导的priming过程,降低NLRP3、pro-IL-1β和pro-IL-18转录;抑制P2X7受体相关K⁺外流;减少线粒体ROS产生;破坏HDAC6–dynein依赖的NLRP3炎症小体组分运输和炎症小体装配(图2)。
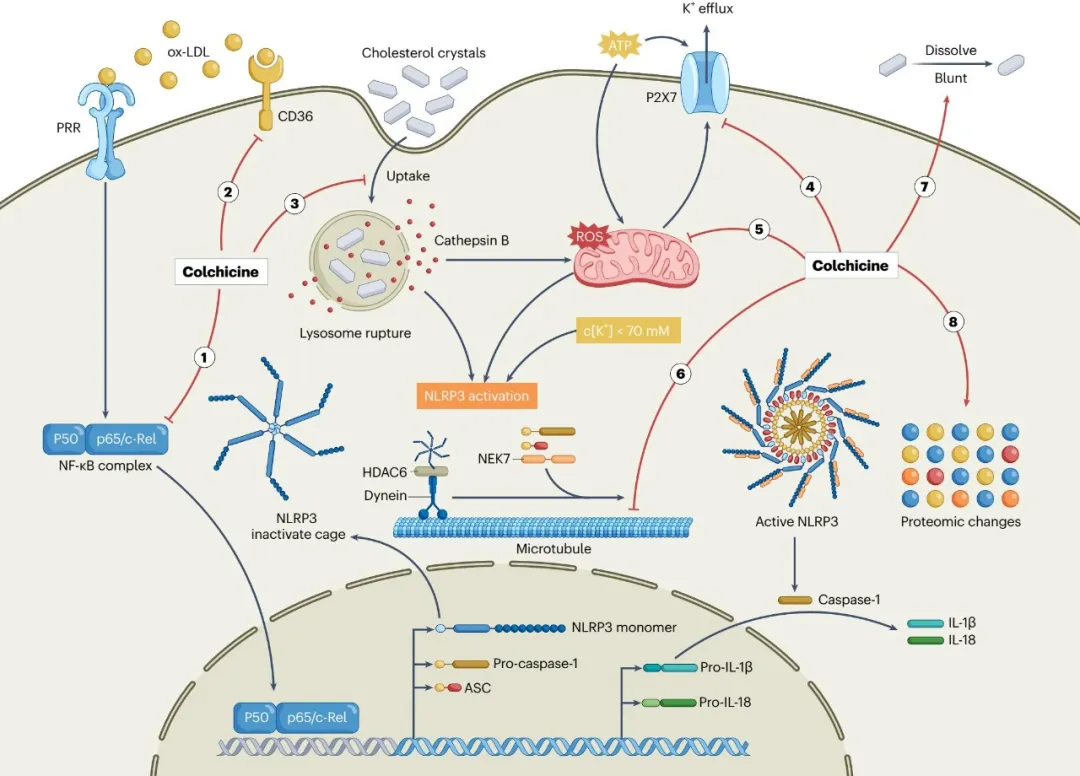
图2. 秋水仙碱抑制炎症小体活化的多重机制。秋水仙碱通过抑制NF-κB priming、降低CD36表达、减少胆固醇晶体摄取、抑制P2X7-K⁺外流、减轻ROS信号并干扰HDAC6–dynein介导的NLRP3炎症小体组装,最终减少炎症因子的释放。同时秋水仙碱还可以改变胆固醇晶体的物理形态以及重塑细胞蛋白组学。
氧化应激、肌动蛋白、胆固醇晶体调节以及蛋白组学重塑
除微管-NLRP3炎症小体轴外,综述还总结了秋水仙碱在ASCVD中的多种作用机制。首先,秋水仙碱可降低炎症因子及黏附分子表达,并减少ROS生成。其次,近期研究提示秋水仙碱可与G-actin结合,影响F-actin/G-actin比例,从而参与白细胞迁移、内皮屏障稳定性和血管细胞力学调节。此外,秋水仙碱可减少胆固醇晶体形成和体积扩张,并使晶体边缘钝化,从而可能通过降低炎症活化和改善晶体形态双重途径稳定斑块。近年来,多组学研究为理解秋水仙碱的系统性抗炎作用提供了新证据。LoDoCo2蛋白组学亚研究显示,低剂量秋水仙碱治疗30天后,稳定性冠心病患者血浆中多种炎症相关蛋白下降,包括IL-18、IL-1RA、IL-6以及中性粒细胞颗粒蛋白PRTN3、MPO、CEACAM8和AZU1等。同时,NEMO和补体相关成分下降,提示上游NF-κB和补体炎症网络受到调控。在氧化低密度脂蛋白刺激的人源巨噬细胞模型中,低纳摩尔浓度秋水仙碱即可改变约850种蛋白表达,涉及内吞、肌动蛋白动态和内质网应激等过程,并可降低CD36转运、减少脂质摄取和泡沫细胞形成(图2)。上述结果表明,秋水仙碱并非仅通过降低单一炎症标志物发挥作用,而是重塑先天免疫和代谢网络。
秋水仙碱对细胞功能的调控
ASCVD的发生发展涉及中性粒细胞、单核/巨噬细胞、内皮细胞、血管平滑肌细胞和血小板等多种细胞。综述系统总结了秋水仙碱在这些细胞中的作用(图3)。
在中性粒细胞中,秋水仙碱抑制迁移、黏附、脱颗粒和NETosis,减少MMP、弹性蛋白酶和α-防御素释放,从而降低斑块炎症和纤维帽降解风险。
在单核细胞和巨噬细胞中,秋水仙碱减少趋化和黏附,降低CD36介导的氧化LDL摄取,抑制泡沫细胞形成,并促进巨噬细胞向抗炎M2样表型转化。
在内皮细胞中,秋水仙碱下调E-selectin、VCAM-1等黏附分子,减少白细胞滚动、黏附和跨内皮迁移,同时抑制胆固醇晶体诱导的内皮焦亡。
在血管平滑肌细胞中,秋水仙碱可能通过维持收缩表型、抑制异常增殖和迁移,促进纤维帽稳定。
在血小板中,秋水仙碱可抑制血小板活化、聚集以及血小板-单核细胞、血小板-中性粒细胞相互作用,提示其抗炎获益可能部分来自血小板炎症功能的调控,而不只是传统意义上的抗栓作用。
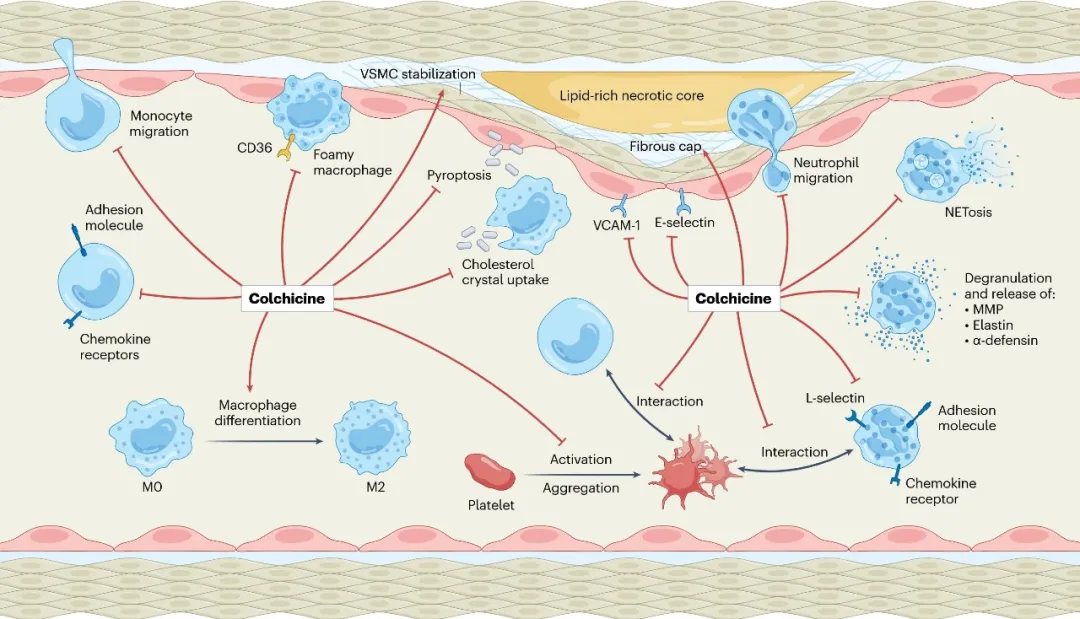
图3. 秋水仙碱对动脉粥样硬化相关细胞功能的调控。秋水仙碱同时作用于中性粒细胞、单核/巨噬细胞、内皮细胞、血管平滑肌细胞和血小板,协同降低血管炎症、抑制泡沫细胞形成、减轻内皮损伤并促进斑块稳定。
冠心病获益更明确,脑血管疾病仍待精准筛选
在临床转化层面,综述系统比较了秋水仙碱在慢性冠脉综合征、急性冠脉综合征、急性卒中及外周动脉疾病中的研究证据。总体而言,低剂量秋水仙碱在冠心病二级预防中的获益最为明确,并已被多项国际指南纳入推荐。相比之下,脑血管疾病领域的结果并不一致。CONVINCE研究的意向性分析未显著降低主要复合终点,CHANCE-3研究中早期短程应用秋水仙碱亦未降低90天复发卒中风险。原文认为,这可能反映冠脉疾病与脑血管疾病在炎症驱动机制、疾病阶段及治疗窗口方面存在差异。此外,ACS患者中秋水仙碱降低hsCRP的效果也呈现异质性,稳定性冠心病中hsCRP下降较为一致,而ACS中结果受心肌坏死范围、给药时机和炎症强度影响更大。
从炎症标志物到斑块稳定:秋水仙碱的临床替代终点证据
综述还系统总结了秋水仙碱对炎症标志物、克隆性造血及斑块稳定性的影响。多项早期临床研究显示,低剂量秋水仙碱可在稳定性冠心病患者中持续降低hsCRP水平。此外,综述还关注了克隆性造血(CHIP)这一新兴炎症风险因素。与此同时,CCTA和OCT等影像学研究显示,秋水仙碱可能改善冠脉高危斑块负荷、增加纤维帽厚度,并降低斑块易损性。这些证据共同提示,秋水仙碱的临床获益不仅体现在事件风险降低,也可能源于对炎症负荷、克隆性免疫重塑和斑块稳定性的多层次调控。
总结与展望
在未来应用方向上,综述强调了几个关键问题。首先,如何优化剂量以在获益和风险之间取得最佳平衡。现有荟萃分析支持低剂量、长期秋水仙碱用于二级预防,但胃肠道不良反应和肝毒性仍可能增加停药风险。由于秋水仙碱治疗窗较窄,低于0.5 mg每日剂量是否能在保持疗效的同时进一步改善安全性,仍需更多研究验证。其次,东亚人群中的疗效和安全性值得重点关注。
此外,秋水仙碱与抗血小板治疗的联合应用也是重要转化方向。如何在降低炎症残余风险的同时避免出血风险增加,是未来临床应用必须回答的问题。早期研究提示,秋水仙碱联合P2Y12受体抑制剂可能同时带来抗炎和抗栓获益,但现有证据仍受样本量小、随访时间短和人群选择限制,仍需进一步临床验证。
更重要的是,秋水仙碱的未来应用不应停留在广谱抗炎,而应走向精准抗炎治疗。hsCRP、IL-6等炎症标志物可用于识别残余炎症风险,CHIP等基因组特征则可提示潜在促炎生物学状态。将炎症标志物、基因组信息、影像学斑块特征和蛋白组学变化进行整合,有望进一步优化患者筛选,推动ASCVD抗炎治疗从经验用药走向机制导向和个体化决策。
本综述由华中科技大学同济医学院附属协和医院心内科程翔团队完成。第一作者为夏心怡博士、杨芬副主任医师、廖雨函博士后;程翔教授为通讯作者。该工作获得以下项目资助:国家科技重大专项、国家自然科学基金、湖北省技术创新计划项目、武汉市重点研发计划项目。
原文链接:
https://doi.org/10.1038/s44161-026-00807-5


