Small:南方医科大学刘瑞源等团队合作研究构建多功能光疗诊断纳米粒用于肿瘤光热/光动力治疗
时间:2025-01-25 12:08:28 热度:37.1℃ 作者:网络
近红外(NIR)触发的I型光敏剂对于解决光疗中缺氧肿瘤微环境的限制至关重要,但仍面临一定挑战。通过选择缺电子单元,上能级态的匹配能隙有助于提高I型电子转移过程的系统间交叉效率。
2025年1月15日,南方医科大学刘瑞源、Li Xiang和江汉大学/广东技术师范大学Hu Liwen共同通讯在Small 在线发表题为“Effective One-for-All Phototheranostic Agent for Hypoxia-Tolerant NIR-II Fluorescent/PA Image-Guided Phototherapy”的研究论文。2-氰基噻唑是一种电子受体,与N,N-二苯基-4-(噻吩-2-基)苯胺共价连接,得到多功能光敏剂(TTNH),具有固有的NIR吸光度和相容的T2能级,促进辐射和非辐射转变。
由TTNH组装而成的纳米颗粒(TTNHNPs)被808nm激光激活并产生O2•−,用于常氧和低氧条件下的耐缺氧I型光动力疗法。TTNHNPs发射NIR-II荧光,NIR-II荧光量子产率为2.08%。TTNHNPs在808nm激光刺激下具有51.8%的高光热转换效率,表现出光热治疗性能,由于其强大的NIR吸收,同时增强了光声成像能力。这些特性使TTNH成为一种有效的NIR触发光疗诊断剂,其性能优于针对低氧肿瘤的NIR-II荧光/光声双模型成像引导的I型光动力疗法/光热疗法,为开发高性能NIR-II发射超氧自由基光疗诊断剂提供了参考。

癌症是世界范围内死亡的主要原因,对人类健康和社会经济发展具有深刻影响。光疗,包括光动力疗法(PDT)和光热疗法(PTT),由于其非侵入性、不良反应风险低和边缘组织损伤最小,已成为癌症治疗的最新策略。在治疗过程中,光疗诊断剂,即光敏剂(PS)或光热剂(PTA),通过捕获吸收的光子产生活性氧(ROS)或产生局部热量,导致肿瘤细胞不可逆的损伤、坏死甚至凋亡。然而,由于PDT中固有的缺氧肿瘤微环境和PTT中获得性热阻特征,单模式光疗很少能达到最佳疗效。
PDT和PTT的整合会产生协同效应,以克服每种疗法的局限性并增强治疗效果。PTT可以通过增强血流来提高氧水平,增强PDT的治疗效果,而PDT会调节肿瘤微环境(缺氧和还原性),破坏肿瘤生理学并使肿瘤细胞对PTT敏感。然而,大多数联合光疗系统同时将PSs和PTA整合到纳米平台中,需要两个或多个具有不同波长的激光器来激活。值得注意的是,PDT主要在可见光区域(400-700nm)被激发,对于治疗深部肿瘤来说并不适用。PSs应该是能够在缺氧肿瘤微环境中发挥抗癌作用的I型PDT材料,而不是对用于肿瘤抑制的O2浓度高度敏感的II型PDT材料。I型PDT/PTT多模式疗法需要近红外(NIR)触发的PS。
1000-1700nm范围内的荧光成像,称为第二近红外(NIR-II)窗口,是一种在定位肿瘤部位、绘制药物分布途径、成像引导手术治疗和评估治疗结果方面具有长期临床应用效果的实用技术。与常规荧光成像相比,该技术具有快速响应、瞬时监测、检测强度低和经济实惠等优点。与NIR-I荧光成像(700–900nm)相比,还表现出更深的组织穿透性和更高的空间分辨率。由于NIR区域的强烈吸收,NIR-II荧光团也可以在一定程度上起PTA的作用,证明了它们在光声(PA)成像中的应用潜力,为同时监测实体瘤提供了一种替代成像模式。有机NIR-II荧光团可以实现PSs的功能,其毒性较低,同时调节光学特性和治疗效果,可以克服PTT和PDT联合治疗的局限性。然而,由于缺乏合适的材料体系,同时具有PTT和I型PDT功能的有机NIR-II荧光团仍然很少。
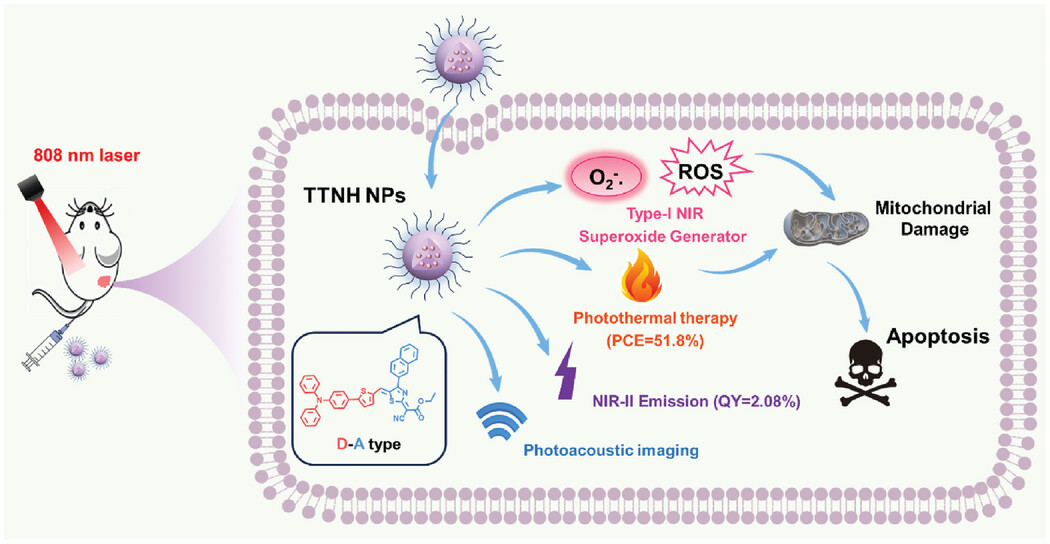
图1 NIR II 发射光疗诊断剂TTNH用于缺氧肿瘤的光动力和光热疗法示意图(摘自Small )
开发一种集成NIR-II FLI、PAI、I型PDT和PTT功能的多功能分子对于为肿瘤提供高质量诊断和协同光疗至关重要。这些诊断和治疗方法存在能量耗散方面的竞争,也缺乏理想的材料系统。因此,需要搭建在NIR-II窗口具有优异荧光量子产率(QY)的高性能光疗纳米平台,通过单波长激光照射实现高诊断准确性和精确的PDT/PTT协同治疗。
该研究开发了一种具有高光热功效的D-A结构化NIR吸收有机光疗诊断剂(TTNH),可同时作为功能性PTA和超氧自由基发生器,用于肿瘤诊断和治疗。TTNH表现出以下光疗诊断特性:1)在808nm激光刺激下,具有出色的光敏特性,通过I型PDT机制产生O2•−。小能隙(ΔES1-T2=0.06)TTNH具有显著的自旋轨道耦合(SOC)常数(ξS1-T2,1.33cm-1),表现出优异的PDT功能。此外,TTNH对光漂白具有抵抗力,提高了其在缺氧肿瘤环境中的抗肿瘤效率;2)由于最高占据分子轨道(HOMO)和最低未占据分子轨道(LUMO)电子云部分重叠,TTNH表现出较强的NIR-II荧光,QY为2.08%;3)TTNH表现出显著的光热效应,光转换效率为51.8%,并且在强大的NIR吸光度和高摩尔消光系数的驱动下,在NIR区域具有卓越的PA能力;4)在I型PDT/PTT联合治疗期间,TTNH损伤线粒体并诱导细胞凋亡。结果表明,TTNH具有优异的体内治疗效果。
参考消息:
https://onlinelibrary.wiley.com/doi/full/10.1002/smll.202406226?saml_referrer


