同济大学附属上海市肺科医院/上海大学《自然·通讯》:开发机械驱动可膨胀贴片,协同微电流与机械力级联促进气管缺损重建
时间:2026-05-06 19:12:57 热度:37.1℃ 作者:网络
背景介绍
气管缺损可由肿瘤切除、狭窄、感染、创伤或先天畸形等多种因素引起,是一种严重且可能危及生命的呼吸系统疾病,可导致进行性气道阻塞、呼吸窘迫甚至致命性窒息。尽管外科技术不断进步,但当前临床干预手段(包括气管吻合术、自体组织移植和人工气管移植)在处理大范围或复杂性缺损时仍存在严重不足。气管吻合术受限于胸段气管的深部位置和有限延展性,术后吻合口狭窄风险高;自体组织移植虽生物相容性好,但供区创伤大、并发症发生率高;人工气管移植则面临血管化不良、易感染和免疫排斥等问题。组织工程虽为有前景的替代方案,但现有策略难以同时模拟天然气管的生物力学特性和生物学复杂性,且无法提供持续、空间和时间可控的再生信号,严重限制了血管重建和组织修复的疗效。
研究思路
针对上述挑战,同济大学附属上海市肺科医院胸外科的陈昶教授、陈瑜教授和上海大学谢雨洁教授团队联合开发了一种机械驱动的3D打印压电系统(PFT)。该系统由聚左旋乳酸(PLLA)3D打印支架经L-二苯丙氨酸(FF)和单宁酸(TA)表面功能化构建压电层,并与负载氢纳米泡(NB)的明胶甲基丙烯酰(GelMA)水凝胶(GN)复合而成。在外源性超声(US)激活下,系统通过氢纳米泡空化诱导水凝胶微膨胀,实现缺损的有效密封;同时,压电支架将机械能转化为局部电信号,协同激活Piezo1-Notch信号通路,促进内皮细胞血管化。通过可编程超声实现持久的电压输出(0-2 V)和时序调控,在兔和羊的气管缺损模型中,四周的序贯刺激实现了100%的气管闭合和通畅率,组织再生效率提高了24.65%。这种机械驱动的可膨胀贴片系统为依赖于血管化的各系统器官再生提供了一种可持续、可控的外部调控策略。相关内容以Mechanically-driven expandable patch promotes tracheal defect reconstruction via synergistic microcurrent and mechanical force cascades为题,发表在Nature Communications!

图片解析
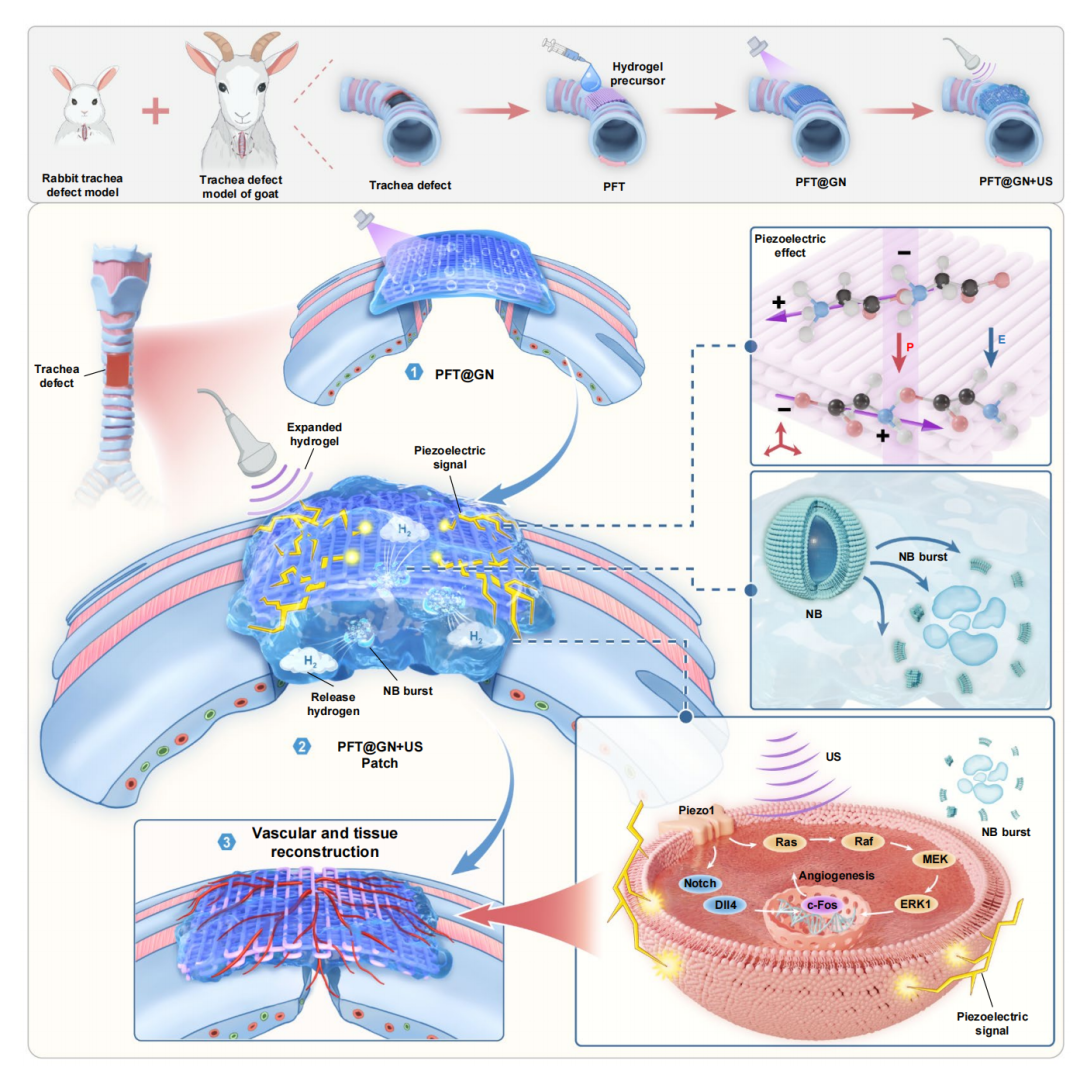
图1. 机械驱动可膨胀贴片的制备及其气管缺损修复原理示意图: (A) 复合贴片应用于兔和羊气管缺损,加入水凝胶前体溶液,经紫外光(365 nm)和超声(1 MHz, 0.98 W/cm²)激发形成复合贴片。超声用于持续可控触发以实现治疗效果。(B) 机械驱动可膨胀贴片的机制示意图:有效密封气管缺损,同时利用压电效应促进微血管重建和组织再生。

图2. 机械驱动可膨胀贴片的制备与表征: (A) 通过挤出打印和表面功能化构建压电PFT 3D打印支架的多步制备策略示意图。(B) 超声触发(1 MHz, 0.98 W/cm²)氢纳米泡破裂诱导水凝胶微膨胀的示意图。(C) PLLA支架的熔融挤出3D打印照片。(D) 经FF/TA浸泡功能化后的冻干3D打印支架(PLLA、PFT)照片。(E) PLLA和PFT 3D打印支架的光学显微镜图像(左标尺1 mm,右标尺300 μm)及SEM图像显示PFT支架上的自组装纳米管结构(标尺50 nm)。(F) 水凝胶超声激活前后的顶部照片。(G) NB结构的TEM图像(标尺50 nm);PFT水凝胶结构和嵌入NB的SEM图像(标尺100 μm和200 nm);EDS磷元素分布图确认NB掺入。(H) EDS能谱显示水凝胶组间元素组成差异,主要体现在磷含量。(I) 荧光标记后共聚焦显微镜图像验证水凝胶基质内NB分布。(J) 机械驱动可膨胀贴片的制备过程及照片,展示PFT@GN+US的原位交联和微膨胀状态。
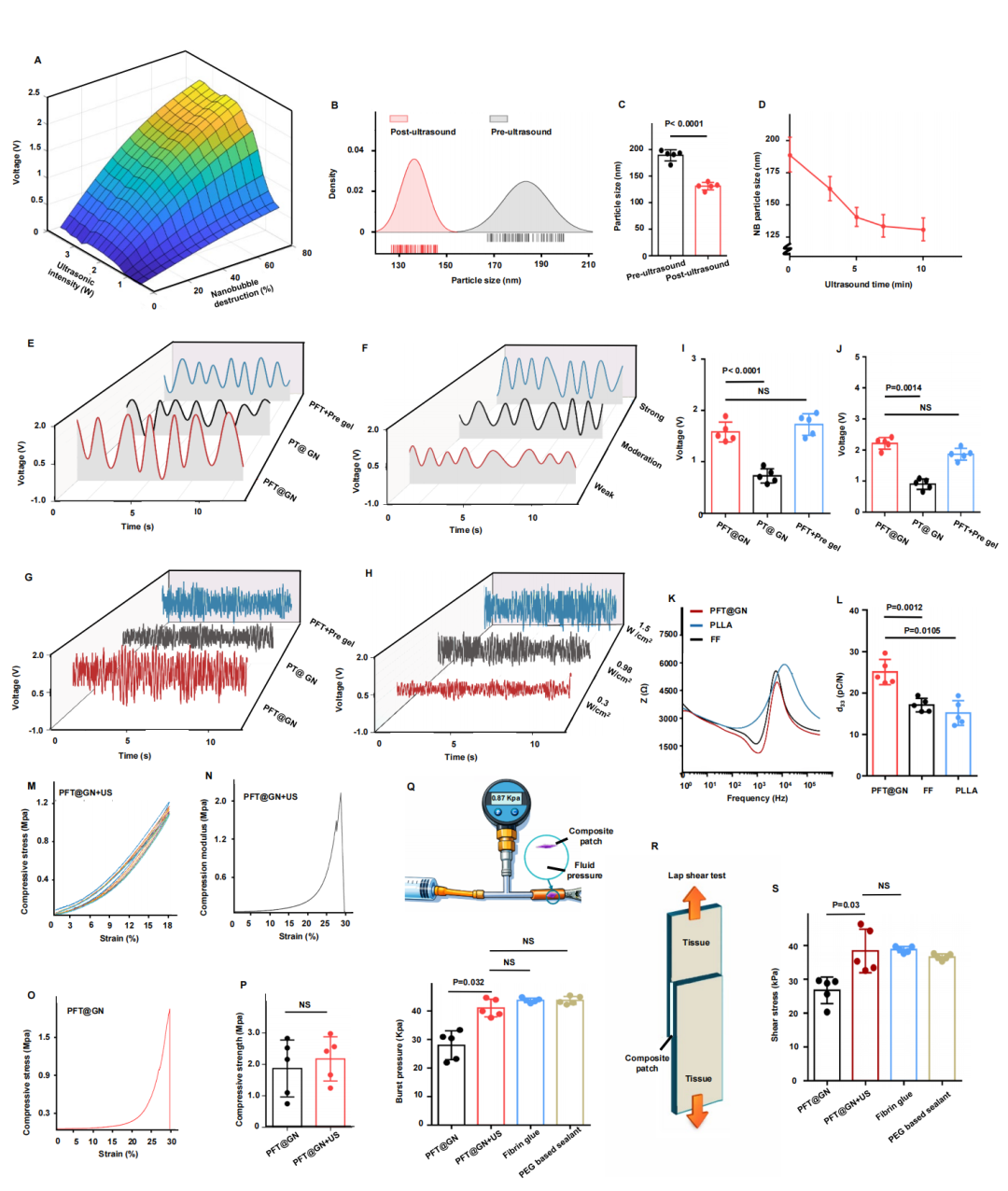
图3. 机械驱动可膨胀贴片的机电表征和压电性能: (A) 超声强度、纳米泡破裂速率与压电输出之间关系的数值拟合模型。(B) 超声暴露前后纳米泡的DLS曲线。(C) 超声暴露前后平均直径的定量比较(P<0.0001,n=5)。(D) 含血清培养基中不同超声暴露时间下NB的水动力学直径(n=3)。(E) 不同配方(PFT+Pre-gel、PT@GN和PFT@GN)在均匀机械压缩后的压电输出变化。(F) PFT@GN贴片在不同压缩力(10 N、30 N、50 N)下的压电输出变化。(G) 各组间的超声触发电压输出。(H) PFT@GN复合贴片在不同超声强度(0.3、0.98、1.5 W/cm²)下的机械输出分析。(I-J) 不同材料组的电压输出定量分析(n=5)。(K) 原始PLLA、FF和PFT@GN的阻抗模量Z随频率的变化。(L) PLLA、FF和PFT@GN的本征压电系数d33(n=5)。(M-P) 通过5次压缩-卸载循环和压缩实验对PFT@GN+US复合贴片的压缩模量和抗爆破压力耐受性进行定量评估(n=5)。(Q) 爆破压力测试示意图及PFT@GN、PFT@GN+US、纤维蛋白胶和PEG基密封剂的爆破压力比较(n=5)。(R-S) 复合贴片的搭接剪切粘附强度测试,与临床用密封剂比较。

图4. 机械驱动可膨胀贴片在体外促血管生成功能、生物相容性及潜在分子机制的探究: (A) HUVECs与PFT+US、PLLA+US和PFT组共培养,共聚焦显微镜观察细胞附着和生长(DAPI蓝,鬼笔环肽红,标尺50 μm)。(B) 放大共聚焦视图分析HUVECs在复合支架表面的生长取向和分布(标尺15 μm)。(C) 极坐标图映射PFT+US和PLLA+US组的细胞表面生长角度。(D) PBS、PFT+Gel+US、PFT@Gel+US、PFT@GN+US和PFT@GN+US组的体外血管化能力评估(Live/Dead染色,标尺100 μm)。(E-F) ImageJ统计分析血管化能力(总网格面积和总长度,n=5)。(G) 复合贴片-HUVEC共培养中Live/Dead染色的统计分析(n=5)。(H) 复合贴片与HUVECs共培养后进行转录组测序的工作流程示意图。(I) 与细胞生长、血管化、代谢调控和免疫反应相关的差异表达基因热图。(J) KEGG通路富集气泡图。(K) 关键DEGs总结用于分析Piezo1相关信号通路。(L) Western blot验证DEGs蛋白表达水平。
图5. 机械驱动电膨胀贴片在体内的气管修复和离体粘附评估: (A-B) 使用猪肌肉和皮肤组织评估粘附性能,贴片制备后用止血钳和水压进行粘附测试。(C) PFT@GN+US贴片治疗兔气管缺损的过程及示意图,超声实现序贯机械触发。(D) 观察PFT@GN+US复合贴片在气管表面的粘附性能,后用止血钳压缩测试进一步评估粘附效果。(E) 气管缺损修复的超声成像研究,关注气管形态(虚线)和复合贴片的降解。(F) PFT@GN+US贴片治疗兔气管缺损的手术流程示意图,包括预附着、前体溶液施加、UV交联(365 nm,15分钟)和超声触发微膨胀(1 MHz, 0.98 W/cm²)及相关放大视图。(G) 超声探头(1 MHz, 0.98 W/cm²)以间歇模式直接辐照猪皮肤的代表性热图像。辐照区内表面温度在1、3、6、10分钟时记录,从21.6°C逐渐升高至42.1°C。(H) PT@Gel+US和PFT@GN+US贴片治疗兔的生存率分析。
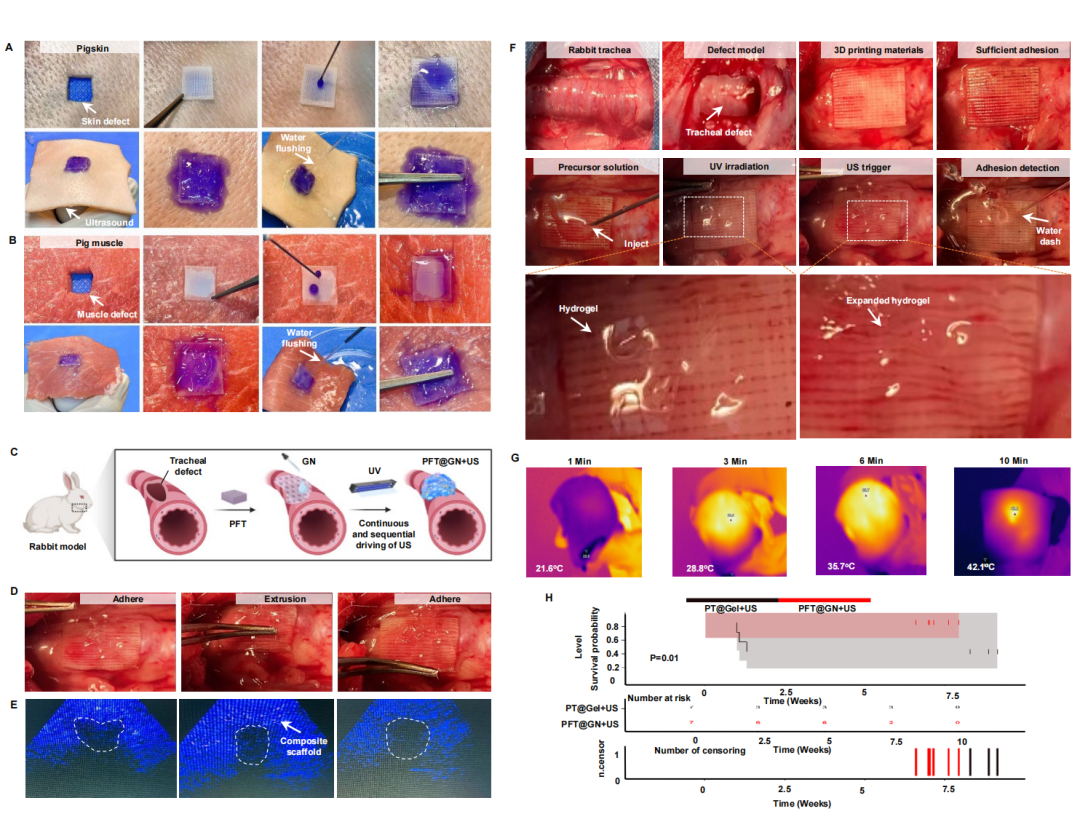
图6. 机械驱动可膨胀贴片在兔气管缺损修复中的治疗效果评估: (A) 贴片植入后支气管镜评估气管腔内情况(气道通畅性、炎症状态和整体修复效果)。(B) 呼吸周期内不同时间点(0、1、1.5、2.5秒)的彩色多普勒超声显示贴片区域的血流信号。(C) 修复区域周围血管再生的肉眼解剖观察。(D-E) 不同组别气管修复的组织学评估:H&E染色和Masson三色染色(天狼星红/固绿),显示软骨、黏膜和血管化基质组织的再生。(F-G) 基于H&E、Masson三色染色的软骨再生和周围组织修复的定量分析(n=4)。(H) 不同治疗组修复区域PDGFRα(红)和DAPI(蓝)免疫荧光染色评估成纤维细胞重塑,标尺100 μm(n=5)。(I) PDGFRα荧光强度定量(n=5)。(J, M-O) 修复区域软骨再生标志物Aggrecan(绿)、Sox9(黄)和Collagen II(红)的免疫荧光染色及定量,DAPI核复染,标尺20 μm(n=5)。(K, P) CK14(红)、乙酰化微管蛋白(Ac-Tub,绿)和DAPI(蓝)免疫荧光共染色评估气管上皮再生,上皮厚度定量以微米表示,标尺50 μm(主图)和5 μm(放大图)(n=5)。(L) 基于H&E、PDGFRα和CD31染色的单位面积血管密度定量(n=5)。
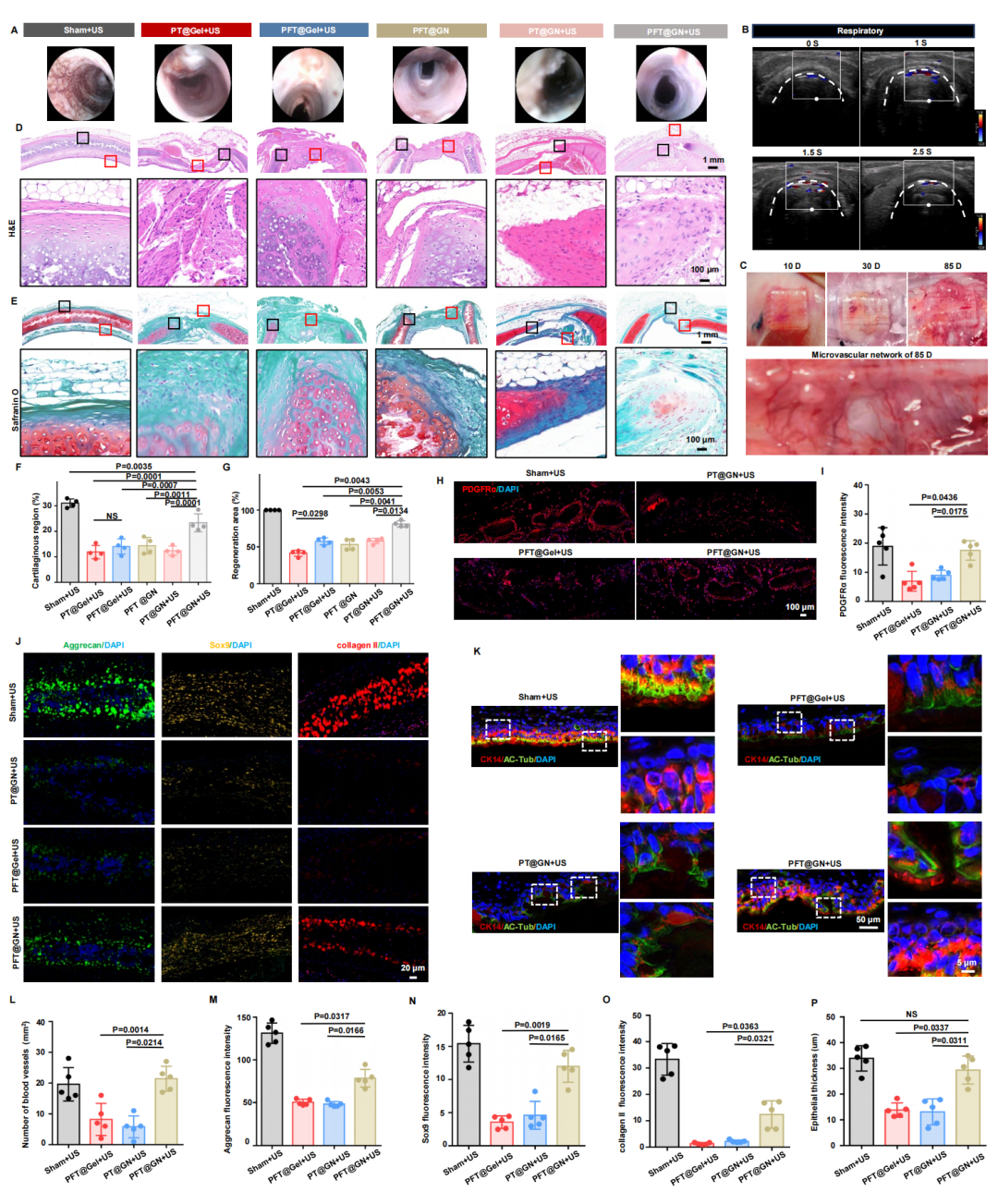
图7. 机械驱动可膨胀贴片在山羊气管缺损修复中的治疗效果研究: (A) 使用复合贴片修复山羊气管缺损的过程示意图,包括局部放大视图。(B) 复合贴片治疗方案的时间线图,包括特定时间点执行的关键步骤。(C) 缺损治疗过程的术中照片记录。(D) 气管修复后的支气管镜评估,评估通畅性、炎症和修复效果等关键指标。(E) 修复后超声成像评估,彩色多普勒显示缺损周围血流信号,虚线表示软骨修复状态。(F, I) 8周术后终点,每组山羊的支气管镜图像、相应H&E染色组织学切片和胶原免疫荧光图像(Collagen/DAPI),以及基于组织学切片的再生面积百分比定量(P=0.0306)和胶原荧光强度定量(P=0.0175)(n=3)。(G, J) PFT@GN+US和PT@Gel+US组的荧光强度定量。(H, K-L) 体内评估Piezo1和CD31在组织修复中表达的双免疫荧光染色(n=3),绿色Piezo1,红色CD31,蓝色DAPI核染色。
结论
本研究成功开发了一种机械驱动的可膨胀贴片系统(PFT@GN+US),通过3D打印压电支架与超声响应性水凝胶的复合设计,同时实现了气管缺损的即时有效密封和持续的促血管化信号提供。该系统利用超声触发氢纳米泡空化诱导水凝胶微膨胀,实现缺损的自适应封闭;同时,压电支架将机械能转化为局部电信号,激活内皮细胞中的Piezo1-Notch信号通路,协同促进血管再生和组织修复。在兔和羊的气管缺损模型中,该系统实现了100%的气管闭合和通畅率,软骨、黏膜和血管化基质组织均得到良好再生,且未观察到热损伤或明显炎症反应。该策略展示了机械-电耦合在组织工程中的巨大潜力,为依赖于血管化的复杂组织缺损修复提供了新的范式。
原文链接:
https://doi.org/10.1038/s41467-026-72593-4


