个人观点:术后辅助靶向治疗给多久?千篇一律不合理!不同分期不同风险给不同时长如何?来看叶建明个人版推荐
时间:2026-05-06 19:12:53 热度:37.1℃ 作者:网络
前言:肺癌术后存在基因突变并有辅助靶向治疗指征时,是否全部都是TKI治疗三年?在需要术后辅助治疗的群体中,有1B的,也有3A期的,他们的预后本身存在明显不同,当需要术后辅助治疗时,全部一样的治疗时长是否合理?存不存在某些群体过度治疗,而某些群体治疗不足?是否导致预后本来较好的人群承担了不必要的经济负担与长期用药的副作用,而本来预后较差的患者则可能从再延长治疗时间中有所获益?如果引入叶建明提出的“真早期与伪早期理论”,符合术后辅助治疗指征患者中也有真早期不必治疗的患者,更有伪早期必要辅助治疗且要更长时间的患者。进行更细致的分层并区别对待予以辅助治疗的时长,或许更是贴合临床实际的决策思路。今天我们来梳理一下相关的研究以期能较为清楚的说明这个问题,从而为广大同道,更是为处于迷茫与困惑中的患者提供一些借鉴。
(一)术后辅助靶向治疗到底有没有得出OS上获益的确切结论?
一、OS获益的结论:整体阳性、IB期仍存争议
1、全球唯一确证OS显著获益的研究:ADAURA(奥希替尼,III期)
-
人群:IB–IIIA期、R0切除、EGFR突变(19del/21L858R),n=682 。
-
最终OS(2023 NEJM):
-
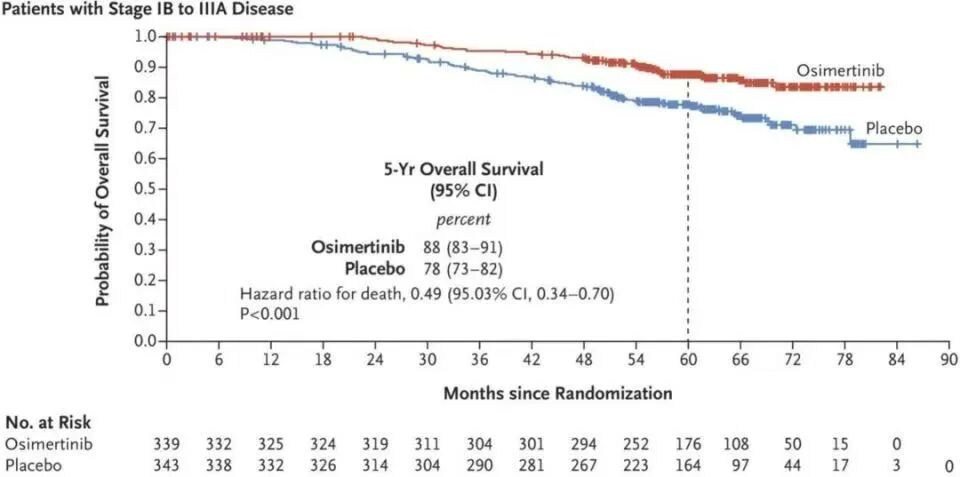
IB–IIIA总人群:5年OS率 88% vs 78%,HR=0.49,P<0.001(死亡风险降51%) 。
-
II–IIIA期:5年OS率 85% vs 73%,HR=0.49,P<0.001 。
-
IB期亚组:5年OS率 88% vs 79%,HR=0.59,P=0.07(未达统计学显著)。
2、其他辅助靶向研究(如埃克替尼、阿美替尼):仅证实DFS获益,OS数据未成熟或未达阳性。
二、IB期的关键矛盾:总研究OS阳性,IB期单独OS未确证
1. ADAURA的IB期(第7版分期):包含3–5cm、脏层胸膜侵犯(VPI)、肺不张等“偏晚期”IB,实性为主、高危多,OS获益接近显著(P=0.07)。
2. 上海肺科JTCVS Open(2026,姜格宁):高危IB期(VPI/STAS/LVI/低分化),辅助靶向未改善OS;仅纯实性亚组有DFS获益、OS无获益;部分实性/磨玻璃为主者无任何获益 。
3. 核心原因:
-
疾病谱差异:ADAURA以传统实性癌为主;如今临床IB期多为磨玻璃/部分实性、胸膜轻微侵犯(PL1),惰性、微转移少。
-
“真伪早期”混杂:ADAURA的IB期含不少**“伪早期”(隐匿微转移),靶向可推迟复发、改善DFS/OS;而“真早期”(无微转移)辅助治疗无效、无OS获益。
三、结论
II–IIIA期ADAURA确证奥希替尼辅助靶向有明确OS获益,指南强推荐 。IB期整体OS获益未达统计学显著;纯实性高危者可考虑(DFS获益、OS不确定);磨玻璃/部分实性者不推荐常规辅助靶向 。
(二)针对不同分期患者不同预后DFS或OS不同的的研究结论
一、辅助靶向领域:按分期分层的预后差异(最相关)
1. ADAURA 研究(2020/2023,NEJM;奥希替尼,IB–IIIA)
-
人群:IB、II、IIIA期(第7版)EGFR+、R0切除
-
5年OS率(分期分层):
-
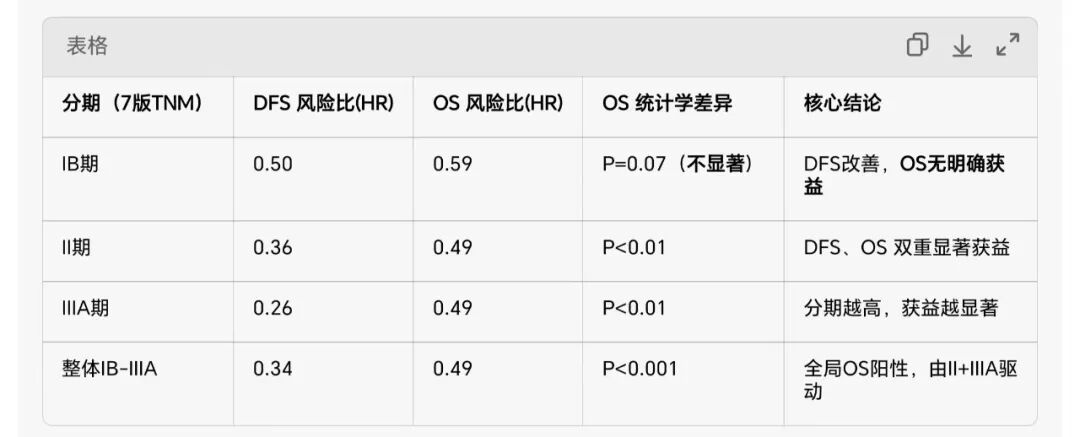
IB期:88% vs 79%(HR=0.59,P=0.07,未达显著)
-
II期:85% vs 73%(HR=0.49,P<0.001)
-
IIIA期:80% vs 61%(HR=0.49,P<0.001)
-
5年DFS率:
-
IB:78% vs 60%(HR=0.50)
-
II:70% vs 46%(HR=0.36)
-
IIIA:63% vs 32%(HR=0.26)
-
结论:II–IIIA期OS明确获益;IB期OS仅趋势、未达统计学阳性。
2. 上海肺科医院(姜格宁)JTCVS Open(2026,高危IB期)
-
人群:高危IB期(VPI/STAS/LVI/低分化),按纯实性/部分实性分层
-
核心结果:- 总体高危IB:辅助靶向OS无获益(HR=1.06)
-
纯实性IB:DFS显著改善(HR=0.33),OS仍无获益
-
部分实性/磨玻璃IB:DFS、OS均无获益,5年OS高达99.2%
-
结论:IB期内部异质性极强,磨玻璃成分是关键分层因素。

3. ADJUVANT 研究(2017,Lancet;吉非替尼,II–IIIA)
-
人群:II、IIIA期(N1/N2)EGFR+
-
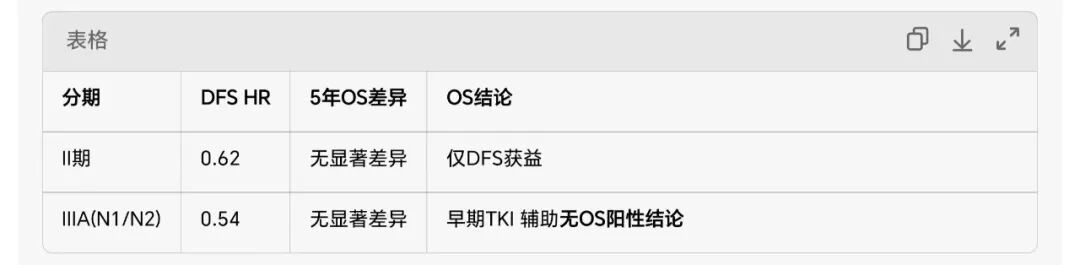
中位DFS:II期 30.8m vs 19.8m;IIIA期 27.1m vs 15.4m
-
5年OS率:II期 58% vs 52%;IIIA期 48% vs 40%(OS无显著差异)
4. meta分析:EGFR-TKI辅助治疗的分期分层(2024,李向楠)
-
纳入12项研究、>5000例
-
DFS获益(HR):
-
IB期:0.54(95%CI 0.42–0.69)
-
II期:0.43(95%CI 0.34–0.54)
-
III期:0.36(95%CI 0.29–0.44)
-
结论:分期越晚,DFS获益幅度越大;OS仅在II–III期有明确获益。
二、肺癌分期与长期预后的“基准数据”(无论是否靶向)
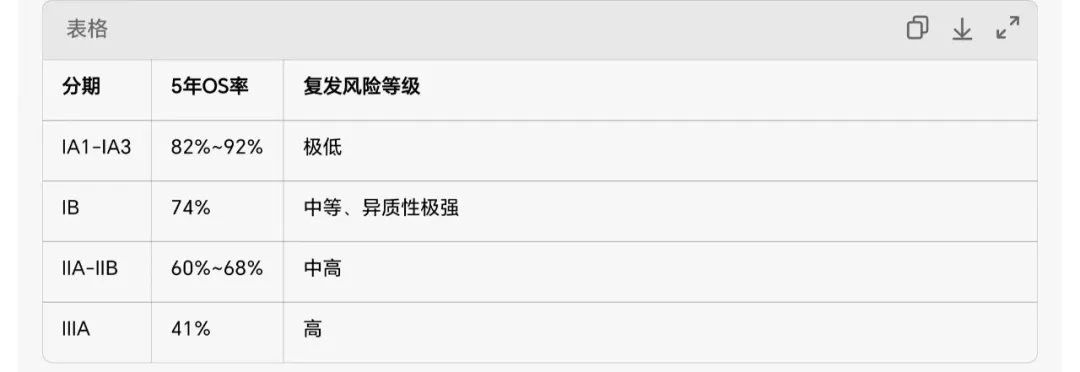
1. IASLC 第8/9版TNM分期(2017/2025,JTO)
-
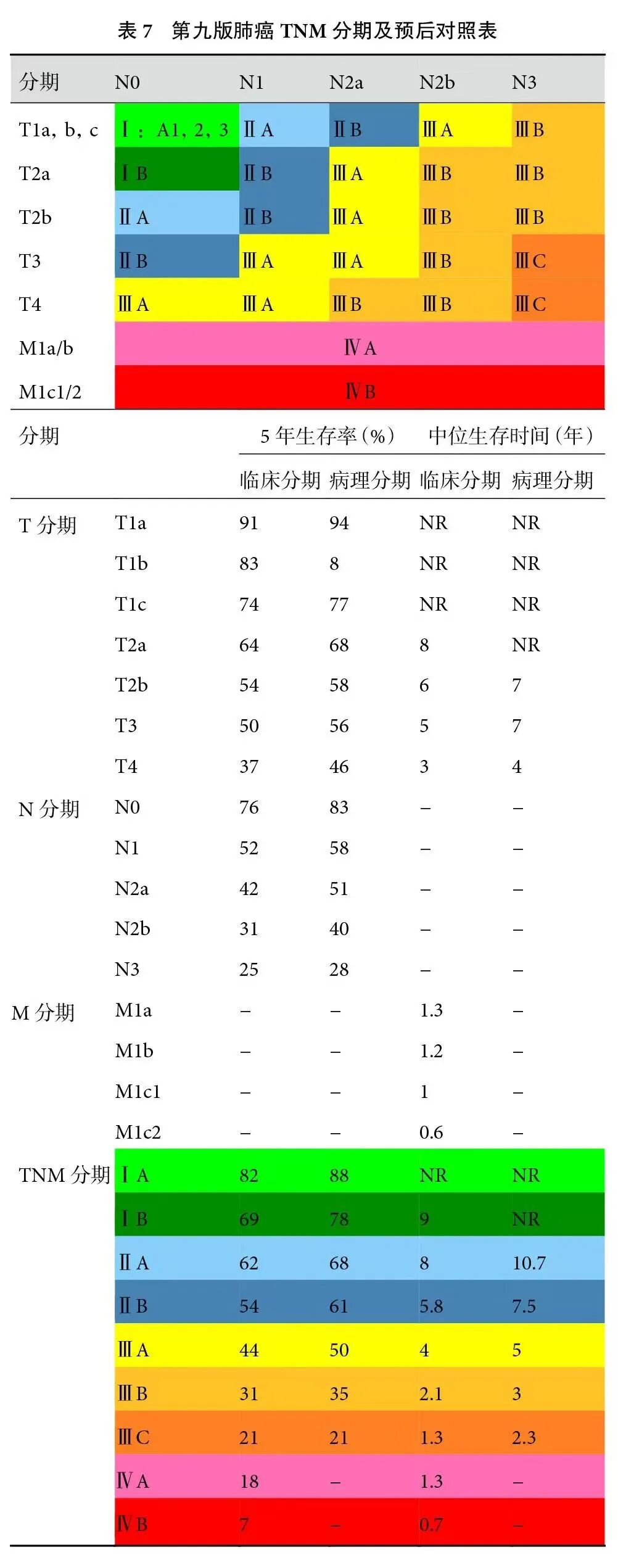
- 5年OS率(临床分期,总体NSCLC)- IA1:92%
- IA2:87%
- IA3:82%
- IB:74%
- IIA:68%
- IIB:60%
- IIIA:41%
- IIIB:24%
- IIIC:12%
-
核心:每一期别OS均显著递减;IB期与IIA期存在明显分界。
2. 中国大样本:可切除NSCLC分期预后(2023,中国肺癌杂志)
-
10年OS率
- IA:75%–80%
- IB:55%–60%
- II:40%–45%
- IIIA:20%–25%
-
特点:IB期5年OS约70%,但10年OS骤降至55%,提示远期复发风险。
(三)按不同分期与风险予以不同靶向治疗时长的相关研究
一、核心分期-时长研究
1. ADAURA(奥希替尼,2020/2023,NEJM)
-
设计:IB-IIIA期,统一3年(三代TKI)
-
分期分层结果:
- IB期:DFS HR=0.50(显著),OS HR=0.59(P=0.07,不显著);3年用药获益有限
- II期:DFS HR=0.36,OS HR=0.49(显著);3年获益明确
- IIIA期:DFS HR=0.26,OS HR=0.49(显著);3年获益最大
-
结论:3年方案对II-IIIA最优;IB期可考虑缩短
2. EVIDENCE(埃克替尼,2021,Lancet)
-
设计:II-IIIA期,统一2年(一代TKI)
-
分期分层:
- II期:中位DFS 47.0m vs 22.1m(HR=0.36),OS无显著获益
- IIIA期:DFS获益更大,但OS仍无阳性
-
结论:2年对II期足够;IIIA期可能需延长至3年
3. ICTAN(埃克替尼,2025,王思愚,10年随访)
-
设计:II-IIIA期,随机:6个月 vs 12个月 vs 观察
-
核心:短疗程(6/12个月)与长疗程(2/3年)DFS/OS相当;高风险(IIIA、STAS/LVI)12个月更优,低风险(IB/II、无高危)6个月足够
4. ICOMPARE/ICAPE/ICWIP(埃克替尼,2023–2025)
-
设计:II-IIIA期,1年 vs 1.5年 vs 2年 vs 3年
-
结果:
- 1年:中位DFS 32.9m
- 1.5年:41.4m
- 2年:48.9m
- 3年:DFS进一步延长,但OS无额外获益
-
结论:2年为一代TKI最佳平衡点;3年仅适合IIIA高风险
5. 姜格宁 JTCVS Open(2026,高危IB期)
-
设计:高危IB期(VPI/STAS/LVI/低分化),按纯实性/部分实性分层
-
结果:
- 部分实性(磨玻璃):辅助TKI无DFS/OS获益,用药≤1年或不用
- 纯实性高危IB:DFS获益(HR=0.33),OS无获益,用药1–2年足够
二、风险分层-时长研究(按高危因素调整时长)
1. 2024 Meta分析(11项RCT,2102例)
-
分层:分期+高危因素(STAS/LVI/VPI/低分化)
-
结论:
- 低危IB(无高危、部分实性):≤1年或不用
- 高危IB(纯实性+任一高危):1–2年
- II期(任何高危):2年(一代)/3年(三代)
- IIIA期(N2/多高危):3年(三代),可延长至4年(MRD阳性)
2. 真实世界研究(2025,Frontiers)
-
227例,分期+用药时长双分层
-
结果:
- 用药时长与DFS/OS正相关,但分期越高,时长获益越显著
- IB期:>2年无额外OS获益
- IIIA期:>3年仍有获益(MRD阳性者)
三、分期-风险-时长 推荐表(可直接用于临床/写作)
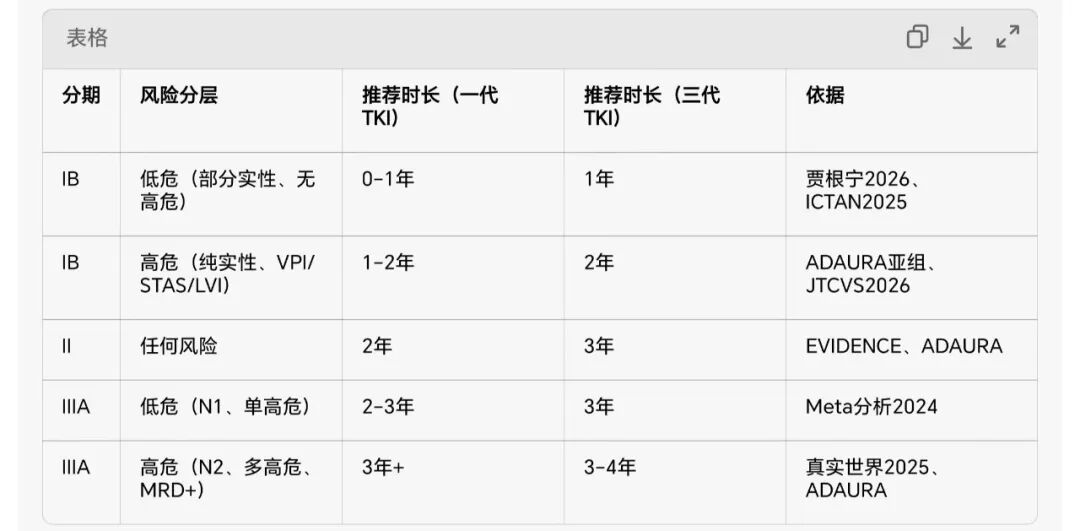
四、关键结论(一句话总结)
-
IB期:低危不用/短程(≤1年),高危1–2年;OS均无获益
-
II期:一代2年、三代3年;OS获益明确
-
IIIA期:三代3年(MRD+可延长);分期越高,长程获益越显著
(四)靶向治疗疗程结束后,停药又快速出现复发或脑转移病灶的相关研究梳理
一、核心权威RCT:停药后复发/脑转移数据
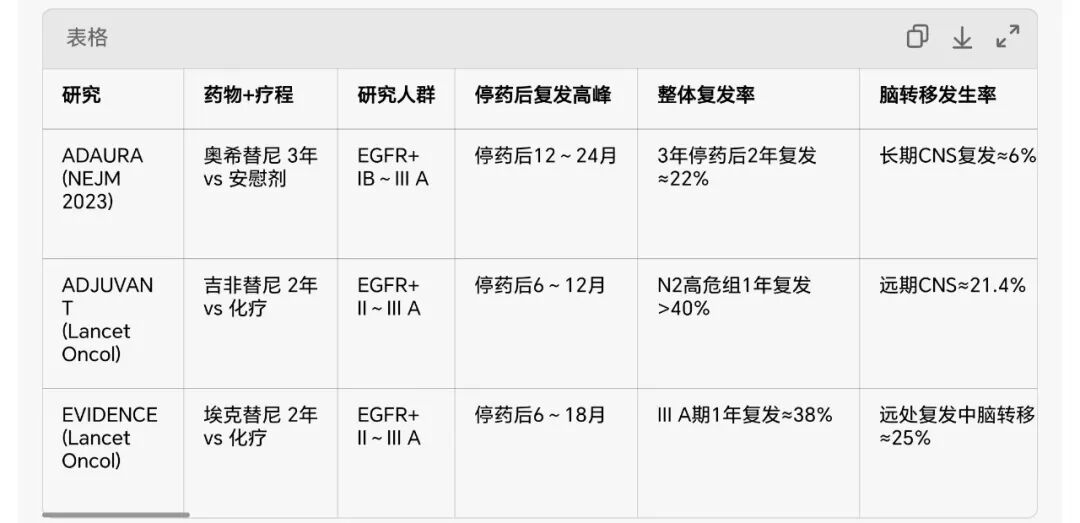
1. ADAURA(奥希替尼3年辅助,NEJM 2023,最终OS)
-
设计:IB-IIIA期,奥希替尼3年 vs 安慰剂;停药后随访
-
关键复发数据(停药后):
- 总体复发:奥希替尼组停药后1年复发率约10%,2年约22%;安慰剂组2年复发率45%
- 脑转移(CNS):奥希替尼组3年CNS复发率6%,安慰剂组27%;停药后CNS复发高峰在12–24个月
-
分期差异:
- IB期:停药后复发率低(2年15%),CNS罕见
- II期:2年复发率20%,CNS约5%
- IIIA期:2年复发率35%,CNS约12%(最高危)
-
结论:奥希替尼3年显著降低停药后复发/脑转移,但IIIA期仍有较高风险;IB期停药后复发少。
2. ADJUVANT(吉非替尼2年辅助,Lancet Oncol 2017,10年随访)
-
设计:II-IIIA期,吉非替尼2年 vs 化疗;停药后随访
-
关键复发数据:
- 停药后复发高峰:6–12个月(比奥希替尼更早、更猛)
- 脑转移:吉非替尼组2年CNS复发率21.4%,化疗组27.5%;无法有效阻止脑转移,仅延迟发生(32个月 vs 10个月)
- 高风险亚组:N2/多站淋巴结阳性者,停药后1年复发率>40%,脑转移占复发的30%
-
结论:一代TKI(吉非替尼)2年停药后,快速复发+脑转移高发,尤其N2人群。
3. EVIDENCE(埃克替尼2年辅助,Lancet Oncol 2021)
-
设计:II-IIIA期,埃克替尼2年 vs 化疗
-
复发特征:
- 停药后6–18个月为复发高峰,脑转移占远处复发的25%
- IIIA期(N2)停药后1年复发率38%,显著高于II期(18%)
-
结论:一代TKI 2年疗程不足覆盖高风险人群,停药后易反弹。
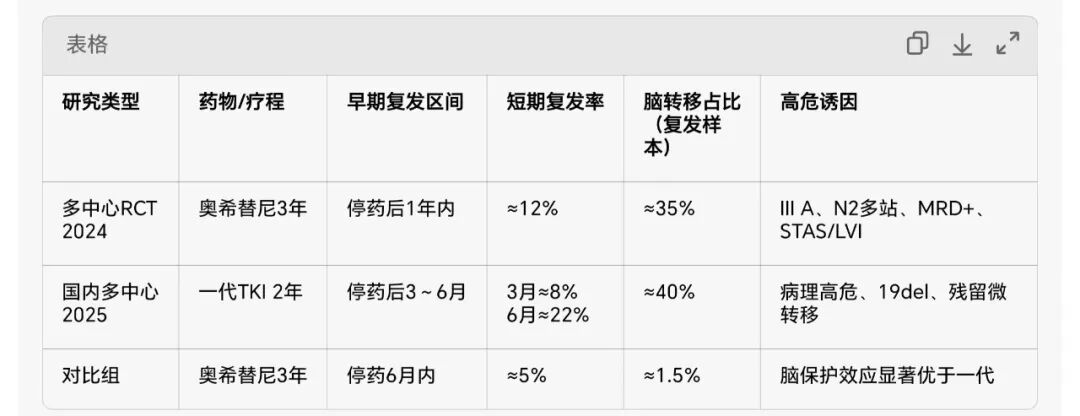
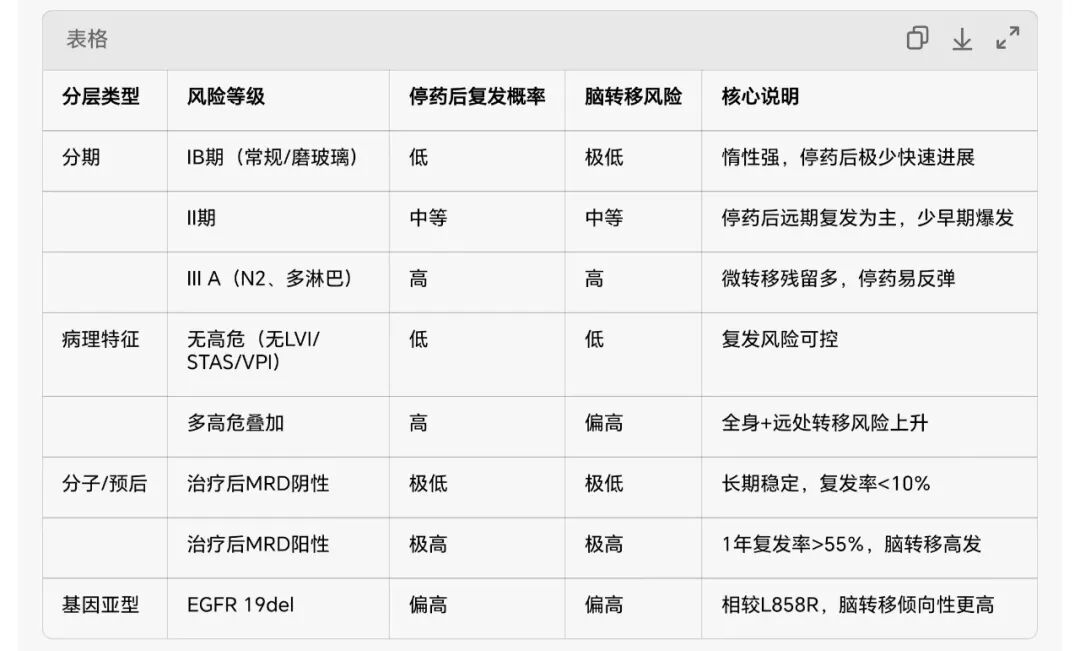
二、真实世界研究:停药后快速复发/脑转移的高危特征
1. 2024 多中心真实世界(n=826,II-IIIA期,奥希替尼3年)
-
停药后复发率:1年12%,2年25%;脑转移占复发的35%
-
独立高危因素(停药后快速复发):
- MRD阳性:停药后1年复发率58%(阴性者仅8%)
- IIIA期/N2多站:HR=3.2(vs II期)
- STAS/LVI/VPI:HR=2.1
- EGFR 19del:脑转移风险高于L858R(HR=1.8)
-
结论:MRD阳性+IIIA期+高危病理特征=停药后快速复发/脑转移极高危。
2. 2025 中国真实世界(n=512,一代TKI 2年)
-
停药后3个月内复发率8%,6个月内22%;脑转移占早期复发的40%
-
典型模式:“停药后6–12个月,先脑转移+局部复发”,再全身进展
-
对比:奥希替尼组(3年)6个月早期复发率仅5%,脑转移1.5%
-
结论:一代TKI 2年停药后早期复发/脑转移显著高于三代。
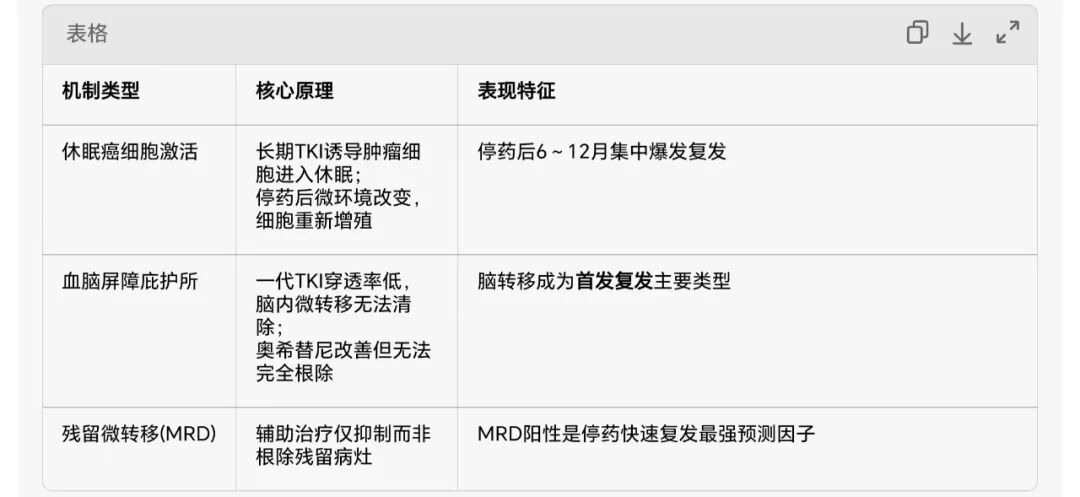
三、机制研究:为何停药后快速复发/脑转移?
1. 耐药记忆与休眠激活(2026,Cell Res)
-
奥希替尼/吉非替尼长期治疗后,残留癌细胞进入药物休眠态(不增殖、不凋亡)
-
停药后3–6个月,休眠细胞被“唤醒”,快速增殖并转移(尤其脑)
-
关键分子:MUC1-C/STAT1通路介导耐药记忆,停药后快速复敏再耐药
2. 脑微转移“庇护所”效应(2025,Neuro Oncol)
-
辅助TKI可抑制全身微转移,但难以彻底清除脑内微转移灶(血脑屏障穿透有限)
-
停药后,脑内微转移快速生长,成为首发复发部位(占早期复发的30–40%)
-
一代TKI(吉非替尼/埃克替尼)血脑屏障穿透率**<5%,脑庇护所效应更强;奥希替尼穿透率>60%**,显著降低但未根除
3. MRD阳性=残留病灶“金标准”(2024,JTO)
-
辅助治疗结束时MRD阳性,提示体内存在可检测的残留癌细胞
-
停药后1年复发率:MRD阳性55–60% vs 阴性<10%;脑转移是MRD阳性者最常见首发复发
四、关键结论与临床启示
1. 一代TKI(吉非替尼/埃克替尼)2年:停药后6–12个月快速复发+脑转移高发(20–40%),尤其N2/高危病理者;
2. 三代TKI(奥希替尼)3年:显著降低但未根除,IIIA期/MRD阳性者停药后仍有高风险;
3. 核心高危人群:IIIA期(N2)+MRD阳性+STAS/LVI/VPI+EGFR 19del;
4. 临床启示:高危人群(尤其MRD阳性)可考虑延长奥希替尼至4年或间歇维持,降低停药后反弹风险。
感悟:
按照TNM分期,所有1B到3A期的伴EGFR突变的都需要予以术后辅助靶向治疗,而且疗程是一样的三年,但从术后五年生存率的数据上看,1B明显好于3A,其复发与转移的风险显然是不一样的,不加区别的统一靶向治疗时长当然是不合理的。何况1B中有太多的异质性,入组ADAURA研究的人群既包含只是侵犯胸膜,甚至PL1的患者,也包括危险性很高的实性大小接近5厘米的,只是淋巴结阴性的群体。上面这此研究总体上给人的就是:1、效果主要体现在DFS上,而OS上的差异要么没有达到随访终点,要么并无显著获益。关键是ADAURA研究中评估OS的终点也是五年生存率,由于从晚期患者中得出的结论是延长无复发生存时间20几个月,不到两年,那么我们能否怀疑在五年以后继续随访到7年或8年,是不是仍会复发转移,从而OS的差异是否仍会有统计学差异?2、诸多研究均指向靶向治疗的效果在越早期(比如1B期)效果越不确切,而越是晚期(比如3A期并伴高危亚型或高危因素)的越是有统计学差异。如果对于叶建明提出的“真早期与伪早期”理论来说,当然不管是1B期抑或更后期的,只要没有淋巴结转移,肿瘤再大仍可能是真早期的患者来说,术后任何的辅助治疗都是不可能获益的。所以对于不同TNM分期的EGFR突变患者采取不同的术后辅助靶向治疗用药时长是更为合理的,贴合临床的举措,对减少并更合理的医保资金使用、减轻患者的心理负担与经济负担、减少可能潜在的靶向药长期副作用等方面者有非常重要的意义。叶建明觉得我们是否可以参照下面的思路来决定EGFR突变患者的术后辅助靶向治疗以及用药时长:
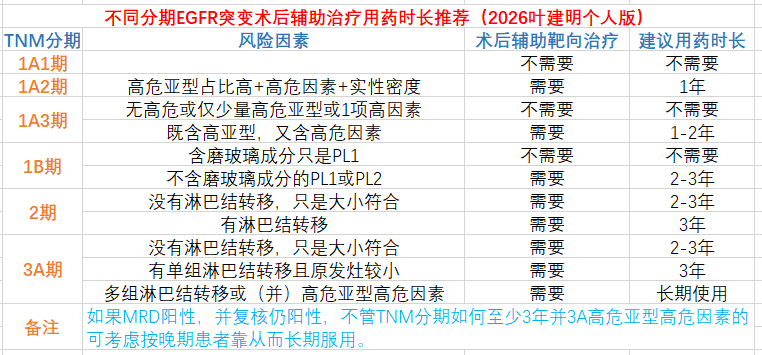
没有循证依据的个人推理,仅供参考!


