广州医科大学Biomaterials:揭示锌基金属通过巨噬细胞源性细胞外囊泡调控早期骨免疫微环境促进血管生成
时间:2026-05-06 19:12:17 热度:37.1℃ 作者:网络
背景介绍
锌(Zn)基可生物降解金属因其适中的降解速率、良好的生物活性和力学性能,在引导骨再生(GBR)领域展现出巨大潜力。与镁(快速降解产氢)和铁(降解过慢、残留物积累)相比,锌具有更平衡的降解行为,能够作为“活性屏障”维持空间并调节局部免疫-血管微环境。然而,锌如何通过免疫调控影响血管生成,特别是巨噬细胞在其中的作用以及细胞外囊泡(EVs)介导的细胞间通讯机制,尚不完全清楚。骨再生是一个多阶段紧密调控的过程,早期免疫微环境对后续修复结局起决定性作用。因此,解析锌基材料调控早期骨免疫微环境的细胞和分子机制,对于开发更高效的骨再生材料具有重要意义。
研究思路
针对上述挑战,广州医科大学口腔医学院/附属口腔医院的李江教授、李萍教授和朱川东教授团队,系统研究了纯锌膜在大鼠颅骨临界骨缺损模型中的成骨和血管生成效果。通过单细胞RNA测序(scRNA-seq)分析术后第3天的再生组织,发现Arg1⁺巨噬细胞是早期骨免疫微环境中的优势亚群,且在锌刺激下显示出增强的囊泡运输相关通路活性。体外实验表明,锌刺激的巨噬细胞条件培养基(Zn-M-CM)可显著促进人脐静脉内皮细胞(HUVECs)的迁移和管形成,而使用EVs抑制剂GW4869则基本消除该效应。进一步分析发现,Zn-M-CM处理的内皮细胞中P2RY11(编码嘌呤能受体P2Y11)表达显著上调。该研究揭示了锌基金属通过促进巨噬细胞释放EVs,进而上调内皮细胞P2Y11表达,促进血管生成的新机制。相关内容以Zinc-based metal orchestrates early osteoimmune microenvironment to promote angiogenesis via macrophage-derived extracellular vesicles发表在Biomaterials!

图片解析
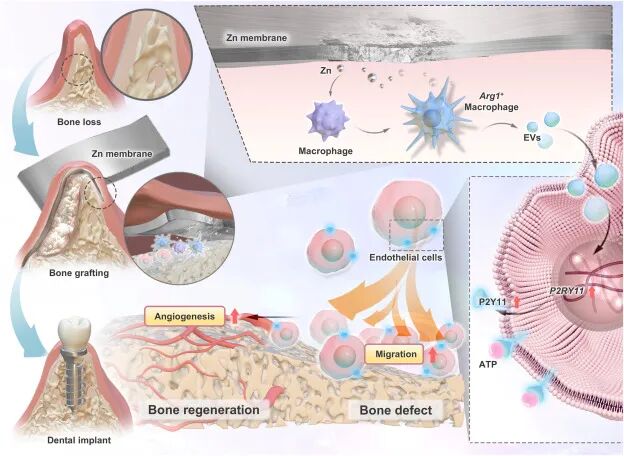
Scheme 1. 锌在骨再生过程中调控血管生成的示意图: 锌膜植入后,早期免疫微环境中出现Arg1⁺巨噬细胞。转录组分析显示这些巨噬细胞富集囊泡运输相关通路。锌刺激增加巨噬细胞EVs释放,巨噬细胞源性EVs参与内皮细胞活化,包括上调P2RY11表达、增强迁移和血管生成反应。
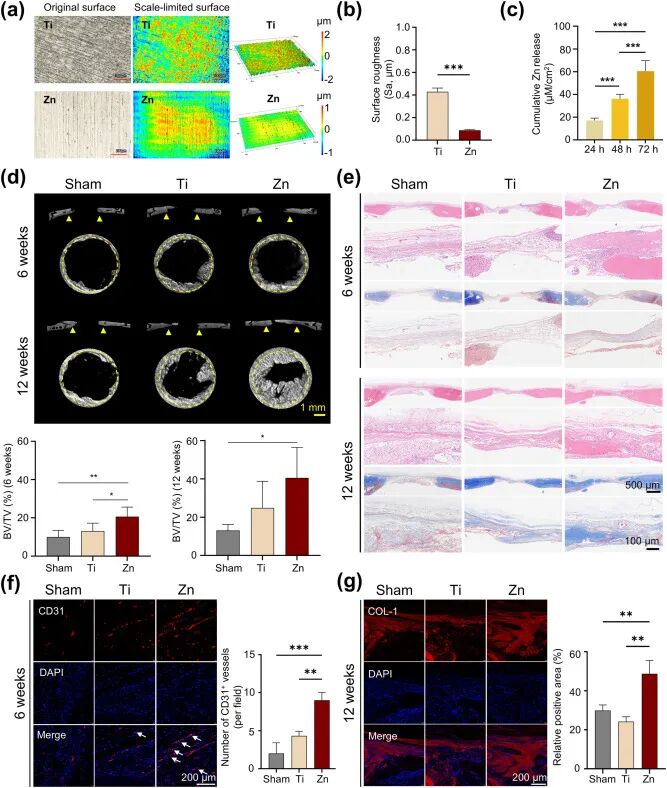
图1. 锌的理化表征及体内骨再生效果: (a) SEM表面形貌:Zn表面较Ti更光滑。(b) 表面粗糙度(Sa)定量:Zn为0.09±0.01 μm,Ti为0.43±0.03 μm(p<0.001)。(c) Zn离子在Hank's溶液中的释放:24 h为17.13±2.09 μM/cm²,48 h为36.09±3.97 μM/cm²,72 h为60.52±9.22 μM/cm²。(d) micro-CT:6周和12周时Zn组骨缺损修复最佳,骨体积分数(BV/TV)显著高于Ti组和Sham组(6周:20.68% vs 13.14% vs 10.04%;12周:40.54% vs 24.82% vs 13.10%)。(e) H&E和Masson染色:Zn组新骨和胶原沉积最丰富。(f) CD31免疫荧光(6周):Zn组新生微血管数量最多。(g) COL-1免疫荧光(12周):Zn组胶原沉积面积最大。
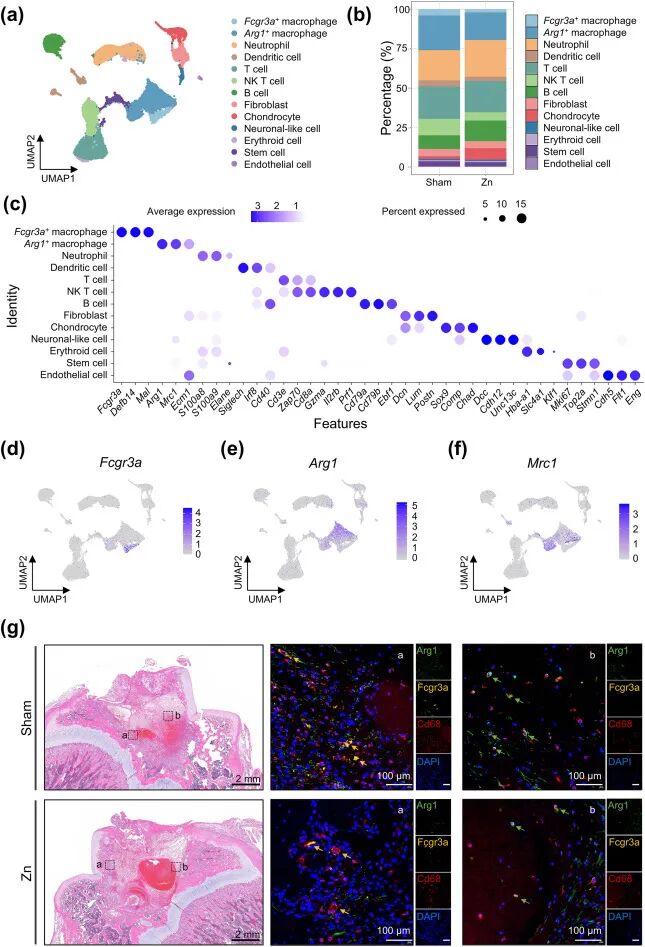
图2. Zn植入缺损的单细胞转录组分析: (a) t-SNE可视化:19个细胞簇,整合为13个主要细胞群。(b) 各组细胞类型比例:Arg1⁺巨噬细胞在两组中均占较大比例,Zn组Fcgr3a⁺巨噬细胞比例降低。(c) 代表性标志基因的点图。(d-f) 特征图:Arg1和Mrc1在巨噬细胞中富集,Fcgr3a表达较低。(g) 组织学验证:H&E显示Sham组炎性渗出,Zn组形成同心圆血凝块结构;三重免疫荧光显示Fcgr3a⁺巨噬细胞(黄色箭头)主要在缺损边缘,Arg1⁺巨噬细胞(绿色箭头)集中在血凝块中央区域。
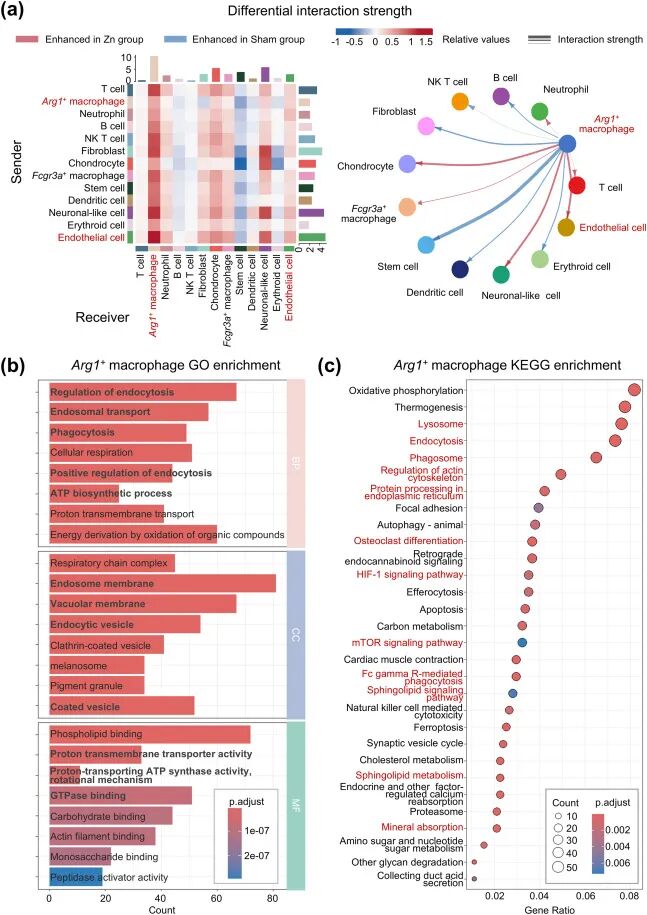
图3. Arg1⁺巨噬细胞的细胞间通讯和功能富集: (a) 热图:Zn组Arg1⁺巨噬细胞向外发送和接收的信号强度均高于Sham组,尤其与内皮细胞、软骨细胞等的相互作用增强。(b) GO富集:Arg1⁺巨噬细胞在生物学过程(BP)中富集于内吞调控、内体运输、吞噬等;细胞组分(CC)富集于内体膜、囊泡等;分子功能(MF)富集于质子跨膜转运、GTPase结合等。(c) KEGG富集:显著富集于溶酶体、吞噬体、内吞作用、FcγR介导的吞噬、HIF-1信号、mTOR信号、鞘脂信号等通路。
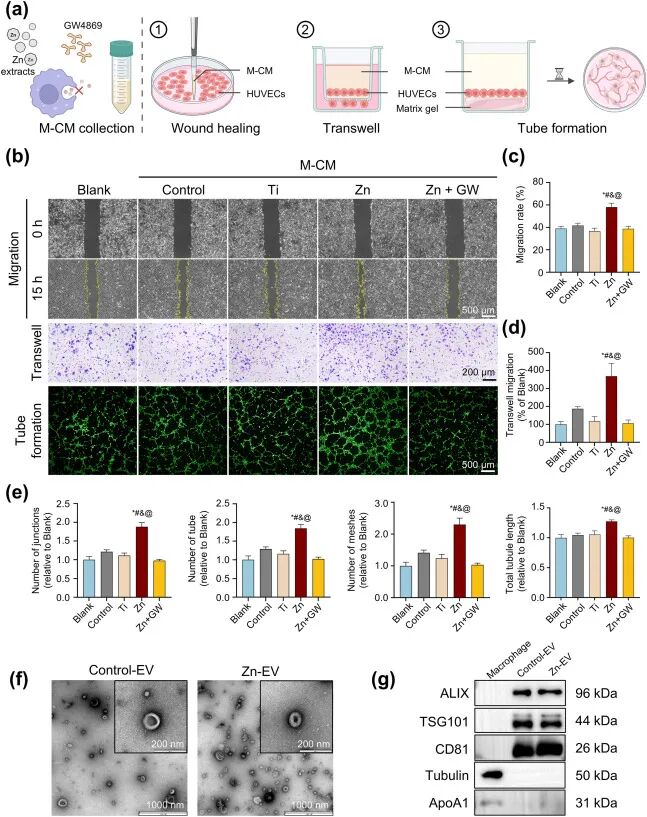
图4. 锌刺激巨噬细胞条件培养基对内皮细胞的功能影响及EVs表征: (a) 实验流程示意图。(b) 伤口愈合、Transwell迁移和管形成代表性图像。(c) 伤口愈合率定量:Zn-M-CM组为58.10±8.50%,显著高于Blank、Control-CM、Ti-M-CM(均约20-30%)和Zn+GW-M-CM(与对照无差异)。(d) Transwell迁移定量:Zn-M-CM组迁移细胞数为Blank组的368.67±158.18%。(e) 管形成参数(连接点、管段、网格数、总管长)定量:Zn-M-CM组均显著高于其他组,Zn+GW-M-CM组降至对照水平。(f) TEM:Zn-M-CM来源的EVs呈杯状,粒径较小。(g) Western blot:EVs阳性标志物ALIX、TSG101、CD81在Control-EV和Zn-EV中均表达,阴性标志物Tubulin和ApoA1几乎不表达。
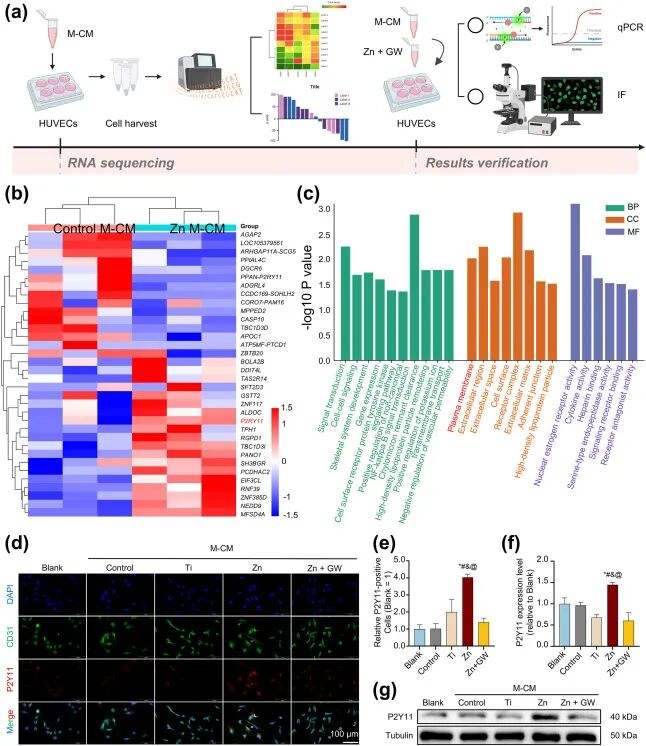
图5. 内皮细胞中P2RY11/P2Y11的鉴定与验证: (a) RNA-seq实验流程。(b) 差异表达基因热图。(c) GO富集:DEGs主要富集于细胞间通讯、受体酪氨酸激酶信号、质膜等。(d) 免疫荧光:CD31(绿)、P2Y11(红)和DAPI(蓝),Zn-M-CM组P2Y11荧光最强。(e) P2Y11阳性细胞百分比定量:Zn-M-CM组约为Blank组的4倍,与Zn+GW-M-CM组有显著差异。(f-g) Western blot定量及代表性条带:Zn-M-CM组P2Y11蛋白表达显著升高,Zn+GW-M-CM组与对照无差异。
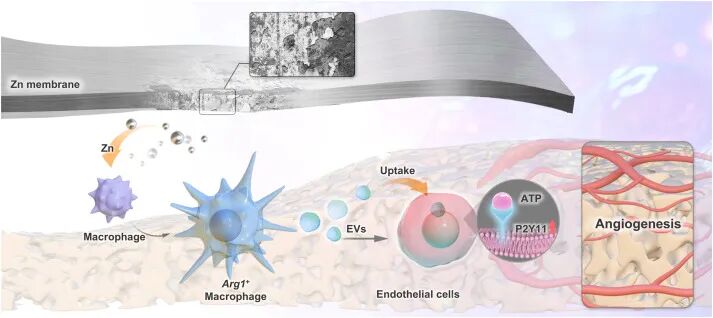
图6. 锌降解产物调控血管生成的作用机制示意图: 总结锌膜植入后,Zn²⁺释放促进巨噬细胞向Arg1⁺表型极化并增强EVs分泌,巨噬细胞源性EVs递送信号至内皮细胞,上调P2RY11表达,从而促进内皮细胞迁移和血管形成,最终加速骨缺损修复。
结论
本研究首次从单细胞层面揭示了锌基金属在早期骨免疫微环境中调控血管生成的细胞和分子机制。主要发现包括:1)锌膜植入后,Arg1⁺巨噬细胞成为早期骨免疫微环境中的关键细胞亚群,并富集囊泡运输相关通路;2)锌刺激的巨噬细胞通过分泌EVs而非直接释放可溶性因子,介导了促血管生成效应;3)内皮细胞中P2RY11表达上调与巨噬细胞源性EVs相关,可能是促迁移和管形成的关键分子事件。该研究为锌基可生物降解金属在引导骨再生中的应用提供了新的免疫-血管调控理论依据,并为开发基于EVs的骨再生治疗策略提供了新思路。
原文链接:
https://doi.org/10.1016/j.biomaterials.2026.124280


