Cardiovasc Res 封面文章 | 西交大一附院王胜鹏团队揭示PIEZO1调控肺血管代谢力学机制
时间:2026-05-05 12:24:57 热度:37.1℃ 作者:网络
肺组织随每一次呼吸循环都承受着周期性的血流动力学与机械应力。作为肺动脉管壁的主要细胞类型,肺动脉平滑肌细胞(PASMCs)持续暴露于周期性应变之中。在病理性机械应力下,PASMCs可从静止的收缩表型转变为增殖、迁移和合成表型,引发肺动脉重构,这是肺动脉高压(PH)和肺纤维化(IPF)共同的细胞病理基础。已知增强的糖酵解代谢会驱动PASMCs从收缩表型向合成表型转化。然而,PASMCs机械力信号与糖酵解代谢究竟如何在肺疾病中耦合,此前一直是未解之谜。
2026年4月25日,西交大一附院王胜鹏/袁祖贻/闫炀团队在国际期刊Cardiovascular Research发表封面文章“PIEZO1 regulates smooth muscle cell plasticity by integrating mechanical stretch with glycolytic metabolism”。该研究首次揭示了机械敏感通道PIEZO1能够整合力学刺激与糖酵解代谢,调控PASMCs表型的可塑性,为肺动脉高压与肺纤维化的治疗提供新靶点,具有重要的临床价值。

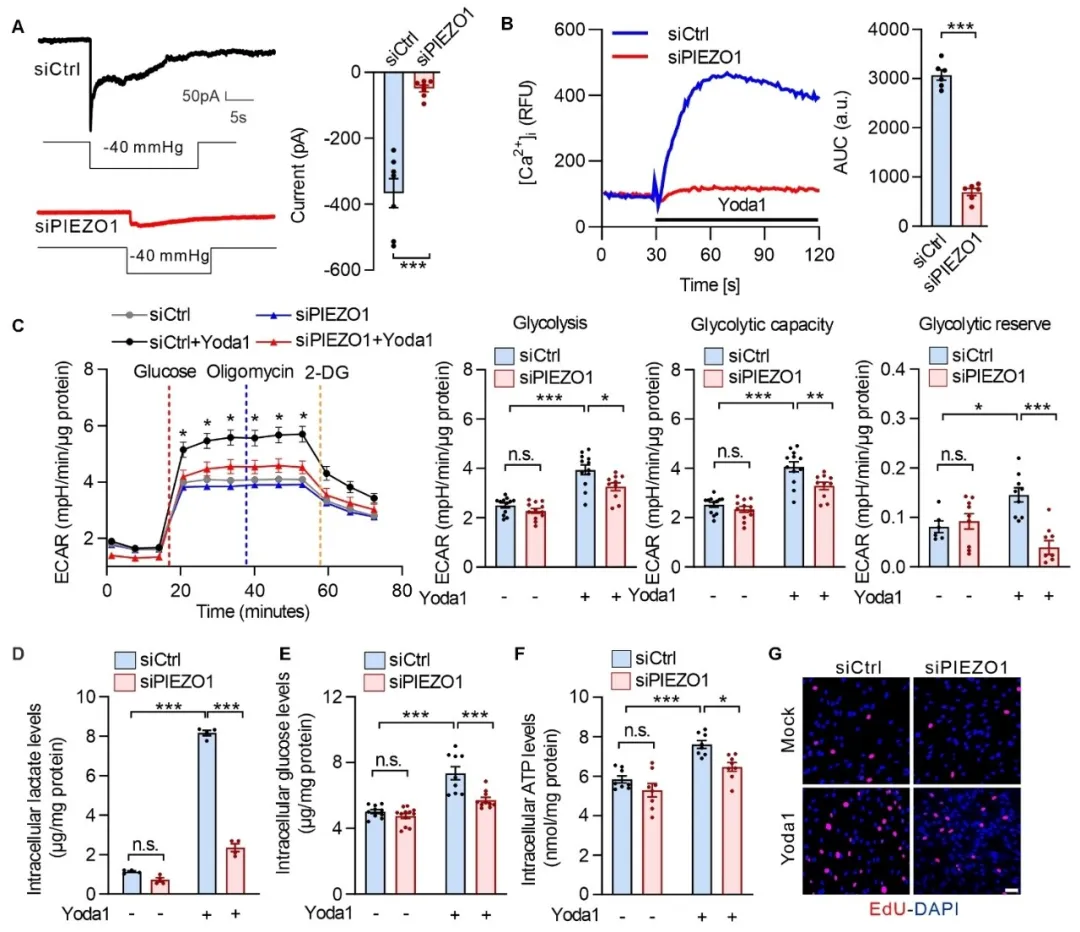
为了探究机械力如何调控PASMC表型可塑性及维持肺稳态,研究团队首先对机械拉伸诱导的PASMCs进行了转录组测序,发现糖酵解通路显著富集。在差异基因分析中,PFKFB3变化水平非常显著,提示PIEZO1可能通过PFKFB3调节PASMCs的糖酵解和增殖。
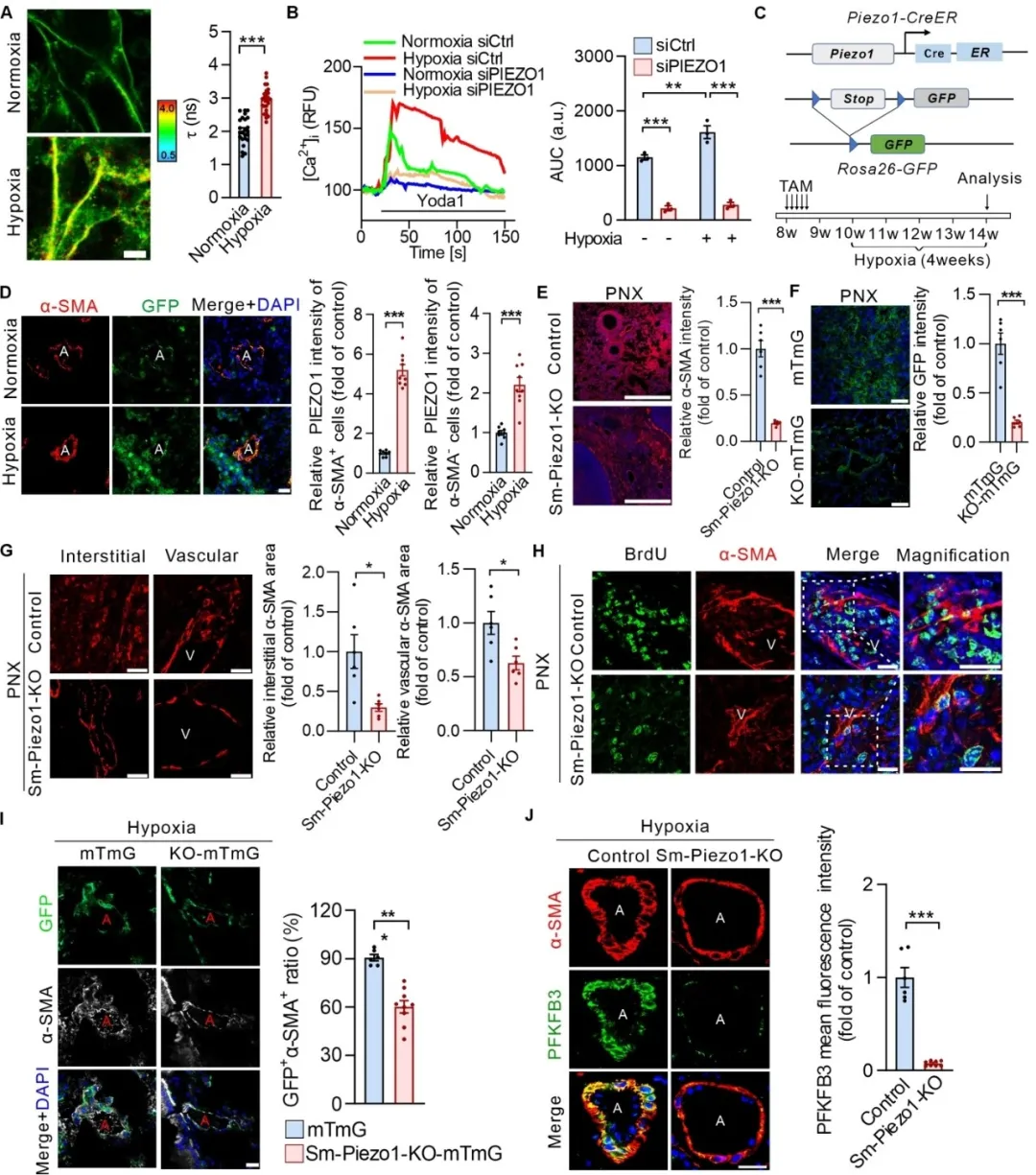
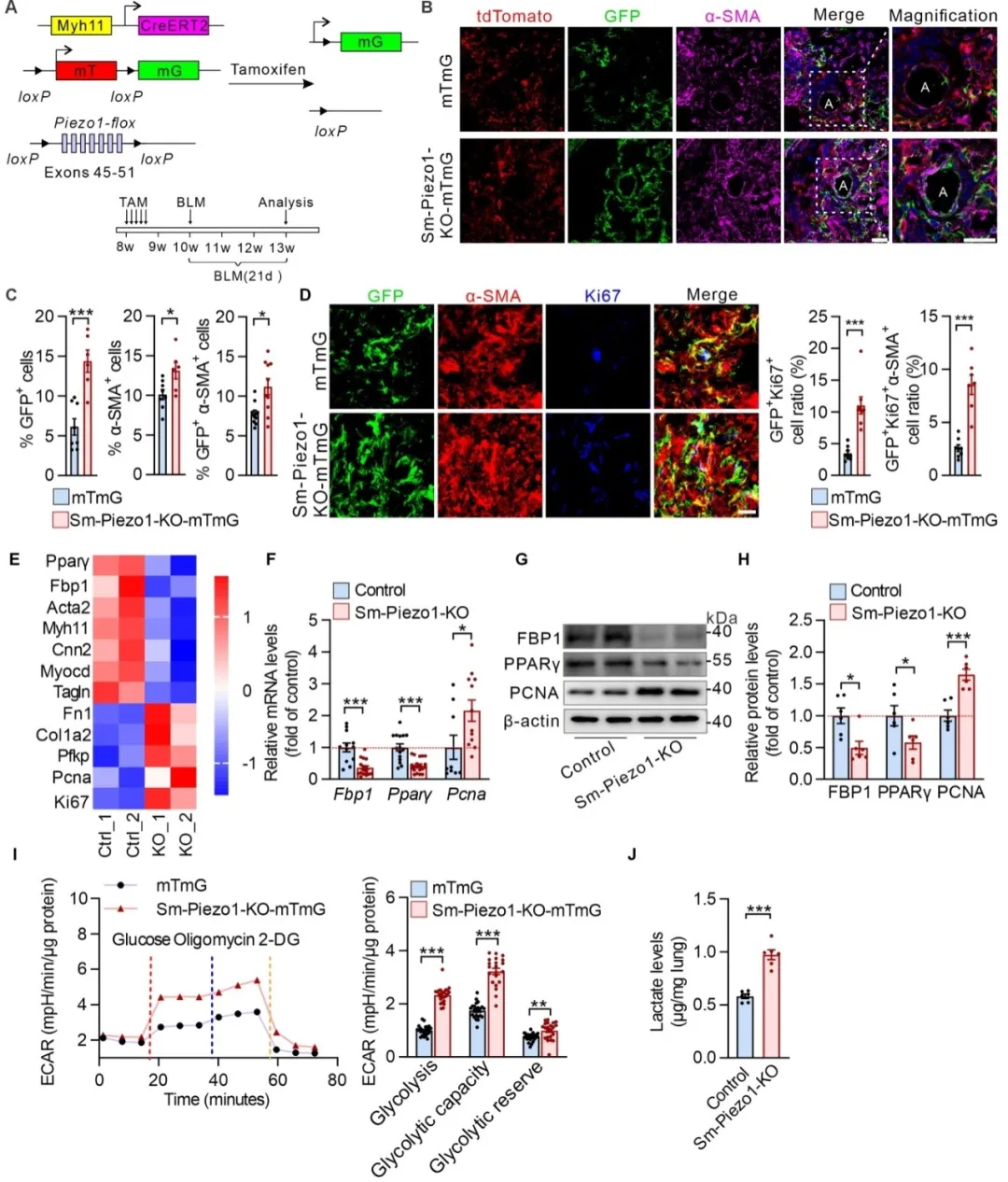
为了明确PIEZO1对肺动脉高压以及肺纤维化的影响,研究团队构建了平滑肌细胞特异性Piezo1敲除(Sm-Piezo1-KO)小鼠以及相应的mTmG示踪小鼠(Sm-Piezo1-KO-mTmG),发现PIEZO1介导的机械激活对于低氧诱导的PASMCs生长至关重要,平滑肌细胞中Piezo1的缺失会显著减轻慢性缺氧诱导的小鼠肺动脉高压进展,然而却加重博来霉素诱导的小鼠肺纤维化程度。
进一步机制探索的结果显示,在缺氧与肺损伤环境下,PIEZO1的下游通路存在显著差异。缺氧时,中等膜张力激活PIEZO1,通过Ca²⁺-NFAT2/HIF1α-PFKFB3通路增强糖酵解、促进乳酸生成,最终诱导PASMC增殖。博来霉素所致肺损伤时,TGFβ介导更高膜张力与更强机械电流,过度激活的PIEZO1经Ca²⁺-SMAD1/5-PPARγ-FBP1通路抑制糖酵解,限制PASMC增殖。两种情境下PASMC膜张力不同,叠加各自特异信号背景,决定了PIEZO1对糖酵解的双向调控效应。
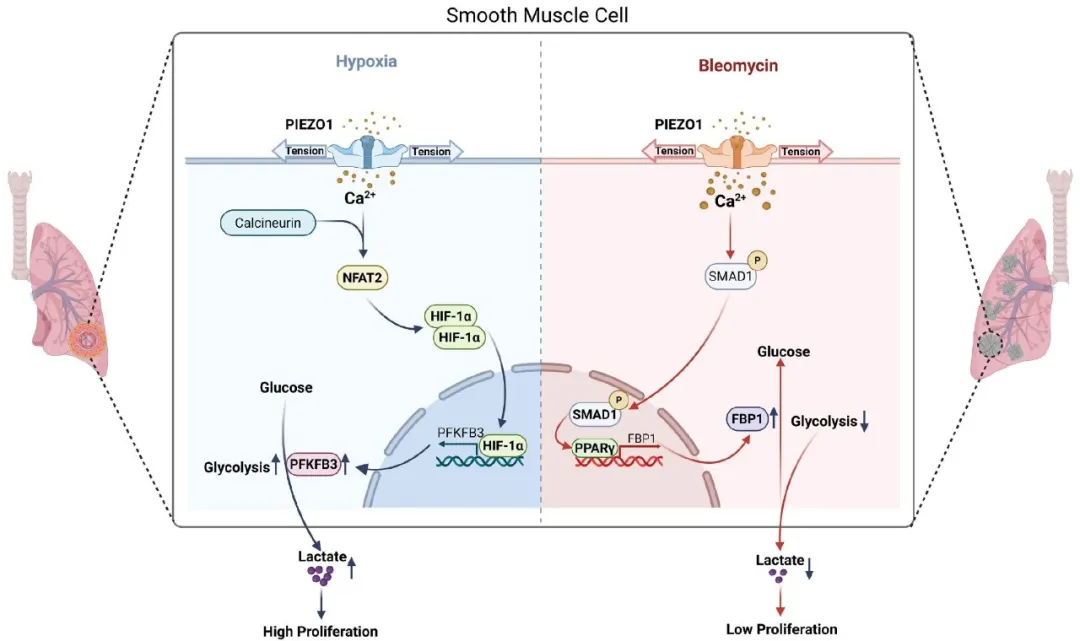
Cardiovascular Research同期发表德国法兰克福大学Ingrid Fleming教授的专题述评。Fleming教授认为该研究揭示了PIEZO1介导的力学-代谢耦合机制:在肺血管重构过程中,PIEZO1不仅是力学感受器,更是“场景感知”的代谢开关: 在缺氧背景下驱动增殖性糖酵解,在纤维化背景下则抑制代谢。靶向PIEZO1-糖酵解耦合轴,为慢性肺疾病的治疗开辟了新方向。

该研究由西安交通大学第一附属医院王胜鹏教授、袁祖贻教授、闫炀教授担任共同通讯作者,曹亚朋博士和徐丽然博士为共同第一作者,本研究受到国家自然科学基金、国家科技重大专项、陕西省自然科学基金及中国博士后科学基金等项目的资助。
原文链接:
https://doi.org/10.1093/cvr/cvag058
https://doi.org/10.1093/cvr/cvag060


