J Hepatol 浙大一院张鸿坤/凌琪/徐清波团队揭示CD34+细胞来源血管内皮参与肝移植血管免疫重塑的机制
时间:2026-05-05 12:24:38 热度:37.1℃ 作者:网络
内皮细胞损伤是肝移植后急性排斥发生的“导火索”。移植后新生内皮细胞究竟从何而来,至今仍有争议;内皮细胞与免疫细胞之间的相互作用机制,也尚未完全阐明。
2026年5月2日,浙江大学医学院附属第一医院张鸿坤/凌琪/徐清波团队在Journal of Hepatology杂志上在线发表题为“CD34+ cell-Derived Endothelial Cells Orchestrate Vascular and Immune Remodeling in the Transplanted Liver”的研究论文,该研究利用人和小鼠的移植肝单细胞转录组数据,结合遗传谱系示踪技术,首次揭示了肝移植后受体CD34⁺细胞来源内皮,通过CXCL12-CXCR4轴招募并激活T细胞,活化的CD8⁺ T细胞则通过CD40L-CD40轴诱导CD34⁺内皮细胞发生焦亡,形成内皮-免疫互作的恶性循环。进一步利用血小板靶向递送抗CXCL12抗体,可有效阻断这一互作、减轻急性排斥反应。这一发现为移植后早期干预提供了全新的细胞与分子靶点。
首先,研究团队通过对比人和小鼠供肝和移植肝的血管内皮密度发现,肝移植后血管内皮发生了剧烈的损伤修复过程,这一结果在小鼠移植肝单细胞转录组数据中也得到了验证(图1)。
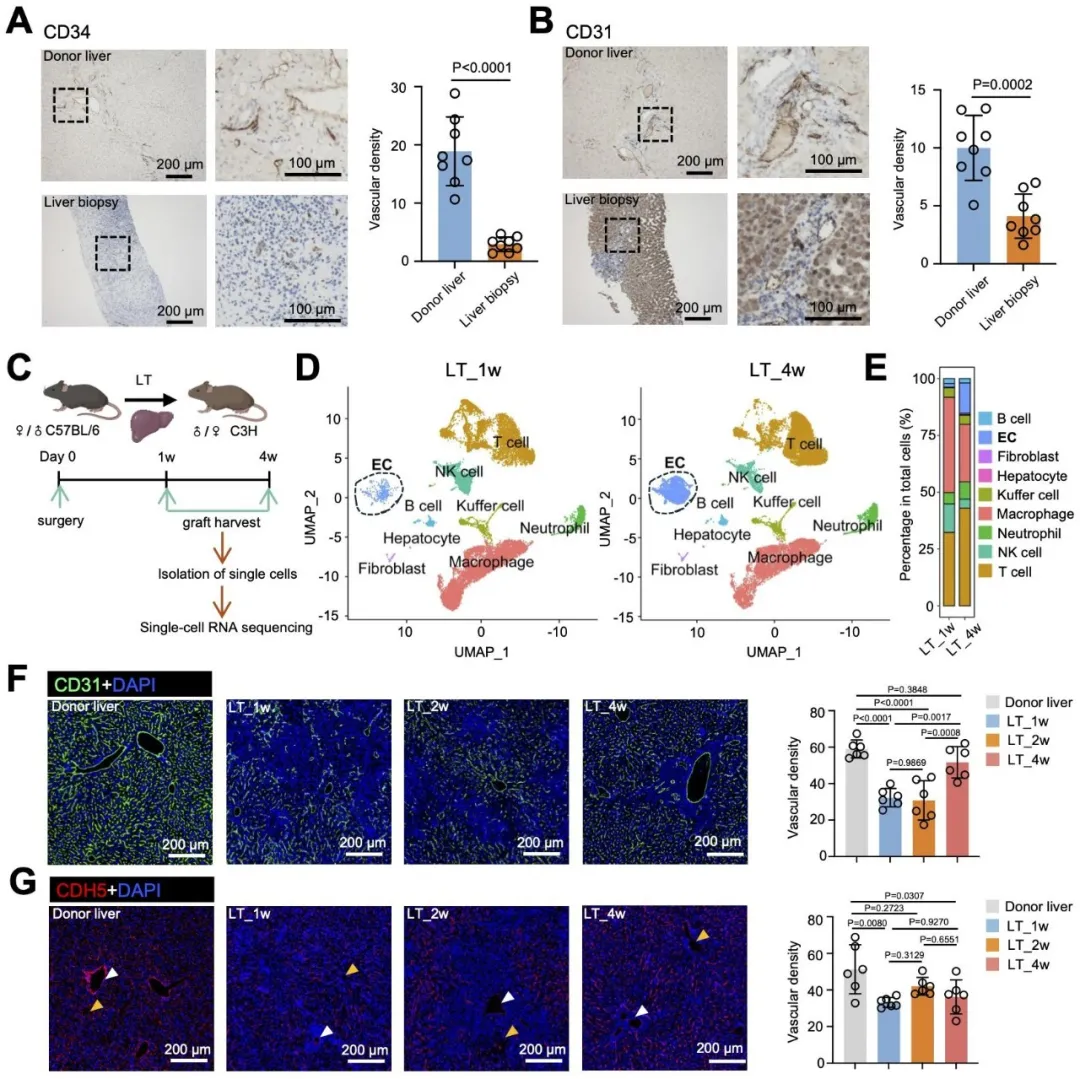
图1. 肝移植后内皮细胞发生显著重塑
接下来该研究分析了公共数据库中人移植肝的单细胞转录组数据,将移植肝内皮细胞分成了8个亚群,其中CD34+内皮细胞亚群在转录水平高表达CD34、CXCL12、ITGA6,在损伤修复和细胞粘附等通路上显著富集,同时具有较低的分化水平。在小鼠移植肝的单细胞转录组数据中同样也发现了这样的一群具有特殊功能的Cd34+内皮细胞亚群(图2)。
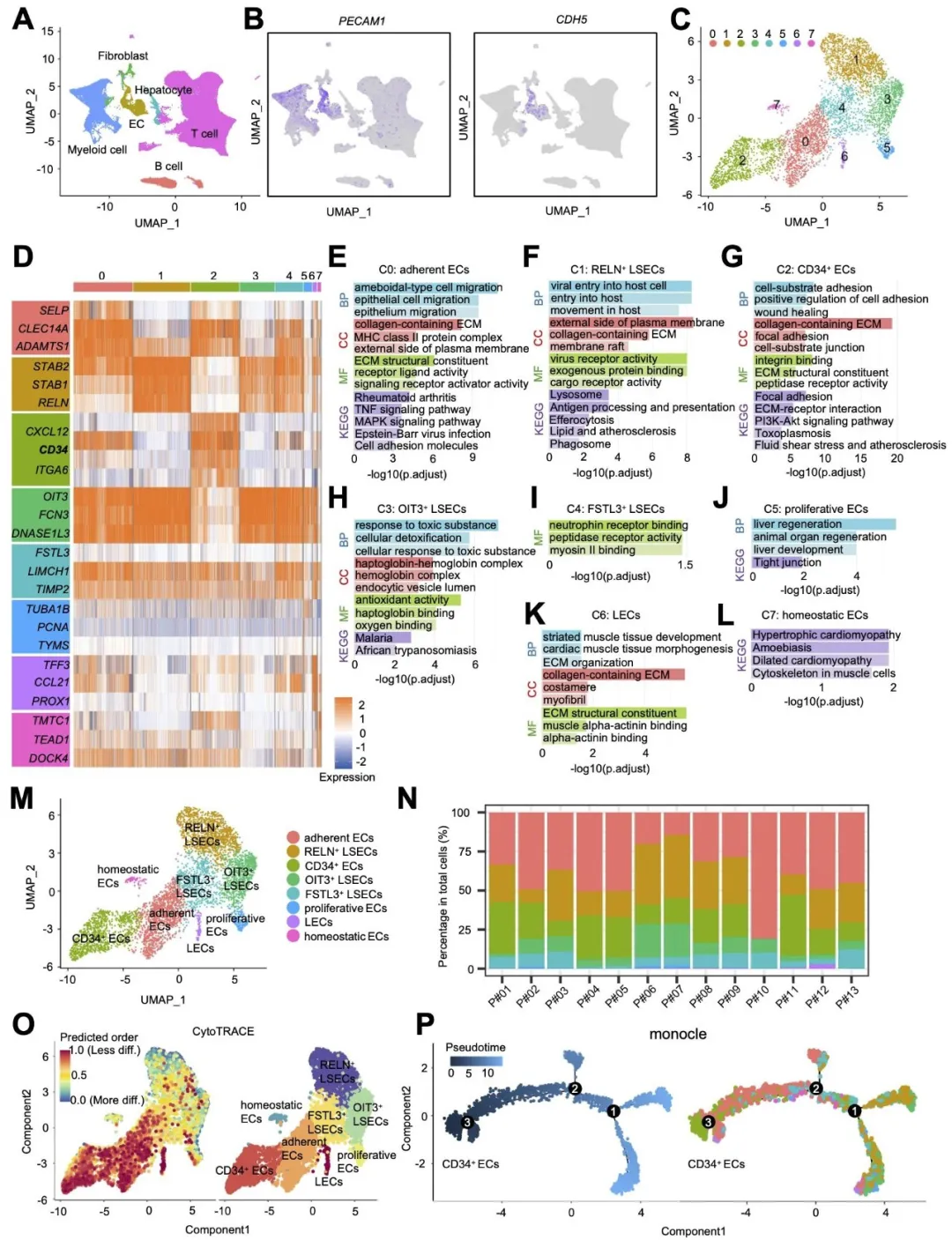
图2. 肝脏移植物内皮细胞的单细胞转录组图谱
传统观点认为肝移植后新生内皮细胞主要源于供者血管内皮的原位增殖。本研究利用性别错配的人移植肝样本(女供男受)的单细胞转录组数据,发现27.7%的移植物内皮细胞为受者来源,其中CD34⁺内皮细胞亚群的嵌合率最高(42.1%)。通过构建CAG;R26-tdTomato小鼠及Cd34-CreERT2;R26-tdTomato小鼠,结合同种异基因小鼠原位肝移植模型,直接证明受者CD34⁺细胞可在移植肝中分化为内皮细胞,其比例在术后2周达峰,随后下降;这些受者CD34+细胞来源的内皮细胞紧密连接蛋白(ZO-1、Claudin5)表达降低,而粘附分子ICAM-1上调。综上,多组学与遗传示踪证据确证了肝移植后受者CD34⁺细胞是移植物新生内皮的重要来源,为靶向内皮-免疫互作提供了新的细胞学基础(图3)。
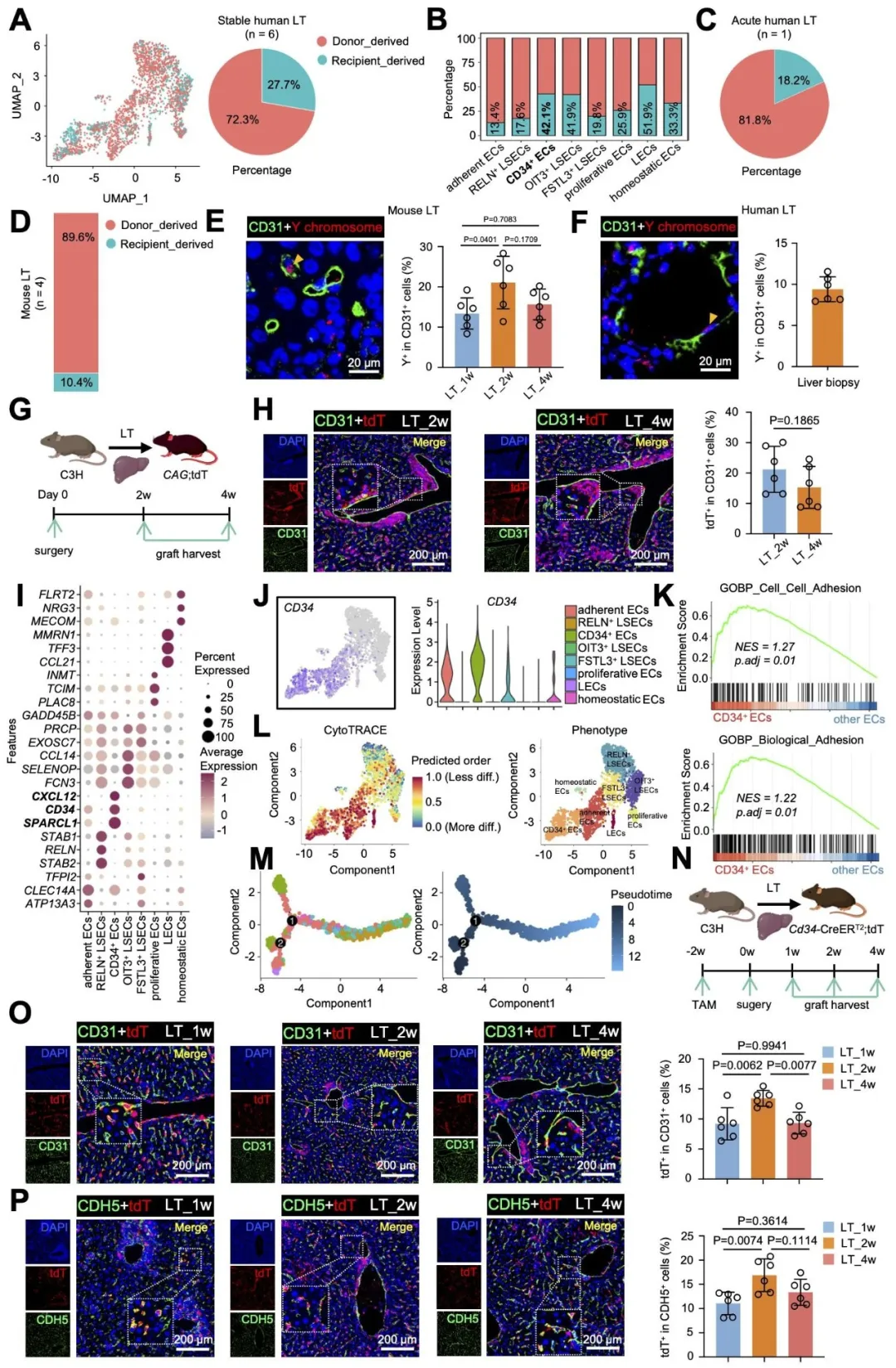
图3. 受者CD34⁺细胞来源的内皮细胞重建肝移植物血管内皮
该研究进一步探索了内皮细胞和免疫细胞的互作机制,CellChat分析表明,CD34⁺内皮细胞是所有内皮亚群中与T细胞交互作用最强的群体,且CXCL信号通路为其特征性通路。进一步的配体-受体网络分析确认,CXCL12-CXCR4轴是CD34⁺内皮细胞亚群与CD4⁺及CD8⁺ T细胞亚群之间最重要的配受体对。成像流式及多重免疫组化在人和小鼠移植物中共同验证了CD34⁺内皮细胞与T细胞的空间直接接触。体外共培养实验显示,CD34⁺人脐静脉内皮细胞通过CXCL12-CXCR4轴显著增强T细胞趋化、增殖及IFN-γ分泌;同时,CD34⁺内皮细胞高表达共刺激分子CD80/CD86,为T细胞活化提供第二信号。阻断CXCL12-CXCR4轴可有效抑制T细胞的招募与活化,并减弱T细胞诱导的CD34⁺内皮细胞CD80/CD86上调。综上,CD34⁺内皮细胞通过CXCL12-CXCR4轴招募并激活CD4⁺/CD8⁺T细胞,从而加剧移植排斥反应(图4、5)。
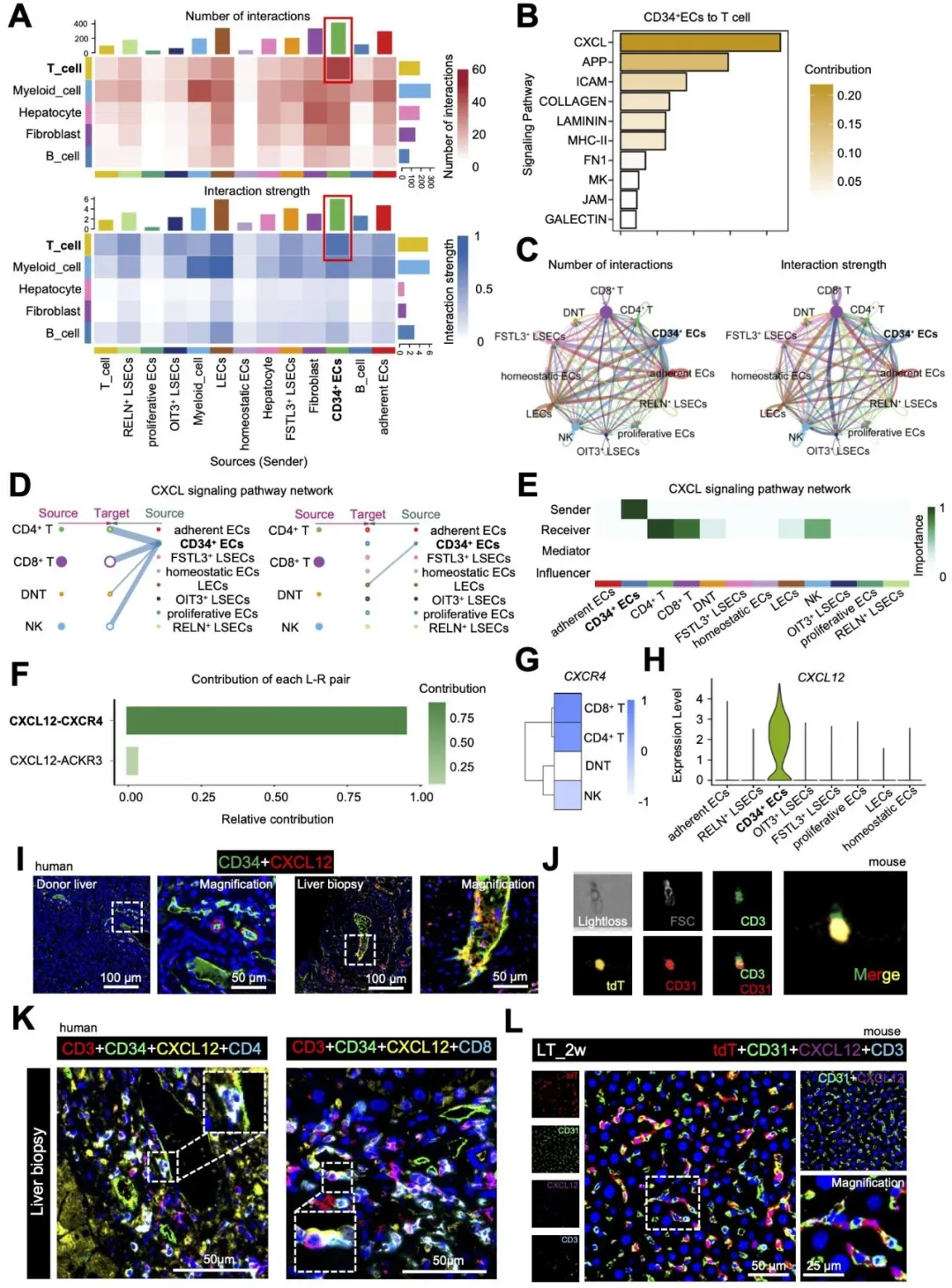
图4. CD34⁺内皮细胞通过CXCL12-CXCR4轴招募T细胞并加剧排斥反应
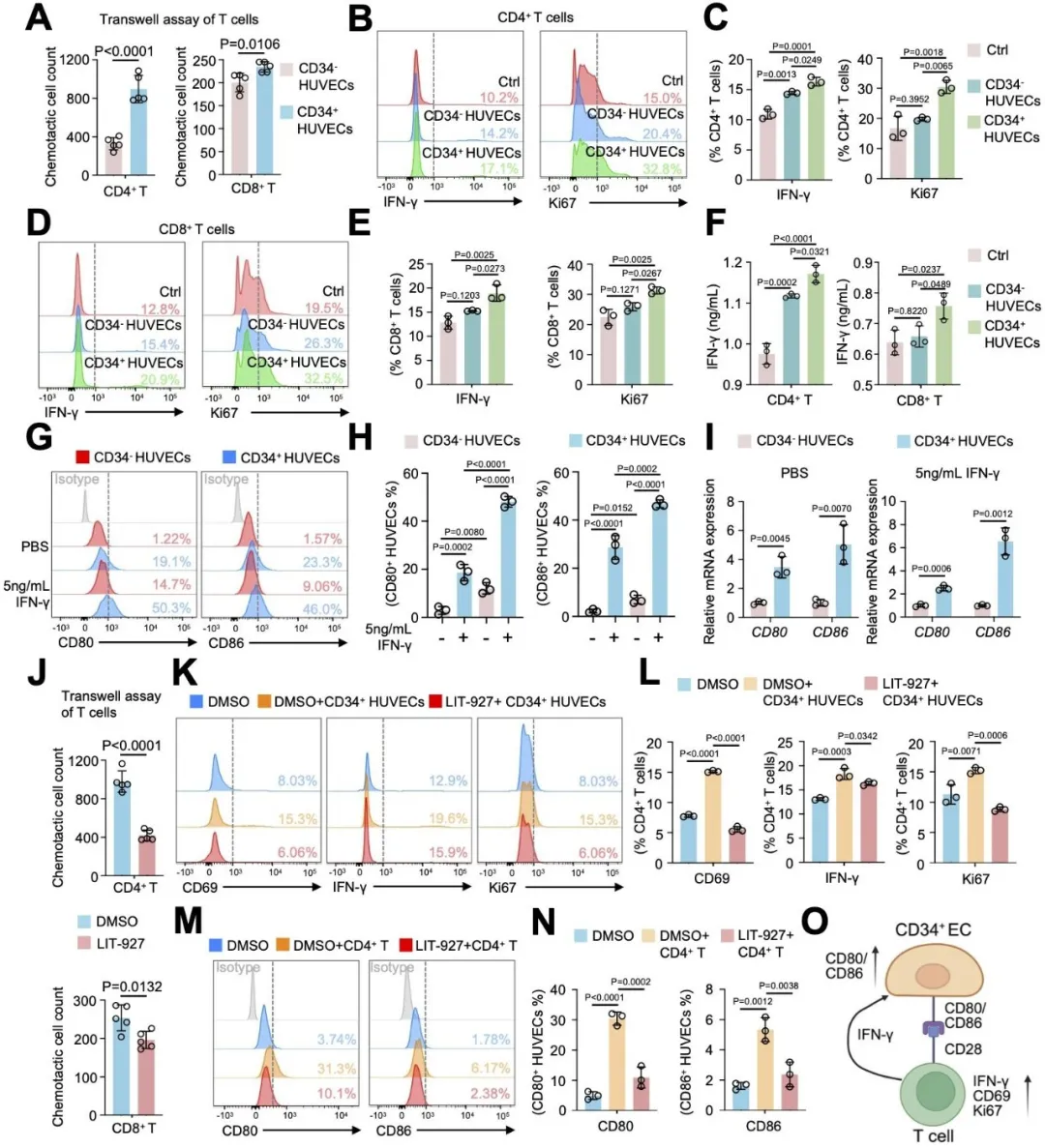
图5. CD34⁺内皮细胞通过CXCL12-CXCR4轴及共刺激分子招募并激活T细胞
研究发现在肝移植术后4周,CD34谱系内皮比例显著下降,单细胞转录组提示其在焦亡通路上富集最高。体外共培养证实,CD8⁺ T细胞通过Caspase-1/GSDMD通路诱导CD34⁺内皮细胞焦亡,并导致CD34⁺内皮的VE-cadherin下调。机制上,CD40L-CD40轴为焦亡过程的核心配受体对,阻断该轴或抑制CXCL12-CXCR4信号均可减轻焦亡。移植物免疫荧光染色进一步验证了CD34谱系内皮焦亡的发生(图6)。
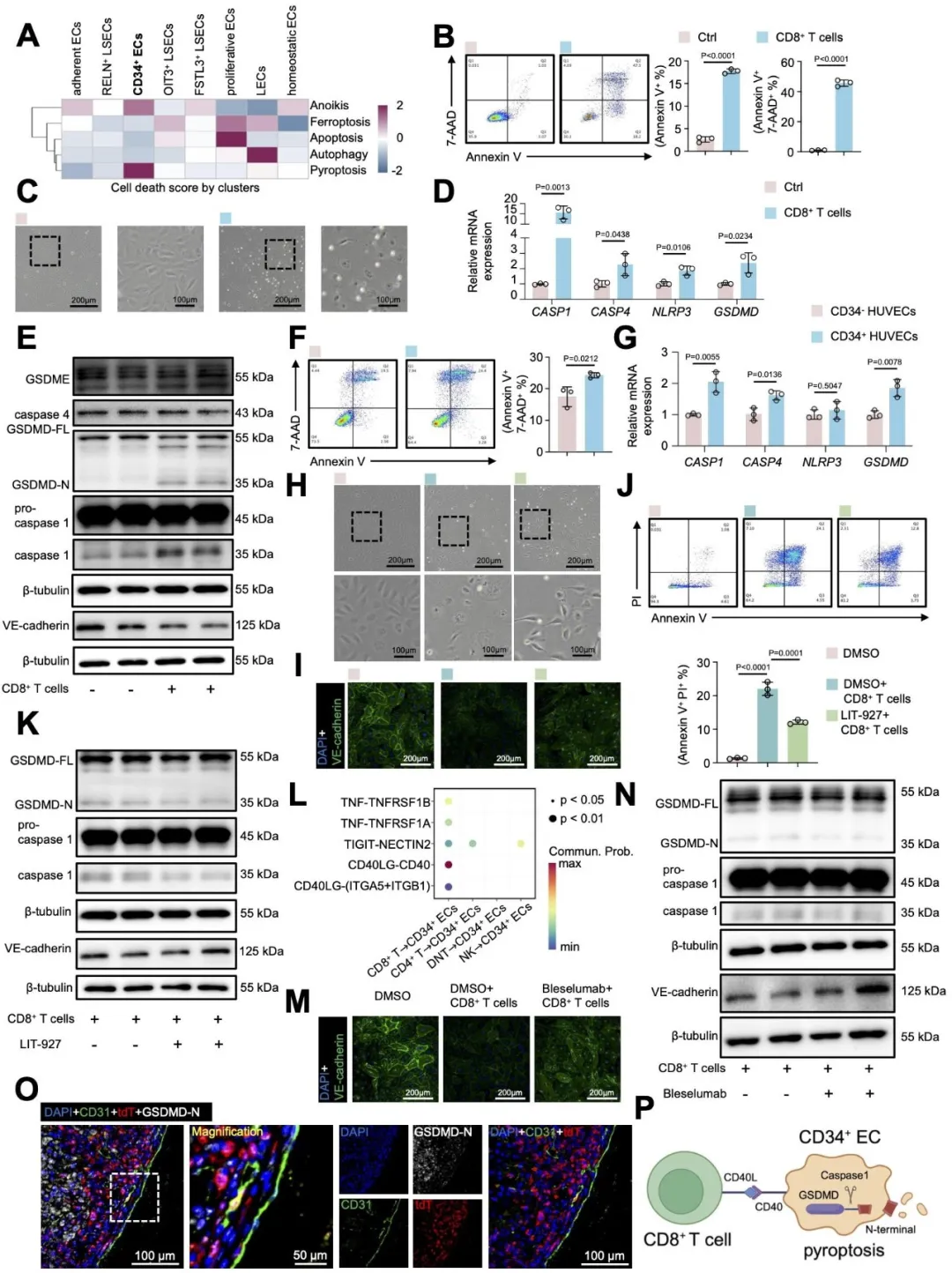
图6. 细胞毒性T细胞通过Caspase-1/GSDMD通路介导CD34⁺内皮细胞焦亡
基于活化血小板的囊泡释放能力,该研究将工程化血小板作为靶向递送抗CXCL12抗体(PLT-αCXCL12)的载体。在肝移植小鼠模型中,血小板可特异性聚集于移植物中CD34谱系内皮细胞周围。与对照组相比,PLT-αCXCL12治疗显著降低了受体小鼠的血清转氨酶及炎症因子(IL-6、TNF-α、IFN-γ)水平,并减少移植物内Th1 (CD4⁺IFN-γ⁺)及细胞毒性T细胞(CD8⁺GZMB⁺)浸润,同时改善了血管密度。此外,采用AAV9-CDH5-shCxcl12特异性敲低肝脏内皮细胞中Cxcl12表达,同样可减轻排斥反应并改善移植物血管密度。上述结果表明,靶向CD34⁺内皮细胞中的CXCL12可有效抑制T细胞的浸润,从而缓解肝脏移植物的排斥反应(图7)。
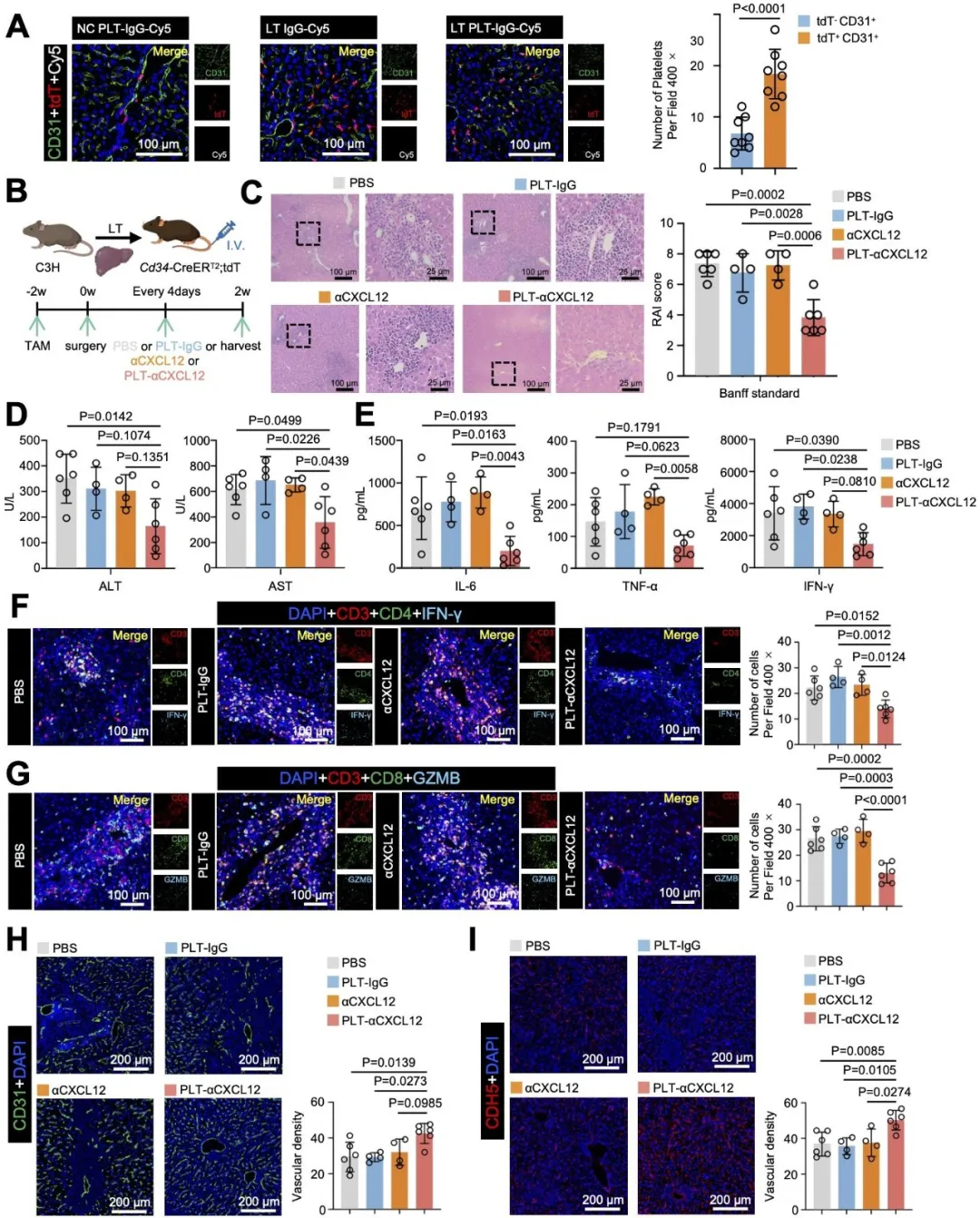
图7. 靶向CD34⁺细胞来源内皮CXCL12可减轻急性T细胞介导的排斥反应
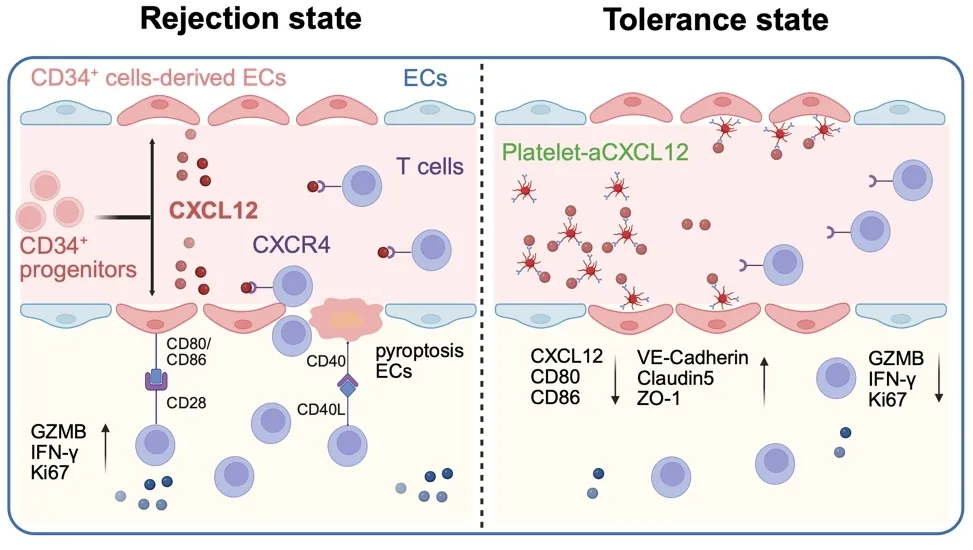
本研究综合利用性别错配的人和小鼠肝移植样本的单细胞转录组数据及遗传谱系示踪小鼠模型,系统揭示了肝移植后CD34⁺内皮细胞的起源、免疫调控功能及其促排斥机制。首先,受者来源的CD34⁺细胞可分化成为肝脏移植物中的新生内皮细胞,且这群细胞的屏障功能受损、粘附分子高表达。其次,单细胞互作分析与体外共培养实验表明,CD34⁺内皮细胞通过CXCL12-CXCR4轴招募CD4⁺/CD8⁺ T细胞,并通过高表达CD80/CD86提供共刺激信号,从而活化T细胞、加剧排斥。进一步研究发现,活化的CD8⁺ T细胞通过CD40L-CD40轴诱导CD34⁺内皮细胞发生Caspase-1/GSDMD依赖的细胞焦亡,导致内皮屏障破坏。最后,靶向CXCL12信号通路—无论是采用血小板工程化递送抗CXCL12抗体,还是利用AAV9介导内皮特异性Cxcl12敲低,均可显著减轻T细胞介导的急性排斥反应。本研究从细胞起源到分子机制再到干预策略,为肝移植排斥防治提供了全新的理论框架与精准靶点。
浙江大学医学院附属第一医院博士研究生陈睿涵、青岛大学附属医院博士研究生李新强为该论文共同第一作者。浙江大学医学院附属第一医院张鸿坤主任医师、凌琪主任医师、徐清波教授为该论文通讯作者。该研究同时得到了浙江大学医学院附属第一医院郑树森院士、青岛大学附属医院蔡金贞主任医师、浙江大学药学院李洪军教授的大力支持。该工作得到了国自然合作创新团队项目(W2541023)、国自然面上项目(82572036, 82370496)、国自然重点项目(32330046)的资助。
原文链接:
https://doi.org/10.1016/j.jhep.2026.04.028


