73岁乙肝患者再发肝占位,看似普通肝癌,实则暗藏双向分化!这种罕见肝癌恶性度极高
时间:2026-05-05 17:37:41 热度:37.1℃ 作者:网络
一、临床资料
患者,女性,73岁。主诉:发现肝占位20余天。
现病史:患者入院前因右上腹部隐痛不适,就诊于外院,查腹部B超发现肝占位,无腰背部放射痛,无恶心呕吐等。患者为进一步治疗就诊于我院,门诊完善上腹部MRI检查提示肝脏右后叶肿物,肝癌可能性大;肝脏右叶被膜下结节,警惕为肝内子灶;心包横膈组、腹膜后多发淋巴结,警惕转移。
既往史:确诊乙肝50余年,口服拉米夫定11年。56年前行右耳后黑色素瘤切除术及右上腹皮瓣移植术。11年前行肝尾叶肿瘤切除及胆囊切除术,外院术后病理:透明型肝细胞癌。
查体:发育正常,神清语利;体温36℃,脉搏78次/分,呼吸18次/分,血压125/70mmHg;全身皮肤黏膜未见黄染,浅表淋巴结未触及明显肿大,右侧肋缘可见5cm×8cm瘢痕皮肤,上腹部反L形切口长约25cm。双侧瞳孔等大等圆,对光反射灵敏。双肺未闻及干湿啰音及胸膜摩擦音,心律齐,各瓣膜听诊区未闻及病理性杂音;腹软,全腹无压痛、反跳痛,肝脾肋下、剑突下未触及,Murphy征阴性;生理反射存在,病理反射未引出。
检查:实验室检查:凝血功能、血生化、肝脏肿瘤标志物均正常;HBsAg(+),HBeAb(+),HBcAb(+)。腹部增强MRI:肝脏右后叶肿物,最大横截面约5.7cm×4.7cm,T₁WI/DUAL低信号,T₂WI/FS高信号,DWI高信号,多期增强早期明显强化,晚期强化减低。肝脏右叶被膜下另见一结节,约1.3cm × 0.8cm,T₁WI/DUAL低信号,T₂WI/FS高信号,DWI稍高信号,多期增强示早期明显强化,晚期持续性环形强化,警惕肝内子灶(图1)。肝脏其余部位散在T₂WI/FS高亮信号,无强化灶。扫描范围内脾、胆囊、胰腺、肾上腺、双肾未见明显异常。心包横膈组、腹膜后多发淋巴结,大者短径约0.6cm。腹腔未见积液。
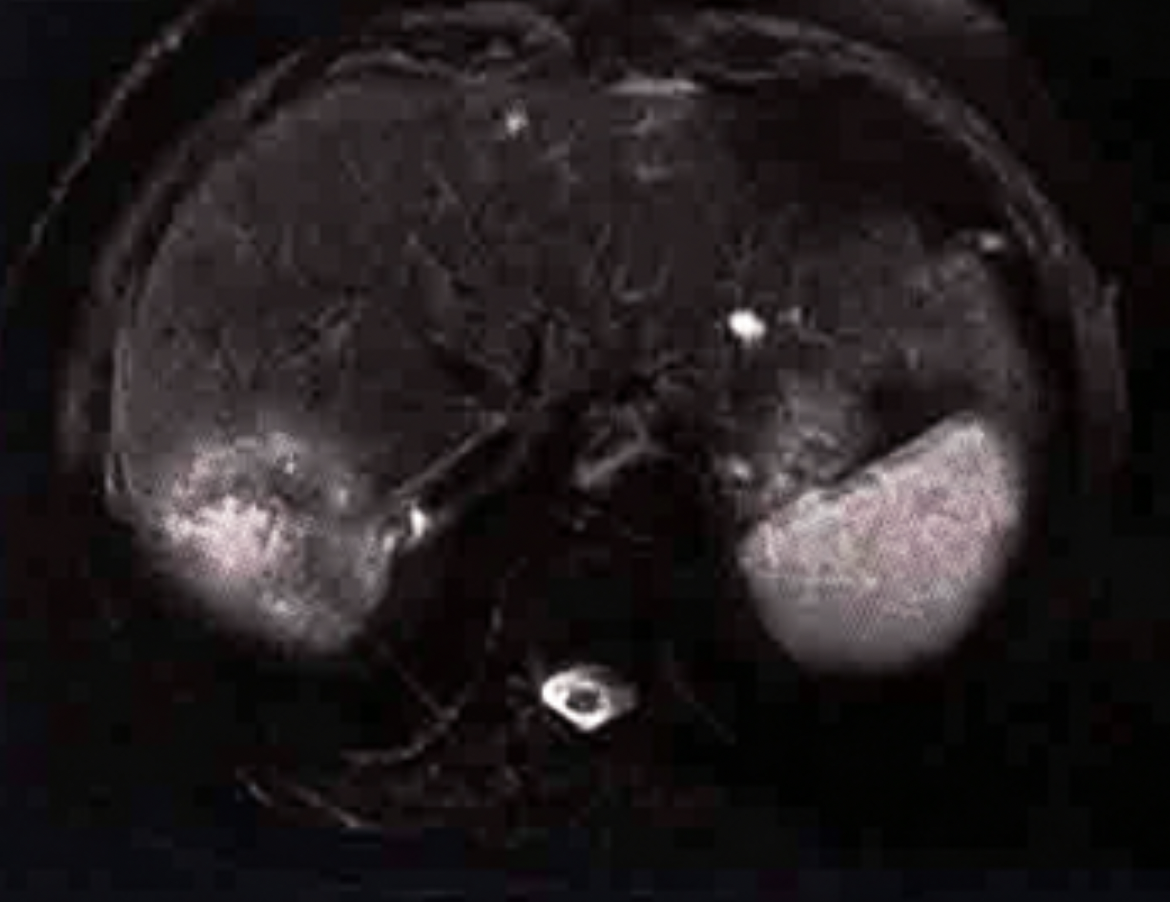
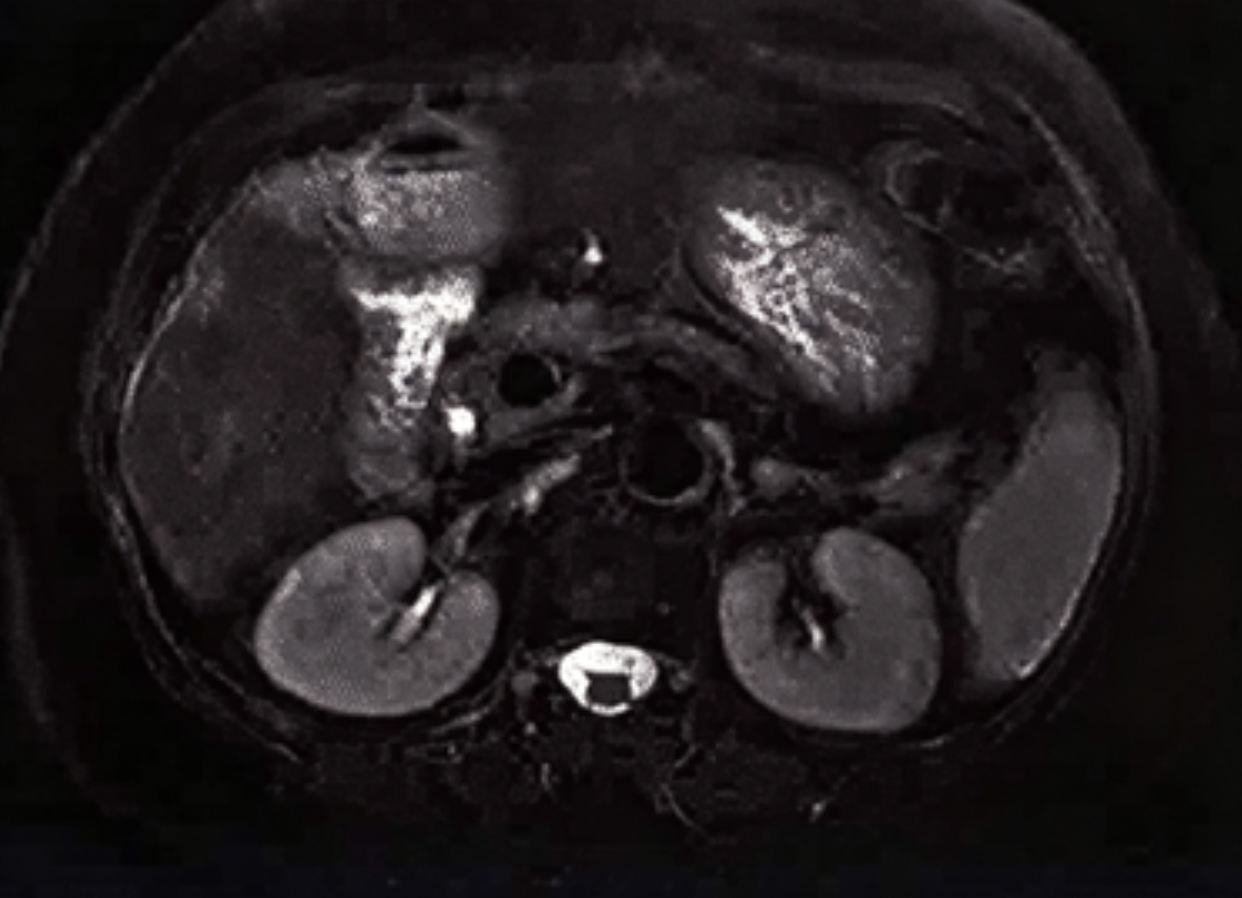
图1腹部增强MRI
二、治疗
入院后积极完善相关检查,凝血功能、血生化、肝脏肿瘤标志物正常,完善手术规划,行全麻下腹腔粘连松解+扩大肝脏右后叶切除+膈肌修补术。
术后病理(图2):肝组织中见癌浸润,结合免疫组化结果,符合混合型肝细胞癌-胆管癌。肿瘤呈两灶,大者大小为7cm×6.1cm×3.7cm,伴多灶间质硬化,累及肝被膜;小者直径为1.3cm,主要呈胆管细胞分化和干细胞形态。肿瘤纤维性粘连少许膈肌组织。(肝切缘)未见癌累及。周围肝Scheuer评分:肝炎分级G2,肝纤维化S4。pTNM分期:pT2(请结合临床)。
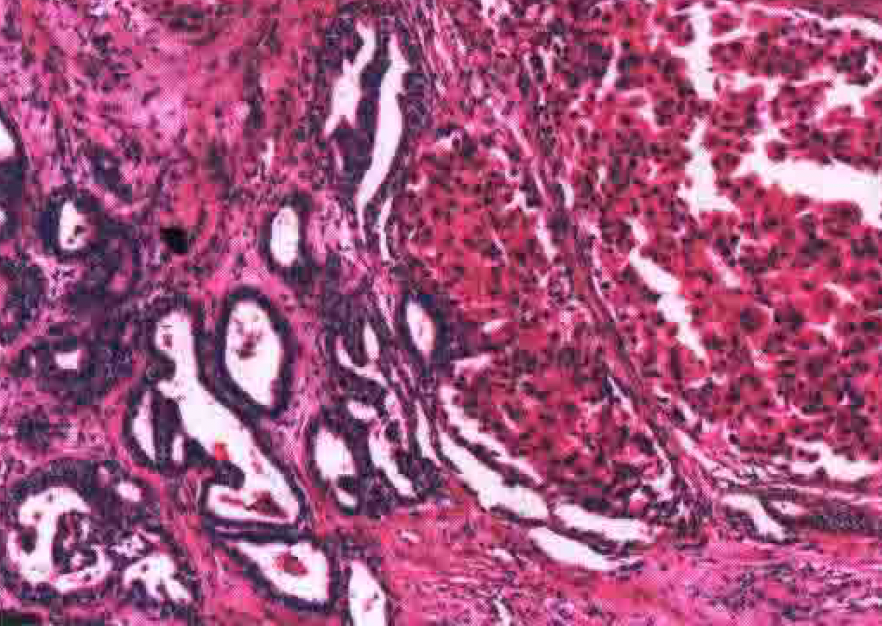
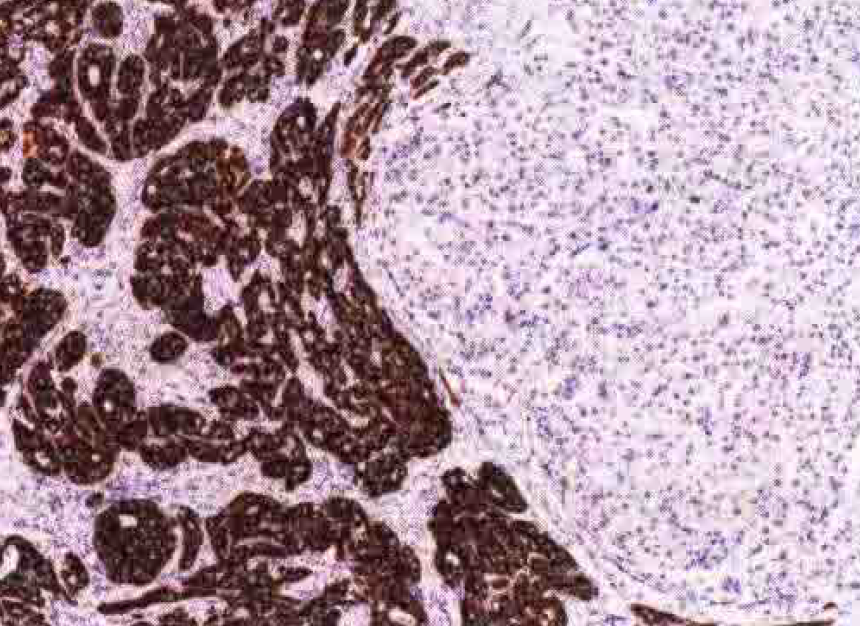
图2术后病理
大肿瘤免疫组化结果:Hepatocyte(肝细胞分化区域+),AFP(肝细胞分化区域+),GPC-3(肝细胞分化区域+),CA19-9(胆管细胞分化区域+),CK7(胆管细胞分化区域+),CK19(胆管细胞分化区域+),Ki-67(25%)。小肿瘤免疫组化结果:Hepatocyte(个别+),AFP(-),GPC-3(-),CA19-9(部分2+),CK7(3+),CK19(2+),CD56(3+),CD117(-),p53(70%),Ki-67(30%)。
治疗结果、随访及转归:术后1个月复查,凝血功能、血生化、肝脏肿瘤标志物均正常,MRI检查未见明显转移复发迹象,PET-CT检查示右侧心包横膈组大淋巴结,较前增大,伴代谢增高,警惕转移;右侧锁骨上区淋巴结较前明显增大,伴代谢增高,警惕转移。患者随访观察,未行治疗。术后2年电话随访患者,身体状况良好。
三、讨论
该患者为老年女性,有乙肝及肝脏恶性肿瘤病史,本次检查发现肝脏结节为恶性肿瘤,增强扫描兼有早期明显强化和多发淋巴结转移的特点,而术前的AFP、CA19-9均正常,不是典型的肝细胞癌或者胆管癌。患者术前未取得病理证据,术后病理证实为cHCC-CCA。治疗的主要方式仍然是手术。但非常遗憾,患者术后1个月PET-CT就发现心包淋巴结及锁骨上淋巴结转移,提示cHCC-CCA为恶性程度很高的恶性肿瘤。
cHCC-CCA占肝脏恶性肿瘤的2%~5%,同时存在肝细胞和胆管上皮分化,从大体和镜下形态观察,可以分成分离型(肝细胞癌和胆管癌形成独立病灶)、碰撞型(同一病灶中肝细胞癌和胆管癌有清晰分界)和混合型(同一病灶中肝细胞癌和胆管癌没有明确分界)三种类型,我们介绍的病例是第三种情况。
对于不同类型肝脏恶性肿瘤的中国患者,马兜铃酸、黄曲霉素、病毒感染都是发病的高危因素。基因分析表明,cHCC-CCA中CTNNB1突变频率显著低于肝细胞癌,而KRAS突变频率显著低于胆管癌。缺乏CTNNB1和KRAS突变是cHCC-CCA的特征之一。表观遗传分析也表明,碰撞型和混合型具有不同的分子亚型:碰撞型更接近肝内胆管细胞,而混合型更接近肝细胞癌。单细胞测序分析表明,分离型cHCC-CCA可以是单克隆起源,也可以是多克隆起源;而碰撞型及混合型cHCC-CCA都是单克隆起源。Nestin蛋白在cHCC-CCA中的表达显著高于肝细胞癌,同时Nestin蛋白高表达的患者预后更差。
cHCC-CCA的临床特点可能与瘤体中的优势成分有关。cHCC-CCA具有类似于肝细胞癌的肝炎病毒背景、门静脉癌栓合并率高等特点,也具有瘤体血供差、较早出现肝门部及腹膜后淋巴结转移等类似肝内胆管癌的特点,其临床特点介于肝细胞癌和肝内胆管癌两者之间。血清标志物甲胎蛋白(AFP)和糖类抗原19-9(CA19-9)已被证实分别是肝细胞癌和肝内胆管癌的潜在诊断标志物。当AFP和CA19-9同时升高或与影像学特征不一致时,应该怀疑cHCC-CCA。存在星状结节、T₂WI高信号、扩散受限、结节中无包膜外观,呈周围性、进行性增强,是cHCC-CCA的一些影像特征。
治疗策略上,手术切除仍然是治疗局限性cHCC-CCA的首要选择。手术目标是R0切除同时保证合适的残余肝功能。肝移植作为cHCC-CCA的治疗选择需要慎重考虑,包括存在终身应用免疫抑制剂的风险和缺乏供肝。对于不能手术或复发的cHCC-CCA患者,局部治疗方式包括TACE、放射栓塞术、肝动脉灌注化疗、消融治疗。对于晚期不能切除的cHCC-CCA的姑息性全身治疗,其标准治疗方案仍没有确定。由于该肿瘤罕见,目前的证据有限,只能依靠病例报告和小型的回顾性研究,参考肝细胞癌和肝内胆管癌来制定一些可能有效的治疗方案,主要为吉西他滨、顺铂、5-氟尿嘧啶及其衍生物。仑伐替尼等酪氨酸激酶抑制剂已经广泛用于肝细胞癌,也不断在胆管癌中进行探索性研究。近年来,免疫治疗(PD-1或PD-L1抗体)已推荐用于肝细胞癌,联合化疗也已经推荐用于胆管癌,可以尝试将免疫治疗应用于cHCC-CCA。
cHCC-CCA是一种罕见的原发性肝脏恶性肿瘤,具有侵袭性强和预后不良等特点。尽管其组织学和表型呈多样性,病理仍然是确立诊断的最终依据,结合形态学和免疫组化结果有助于鉴别诊断。由于其与肝细胞癌和胆管癌的临床表现相似及其模糊的影像学特征,术前确诊较为困难。当影像学结果和肿瘤标志物检查结果不一致时,应考虑诊断cHCC-CCA,必要时进行肿瘤多区域穿刺活检证实。
参考文献
[1] Ye L, Schneider JS, Ben Khaled N, et al. Combined Hepatocellular-Cholangiocarcinoma: Biology, Diagnosis, and Management. Liver Cancer. 2023;13(1):6-28.
[2] Beaufrère A, Calderaro J, Paradis V. Combined hepatocellular-cholangiocarcinoma: An update. J Hepatol. 2021;74(5):1212-1224.
[3] Vij M, Veerankutty FH, Rammohan A, Rela M. Combined hepatocellular cholangiocarcinoma: A clinicopathological update. World J Hepatol. 2024;16(5):766-775.


