【NEJM】CD19 CAR-T治疗B-ALL并发慢性GVHD的一例报道
时间:2026-05-05 17:06:26 热度:37.1℃ 作者:网络
慢性移植物抗宿主病(cGVHD)是异基因造血干细胞移植(allo-HCT)后主要的并发症和死亡原因之一,异常活化的B细胞在cGVHD发病中起重要作用,因此靶向B细胞可成为治疗策略。CD19 CAR-T细胞疗法已在B细胞肿瘤和部分自身免疫病中显示出良好疗效,但在同种免疫性疾病(如cGVHD)中的应用尚缺乏研究。
新英格兰医学杂志近日发表一例报道,作者使用自体CD19 CAR-T细胞治疗一例B-ALL患者及其慢性GVHD(前期异基因移植导致的慢性GVHD)。

患者基本情况
年龄/性别:32岁女性
原发病:复发难治性B细胞急性淋巴细胞白血病(B-ALL)
既往治疗:化疗 + 2次allo-HCT,均未获得持续缓解
cGVHD表现:严重硬化性cGVHD(皮肤硬皮病样病变)
cGVHD治疗:对西罗莫司、贝舒地尔、体外光化学疗法、芦可替尼均无效(所有cGVHD治疗在CAR-T细胞治疗前2个月停用)
CAR-T治疗过程
治疗方案:自体CD19 CAR-T细胞(obecabtagene autoleucel)分次输注
治疗目的:同时治疗B-ALL复发和活动性cGVHD
安全性:
-
无细胞因子释放综合征(CRS)
-
无神经毒性
-
无感染并发症或无热性病
-
仅需输注2个单位血小板,无其他血液制品输注
CAR-T细胞在外周血中可检测至输注后1年
疗效结果
1. 对cGVHD的疗效
显著且持续的临床缓解:
-
硬皮病样cGVHD逐渐缓解
-
无需继续使用免疫抑制剂
-
无新发病变部位出现
功能改善:
-
下肢力量显著改善
-
腕关节和踝关节活动度部分恢复(6个月时)
生活质量:PS评分和QoL持续改善
2. 对B-ALL的疗效
骨髓和中枢神经系统(CNS)白血病持续缓解1年
但在输注后14个月出现孤立性CNS复发(CD19+)
3. 免疫学与血液学变化
B细胞再生障碍持续存在
低丙种球蛋白血症(需定期补充IgG)
血小板水平正常化(6个月时)
持续性中性粒细胞减少
CAR-T细胞在血液中可检测长达1年
免疫学分析(单细胞RNA+TCR测序)
输注前:存在扩增的CD8+和CD4+效应记忆T细胞克隆
输注后6–10个月:这些克隆持续存在,但转录特征显著重塑:
-
上调:I型干扰素刺激基因、免疫调节程序
-
下调:早期T细胞活化、细胞增殖、细胞周期、IFN-γ介导效应
提示CAR-T细胞可能通过重塑T细胞功能而非清除B细胞来缓解cGVHD。
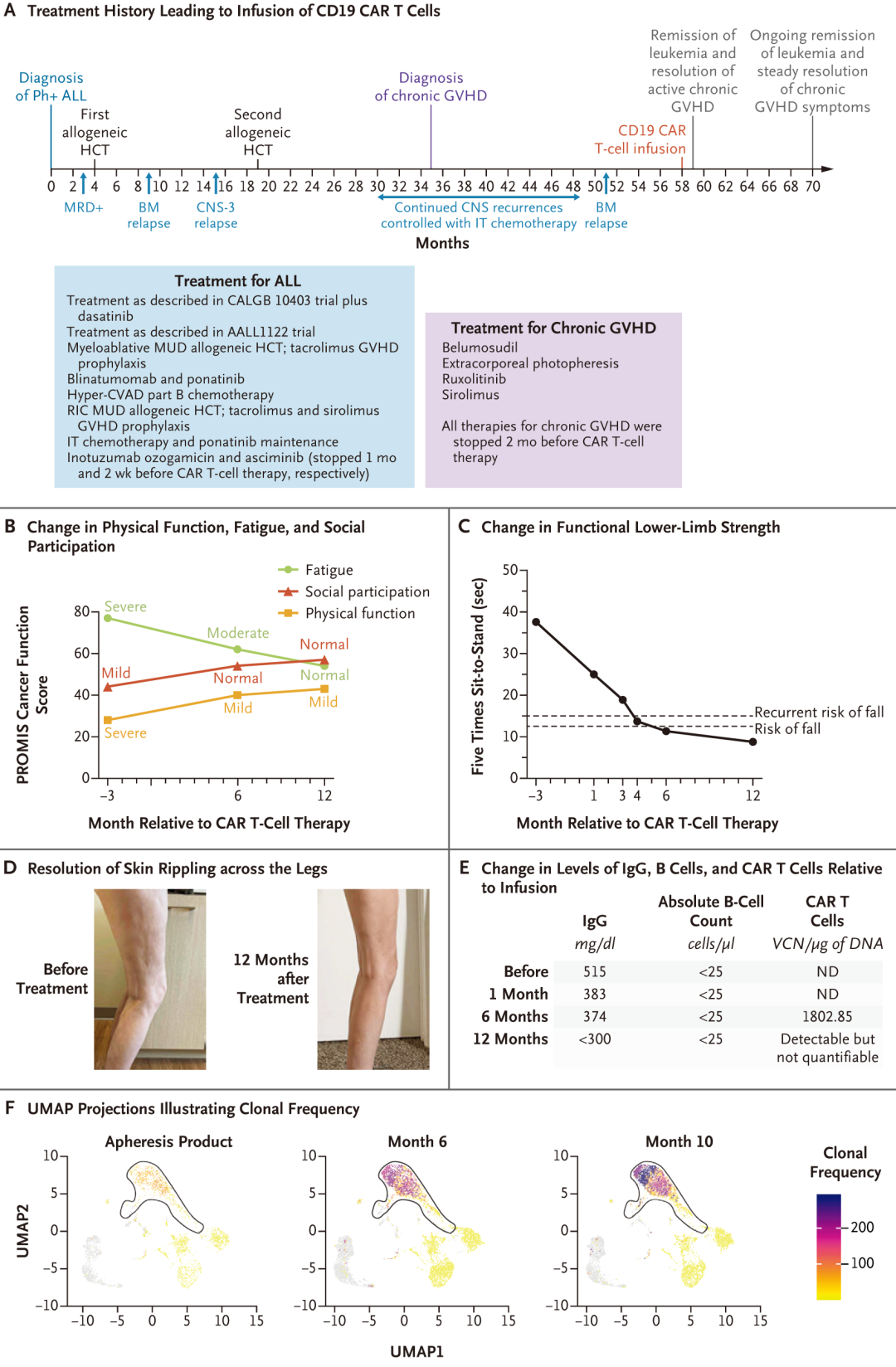
患者的治疗经过及慢性GVHD的缓解过程。
图A为患者接受CD19 CAR-T细胞输注前的治疗史,包括B-ALL多次复发的治疗经过以及慢性GVHD的治疗经过。Hyper-CVAD B方案化疗包含大剂量阿糖胞苷和甲氨蝶呤。图B为CD19 CAR-T细胞输注前后,采用患者报告结局测量信息系统(PROMIS)癌症功能简明三领域量表评估的身体功能、疲劳和社会参与结局。评分采用T分数,以一般人群均值为50分。身体功能评分范围为17.9–58.9分,疲劳为38.5–77.2分,社会参与为28.1–63.4分。身体功能和社会参与得分越高,表示功能越好、参与越多;而疲劳得分越高,表示严重程度越高(即症状负担越重)。图C为根据五次坐立试验(测量在不使用手臂的情况下站立和坐下五次所需时间)评估的CD19 CAR-T细胞输注前后功能性下肢力量的变化。图D为CD19 CAR-T细胞输注后腿部显著皮肤皱褶的消退情况。图E为输注前后IgG、B细胞和CAR-T细胞的水平。图F为采用统一流形逼近与投影(UMAP)绘制的患者单采时以及CAR-T细胞输注后6个月和10个月血液中T细胞和自然杀伤细胞亚群的克隆频率。CD8+和CD4+ T细胞效应记忆群落在图中以黑色轮廓标出。克隆定义为具有相同T细胞受体互补决定区3氨基酸序列的α和β可变链的细胞。CNS-3指脑脊液白细胞计数≥5个/μl且存在原始细胞,或具有中枢神经系统受累的临床体征。
总结
CD19 CAR-T细胞在活动性cGVHD患者中可安全使用(即使是异基因移植后)
可逆转难治性硬化性cGVHD,且无需联合免疫抑制治疗
为cGVHD的治疗提供了全新策略,尤其适合伴或不伴B细胞肿瘤的患者
需进一步研究验证其广泛适用性
参考文献
N Engl J Med . 2026 Apr 30;394(17):1759-1762. doi: 10.1056/NEJMc2517629.


