Hypertension 南京医科大学韩莹、褚嫒嫒/广州医科大学汤海洋团队发现血管活性肽Salusin-α在肺动脉高压中的新机制
时间:2026-05-05 17:02:18 热度:37.1℃ 作者:网络
肺动脉高压(PH)是一类以肺动脉压力升高和肺血管阻力增加为特征的疾病,其中动脉性肺动脉高压(PAH)为罕见且致死性疾病,最终可因右心衰竭导致死亡。其核心病理机制包括持续性血管收缩与肺血管重构,而内皮损伤被认为是起始关键事件。内皮功能受损导致肺动脉内皮细胞(PAECs)释放的舒张因子(如一氧化氮(NO))减少、收缩因子增加,其中eNOS功能下降是NO减少的重要原因,从而削弱血管内皮依赖性舒张功能。同时,肺动脉平滑肌细胞(PASMCs)对舒张刺激反应减弱,ROS过度生成进一步抑制sGC–cGMP–PKG信号通路,并促进细胞增殖与迁移,推动血管重构与管腔狭窄。然而,连接血管内皮、平滑肌损伤与重构的关键机制仍不清楚。
2026年4月10日,南京医科大学韩莹、褚嫒嫒和广州医科大学汤海洋团队在Hypertension上发表了题为“Salusin-α Restores Vascular Relaxation and Remodeling in Pulmonary Hypertension”的研究论文。该研究围绕salusin-α展开,提出其作为一种具有血管调控作用的内源性多肽,可能是肺血管保护及PH干预的新型潜在治疗靶点。研究采用外源性应用salusin-α及抗体中和策略抑制内源性salusin-α,在PH动物模型中发现,调控salusin-α可显著改善肺动脉舒张功能并抑制血管重构,其作用机制与增强内皮eNOS/NO信号及抑制平滑肌ROS相关通路密切相关。

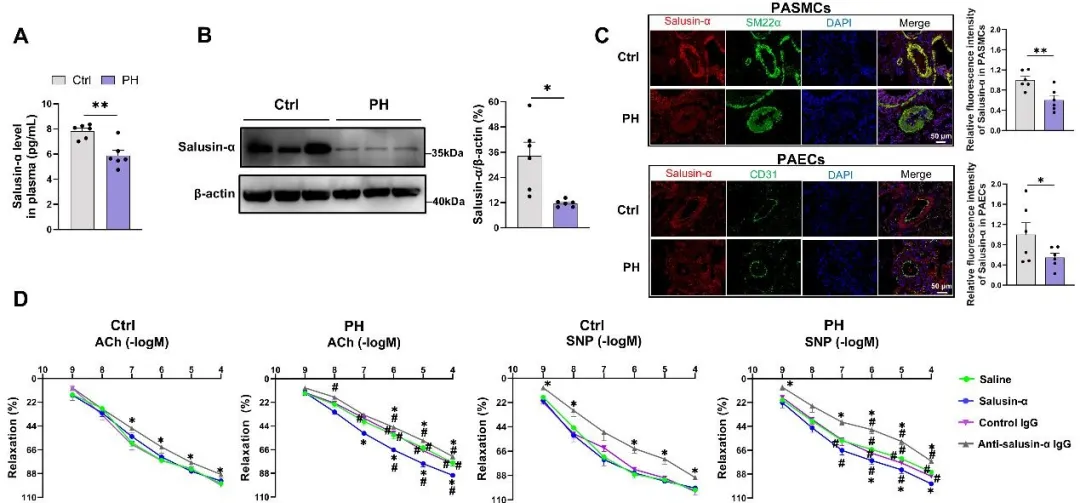
为了探究salusin-α在肺血管中的作用,研究团队首先在MCT诱导的PH大鼠模型中检测其表达水平。结果显示,无论在PH血浆还是肺动脉组织中,salusin-α均显著下降,且在内皮与平滑肌层均呈一致性减少;同时PH来源的肺动脉内皮细胞和平滑肌细胞分泌salusin-α能力亦明显降低,提示其生成与释放环节均受损。PH大鼠肺动脉表现出显著的内皮依赖性(Ach诱导)和非依赖性(SNP诱导)舒张功能障碍,外源性应用salusin-α改善,而抑制内源性salusin-α进一步损伤血管舒张功能。
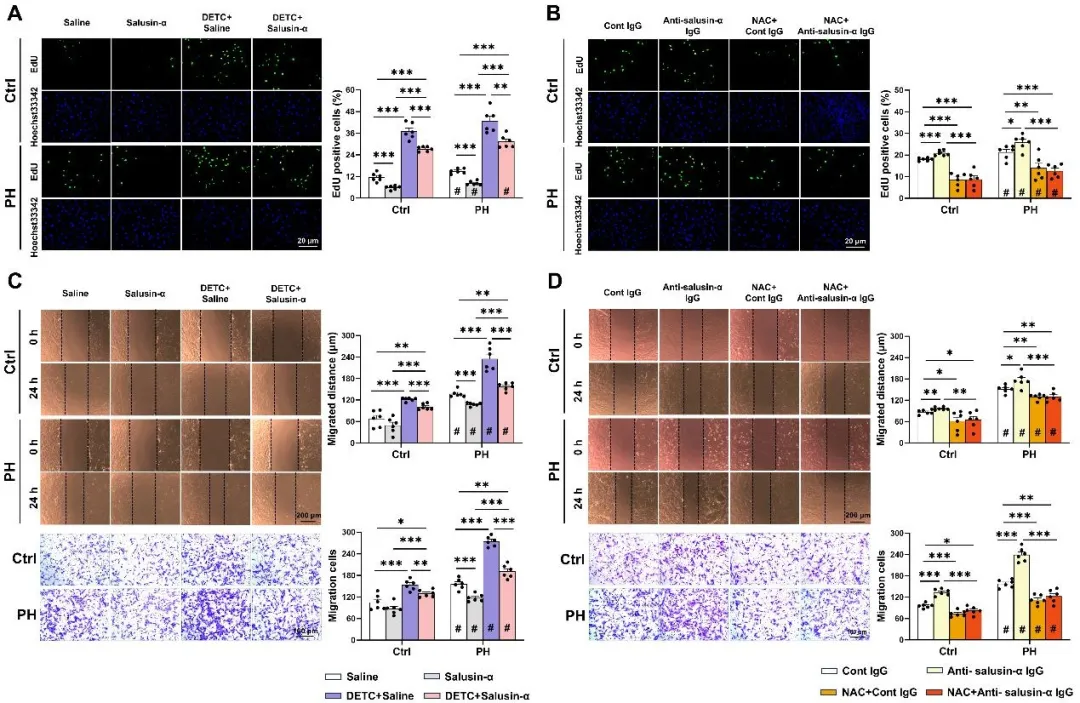
在进一步机制探索中,研究团队发现salusin-α对PH肺动脉内皮细胞(PAECs)中eNOS/NO信号通路有明显增强效应,而对平滑肌细胞(PASMCs)的氧化还原失衡具有显著纠正作用。Salusin-α孵育显著改善,而抑制内源性salusin-α进一步加重肺动脉高压大鼠PASMCs的增殖和迁移,此效应被ROS清除剂或SOD酶抑制剂所调控。
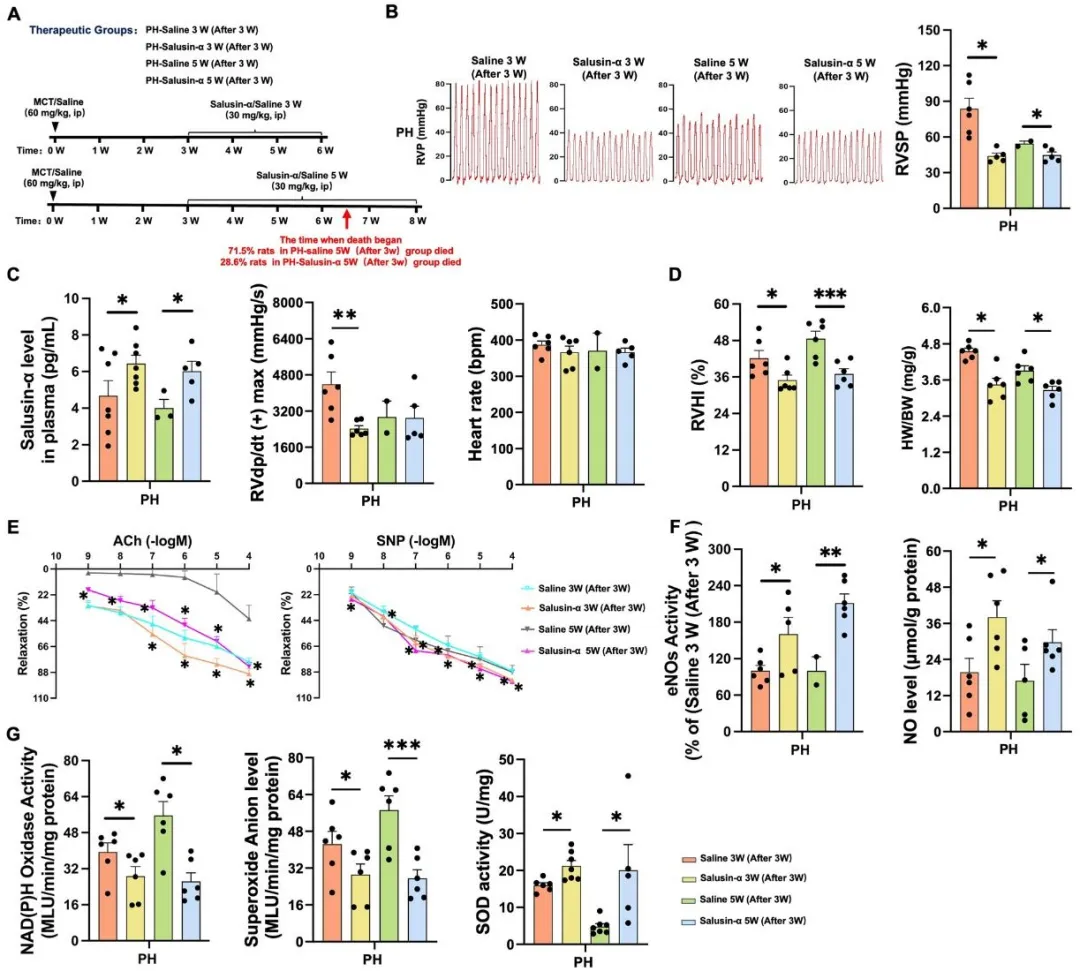
在慢性动物实验中,持续给予salusin-α显示出明确的保护与治疗效应。外源性补充salusin-α恢复eNOS/NO通路、增强SOD活性,同时抑制NAD(P)H氧化酶活性及ROS生成,纠正氧化应激失衡,改善肺动脉内皮依赖性及非依赖性舒张功能,降低肺血管阻力。同时salusin-α显著减轻肺动脉高压肺血管及右心室重构,且短期干预即已可见改善,降低右心室压和死亡率。
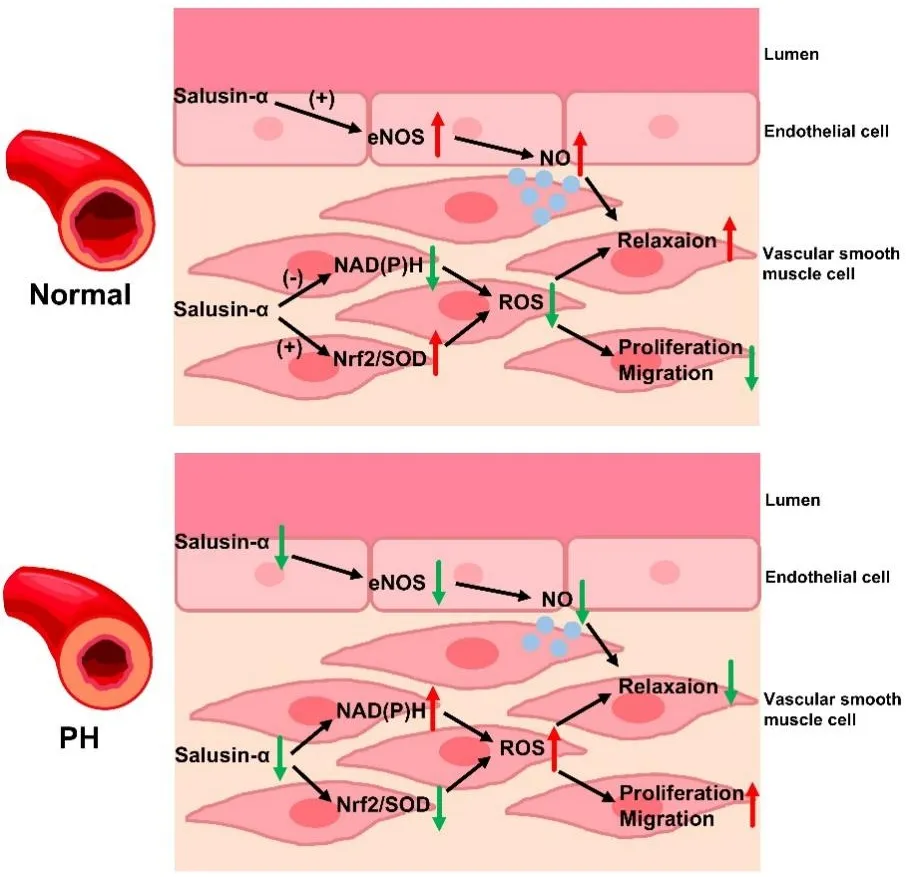
综上,salusin-α在PH肺动脉中呈明显缺失状态,其外源性补充可通过激活eNOS/NO通路、氧化应激调控、抑制血管重塑等恢复肺血管稳态,为肺动脉高压内皮和平滑肌靶向干预与治疗提供了新思路。
该研究由南京医科大学研究生胡瑞华、白洁和潘艳为本文的共同第一作者,南京医科大学基础医学院生理学系韩莹教授、南京医科大学第二附属医院褚嫒嫒主任和广州医科大学呼吸疾病全国重点实验室汤海洋教授为本文的共同通讯作者。
原文链接:
https://www.ahajournals.org/doi/10.1161/HYPERTENSIONAHA.125.25722


