苏州大学Biomaterials:开发静电共组装细胞外囊泡水凝胶,有效修复老龄骨缺损
时间:2026-05-05 17:01:21 热度:37.1℃ 作者:网络
背景介绍
年龄相关的骨缺损是临床面临的重大挑战,其特征为骨微结构退化和脆性增加。随着全球人口老龄化加剧,骨质疏松及老年性骨缺损的发病率持续上升。目前临床治疗手段包括药物干预和手术修复,但存在患者依从性差、移植物排斥、修复效果不理想等问题。骨髓间充质干细胞(BMSCs)具有分化为成骨细胞的能力,然而随着年龄增长,BMSCs的成骨潜能显著下降,这使得利用老年患者自身干细胞进行修复变得困难。异体干细胞移植又面临遗传不稳定、免疫排斥和致瘤风险。因此,亟需开发能够恢复老年BMSCs成骨能力的新型无细胞治疗策略。细胞外囊泡(EVs)作为细胞分泌的纳米级囊泡,携带miRNA、蛋白等生物活性分子,具有低免疫原性、可模拟亲代细胞功能等优势,但其体内易扩散、滞留时间短等问题限制了疗效。
研究思路
针对上述挑战,苏州大学附属第一医院骨科杨惠林教授、徐永教授和施勤教授团队联合设计了一种静电共组装的可注射水凝胶系统(P-GA/KA7),用于负载年轻BMSCs来源的EVs(Y-EVs)。该水凝胶由带正电的星形PEG-KA7肽和带负电的聚磷酸-明胶(P-GA)通过静电和疏水相互作用非共价组装而成。P-GA组分可水解释放磷酸根,提供骨矿化所需的磷源并激活BMP-2/Smad信号通路;KA7肽则通过结合硫酸乙酰肝素蛋白聚糖增强细胞粘附。该系统实现了Y-EVs的缓释和局部滞留,在体外显著促进老年BMSCs(A-BMSCs)的成骨分化并缓解其衰老表型。在18月龄老龄大鼠颅骨临界骨缺损模型中,P-GA/KA7@Y-EVs水凝胶显著加速了新骨形成,效果优于单独使用Y-EVs或水凝胶。转录组和miRNA测序分析揭示,Y-EVs通过调控PI3K-Akt、TGF-β、MAPK等信号通路以及下调衰老相关基因发挥 rejuvenation 作用。相关内容以An Electrostatic Co-Assembled Extracellular Vesicles Infused Hydrogel for Bone Regeneration in Aged Defects为题,发表在Biomaterials!

图片解析
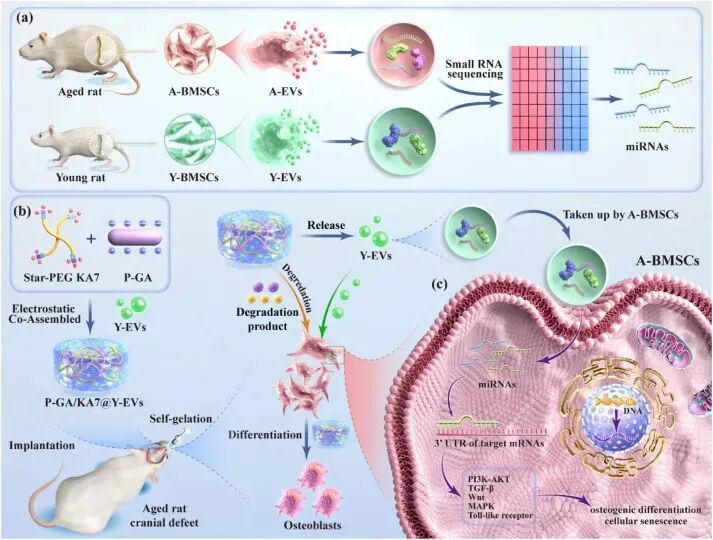
Scheme 1. P-GA/KA7@Y-EVs水凝胶修复老龄大鼠颅骨临界骨缺损的示意图: (a) 从年轻和老龄BMSCs中分离Y-EVs和A-EVs,并分析两者差异miRNA表达谱。(b) P-GA/KA7@Y-EVs水凝胶的制备及其用于修复老龄大鼠颅骨临界骨缺损。(c) 差异miRNA调控成骨分化和细胞衰老的机制示意图。
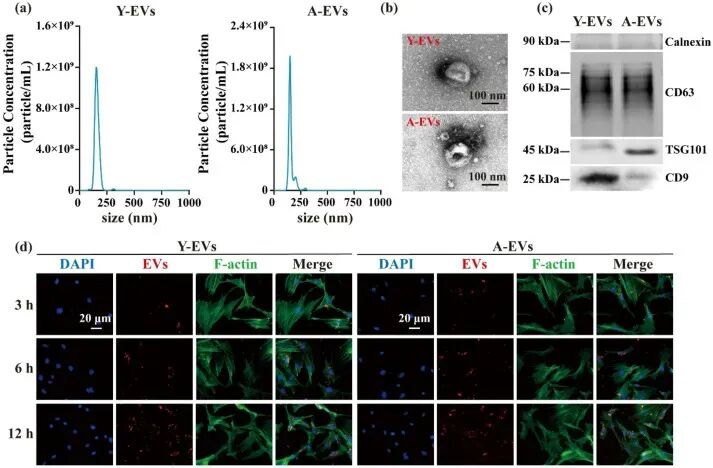
图1. Y-EVs和A-EVs的表征与摄取: (a) NTA分析:Y-EVs和A-EVs粒径分布相似(~162 nm)。(b) TEM图像:两者均呈典型杯状形态。(c) Western blot:两者均阳性表达CD9、TSG101、CD63,阴性表达Calnexin。(d) 共聚焦显微镜:Dil标记的Y-EVs和A-EVs被A-BMSCs摄取后主要定位于核周区域,且摄取随时间(3、6、12 h)增加。
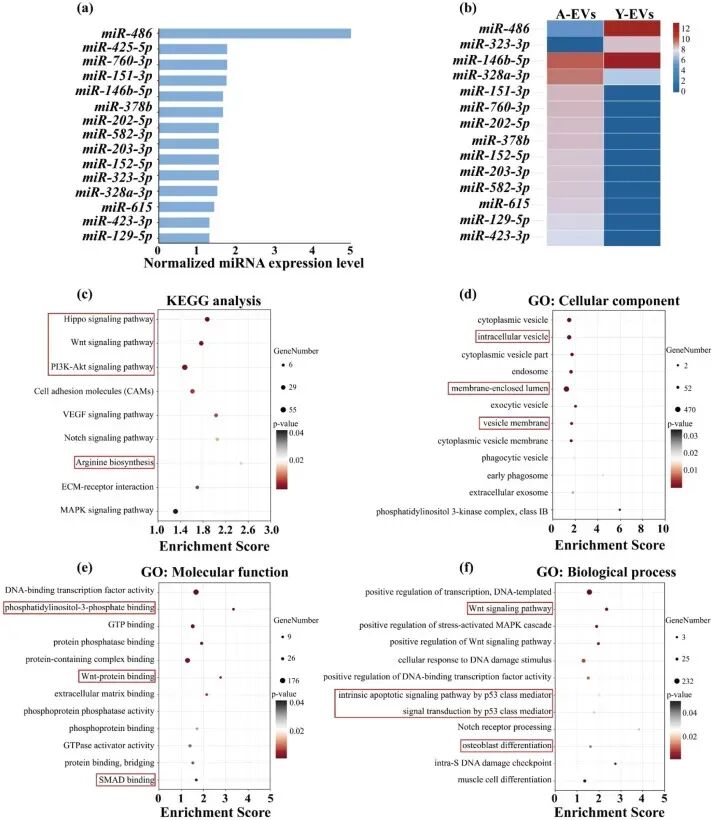
图2. Y-EVs与A-EVs中成骨和衰老相关miRNA的差异表达: (a) 成骨相关miRNA在Y-EVs和A-EVs中的差异表达水平。(b) 成骨相关miRNA的热图,显示Y-EVs中促成骨miRNA(miR-486、miR-323-3p、miR-146b-5p)上调,抑成骨miRNA下调。(c-f) KEGG和GO富集分析:差异miRNA的靶基因富集于PI3K-Akt、Wnt、Hippo等成骨通路以及p53介导的衰老相关通路。
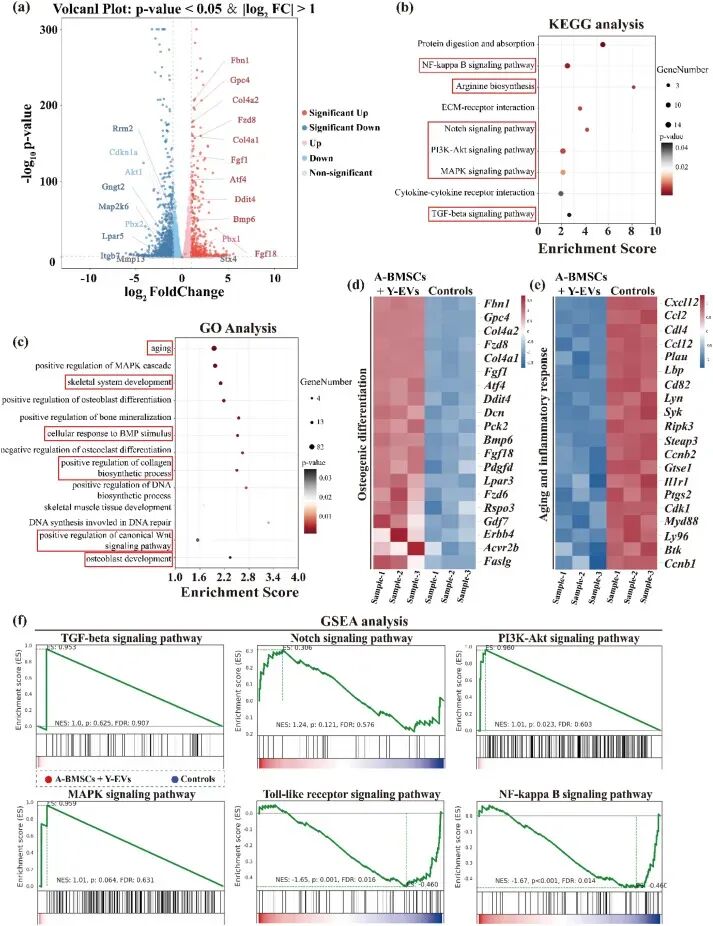
图3. Y-EVs处理A-BMSCs后的转录组分析: (a) 火山图:Y-EVs处理后A-BMSCs中478个基因上调、957个下调。(b) KEGG分析:富集于PI3K-Akt、TGF-β、Notch、MAPK成骨通路及NF-κB等衰老相关通路。(c) GO分析:涉及BMP刺激应答、Wnt信号正向调控、成骨细胞发育等生物过程,以及DNA修复、衰老等。(d-e) 热图:Y-EVs上调成骨基因(Bmp6、Atf4等),下调衰老和炎症基因。(f) GSEA:Y-EVs增强成骨相关模块富集分数,降低衰老相关模块(Toll样受体、NF-κB信号)富集分数。
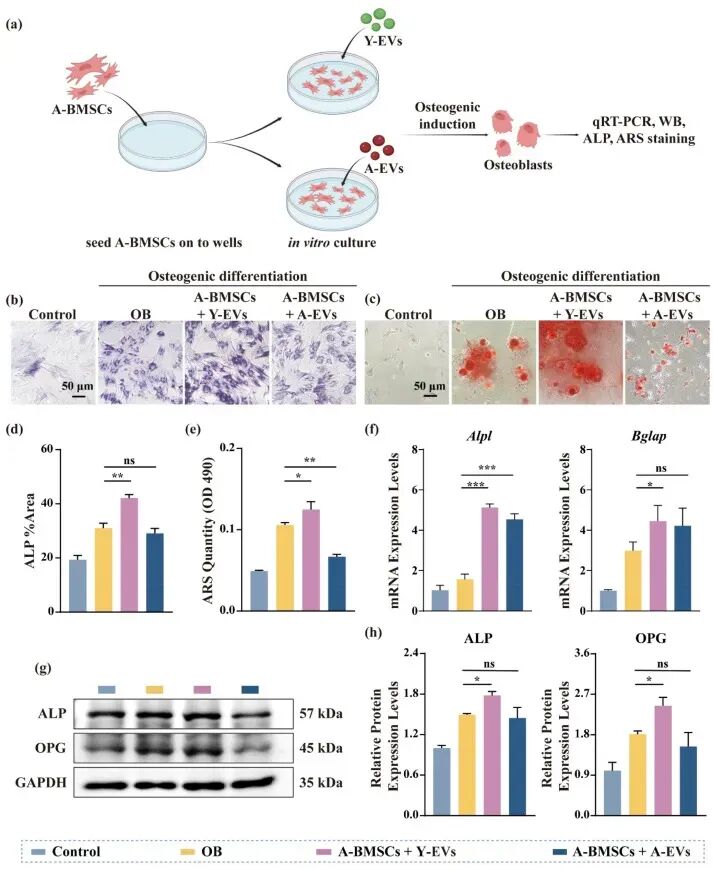
图4. Y-EVs促进A-BMSCs成骨分化优于A-EVs: (a) 体外实验示意图。(b, d) ALP染色及定量:Y-EVs组ALP活性较成骨诱导组(OB)提高1.4倍。(c, e) ARS染色及定量:Y-EVs组钙沉积较OB组提高1.3倍,A-EVs组反而降低。(f) qRT-PCR:Y-EVs组Alpl和Bglap表达分别较OB组提高3.3倍和1.5倍。(g, h) Western blot及定量:Y-EVs组ALP和OPG蛋白表达较OB组分别提高1.2倍和1.3倍,A-EVs组无显著差异。
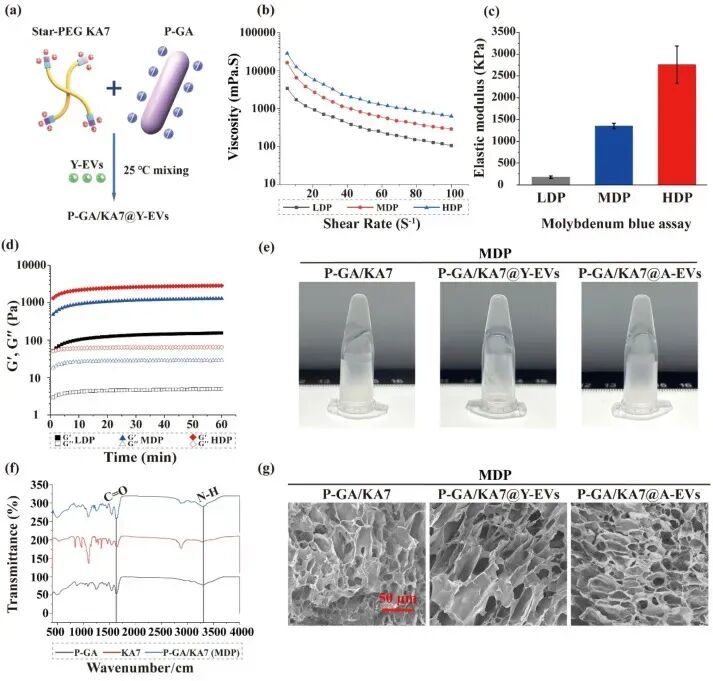
图5. P-GA/KA7水凝胶的表征: (a) 水凝胶形成示意图:P-GA与KA7通过非共价相互作用自组装。(b) 三种磷酸根取代度(LDP、MDP、HDP)水凝胶的剪切稀释曲线,均具有自愈合性和可注射性。(c) 弹性模量随取代度增加而增加(LDP 64.9 KPa,MDP 108.8 KPa,HDP 167.1 KPa)。(d) 储存模量(G')和损耗模量(G")随时间变化,MDP组用于后续实验。(e) P-GA/KA7、P-GA/KA7@Y-EVs和P-GA/KA7@A-EVs水凝胶成胶后大体照片。(f) FTIR光谱。(g) SEM图像:水凝胶呈均匀多孔三维网络结构。
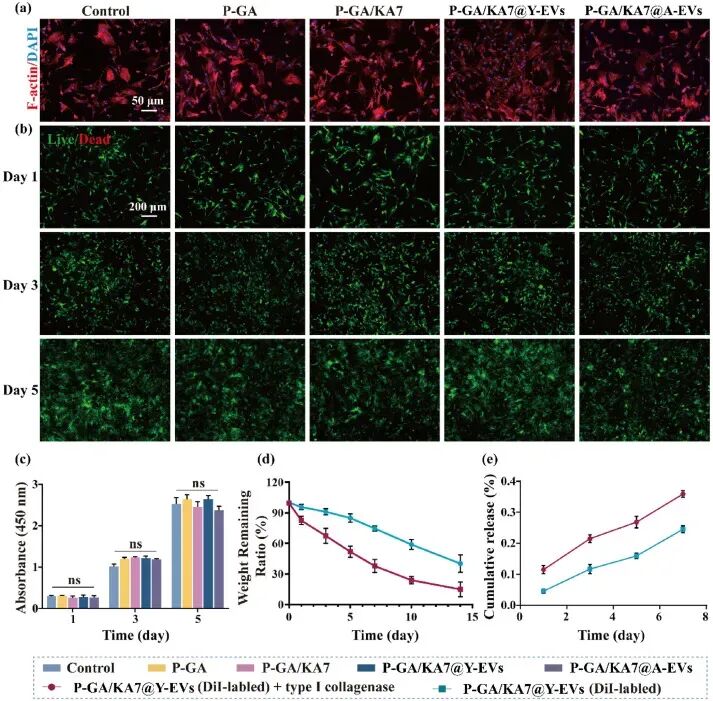
图6. 水凝胶的生物相容性与EVs释放曲线: (a) A-BMSCs在各组水凝胶表面的细胞骨架染色(Phalloidin),细胞粘附良好。(b) Live-Dead染色:细胞活率高,且随培养时间(1、3、5天)细胞密度增加。(c) CCK-8:各组成骨细胞增殖无显著差异。(d) 水凝胶降解曲线:7天后PBS中剩余质量约65%,胶原酶组加速降解。(e) DiI标记Y-EVs的累积释放曲线:7天时胶原酶组释放约35%,无酶组释放约22%,呈时间依赖性。
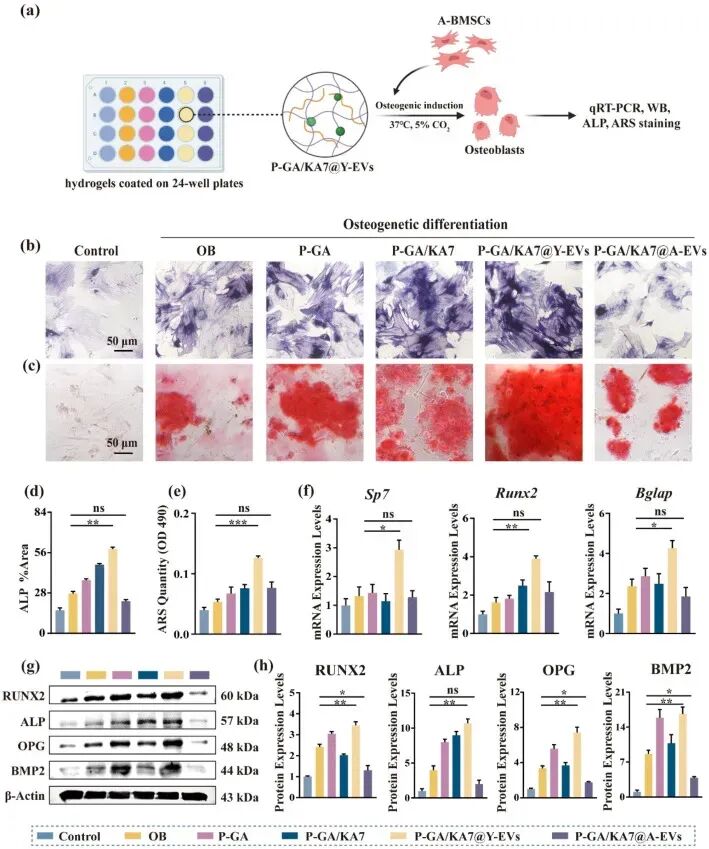
图7. P-GA/KA7@Y-EVs水凝胶促进A-BMSCs成骨分化: (a) 体外实验示意图。(b, d) ALP染色及定量:P-GA/KA7@Y-EVs组ALP活性显著高于OB组和P-GA/KA7@A-EVs组。(c, e) ARS染色及定量:P-GA/KA7@Y-EVs组钙结节最多、矿化最显著。(f) qRT-PCR:P-GA/KA7@Y-EVs组Sp7、Runx2、Bglap表达分别较OB组提高2.2、2.4、1.8倍。(g, h) Western blot及定量:P-GA/KA7@Y-EVs组RUNX2、ALP、OPG、BMP2表达较OB组分别提高1.4、2.7、2.2、1.8倍,而A-EVs组降低。
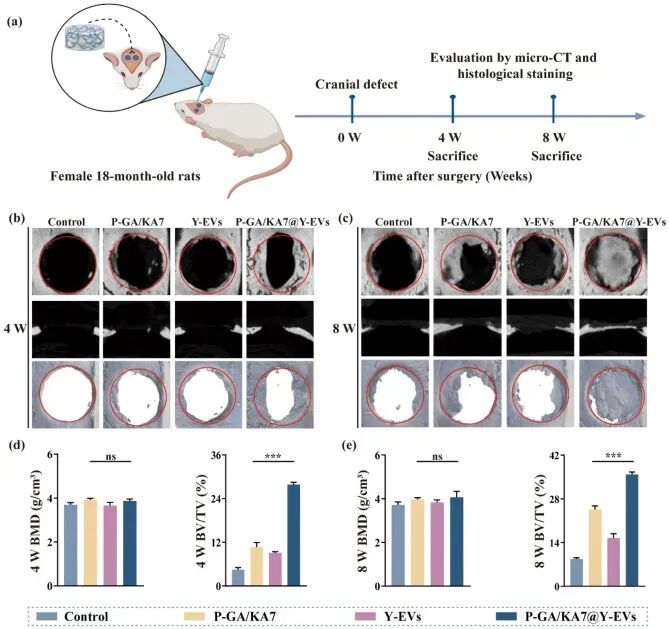
图8. P-GA/KA7@Y-EVs水凝胶加速老龄大鼠颅骨临界骨缺损修复: (a) 动物实验设计:18月龄雌性SD大鼠颅骨双侧5 mm缺损,分别给予PBS、游离Y-EVs、P-GA/KA7水凝胶或P-GA/KA7@Y-EVs水凝胶。(b, c) 术后4周和8周的micro-CT三维重建图像:P-GA/KA7@Y-EVs组骨缺损最小、新生骨最多。(d, e) 定量分析:4周时P-GA/KA7@Y-EVs组BV/TV为27.9±0.6%,显著高于Y-EVs组(9.1±3.2%)、P-GA/KA7组(10.7±1.2%)和对照组(4.5±5.9%);8周时P-GA/KA7@Y-EVs组BV/TV增至34.8±2.3%,仍优于其他组。
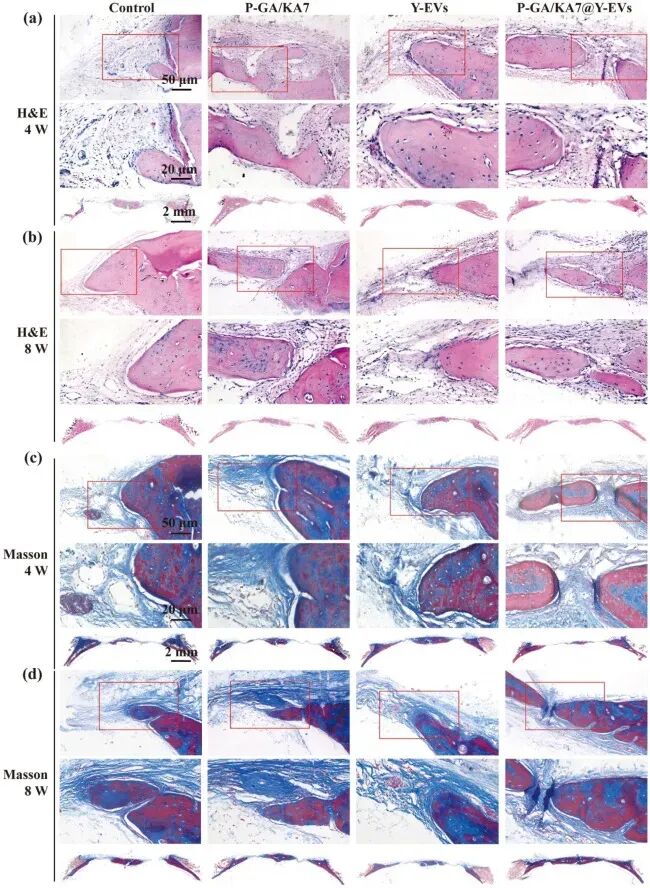
图9. 组织学染色显示P-GA/KA7@Y-EVs促进新骨形成: (a, b) H&E染色:术后4周和8周,P-GA/KA7@Y-EVs组缺损边缘大量新骨形成,可见骨样组织和编织骨;8周时几乎完全覆盖缺损。(c, d) Masson三色染色:P-GA/KA7@Y-EVs组胶原纤维和新生骨组织最丰富,染色深度和范围均优于其他组。
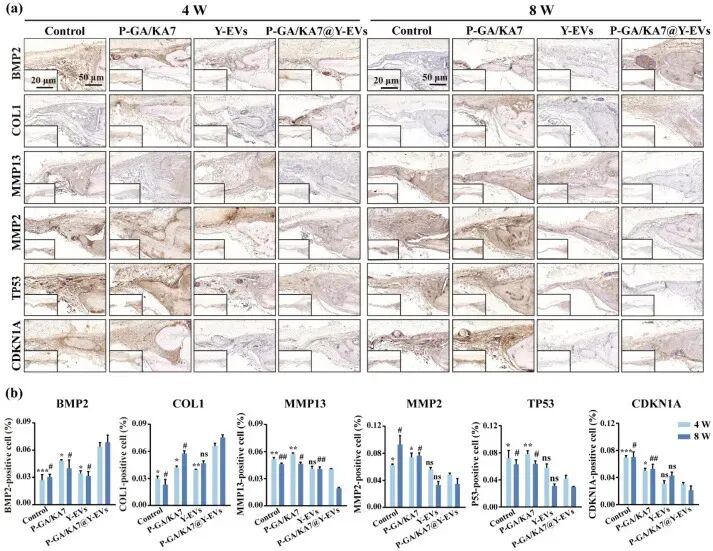
图10. 免疫组化检测成骨及衰老相关指标: (a) IHC染色:4周和8周时,P-GA/KA7@Y-EVs组BMP2和COL1表达最强,而衰老标志物CDKN1A(p21)、TP53(p53)、MMP2、MMP13表达最弱。(b) 定量分析:P-GA/KA7@Y-EVs组BMP2和COL1阳性面积百分比显著高于其他组,CDKN1A、TP53、MMP2、MMP13阳性面积显著低于其他组。
结论
本研究成功构建了一种静电共组装的可注射P-GA/KA7@Y-EVs水凝胶系统,用于修复年龄相关的骨缺损。该系统通过非共价相互作用实现温和、快速的原位凝胶化,具有良好的可注射性、生物相容性和酶响应性降解特性。水凝胶缓释Y-EVs可显著促进老年BMSCs的成骨分化并减轻其衰老表型,机制上涉及Y-EVs中富集的促成骨miRNA对PI3K-Akt、Wnt、TGF-β等信号通路的调控以及抑制衰老相关基因表达。在老龄大鼠颅骨临界骨缺损模型中,P-GA/KA7@Y-EVs水凝胶组的新骨形成量(BV/TV达34.8%)显著优于单独Y-EVs或水凝胶组,同时降低了缺损区域的细胞衰老标志物水平。该研究为利用生物材料增强EVs治疗老年性骨缺损提供了一种微创、高效且具有临床转化潜力的新策略。
原文链接:
https://www.sciencedirect.com/science/article/pii/S0142961226002784


