四川大学Biomaterials:开发基因工程细胞外囊泡仿生支架,实现肌腱再生修复
时间:2026-05-05 17:01:19 热度:37.1℃ 作者:网络
背景介绍
肌腱损伤,尤其是大面积肌腱缺损,在临床上仍面临巨大挑战。肌腱组织再生能力极为有限,且对生物力学环境要求苛刻,这使得传统治疗手段(如自体移植)往往受限于供体来源不足、供区病损以及修复后易形成瘢痕组织、力学性能差等问题。脱细胞肌腱支架虽然能够提供仿生的各向异性结构和力学支持,但其本身缺乏调控细胞行为的生物活性信号。近年来,干细胞来源的细胞外囊泡(EVs)因其低免疫原性、高稳定性和强大的旁分泌调控功能,在组织再生领域展现出巨大潜力,然而天然EVs存在批次差异大、体内清除快、靶向性不足等问题。因此,如何构建兼具仿生结构与生物活性信号的空间靶向递送系统,成为肌腱再生研究的重点。
研究思路
针对上述挑战,四川大学华西医院骨科、生物治疗国家重点实验室的秦廷武教授团队开发了一种创新性的双工程化仿生支架(TDSCs^Bgn/Fmod/CTP^ EVs-DBTS)。研究首先对肌腱源性干细胞(TDSCs)进行基因工程改造,利用T2A/E2A自剪切多肽系统使其共过表达双聚糖(Biglycan, Bgn)和纤调蛋白(Fibromodulin, Fmod),这两种蛋白是维持肌腱结构完整性和力学特性的关键蛋白聚糖。从该工程化细胞中提取的EVs(TDSCs^Bgn/Fmod^ EVs)富含肌腱相关分子,并通过下调miR-145-5p进而激活TGFβ2/Smad信号通路,显著促进TDSCs的成腱分化,同时抑制其向成骨和成软骨方向的异常分化。为进一步提高EVs在体内的滞留和靶向能力,研究团队通过表面等离子体共振(SPR)筛选出对I型胶原具有最高亲和力的胶原靶向肽(CTP),并将其基因工程化展示在EVs表面(CD63-CTP融合)。最后,将这些双工程化EVs负载于脱细胞牛肌腱片(DBTS)上,构建成仿生支架。该支架在体外显著促进了TDSCs的增殖、迁移和成腱分化;在大鼠跟腱缺损模型中,支架实现了EVs的持续释放,有效诱导M2型巨噬细胞极化、招募内源性干细胞(CD44+/CD90+),并最终实现了高质量的肌腱再生,其胶原纤维排列、直径分布以及生物力学性能(最大载荷、杨氏模量、刚度)均显著优于对照组。相关内容以Genetically engineered extracellular vesicles-based collagen-targeting bioinspired scaffold for tendon regenerative repair为题,发表在Biomaterials!

图片解析
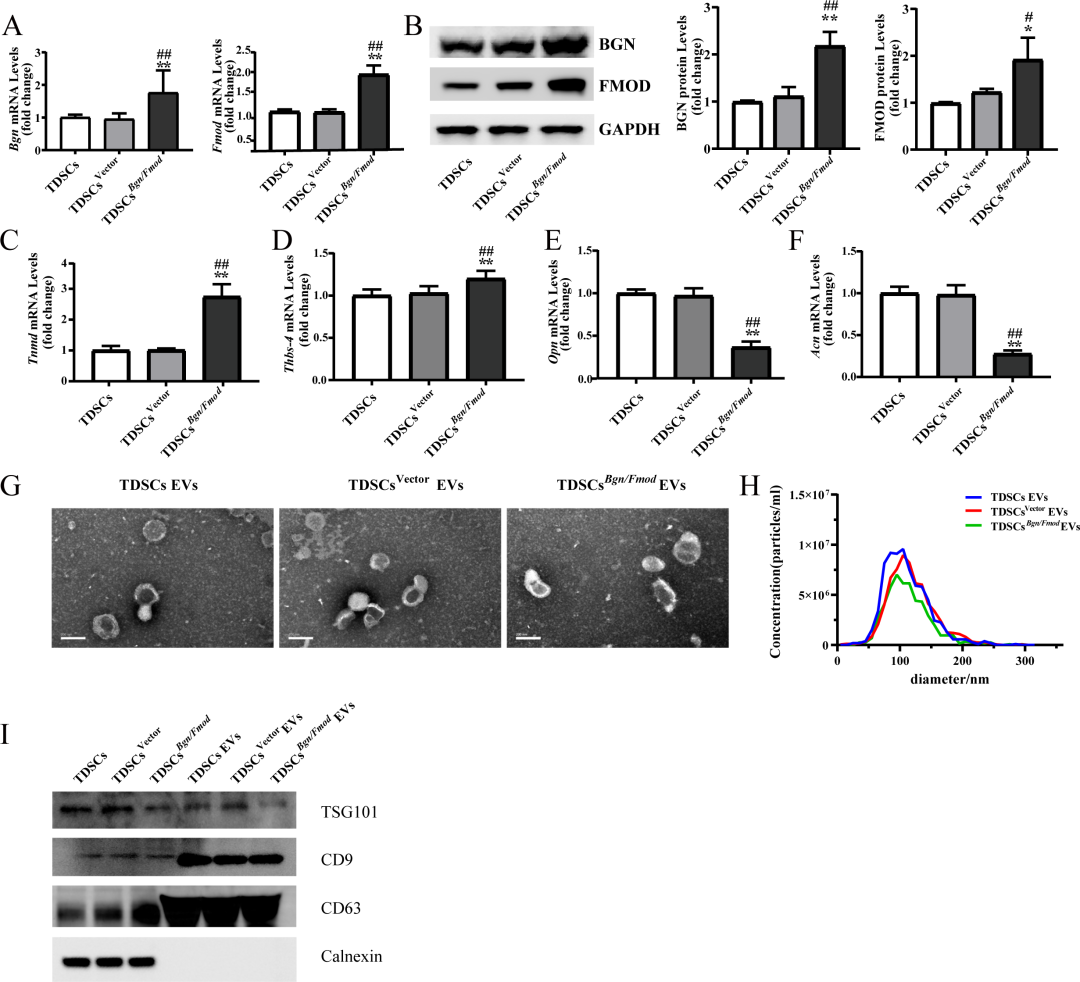
图1. TDSCs^Bgn/Fmod^ EVs的表征: (a) RT-qPCR显示TDSCs^Bgn/Fmod^细胞中Bgn和Fmod mRNA水平显著升高。(b) Western blot证实BGN和FMOD蛋白表达上调。(c-f) RT-qPCR:TDSCs^Bgn/Fmod^组中成腱标志物Tnmd和Thbs-4表达升高,而成骨标志物Opn和成软骨标志物Acn表达降低。(g) TEM显示EVs呈典型杯状形态,标尺200 nm。(h) NTA显示EVs粒径约120 nm。(i) Western blot:EVs阳性表达TSG101、CD9、CD63,阴性表达Calnexin。
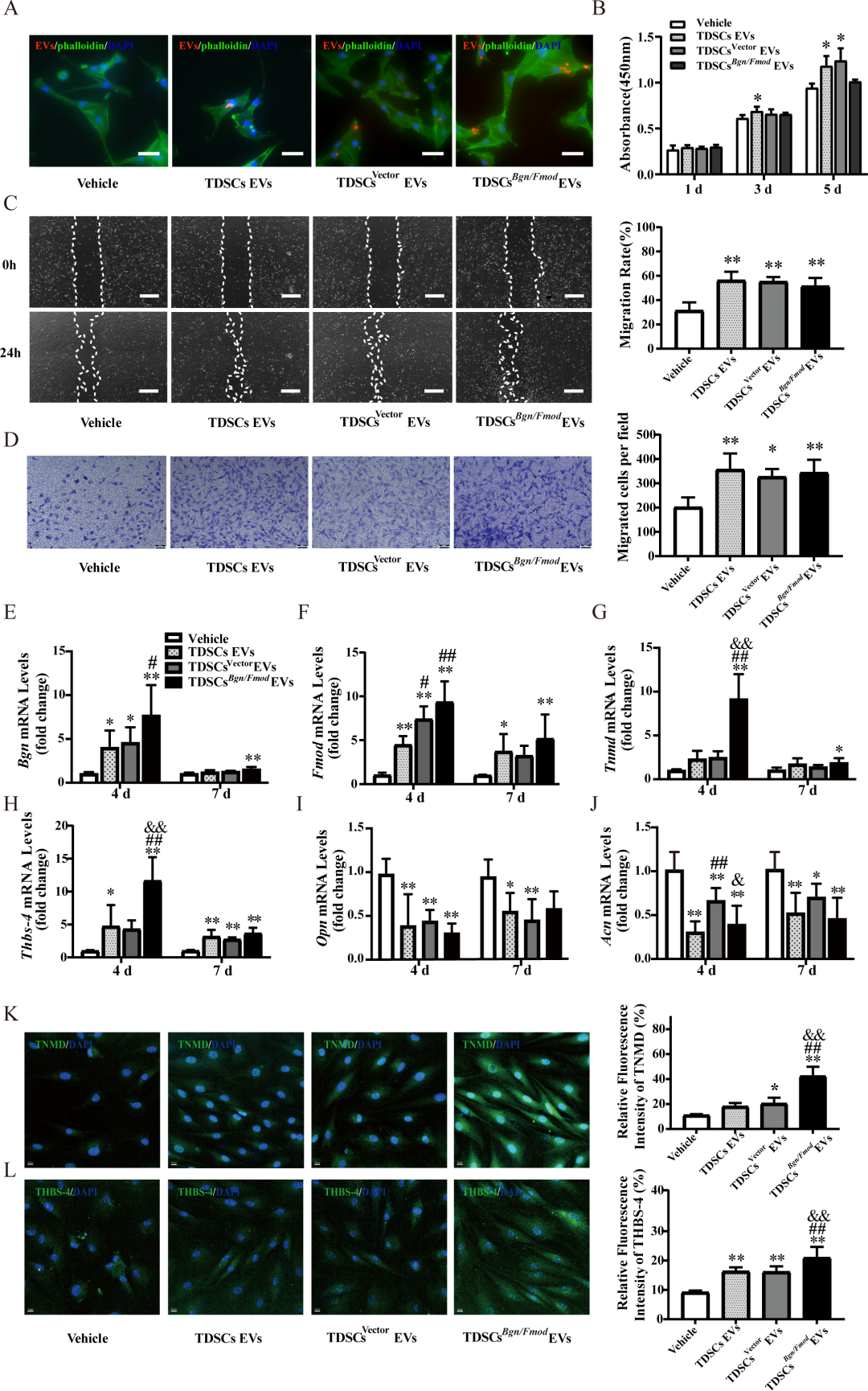
图2. TDSCs^Bgn/Fmod^ EVs对TDSCs功能的调控: (a) 共聚焦显微镜显示DiI标记的EVs(红色)被TDSCs(鬼笔环肽染细胞骨架绿色,DAPI染核蓝色)有效内化,标尺50 μm。(b) CCK-8:TDSCs^Bgn/Fmod^ EVs促进TDSCs增殖。(c-d) 划痕实验和Transwell实验:TDSCs^Bgn/Fmod^ EVs显著增强TDSCs迁移能力,标尺400 μm和50 μm。(e-j) RT-qPCR:TDSCs^Bgn/Fmod^ EVs组中成腱标志物Tnmd、Thbs-4表达上调,Opn和Acn表达下调。(k-l) 免疫荧光:TDSCs^Bgn/Fmod^ EVs组中TNMD和THBS-4蛋白表达最强,标尺10 μm。
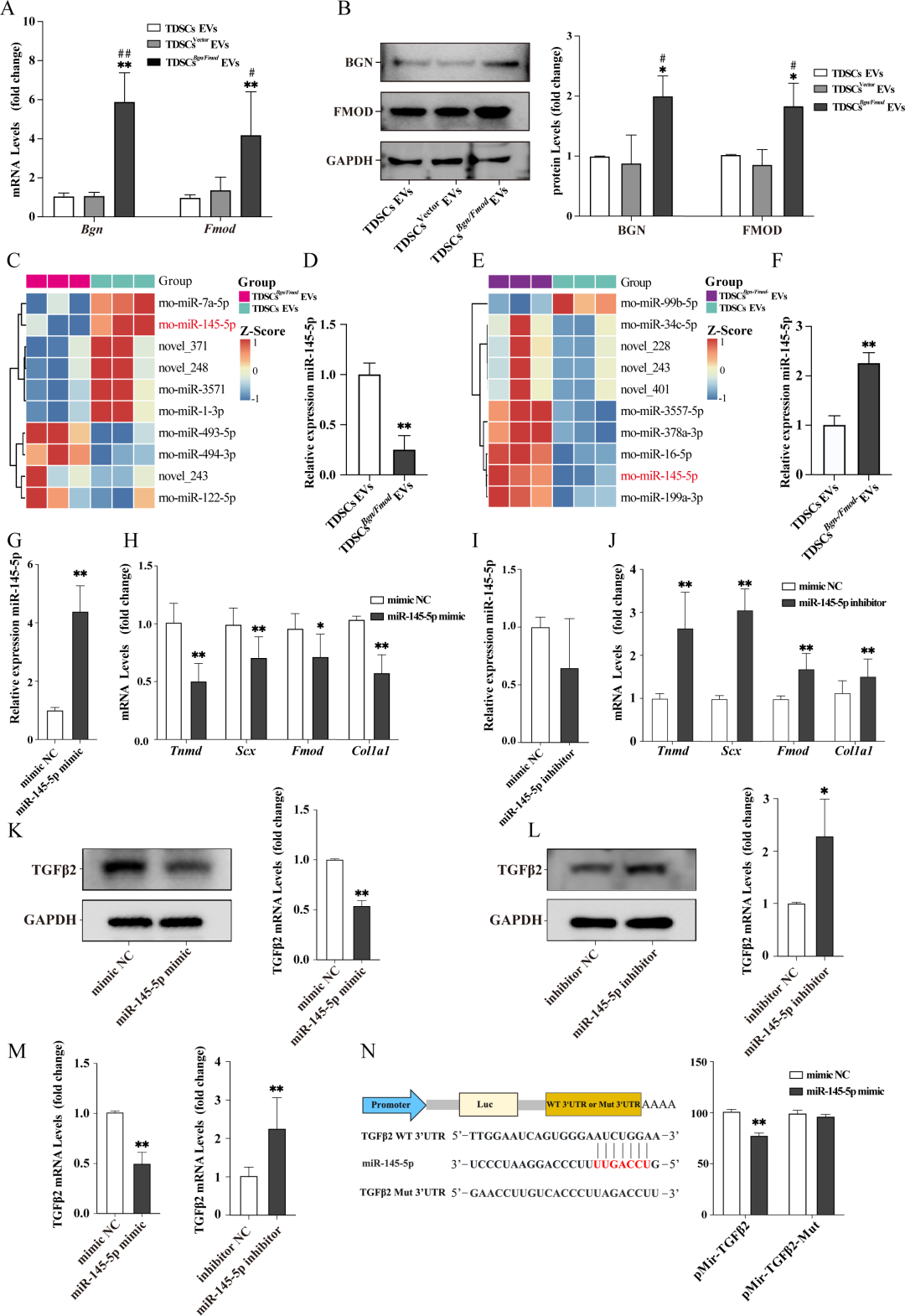
图3. TDSCs^Bgn/Fmod^ EVs调控成腱分化的分子机制: (a-b) RT-qPCR和Western blot证实TDSCs^Bgn/Fmod^ EVs中Bgn和Fmod mRNA及蛋白水平升高。(c) miRNA聚类热图显示TDSCs^Bgn/Fmod^ EVs与对照组EVs的miRNA表达谱存在显著差异。(d) RT-qPCR验证TDSCs^Bgn/Fmod^ EVs中miR-145-5p表达下调。(e) miRNA表达谱分析。(f) RT-qPCR显示TDSCs^Bgn/Fmod^- EVs中miR-145-5p表达上调。(g-j) miR-145-5p mimic抑制成腱标志物(Tnmd、Scx、Fmod、Col I)表达,而miR-145-5p inhibitor促进其表达。(k-m) Western blot和RT-qPCR:miR-145-5p mimic下调TGFβ2表达,inhibitor上调TGFβ2表达。(n) 双荧光素酶报告基因实验证实miR-145-5p直接靶向TGFβ2。
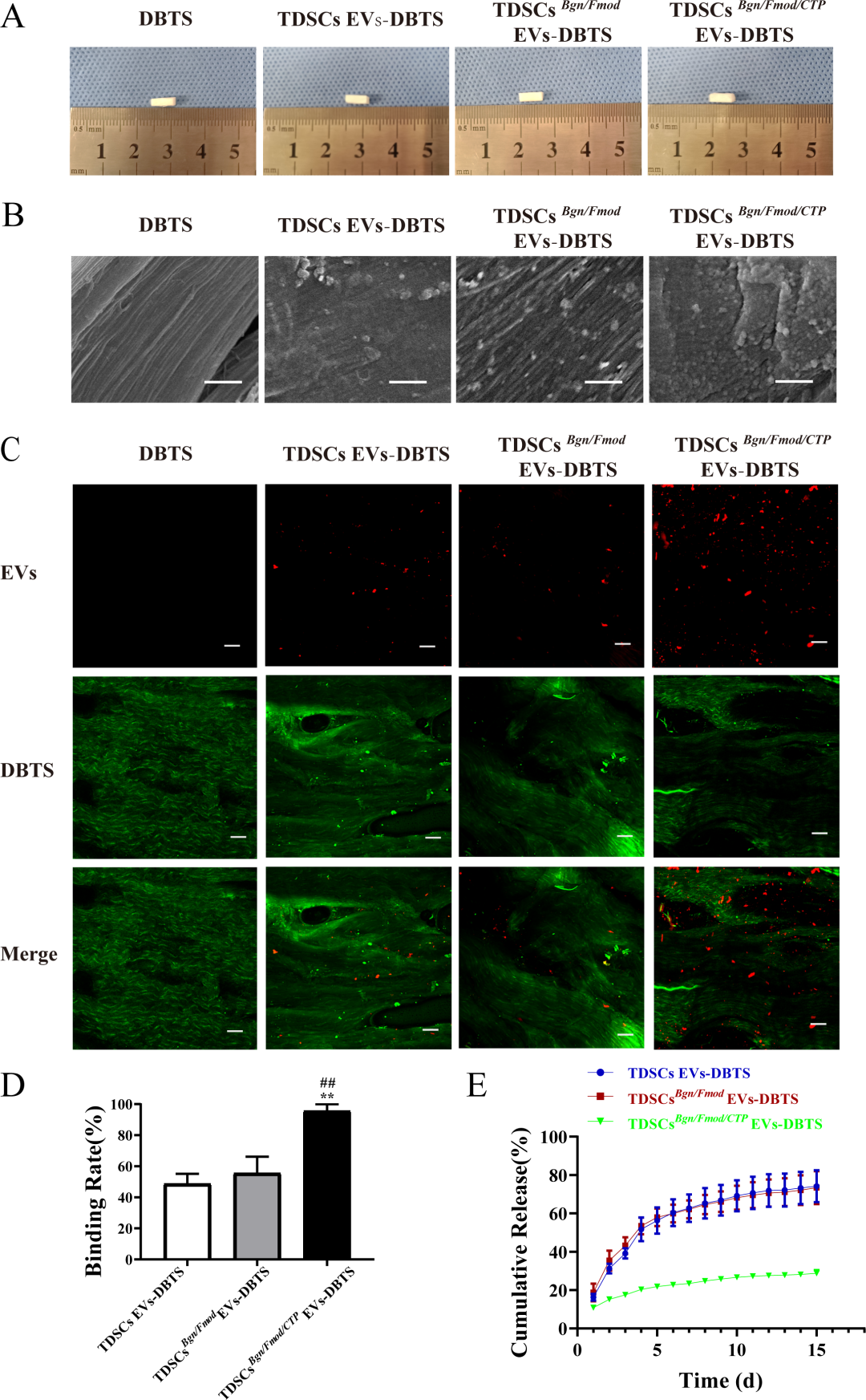
图4. TDSCs^Bgn/Fmod/CTP^ EVs-DBTS支架的表征: (a) 支架大体照片。(b) SEM显示支架呈纳米纤维结构,标尺1 μm(插图为5倍放大)。(c) 共聚焦显微镜:DiI标记的EVs(红色)均匀分布于DBTS基质(自发荧光绿色)中,标尺50 μm。(d) EVs结合率定量:CTP修饰组结合率显著高于非CTP组。(e) EVs累计释放曲线:CTP修饰组在14天内释放速率更慢、更持续。
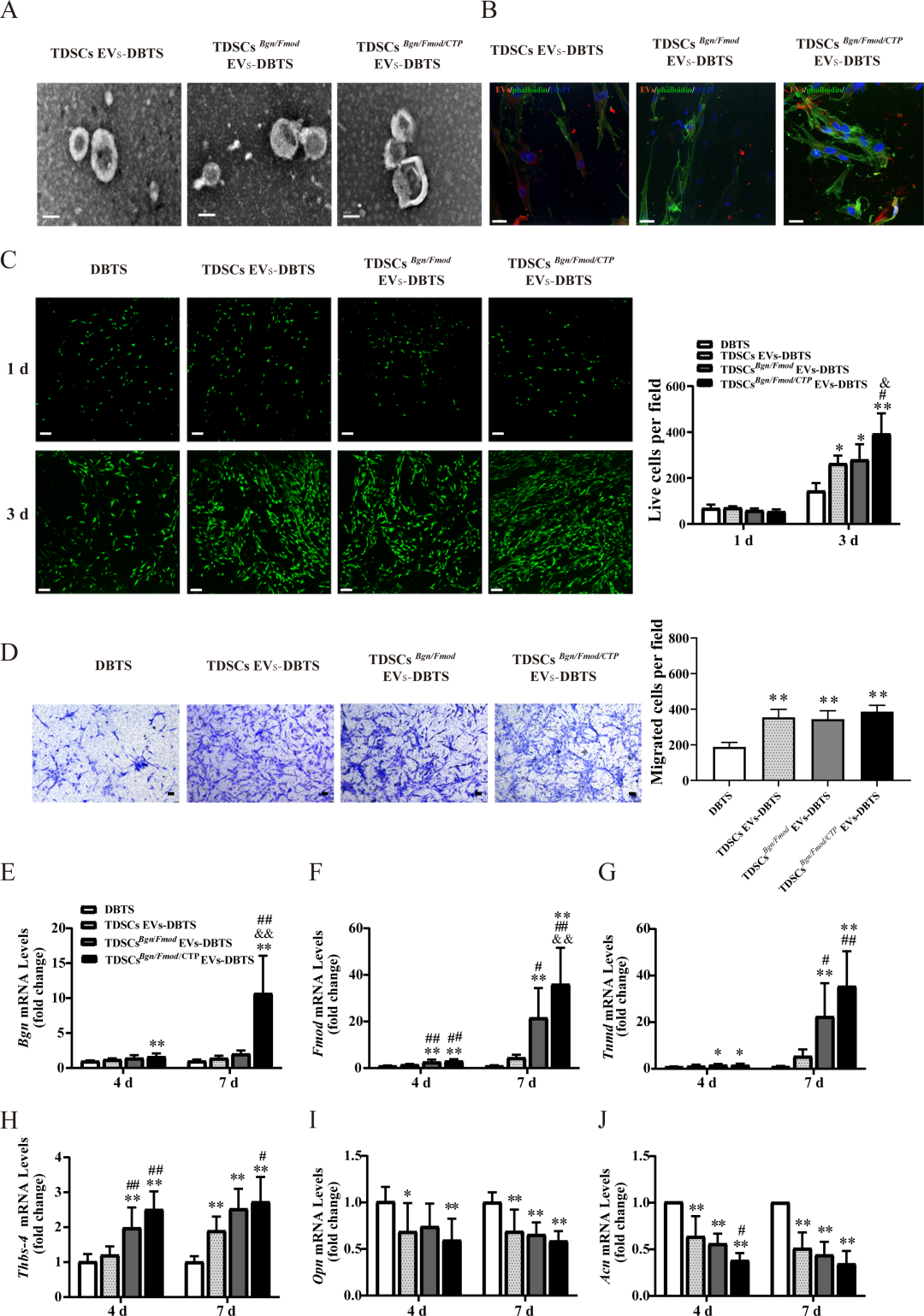
图5. TDSCs^Bgn/Fmod/CTP^ EVs-DBTS支架对TDSCs的生物活性诱导: (a) TEM显示从支架中释放的EVs保持完整形态,标尺100 nm。(b) 共聚焦:DiI标记EVs(红色)被TDSCs内化,标尺20 μm。(c) Live/Dead染色:TDSCs^Bgn/Fmod/CTP^ EVs-DBTS组细胞活性最高,标尺50 μm。(d) Transwell实验:该组迁移能力最强。(e-j) RT-qPCR:该组成腱标志物Tnmd和Thbs-4表达最高,成骨标志物Opn和成软骨标志物Acn表达最低。
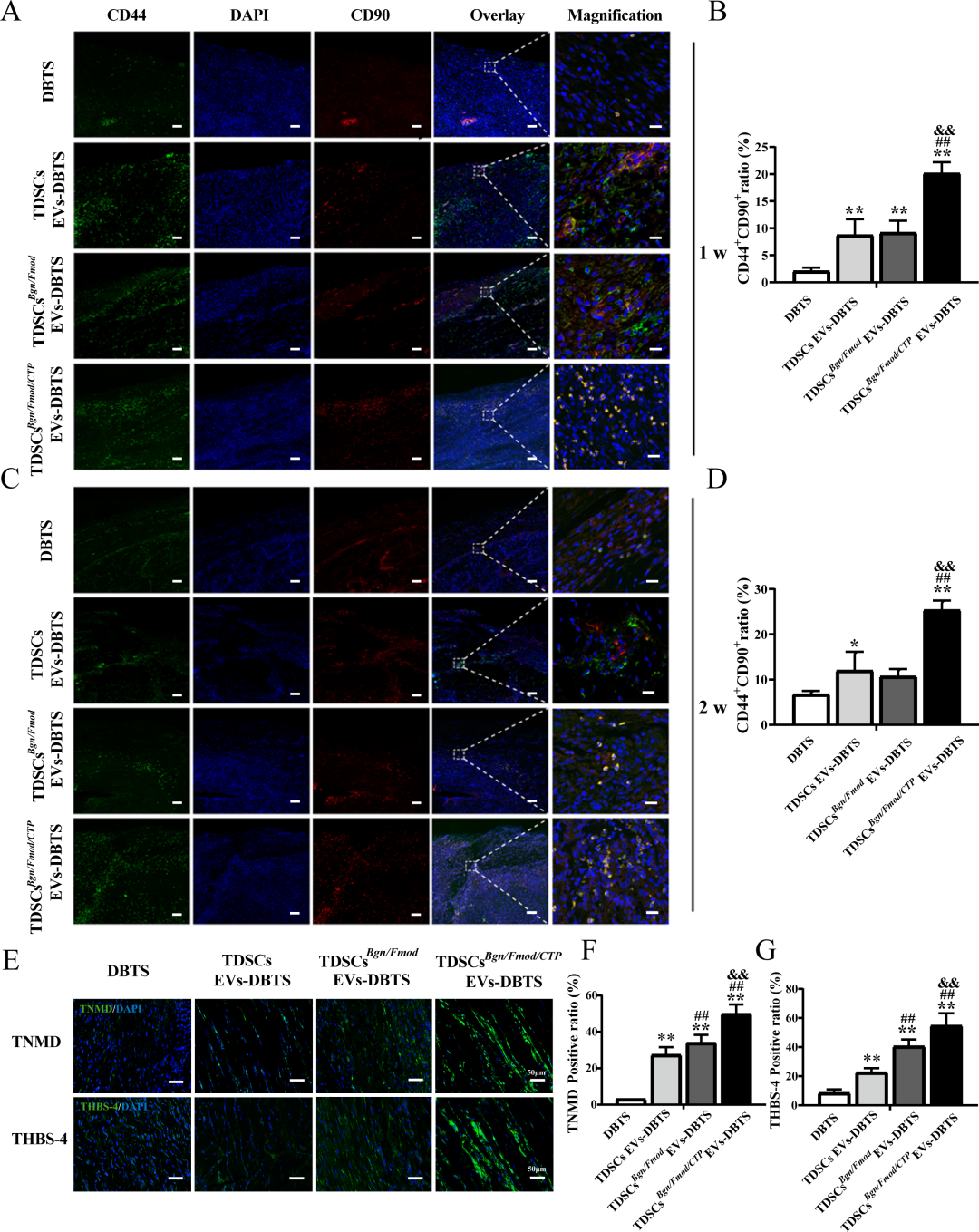
图6. TDSCs^Bgn/Fmod/CTP^ EVs-DBTS支架介导的内源性干细胞招募与成腱分化: (a, c) 免疫荧光:术后1周和2周,TDSCs^Bgn/Fmod/CTP^ EVs-DBTS组中CD44+/CD90+双阳性内源性干细胞数量最多,标尺200 μm(主图)和20 μm(插图中放大部分)。(b, d) 双阳性细胞定量。(e) 肌腱再生组织中TNMD和THBS-4免疫荧光染色,该组表达最强,标尺50 μm。(f, g) 荧光强度定量。
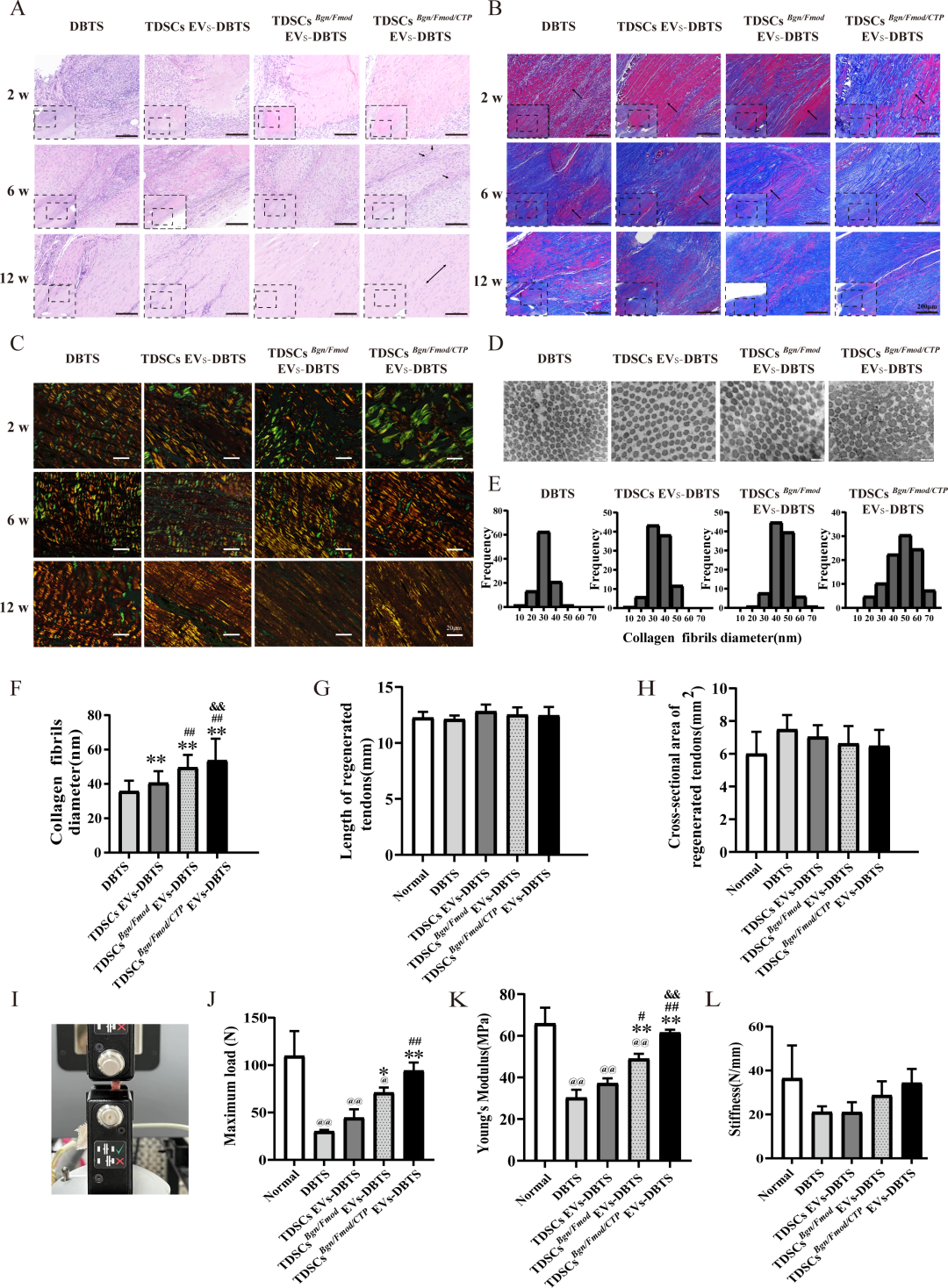
图7. 再生肌腱的组织学、超微结构与生物力学评估: (a) H&E染色:术后2、6、12周,TDSCs^Bgn/Fmod/CTP^ EVs-DBTS组炎症最轻、胶原纤维排列最有序(双向箭头)、新生血管形成最明显(单向箭头),12周时缺损完全被新生肌腱组织替代,标尺100 μm(主图)和200 μm(左下角插图中低倍视野)。(b) Masson三色染色:该组胶原成熟度最高,标尺同上。(c) 天狼星红偏振光:该组最早出现III型胶原(绿色)向I型胶原(橙色/红色)的转换,标尺20 μm。(d) TEM:该组胶原纤维排列紧密、直径更大,标尺100 nm。(e) 胶原纤维直径分布。(f) 平均直径定量:该组显著大于其他组。(g) 再生肌腱长度、(h) 横截面积:各组与正常组无显著差异。(i) 单轴拉伸测试装置。(j) 最大载荷、(k) 杨氏模量、(l) 刚度:TDSCs^Bgn/Fmod/CTP^ EVs-DBTS组均显著优于其他组,接近正常肌腱水平。
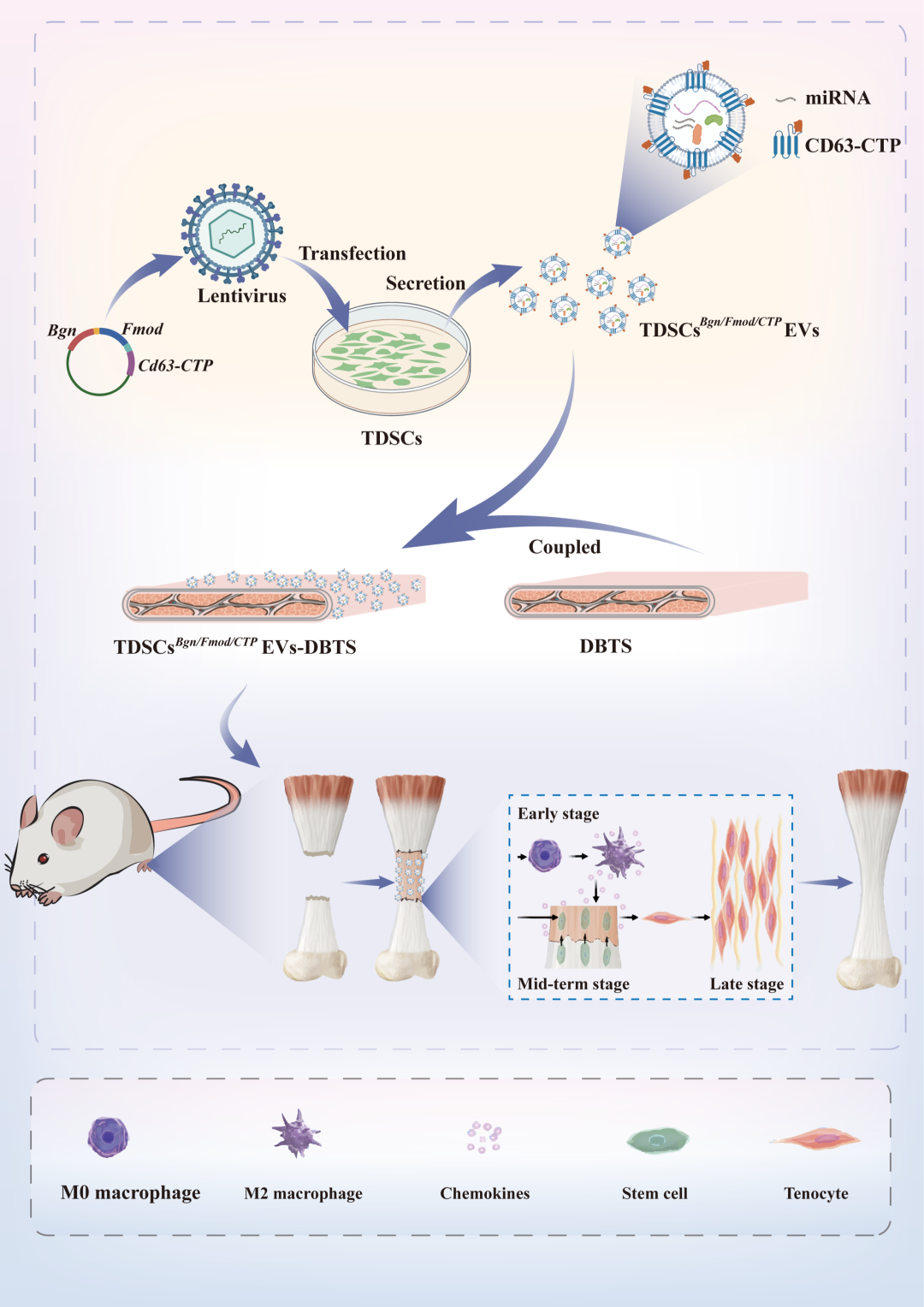
图8.(Scheme/机制总结图,文中未标注但在结论中提及): (文中未提供具体图号,但根据结论描述) 双工程化仿生支架通过miR-145-5p/TGFβ2信号通路驱动成腱分化,同时实现M2巨噬细胞极化、内源性干细胞招募和持续EVs释放,最终实现功能性肌腱再生。
结论
本研究成功构建了一种双基因工程化、胶原靶向的EVs仿生支架(TDSCs^Bgn/Fmod/CTP^ EVs-DBTS)。该支架通过Bgn和Fmod的共过表达,富集了EVs中的肌腱再生相关分子,并通过miR-145-5p/TGFβ2信号轴显著促进了TDSCs的成腱分化,同时抑制了异常的骨/软骨分化。CTP修饰赋予了EVs对DBTS支架的高亲和力,实现了EVs的局部缓释。在大鼠跟腱缺损模型中,该支架有效诱导了M2型巨噬细胞极化、招募了内源性干细胞,最终实现了组织学结构和生物力学功能均接近天然肌腱的高质量再生。该研究为基因工程化EVs结合仿生支架治疗肌腱损伤提供了新策略,具有重要的临床转化潜力。
原文链接:
https://doi.org/10.1016/j.biomaterials.2026.124227


