论文解读 | Yin S/ Deng W教授团队揭示SF3B1K700E突变驱动造血祖细胞转录失调导致血液肿瘤病理机制
时间:2026-05-05 16:59:34 热度:37.1℃ 作者:网络
SF3B1(splicing factor 3b subunit 1)突变,尤其是K700E热点突变,参与多种血液系统恶性肿瘤的发病过程。现有小鼠模型与人类疾病表现存在明显差距,难以完全重现患者的转录失调特征。因此,需要能够更准确模拟人类疾病表型的替代模型,以阐明SF3B1突变在肿瘤发生中的机制。目前尚不清楚由SF3B1突变特异性诱导的哪些转录失调事件在血液肿瘤早期阶段起关键作用。
爱因斯坦医学院的Shanye Yin教授团队与哈佛医学院的Wenjun Deng教授团队合作,在本刊发表题为“SF3B1K700E-driven transcriptional alterations in hematopoietic progenitors underlie blood cancer pathophysiology”的研究快讯。该研究发现SF3B1K700E突变通过改变关键造血基因的剪接模式和表达水平驱动血液肿瘤早期分子事件,并提出TMEM14C 3'剪接位点误剪接可作为MDS早期诊断标志物。
1.方法
研究采用CRISPR/Cas9在人胚胎干细胞(ESC)中单等位基因引入SF3B1K700E突变构建杂合细胞系(MT),诱导ESC分化为造血祖细胞(HPC)后,对野生型(WT)和MT细胞进行RNA测序,使用SplAdder算法分析剪接事件,Western blot验证DVL2剪接变化;整合骨髓增生异常综合征(MDS)患者(GSE204845)、继发性急性髓系白血病(AML)患者(GSE205490)及健康供体(GSE180298)的公开单细胞数据,评估关键基因表达差异。
2.结果
MT ESC中突变与WT转录本比例为1:1,鉴定出1545个显著误剪接事件,主要表现为内含子保留减少及可变3'剪接位点使用(图1A、1B),提示SF3B1K700E促进原本被跳过的外显子使用。这些外显子可能含有弱3'ss,不利于WT SF3B1识别,但可被突变蛋白优先使用。研究鉴定出多个已报道的隐性3'ss事件,涉及红系分化基因(FOXRED1、TMEM14C、PPOX、STAU1)、RNA加工基因(THOC1)及经典靶点DVL2;功能富集显示误剪接基因高度富集于造血细胞类型特异性标志基因(图1C–E)。
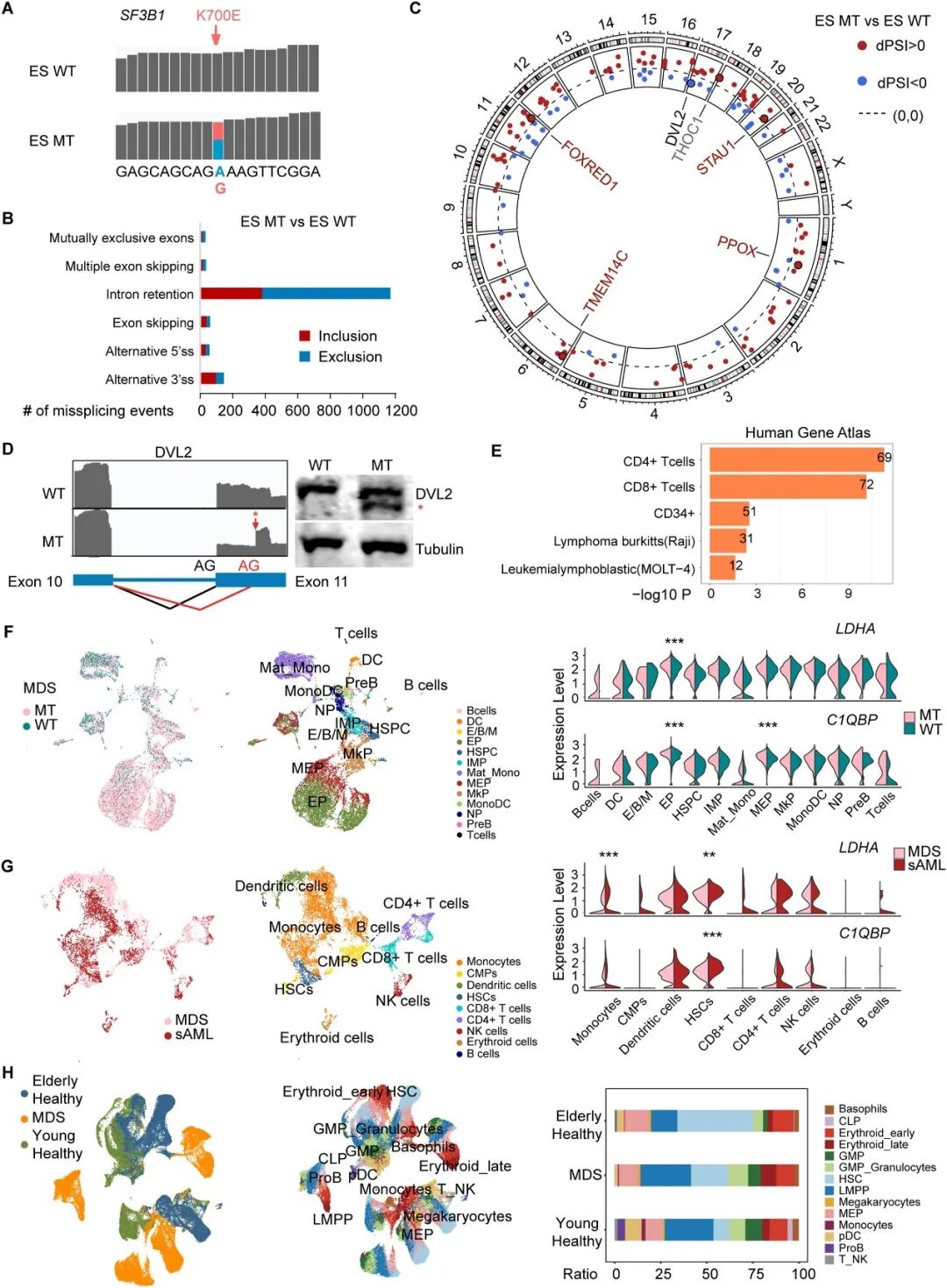
图1 SF3B1K700E突变诱导的转录失调事件与MDS和AML相关
单细胞数据验证显示,携带SF3B1K700E突变的MDS患者中LDHA和C1QBP在红系祖细胞表达升高,C1QBP在巨核-红系祖细胞也呈高表达;同一患者继发sAML后,两种基因在造血干细胞和单核细胞中表达升高(图1F、G)。比较年轻健康供体、老年健康供体和MDS患者的数据,发现红系晚期细胞与造血干细胞的比例变化显著(图1H),表明该突变导致MDS独特基因表达模式,与正常HPC明显不同。
3.结论
该研究建立人ESC/HPC平台模拟SF3B1K700E突变诱导的肿瘤转录失调,发现突变改变红白血病及剪接体动态相关关键基因的剪接和表达。TMEM14C的3'ss误剪接可作为MDS早期诊断标志物。HPC中的基因调控方向与MDS患者细胞相反,这种差异可能反映不同疾病阶段、微环境及病理状态下能量代谢机制的不同。在血液肿瘤早期阶段研究该突变,有助于开发针对性治疗策略。
文章来源
免费全文下载链接:
引用这篇文章:


