胸膜肿块考虑滑膜肉瘤等多种诊断方向,免疫组化结合ACTB-GLI1融合确诊GLI1基因改变的软组织肿瘤
时间:2026-05-05 17:37:18 热度:37.1℃ 作者:网络
GLI1基因改变的间叶源性肿瘤是极为罕见的间叶源性肿瘤,近期分子研究表明其发病与GLI1基因融合或扩增相关。本文报道 1 例 39 岁非吸烟女性患者,该患者因偶然检出右侧胸膜基底性肿块就诊,横断面成像显示其T5-T6水平存在椎旁胸膜病变,无椎管内延伸。电视辅助胸腔镜下切除术后可见肿瘤为双相型,二代测序证实存在ACTB-GLI1融合,据此确诊为GLI1基因改变的间叶源性肿瘤。经多学科讨论,患者选择接受影像学监测而非辅助治疗,随访 1 年时患者仍保持无病状态。本病例拓展了GLI1基因改变肿瘤的解剖学发生谱,同时凸显了分子检测在将该类肿瘤与其他胸膜肿瘤相鉴别时的应用价值。
背 景
GLI1基因改变的间叶源性肿瘤是近年被确认的一类由分子特征定义的软组织肿瘤,以GLI1基因融合或扩增为核心特征,最常见的融合伴侣基因包括ACTB、PTCH1或MALAT1。这类肿瘤形态学表现多样,常存在上皮和间叶双相分化,恶性潜能为中度。虽然已有报道显示GLI1基因改变的肿瘤解剖学分布范围较广,可发生于软组织、骨、胃肠道和女性生殖道,但胸腔受累十分罕见,以胸膜为原发部位的病例更是极为少见。截至目前,仅见累及肺实质或胸膜的散发病例被报道,且大多以单病例报道或小样本病例系列的形式发表(表1)。在此背景下,更多特征明确的胸腔发病病例对于完善该类肿瘤的诊断标准、为临床管理提供依据仍具有重要价值。本文报道 1 例携带ACTB-GLI1融合基因的胸膜起源GLI1基因改变间叶源性肿瘤,患者经手术治疗后采取主动监测随访。本病例凸显了GLI1融合肿瘤的诊断陷阱、分子关联特征以及靶向治疗领域的新兴临床考量。
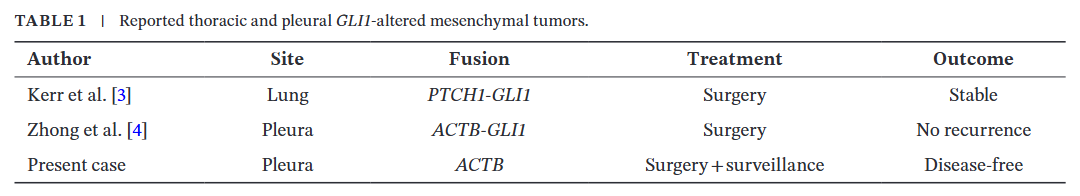
▲表1 已报道的胸腔和胸膜GLI1改变的间叶肿瘤
病 例
患者女,39 岁,无吸烟史,既往体健,在常规健康筛查中偶然发现右肺上叶阴影。胸片显示右肺上叶存在一大小为 3.0 cm的肿块,其余肺野清晰,心脏轮廓正常,提示需开展进一步评估(图1A)。
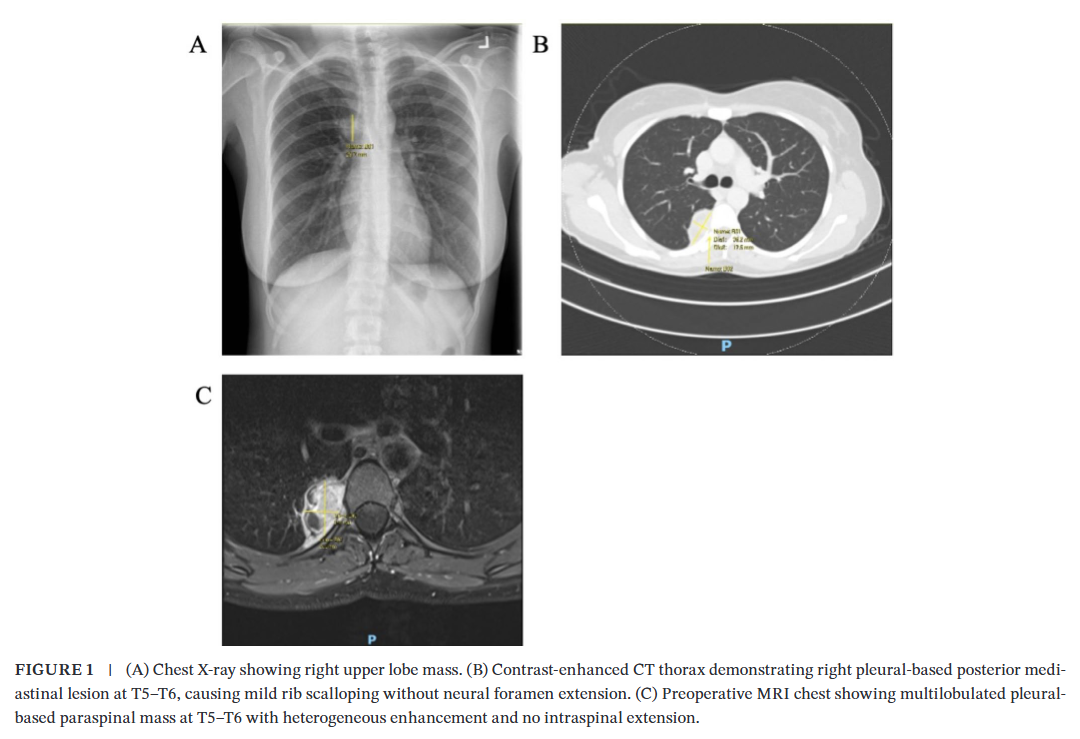
▲图1 影像学检查结果
胸部计算机断层扫描(CT)显示,T5-T6水平、沿右肺上叶后段及右肺下叶尖段分布的右侧胸膜基底性病变大小为 3.9×1.8 cm,呈不均匀强化。肿块导致轻度压迫性肺不张,右侧第 6 肋近肋椎关节处呈扇贝样压迹,无肋间隙增宽或神经孔侵犯,未见胸腔积液或纵隔淋巴结肿大(图1B)。胸部磁共振成像证实该分叶状胸膜起源椎旁肿块T2加权像呈混杂信号,增强后呈不均匀强化,大小为 3.3×2.9×1.9 cm,无椎管内延伸、神经孔受累或椎体信号异常(图1C)。患者接受电视辅助胸腔镜(VATS)肿块切除术,同时对邻近肺组织行楔形切除,术中可见一大小 3 cm、边界清晰的病变邻近交感干及奇静脉,与右肺下叶致密粘连。肿块大体检查显示肿瘤大小为 4×3.5×3 cm,肿瘤呈“推挤式”边界侵犯邻近肺组织(图2A),未受累的肺实质未见异常。镜下可见肿瘤部分有包膜,以软组织为中心生长,呈多结节状生长模式毗邻胸膜;肿瘤呈双相形态,间叶成分包括透明变性区域以及形成短束状排列的梭形细胞区域(图2B);上皮样成分由巢状和梁状排列的形态相对单一的细胞组成,细胞核呈圆形至卵圆形,胞质中等量,嗜酸性至透亮,周围伴纤细的毛细血管网(图2C)。核分裂象计数低,约为 2 个/10 高倍视野,未见高级别细胞异型性或坏死,肿瘤毗邻软组织切缘。
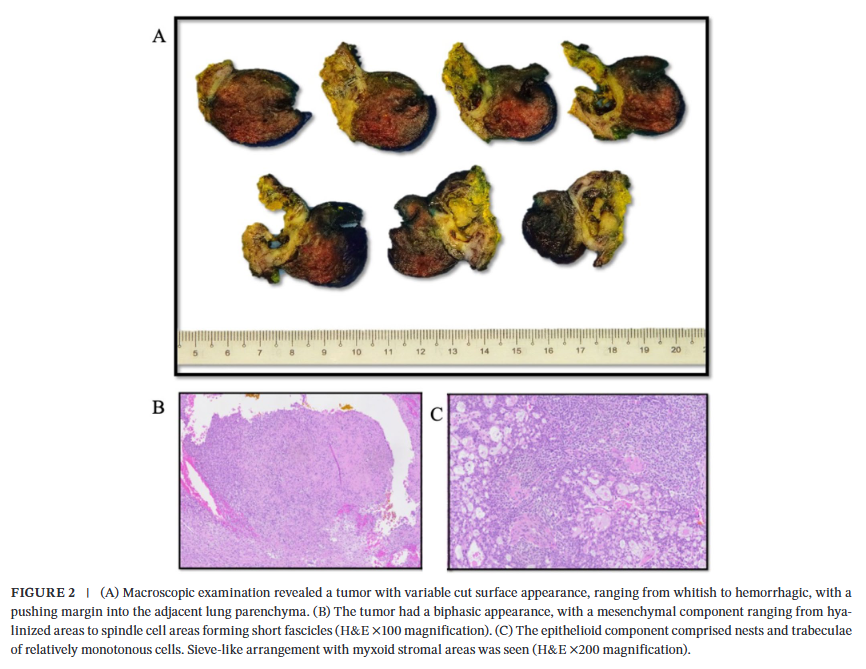
▲图2 组织学检查结果
鉴于该疾病实体罕见且诊断复杂,作为美国波士顿布莱根妇女医院外部专家会诊的一部分,研究人员开展了GLI1免疫组织化学检测以支持疑似诊断。免疫染色显示,肿瘤细胞GLI1和S100蛋白呈强阳性,SOX10呈阴性;CD56在上皮样和梭形细胞成分中均呈弥漫阳性;上皮样成分广谱细胞角蛋白AE1/AE3、CK19呈阳性,TTF-1呈弱阳性;Ki67增殖指数较低,热点区域约为 5%-10%;神经内分泌标志物及包括SMA在内的肌源性标志物均为阴性;MelanA、HMB45等黑色素细胞标志物也呈阴性。本次外部免疫组化分析的代表性图片无法纳入本文。鉴于肿瘤呈双相形态且位于胸腔胸膜部位,最初研究人员考虑了数种诊断方向:由于存在上皮和梭形细胞成分,考虑滑膜肉瘤,但SS18重排阴性、梭形细胞群无弥漫性细胞角蛋白表达,不支持该诊断;肉瘤样间皮瘤因钙视网膜蛋白、WT1、D2-40表达阴性,且肿瘤呈边界清晰的生长模式、无弥漫性胸膜受累,故予以排除;因肿瘤位于胸膜部位曾考虑孤立性纤维性肿瘤,但STAT6免疫染色呈阴性,且不存在该肿瘤特征性的无序排列结构,故排除;包括恶性外周神经鞘膜瘤在内的外周神经鞘肿瘤,因SOX10表达阴性、组织学呈低级别特征,也予以排除。双相形态、GLI1免疫反应强阳性、免疫表型支持,联合二代测序检出ACTB-GLI1融合的特征,共同确立了GLI1基因改变的间叶源性肿瘤的诊断。二代测序检出ACTB(1号外显子):GLI1(6号外显子)基因融合(图3),进一步证实了该诊断。布莱根妇女医院的专家会诊也同意该诊断结论,同时强调该肿瘤的恶性潜能尚不明确。
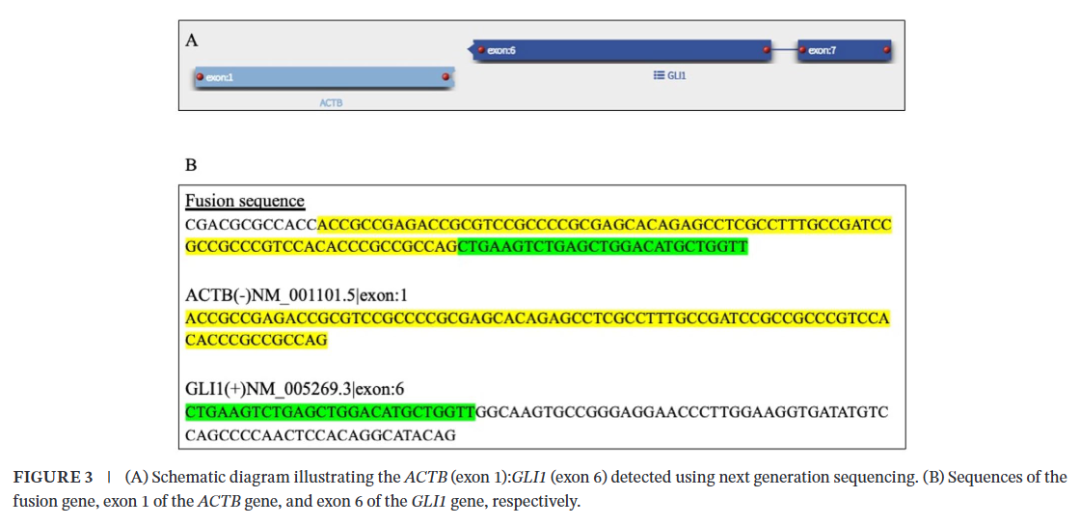
▲图3 NGS检测结果
该病例在肉瘤多学科肿瘤讨论会上进行了研讨,鉴于存在软组织近切缘但无转移征象,可考虑行辅助放疗。经详细病情告知与沟通后,患者选择接受密切影像学监测。术后 1 年正电子发射断层显像/CT(PET-CT)检查未见肿瘤复发或转移,患者在后续随访中仍保持良好临床状态。
讨 论
GLI1基因改变的间叶源性肿瘤是近年被识别的一类间叶源性肿瘤亚型,特征为Hedgehog(HH)通路异常激活。这类肿瘤的胸腔受累十分罕见,已报道的胸腔发病病例包括起源于肺实质、纵隔的肿瘤,其中以胸膜为起源的病例最为罕见。ACTB-GLI1融合可导致不依赖SMO或PTCH1信号的GLI1转录本组成性上调,驱动间叶分化。近年的综述研究指出,这类肿瘤解剖学分布广泛、上皮分化程度不一,生物学行为总体呈惰性至中度恶性,不过也有局部复发和罕见转移的相关报道。近期一项针对胸膜起源GLI1基因改变肿瘤的综述指出,这类肿瘤多表现为边界清晰的肿块,影像学和组织学表现常与更常见的胸膜肿瘤相似。本病例与上述特征相符,进一步扩充了为数不多但不断增加的胸腔发病病例库,凸显了分子检测确诊的重要性。近年GLI1激活的生物学意义引发了治疗层面的关注,Hedgehog通路抑制剂(HHI)包括维莫德吉(vismodegib)和索尼德吉(sonidegib),已获批用于以配体依赖型SMO激活为主要特征的基底细胞癌的治疗。但GLI1融合蛋白作用于SMO下游,因此这类药物很难抑制GLI1介导的转录过程。直接GLI1抑制剂如GANT61、Glabrescione B及相关化合物已在临床前研究中被证实可抑制GLI1与DNA结合,但目前仍处于研究阶段。目前尚无专门针对ACTB-GLI1融合蛋白或其他GLI1融合蛋白的临床试验。仅有 1 例病例报道显示,PTCH1-GLI1融合阳性的卵巢肿瘤患者经验性使用帕唑帕尼(pazopanib)治疗后获得了长期病情稳定,但该效应可能来源于药物的非特异性抗血管生成作用,而非通路抑制作用。由于目前尚无经证实的系统性治疗方案,完整手术切除仍是首选治疗手段,对于无不良组织学特征的局限性病变,主动监测是适宜的处理策略。对于复发或转移性病例,可考虑转诊至有早期篮子临床试验或分子肿瘤委员会的中心就诊。准确记录ACTB-GLI1融合变异型有助于患者符合未来研究及协作研究的入组条件。本病例进一步扩充了为数不多的胸膜起源GLI1基因改变肿瘤的病例库,凸显了整合组织病理学、免疫组化及分子谱分析在鉴别该类肿瘤与滑膜肉瘤、间皮瘤等形态学类似疾病中的诊断价值。
本文报道了一例罕见的携带ACTB-GLI1融合的胸膜起源GLI1基因改变软组织肿瘤,患者经胸腔镜切除及监测随访后预后良好。识别该疾病实体可避免诊断分类错误及过度治疗。尽管GLI1融合是潜在可靶向的驱动变异,但目前尚无经验证的治疗方案,这凸显了开展进一步转化研究、将这类病例纳入罕见肿瘤登记库的必要性。
参考文献:
M.Lizwan, L.Xiao, C. Y.Chow, H. Y.Lau, and B.-H.Ong, “Pleural-Based GLI1-Altered Mesenchymal Tumor With ACTB-GLI1 Fusion: A Rare Pulmonary Entity Mimicking Synovial Sarcoma,” Thoracic Cancer17, no. 7 (2026): e70271, https://doi.org/10.1111/1759-7714.70271.


