专家论坛|隋建华 李文辉:丁型肝炎病毒治疗药物的研究进展
时间:2026-05-05 13:04:53 热度:37.1℃ 作者:网络
病毒性肝炎中,丁型肝炎病毒(HDV)与乙型肝炎病毒(HBV)合并感染是最为严重的类型。相比于HBV单一感染,HDV/HBV合并感染会加快肝纤维化、肝硬化进程,在5~10年内可导致50%~60%的患者发展为肝硬化,并显著增加肝功能失代偿和肝脏相关死亡风险。据世界卫生组织估计,全球约1 200万的慢性HBV感染者合并HDV感染,其疾病负担可能被低估。然而,针对HDV感染的治疗选择极其有限,抗HBV药物核苷(酸)类似物[NA]对HDV感染无直接抑制作用;聚乙二醇干扰素-α(PEG-IFN-α)虽常被用于HDV感染的治疗,但其临床应答率欠佳、不良反应显著且病毒学复发率高。因此,开发抗HDV感染药物已成为当前亟待满足的临床需求。近年来,随着对HDV研究的不断深入,多个新型抗HDV靶标及相关抑制剂被陆续发现,HDV感染的治疗已逐步进入以特异、高效、安全为特点的新时期。本文旨在系统梳理HDV治疗新药领域的基础研究和临床研发进展,以期为临床医生和新药研究人员提供参考。
1病原学
HDV是一种缺陷型RNA病毒,其感染肝细胞及完成病毒颗粒组装与释放的过程均依赖于HBV的包膜蛋白。因此,HDV感染仅发生在合并HBV感染的情况下。HDV是目前已知能够感染人类的最小病毒,其基因组自身仅编码1种蛋白质——丁型肝炎病毒抗原(HDAg)。病毒颗粒内部由HDAg和RNA基因组共同组成核糖核蛋白(RNP)复合体;病毒颗粒外层由HBV的3种包膜蛋白[HBV表面抗原大蛋白(L-HBsAg)、HBV表面抗原中蛋白(M-HBsAg)和HBV表面抗原小蛋白(S-HBsAg)]组成。HDV首先通过硫酸乙酰肝素蛋白聚糖黏附于肝细胞表面,然后通过病毒L-HBsAg包膜蛋白上的HBV前S1抗原(PreS1)结构域与HBV的共同受体钠离子牛磺胆酸共转运蛋白(NTCP)特异性结合,从而介导病毒进入肝细胞。进入宿主细胞后,HDV在肝细胞核内利用宿主RNA聚合酶Ⅱ,以滚环复制方式完成RNA基因组的复制,并产生小HDAg(S-HDAg)或大HDAg(L-HDAg)调控病毒复制,二者与RNA基因组结合形成新的RNP复合体。最终,RNP被转运至细胞质,经宿主细胞法尼基转移酶异戊二烯化修饰的L-HDAg与乙型肝炎表面抗原(HBsAg)发生相互作用,被HBV的3种包膜蛋白包裹,组装成具有感染性的成熟HDV病毒颗粒,释放至细胞外。目前,HDV感染的致病机制尚未完全阐明。现有证据表明,HDV本身对感染肝细胞无直接的细胞病变效应,HDV感染所致的肝损伤可能是由病毒感染引起的免疫应答和炎症所介导。其典型的组织病理学特征主要表现为肝细胞坏死和炎症细胞的浸润,且肝内炎症活动水平与HDV复制程度密切相关。研究证实,持续的HDV病毒血症是与肝硬化进展以及病死率相关的独立危险因素。
由于HDV的复制高度依赖HBV及宿主肝细胞相关因子,因此缺乏直接针对HDV自身的有效药物作用靶点。目前,针对HDV的新型治疗策略主要围绕以下破坏其病毒生命周期的环节展开,包括阻断病毒进入肝细胞的通路、抑制HBsAg的表达,以及阻止病毒颗粒的组装和释放(图1)。
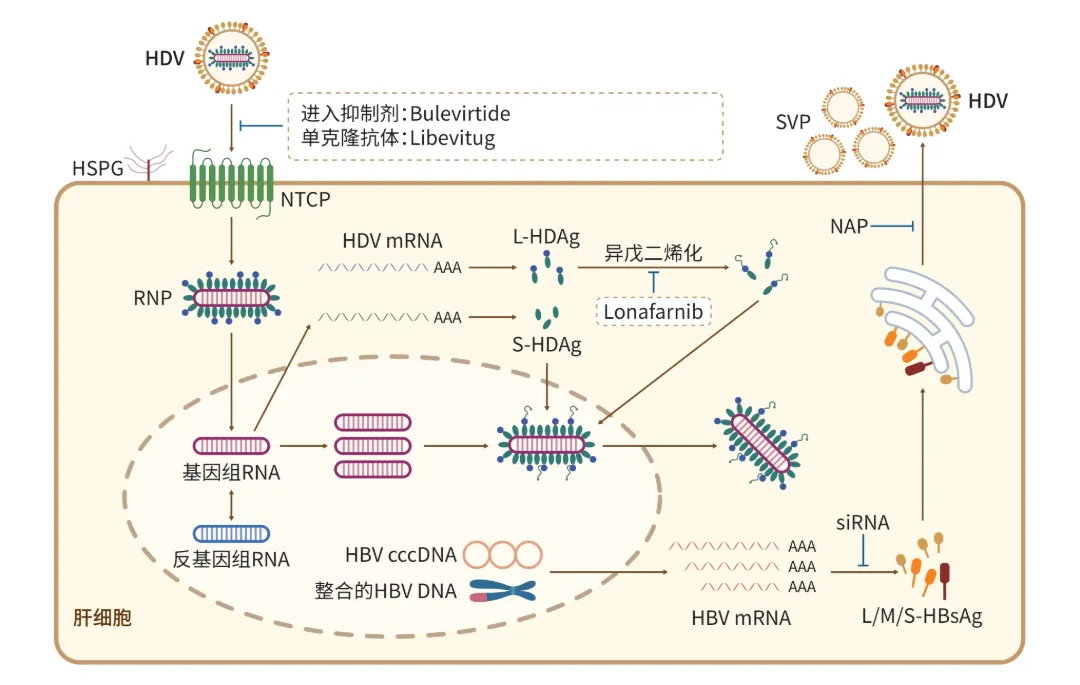
注: HBV,乙型肝炎病毒;RNP,核糖核蛋白;NTCP,钠离子牛磺胆酸共转运蛋白;HDV,丁型肝炎病毒;HSPG,硫酸肝素蛋白聚糖;NAP,核酸聚合物;L-HDAg,大丁型肝炎病毒δ抗原;S-HDAg,小丁型肝炎病毒δ抗原;L/M/S-HBsAg,乙型肝炎表面抗原大/中/小蛋白;mRNA,信使RNA;siRNA,小干扰RNA;Bulevirtide,布来韦肽;Libevitug,立贝韦塔单抗;Tobevibart,托韦拜单抗;SVP,亚病毒颗粒。
图1 HDV生活史及药物靶点
2HDV感染治疗的目标和终点
HDV感染治疗的目标为减缓肝脏疾病进展,最大限度降低肝硬化、肝功能失代偿、肝细胞癌及肝脏相关死亡的发生风险,同时改善患者的长期生活质量。驱动慢性丁型肝炎疾病进展的主要因素是肝脏中HDV的持续复制,其水平与不良临床结局密切相关。在慢性病毒性肝炎中,丙氨酸氨基转移酶(ALT)是肝细胞坏死和炎症活动的直接生化标志,其水平持续升高提示肝病进展风险显著增加,而其复常则意味着疾病进展风险降低。因而,外周血HDV RNA水平下降且ALT复常,可作为预测临床长期获益的指标。目前,在慢性HDV感染治疗药物的临床试验中,这一复合终点常被作为评估药物疗效的替代终点。对于以长期治疗抑制病毒为目标的治疗方案,以治疗期间HDV RNA检测不到或HDV RNA下降≥2 log10 IU/mL,且ALT复常作为疗效替代终点;而对于有限疗程治疗方案,则以治疗结束后6个月时HDV RNA持续检测不到作为主要疗效终点。尽管上述研究终点在临床实践中尚缺乏充分或完整的验证,但仍可合理用于慢性HDV感染患者的临床管理。
3HDV抗病毒治疗药物
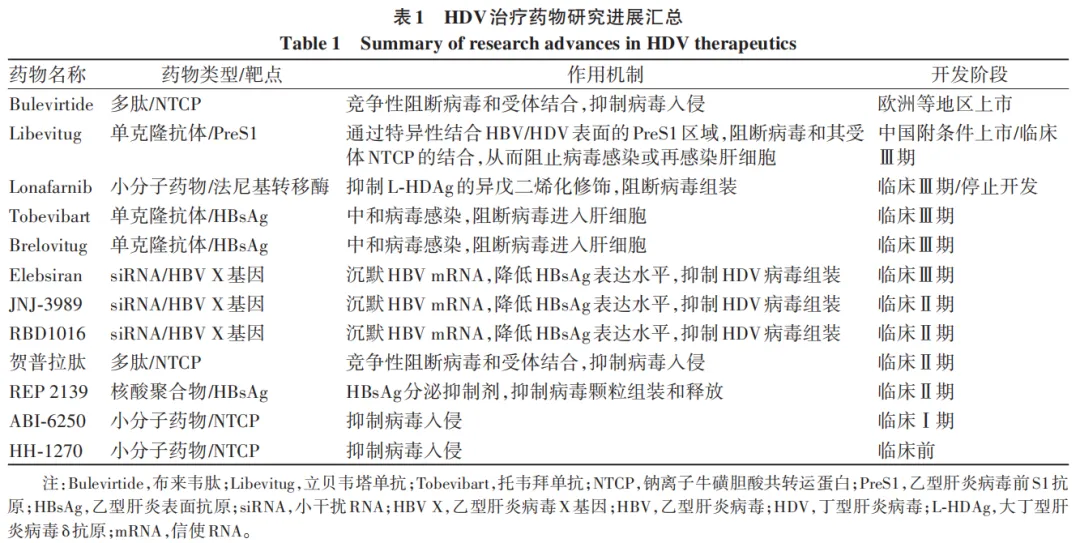
近年来,靶向HDV生命周期的特异性抗病毒药物研发进展迅速。其中,靶向病毒入侵阶段的病毒进入抑制剂布来韦肽(BLV)和单克隆抗体药物立贝韦塔单抗(HH-003)已获得上市批准,另有多种药物处在临床前和临床试验阶段(表1)。
3.1 靶向NTCP的进入抑制剂
BLV是一种由HBV大包膜蛋白PreS1结构域N端的47个氨基酸组成的豆蔻酰化合成脂肽,可通过结合肝细胞表面受体NTCP,竞争性阻断HDV/HBV进入肝细胞。BLV(2 mg)于2023年获得欧盟药品管理局的上市批准,但其尚未在中国和美国获批上市。2023年《欧洲肝病学会丁型肝炎临床实践指南》建议,伴有代偿期肝病的慢性HDV感染者均应考虑接受BLV长期治疗(建议剂量2 mg/d),但最佳剂量和疗程尚未明确。在BLV单药治疗慢性HDV感染者临床Ⅲ期(MYR 301)研究中,患者的基线HDV RNA为5.0 log10 IU/mL,接受每日皮下注射2 mg或10 mg BLV单药治疗48周,HDV RNA病毒学及ALT生化学的复合应答率分别为45%和48%,显著高于未接受治疗的延迟治疗组(2%)。延长治疗至144周,复合应答率进一步提高至57%和54%,其中HDV RNA检测不到的比例分别为29%和50%。经144周治疗停药随访96周时,分别有20%和22%的患者维持了HDV RNA检测不到的水平。另外,多项真实世界研究表明,长期使用2 mg BLV单药治疗可使50%以上的HDV患者实现病毒学与ALT生化学复合应答,并伴随肝组织学改善。既往研究表明,PEG-IFN-α单药或联合NA治疗48周后的持续HDV RNA病毒学应答率(定义为治疗后6个月HDV RNA水平检测不到)为25%~30%,其中50%的应答者在治疗结束后5年发生病毒学复发。在BLV联合PEG-IFN-α治疗的临床研究(MYR 204)中,经48周BLV(10 mg)联合PEG-IFN-α治疗,停药后24周HDV RNA检测不到的病毒学应答率为46%。BLV在已报道的临床研究中总体安全性和耐受性良好,主要不良反应包括血清总胆汁酸水平升高、注射部位反应、头痛及瘙痒。值得注意的是,BLV与NTCP结合可阻断胆汁酸转运,也可造成其他后果,其临床应用的风险获益比仍需更多的临床研究进一步验证。在使用BLV治疗慢性HDV感染患者时,应考虑潜在的药物相互作用,尤其避免与NTCP转运有关的药物联合使用。
此外,一种类似于BLV的合成多肽类药物贺普拉肽,目前正处于临床试验阶段。近年来,多种新型高活性、可口服的小分子NTCP抑制剂已进入或即将进入临床试验阶段。ABI-6250是一种具有高抑制活性的进入抑制剂,目前已进入临床Ⅰ期阶段;HH-1270是一种基于天然胆汁酸结构衍生设计的靶向NTCP进入抑制剂,临床前研究表明其能够有效阻断NTCP人源化小鼠模型的HDV感染,且安全性良好。
3.2 单克隆抗体药物
利用人单克隆抗体药物阻断HDV侵入肝细胞是治疗HDV感染的有效策略。HDV需要借助HBV包膜蛋白作为其外膜蛋白进入肝细胞进行复制,L-HBsAg PreS1区域的1~47氨基酸部分主要负责HBV和HDV特异性结合受体NTCP,介导病毒入侵肝细胞,阻断PreS1和NTCP的结合能够有效阻断病毒感染。此外,HBV包膜蛋白(L-HBsAg、M-HBsAg和S-HBsAg)共有的S结构域参与病毒与肝细胞的非特异黏附,干预这一过程也可以阻断病毒感染。
3.2.1 靶向PreS1的单克隆抗体药物
立贝韦塔单抗是全球首款靶向L-HBsAg PreS1区域的全人源单克隆抗体药物。其主要作用机制为通过特异性结合HBV/HDV表面的PreS1区域,阻断病毒和其受体NTCP的结合,从而阻止病毒感染或再感染肝细胞。立贝韦塔单抗已相继获得国家药品监督管理局及美国食品药品监督管理局授予的“突破性疗法”认定,并于2026年1月获得国家药品监督管理局附条件批准上市,用于治疗慢性HDV感染。在一项临床Ⅱ期概念性验证研究(HH003-201)中,9例HBV/HDV合并感染者接受每2周1次20 mg/kg的立贝韦塔单抗单药静脉输注,持续24周。结果显示,治疗24周时HDV RNA病毒学应答率为77.8%,病毒学与ALT生化学复合应答率达60%;停药随访24周后,上述应答率仍分别维持在66.7%和40%,且整体安全性良好。另一项国际多中心、随机、对照和开放标签关键临床Ⅱb期研究(HH003-204)共纳入100例慢性HDV感染者,按2∶2∶1比例随机分配至立贝韦塔单抗10 mg/kg组、立贝韦塔单抗20 mg/kg组和对照组,所有患者均接受富马酸丙酚替诺福韦的背景治疗。其中94例基线ALT异常的慢性HDV感染者的基线HDV RNA为6.1 log10 IU/mL。治疗24周后,立贝韦塔单抗10 mg/kg组和20 mg/kg组HDV RNA病毒学应答率分别为35.5%和42.5%,ALT复常率为58.8%和77.5%,病毒学和ALT的复合应答率分别为32.4%和35%。治疗48周后,HDV RNA病毒学应答率分别提高至50.0%和60.0%,ALT复常率为55.9%和70%,复合应答率分别提高至44.1%和42.5%。3项指标的应答率均显著优于对照组。此外,基线异常患者的肝硬度显著改善。立贝韦塔单抗治疗的耐受性和安全性良好,主要不良反应有头痛、乏力和瘙痒。
3.2.2 靶向HBsAg的单克隆抗体药物
Tobevibart(Vir-3434)和Brelovitug(BJT-778)均为靶向HBsAg的单克隆中和抗体,通过中和病毒感染和阻断病毒进入肝细胞发挥抗病毒作用,并可结合亚病毒颗粒(SVP)中的HBsAg。一项正在进行中的SOLSTICE临床Ⅱ期研究中,33例慢性HDV感染者接受300 mg每2周1次皮下注射Tobevibart的单药治疗,治疗至24周时,病毒学应答率为82%,ALT复常率为76%,70%患者达到病毒学和ALT生化学复合应答。治疗至48周时,HDV RNA检测不到的比例为48%,ALT复常率为61%,复合应答率为61%。而联合靶向HBV RNA的小干扰RNA(siRNA)药物Elebsiran(VIR-2218)后,32例慢性HDV感染者接受300 mg Tobevibart联合200 mg Elebsiran每4周1次皮下注射,治疗24周时病毒学应答率、ALT复常率和复合应答率分别为47%、100%和47%。治疗48周时,HDV RNA检测不到的比例、ALT复常率和复合应答率分别为56%、66%和56%。联合治疗组虽然在实现HDV RNA检测不到的应答率方面更具优势,但在ALT复常率方面的疗效不及单药治疗组。Tobevibart单药或联合治疗期间不良事件发生率分别为94%和81%,主要表现为流感样症状与寒战。在Brelovitug单药治疗慢性HDV感染者的临床Ⅱ期研究中,18例患者接受300 mg Brelovitug每周1次皮下注射,治疗24周时,67%的患者达到病毒学和ALT的复合应答,至第48周时,复合应答率为65%(11/17),病毒学应答率为100%,ALT复常率为65%,44%患者HDV RNA检测不到。目前,Tobevibart联合Elebsiran方案和Brelovitug均已进入HDV感染患者的Ⅲ期临床研究阶段。
在HDV感染者外周血中,除具有感染性的完整病毒颗粒外,还存在大量主要由HBsAg组成的SVP和不具有感染性的病毒样颗粒,其水平远高于具有感染性的病毒颗粒。在具有感染性的HDV病毒包膜蛋白中,不同形式HBsAg的分布比例存在显著差异:S-HBsAg约占95%;M-HBsAg约占5%;而含有PreS1结构域,对病毒进入肝细胞至关重要的L-HBsAg仅占约1%。靶向PreS1的单抗特异性识别结合的PreS1结构域,是L-HBsAg包膜蛋白的一个特定结构域,主要存在于具有感染性的HDV/HBV病毒颗粒,而在非感染性的SVP上仅少量存在。通过选择性识别PreS1结构域,抗PreS1抗体可最大程度减少抗体-抗原复合物过度形成,从而尽可能地降低免疫复合物相关风险。该类风险在抗HBsAg单抗中值得关注,因其能结合血液中大量存在的以HBsAg为主的SVP。
3.3 靶向HDV其他生命周期的在研药物
Lonafarnib(LNF)是一种抑制宿主细胞法尼基转移酶的小分子药物,通过抑制HDV组装过程中L-HDAg的异戊二烯化,阻断HDV病毒组装。在一项多中心、随机、Ⅲ期临床试验D-LIVR中,研究人员评估了50 mg LNF联合100 mg利托那韦(2次/d)方案(含或不含PEG-IFN-α)治疗48周的疗效与安全性。结果显示,LNF+利托那韦组和LNF+利托那韦+PEG-IFN-α组在治疗48周时达到的病毒学和ALT复合应答比例分别为10.1%(18/178)和19.2%(24/125),显著高于安慰剂组的1.9%(1/52),并且患者肝组织学得到显著改善。但公开资料显示,该药物已停止研发。
siRNA为双链RNA序列,通过沉默HBV mRNA降低HBV包膜蛋白表达水平,抑制HDV病毒组装。目前处于HDV临床阶段的siRNA包括Elebsiran、JNJ-3989和RBD1016,三者均靶向HBV基因组各转录本共有的X基因区段。如前所述,Elebsiran与单抗药物Tobevibart联合用于治疗HDV感染。在JNJ-3989的概念验证研究(REEF-D)中,27例接受NA治疗的HDV/HBV感染受试者接受JNJ-3989治疗48周时,11例患者达到病毒学和ALT生化学的复合应答,14例患者获得病毒学应答,但基线HBsAg高水平患者在治疗期间均出现ALT异常升高。RBD1016于近期获得欧盟药品管理局授予孤儿药资格认定,用于治疗HDV感染。
REP 2139是一种核酸聚合物,可选择性抑制HBsAg的组装和分泌。在临床Ⅱ期REP 301研究中,12例慢性HBV/HDV共感染者先接受每周500 mg REP 2139-Ca静脉给药治疗15周,随后改为每周250 mg REP 2139-Ca联合PEG-IFN-α治疗15周,最后单用PEG-IFN-α治疗33周。治疗结束时,50%的患者实现HBsAg清除,其中5例在1年随访时仍维持阴性;治疗期间11例患者达到HDV RNA检测不到,7例在1年随访时仍维持检测不到。长期随访REP 301-LTF研究对11例患者进行了3.5年监测,其中7例维持HDV RNA检测不到和生化应答,4例实现HBV DNA检测不到和HBsAg清除。尽管目前显示的临床数据良好,但仍需更多临床数据来进一步验证REP 2139的疗效和安全性。
4讨论与展望
近年来,随着对HDV生命周期的深入认识,新型HDV治疗候选药物持续涌现。目前,多种抗HDV新药已进入临床试验阶段,尤其在靶向病毒进入环节的药物研发方面取得突破性进展,通过阻断HDV与NTCP受体结合的药物BLV和立贝韦塔单抗先后获批上市,为治疗丁型肝炎这一严重危害人类健康的疾病提供了崭新的治疗选择。尽管上述新型治疗药物在疗效和安全性方面展现出显著优势,但仍面临若干值得关注的事项。NTCP是重要的肝脏胆汁酸盐转运体,直接靶向NTCP的抑制剂(如BLV)会影响胆汁酸代谢,且BLV存在较为广泛的药物相互作用(涉及至少29种联用药物),在临床应用中需予以重视。目前,包括BLV、立贝韦塔单抗以及处于临床试验阶段的其他单药或联合治疗方案,多以长期治疗抑制病毒为目标。然而,在临床实践中,其具体疗程、停药标准、病毒复发风险、长期安全性特征、长期临床结局及耐药性发生情况等尚不完全明确,仍有待进一步研究加以阐明。未来,随着相关研究的持续推进,将有助于优化HDV感染的整体治疗策略,为个体化选择单药或联合方案提供循证依据,并有望推动丁型肝炎这一最为严重的慢性病毒性肝炎,转变为在有限疗程内可实现大部分患者临床治愈的疾病。
全文下载
https://www.lcgdbzz.org/cn/article/doi/10.12449/JCp60205


