mRNA疫苗,最新Nature Biotechnology!
时间:2026-05-05 17:16:01 热度:37.1℃ 作者:网络
信使RNA疫苗作为新一代药物形态,能够在体内短暂表达包括病毒抗原和肿瘤抗原在内的多种蛋白质。然而,mRNA脂质纳米颗粒在体内会转染多种细胞类型,包括肝细胞、肌细胞和树突状细胞等专业抗原呈递细胞。长期以来,科学界认为mRNA疫苗诱导免疫应答的关键在于抗原需要在树突状细胞等专业抗原呈递细胞中直接表达。但不同细胞类型对mRNA疫苗免疫效果的影响究竟如何,一直是一个未解之谜。这一认知空白限制了mRNA疫苗的优化设计,也影响了mRNA疗法在需要避免免疫反应的场景中的应用。
为了揭开这一谜题,西奈山伊坎医学院Brian D. Brown团队通过在人造mRNA中引入特定的microRNA靶点序列,实现了在特定细胞类型中选择性沉默mRNA表达的技术突破。研究发现,mRNA在专业抗原呈递细胞中的表达对于启动抗原特异性T细胞应答并非必需;相反,肌细胞中的mRNA表达能够诱导相当甚至更强的免疫反应。更为重要的是,肝细胞中的mRNA表达会通过PD1/PDL1通路部分抑制抗原特异性T细胞应答。在携带表达肿瘤相关抗原的淋巴瘤细胞的小鼠模型中,通过miRNA介导的肝细胞沉默策略,肿瘤抗原mRNA疫苗显著增强了免疫应答并减少了肿瘤负荷。相关成果以“mRNA vaccine immunity is enhanced by hepatocyte detargeting and not dependent on dendritic cell expression”为题发表在《Nature Biotechnology》上。

研究团队首先验证了miRNA靶点序列对mRNA表达的调控效果。实验表明,在编码绿色荧光蛋白的mRNA中引入四个拷贝的miR-122靶点序列后,肝细胞中的绿色荧光蛋白表达被抑制了95%以上,且这种沉默效果不受mRNA修饰碱基的影响。更重要的是,这种沉默具有惊人的细胞特异性——在同样注射了含miR-122靶点序列的mRNA的小鼠肝脏中,肝细胞几乎检测不到绿色荧光蛋白表达,但肝脏中的巨噬细胞和内皮细胞依然保持绿色荧光蛋白阳性。与此形成鲜明对比的是,通过引入miR-142靶点序列,研究人员能够在巨噬细胞、树突状细胞、单核细胞等免疫细胞中实现mRNA的完全沉默,且不影响mRNA的先天免疫激活特性。
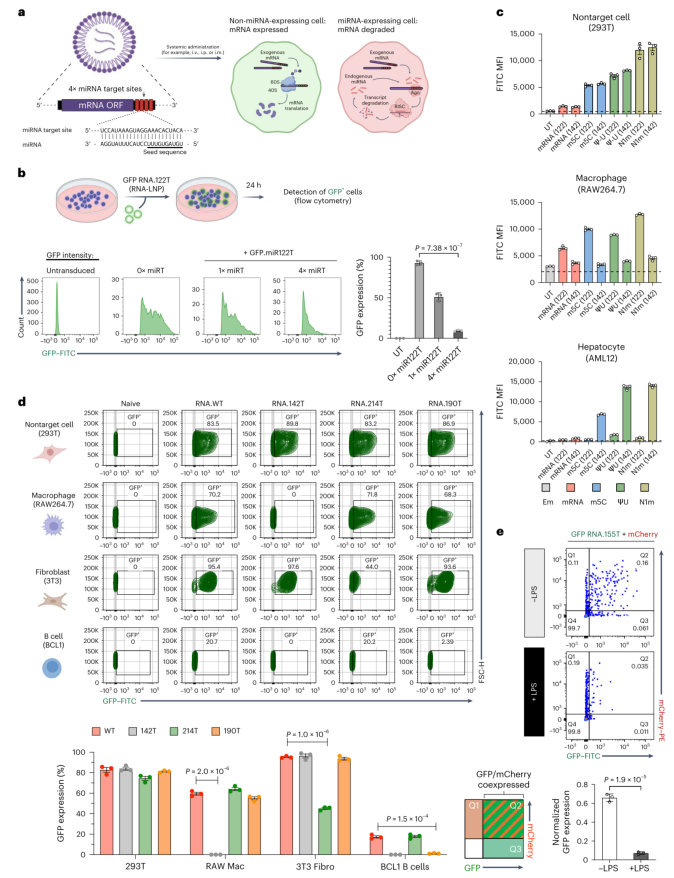
图1 | 利用miRNA对mRNA-LNP进行细胞类型特异性编程。 a, 示意图展示了miRNA介导的mRNA表达调控机制。将miRNA互补靶点序列整合到mRNA的3‘非翻译区后,如果mRNA进入表达相应miRNA的细胞,miRNA会结合并导致mRNA降解,从而阻止蛋白翻译;在不表达该miRNA的细胞中,mRNA正常翻译产生蛋白。b, 不同数量miR-122靶点序列对AML12肝细胞中GFP表达的影响。数据显示,单个122T使GFP阳性细胞减少约50%,而四个拷贝的122T导致GFP表达降低95%以上。c, 不同核苷酸修饰条件下,miRT对293T细胞(不表达靶miRNA)、AML12细胞(表达miR-122)和BCL1B细胞(表达miR-142)中GFP表达的影响。结果表明,无论是否使用修饰核苷酸,miRT都能实现细胞类型特异性沉默。d, 在不同细胞系中测试miR-214、miR-190b靶点序列的沉默效果。数据显示,RNA.214T在NIpT3成纤维细胞中特异性沉默GFP表达,RNA.190T在BCL1B B细胞中实现特异性沉默。e, 原代骨髓来源巨噬细胞中miR-155靶点序列的沉默效果。LPS激活的巨噬细胞中,RNA.155T的GFP表达相对于野生型降低了4倍以上。
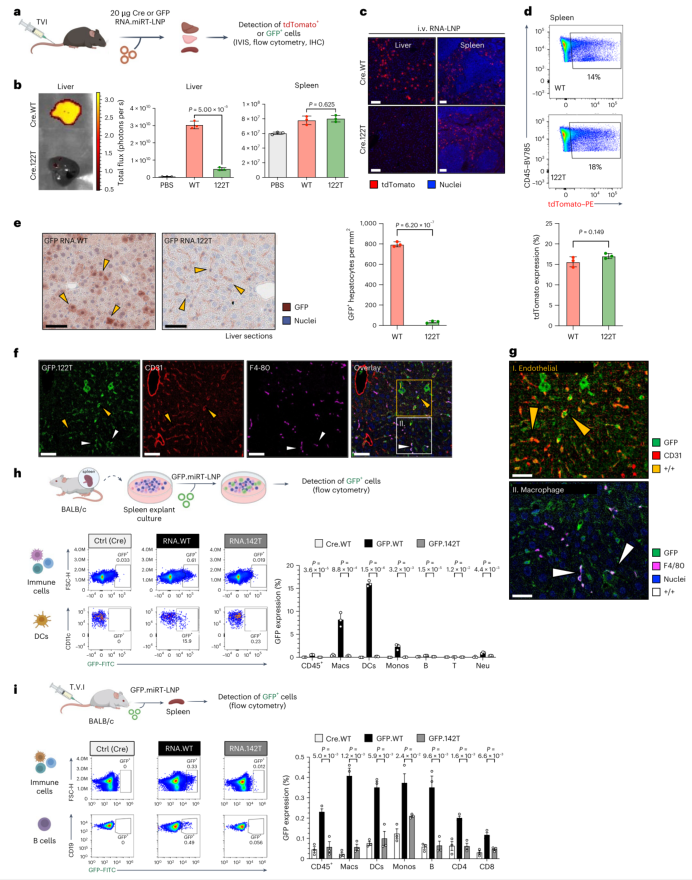
图2 | 利用miRT在体内实现细胞类型特异性mRNA沉默。 a, 使用Cre-LoxP报告系统验证miRNA介导的mRNA沉默示意图。b, Ai14小鼠注射Cre RNA.WT或Cre RNA.122T后肝脏和脾脏的离体荧光成像。结果显示RNA.122T组肝脏tdTomato信号显著降低。c, 肝脏中tdTomato阳性细胞的定量分析。RNA.122T组肝细胞中tdTomato阳性细胞大幅减少,但间质细胞(包括枯否细胞和内皮细胞)仍为tdTomato阳性。d, 脾脏中tdTomato阳性细胞的定量分析,两组无显著差异。e, 注射GFP RNA.WT或RNA.122T后小鼠肝脏切片的免疫组化染色与定量分析。RNA.122T组GFP阳性肝细胞从每平方毫米约800个降至20个以下。f-g, 肝脏免疫荧光染色显示RNA.122T组中GFP阳性细胞为内皮细胞(CD31阳性)和肝巨噬细胞(F4/80阳性),而非肝细胞。h, 脾脏单细胞悬液离体转染GFP RNA.WT或RNA.142T后的流式细胞术分析。RNA.142T组巨噬细胞、树突状细胞和单核细胞中检测不到GFP表达。i, 小鼠静脉注射GFP RNA.WT或RNA.142T 24小时后脾脏的流式细胞术分析。RNA.142T组所有造血细胞类型均检测不到GFP表达。
值得注意的是,令人意想不到的是,研究发现在树突状细胞中沉默mRNA表达并未削弱疫苗的免疫效果。 无论是编码绿色荧光蛋白、新冠病毒刺突蛋白还是卵清蛋白的mRNA疫苗,当mRNA在专业抗原呈递细胞中被完全沉默后,小鼠依然产生了强烈的抗原特异性CD8阳性T细胞应答和抗体反应。通过骨髓移植实验,研究人员发现树突状细胞和巨噬细胞能够从被转染的非造血细胞获得抗原——在注射了Cre重组酶mRNA的小鼠肝脏中,约10-20%的树突状细胞和巨噬细胞表达报告基因tdTomato,这意味着这些专业抗原呈递细胞是通过交叉呈递或交叉装扮的方式获取抗原,而非自身直接表达mRNA。
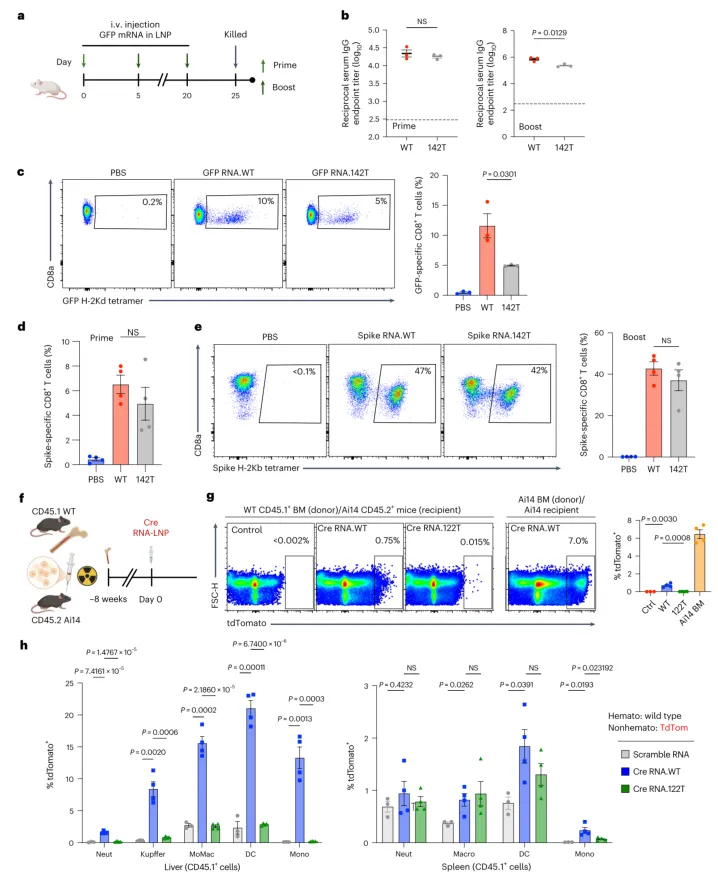
图3 | 造血细胞中mRNA沉默不影响抗原特异性免疫诱导。 a, 疫苗接种实验方案示意图。b, GFP特异性抗体滴度检测,RNA.WT和RNA.142T组之间无显著差异。c, 脾脏中GFP特异性CD8阳性T细胞频率分析。RNA.142T组GFP特异性T细胞占CD8阳性T细胞的比例约为5%,而野生型组约为10%。d-e, 新冠病毒刺突蛋白疫苗接种实验。i.m.注射后,RNA.WT和RNA.142T组诱导的刺突蛋白特异性CD8阳性T细胞频率无显著差异。f, 骨髓嵌合体实验方案示意图。将CD45.1野生型骨髓移植到致死性照射的CD45.2 Ai14受体小鼠中。g-h, 肝脏和脾脏中CD45.1阳性骨髓源性细胞的流式细胞术分析。结果显示,即使在没有直接表达Cre mRNA(RNA.142T)或Cre在肝细胞中沉默(RNA.122T)的情况下,约10-20%的肝脏巨噬细胞和树突状细胞仍为tdTomato阳性,表明这些细胞通过外源性抗原获取获得了tdTomato。
与此形成对比的是,mRNA在肝细胞中的表达反而抑制了免疫应答。 当使用含有miR-122靶点序列的绿色荧光蛋白mRNA疫苗时,肝细胞中的抗原表达被成功沉默,而绿色荧光蛋白特异性CD8阳性T细胞的比例从10%显著提升至28%,提高了近三倍。在A20淋巴瘤小鼠模型中,使用肝细胞沉默的肿瘤相关抗原mRNA疫苗后,肿瘤体积比对照组减少了50%以上。进一步分析显示,肝细胞沉默组小鼠肿瘤内和外周血中的抗原特异性CD8阳性T细胞数量增加,且这些T细胞的耗竭程度更低——PD1和TIM3表达水平显著下降,同时表达更高水平的CD44、IFNγ和颗粒酶B,展现出更强的活化状态和效应功能。机制研究表明,肝细胞表达抗原会通过PD1/PDL1通路抑制T细胞应答,当使用抗PD1抗体阻断该通路后,两种疫苗诱导的T细胞应答差异消失。
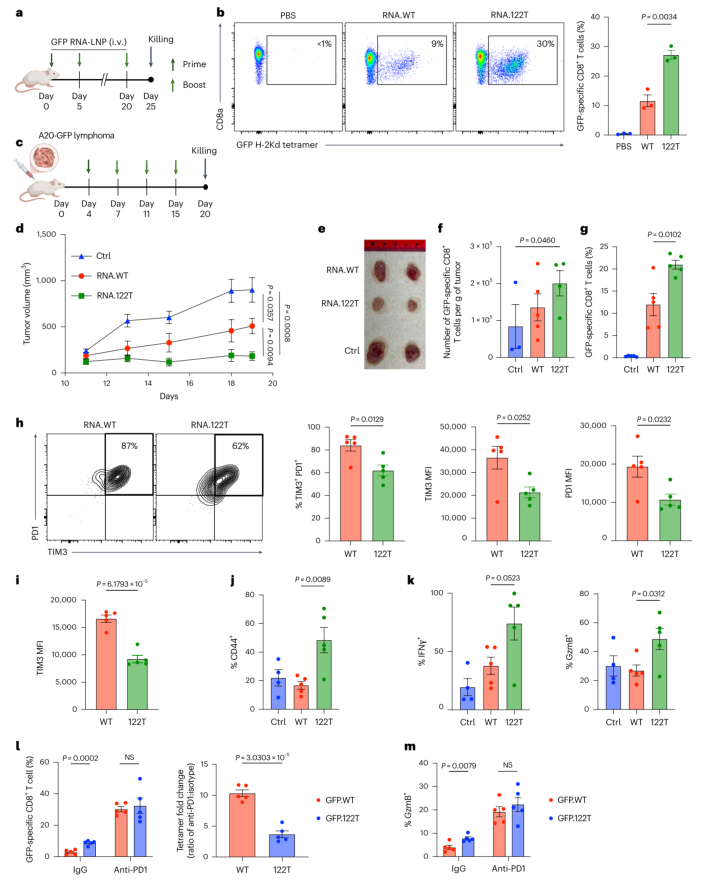
图4 | 肝细胞中的mRNA表达抑制抗原特异性CD8阳性T细胞应答并削弱癌症疫苗效果。 a, 疫苗接种方案示意图。b, 脾脏中GFP特异性CD8阳性T细胞频率分析。RNA.122T组GFP特异性T细胞占CD8阳性T细胞的比例达到约28%,而野生型组仅为10%。c, A20淋巴瘤模型治疗方案示意图。d-e, 肿瘤生长曲线和终点肿瘤照片。RNA.122T组肿瘤体积比野生型组减少50%以上。f, 肿瘤组织中GFP特异性CD8阳性T细胞频率,RNA.122T组显著高于野生型组。g, 脾脏中GFP特异性CD8阳性T细胞频率,RNA.122T组较野生型组提高约一倍。h-i, 肿瘤浸润GFP特异性CD8阳性T细胞中TIM3和PD1的表达水平。RNA.122T组TIM3和PD1阳性细胞频率及表达强度均显著降低。j, 肿瘤浸润CD44阳性CD8阳性T细胞频率,RNA.122T组显著升高。k, 肿瘤浸润CD8阳性T细胞在体外再刺激后的IFNγ和颗粒酶B产生水平,RNA.122T组显著高于野生型组。l-m, 抗PD1阻断实验。结果显示,抗PD1处理消除了RNA.WT和RNA.122T之间GFP特异性CD8阳性T细胞频率和颗粒酶B表达的差异。
肝细胞表达抗原不仅抑制免疫应答,还会带来安全性隐患。 当研究团队向预先移植了绿色荧光蛋白特异性Jedi T细胞的小鼠注射编码绿色荧光蛋白的mRNA-LNP后,野生型mRNA组小鼠肝脏中出现大量CD8阳性T细胞浸润(平均每平方毫米1100个),血清中ALT和AST水平显著升高,表明发生了肝细胞损伤。而使用含有miR-122靶点序列的mRNA组小鼠,肝脏CD8阳性T细胞浸润大幅减少,ALT和AST水平显著降低。类似的现象也在人CD19 CAR-T细胞模型中得到验证——接受野生型mRNA注射的小鼠肝脏中出现更多凋亡细胞和T细胞浸润。这一发现对于使用mRNA疫苗扩增CAR-T细胞或TCR转基因T细胞的临床策略具有重要警示意义。
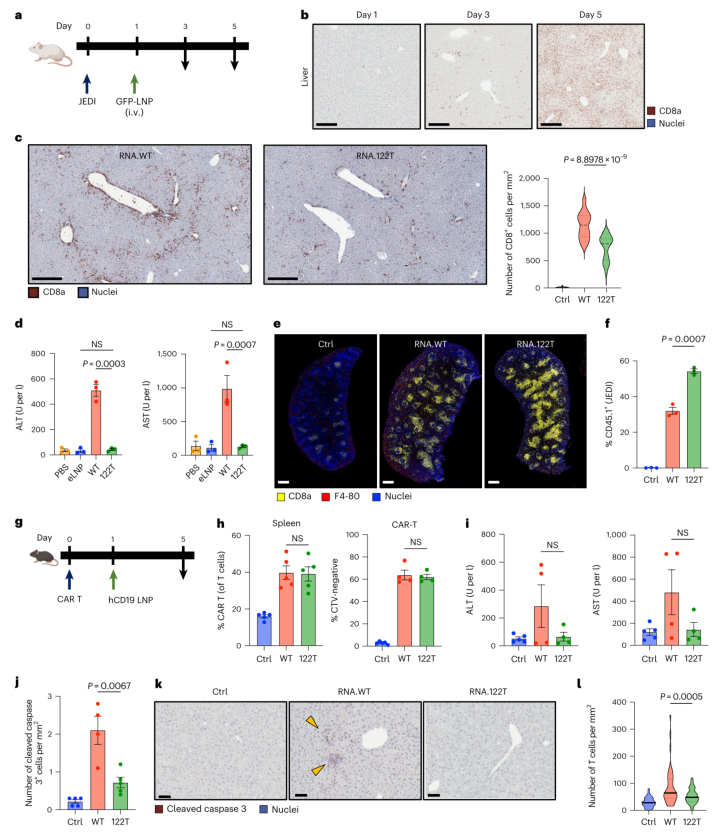
图5 | RNA-LNP诱导的抗原特异性T细胞导致肝损伤,122T可改善这一损伤。 a, 实验方案示意图。将CD45.1阳性Jedi T细胞(表达GFP特异性TCR)过继转移到CD45.2阳性BALB/c小鼠中。b-c, 肝脏CD8阳性T细胞浸润的免疫组化染色与定量分析。RNA.WT组肝脏中CD8阳性T细胞密度约为每平方毫米1100个,而RNA.122T组显著减少。d, 血清ALT和AST水平检测。RNA.WT组ALT和AST显著升高,RNA.122T组接近对照组水平。e-f, 脾脏中CD8阳性T细胞和Jedi T细胞的流式细胞术分析。RNA.122T组Jedi T细胞扩增优于野生型组。g, hCD19 CAR-T细胞实验方案示意图。h, 脾脏中CAR-T细胞频率和分裂指数分析。i, 血清ALT和AST水平,RNA.WT组部分小鼠ALT超过400 U/L,RNA.122T组维持在200 U/L以下。j-k, 肝脏中cleaved caspase 3染色与定量,RNA.WT组凋亡细胞显著增多。l, 肝脏CD8阳性T细胞浸润定量,RNA.122T组显著减少。
与肝细胞相反,肌细胞中的mRNA表达反而促进了免疫应答。 研究人员设计了含有肌肉特异性miR-133和miR-206靶点序列的mRNA,使其在肌纤维中完全沉默,但肌肉间质细胞和脾脏中的免疫细胞表达不受影响。令人惊讶的是,在多次免疫实验中,肌细胞沉默组小鼠的绿色荧光蛋白特异性CD8阳性T细胞应答显著降低,且这些T细胞的颗粒酶B和CD69表达水平下降,表明其功能受损。在新冠病毒刺突蛋白疫苗实验中,肌细胞沉默同样导致刺突蛋白特异性CD8阳性T细胞减少了约30%。这一结果的影响不可忽视——在专业抗原呈递细胞中表达完全沉默的情况下,T细胞应答未受影响,而仅在肌细胞中沉默抗原表达就导致T细胞应答显著降低,这意味着肌细胞对mRNA疫苗诱导的T细胞免疫贡献甚至超过了树突状细胞本身。研究发现,mRNA-LNP注射后,肌细胞中MHC-I分子表达显著上调,使其具备了直接向CD8阳性T细胞呈递抗原的能力。
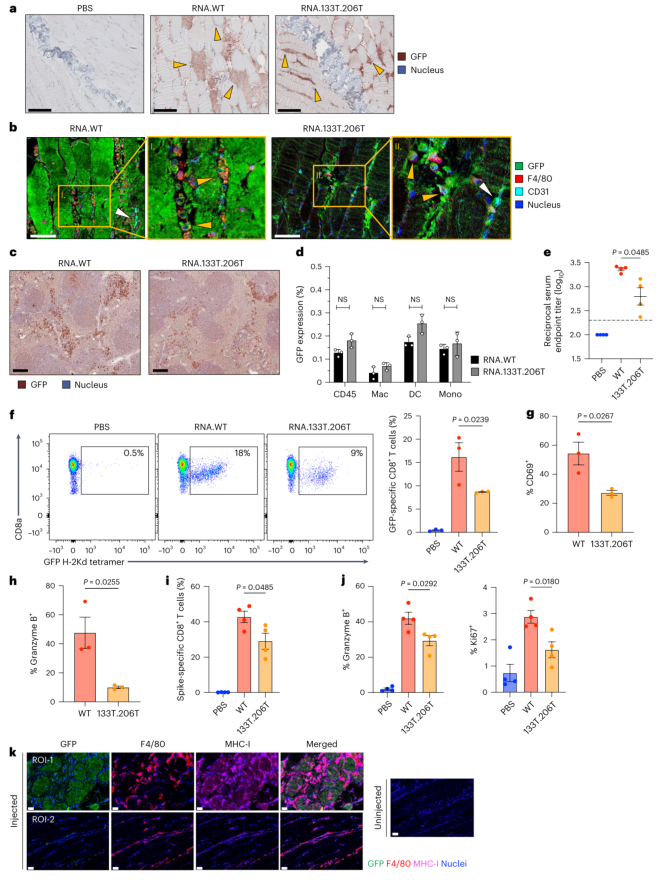
图6 | 肌纤维中的mRNA表达促进CD8阳性T细胞应答。 a, 肌肉组织GFP表达成像。RNA.133T.206T组肌纤维中检测不到GFP表达。b, 肌肉组织多重染色显示,两种制剂在肌肉间质细胞(巨噬细胞和内皮细胞)中GFP表达相当。c-d, 脾脏GFP表达成像和流式细胞术分析。两种制剂在脾脏免疫细胞中的转染效率无差异。e, GFP特异性抗体滴度,RNA.133T.206T组略有降低。f, 脾脏中GFP特异性CD8阳性T细胞频率,RNA.133T.206T组显著降低。g-h, GFP特异性CD8阳性T细胞中CD69和颗粒酶B的表达,RNA.133T.206T组显著降低。i, 新冠病毒刺突蛋白特异性CD8阳性T细胞频率,RNA.133T.206T组降低约30%。j, 刺突蛋白特异性CD8阳性T细胞中颗粒酶B和Ki67的表达,RNA.133T.206T组显著降低。k, 肌肉组织MHC-I多重染色显示,mRNA-LNP注射后,肌纤维中MHC-I分子表达上调,使其具备抗原呈递能力。
总结与展望
这项研究从根本上重塑了我们对mRNA疫苗免疫机制的理解——直接感染并表达抗原的树突状细胞并非启动T细胞免疫所必需,而肌细胞和肝细胞等非专业抗原呈递细胞对免疫应答的影响远超预期。通过合理设计miRNA靶点序列,我们可以在不改变mRNA序列本身的情况下,精确控制其在特定细胞类型中的表达,从而增强疫苗免疫效果或避免不必要的免疫攻击。随着自扩增mRNA和环状mRNA等新型RNA技术的不断发展,mRNA在细胞内停留的时间将更长,转染的细胞类型也将更多样化,这使得精准调控mRNA的细胞类型特异性表达变得愈发重要。miRNA策略提供了一种理性、稳健且模块化的解决方案,为下一代mRNA疫苗和疗法的优化设计开辟了新方向。


