TREM2在皮肤疾病领域的研究进展及应用
时间:2026-05-05 17:14:36 热度:37.1℃ 作者:网络
髓系细胞触发受体2(triggering receptor expressed on myeloid cells 2, TREM2)是髓系细胞表面关键的免疫调节受体。自2001年首次被报道以来,研究逐步揭示其具有多种生物学功能。研究表明,TREM2在巨噬细胞介导的固有免疫应答中发挥核心调控作用,并参与调控多种组织器官的纤维化进程、上皮细胞损伤修复以及脂质代谢稳态维持等重要病理生理过程。TREM2⁺巨噬细胞作为一个功能特化的亚群,不仅通过其复杂的信号网络参与全身多个系统的免疫调节,还可以作为疾病诊断和预后评估的生物标志物,为临床诊断和治疗提供重要的参考依据。深入探究TREM2在皮肤疾病中的作用机制,不仅有助于深化对皮肤疾病病理过程的理解,还有望为临床干预提供新的分子靶点和治疗策略。
1.概述
TREM2基因编码一种典型的跨膜糖蛋白,属于免疫球蛋白超家族,是病理状态下免疫信号转导的关键枢纽。该蛋白主要表达于巨噬细胞、树突状细胞等髓系细胞表面,其结构包括信号肽、Ig样胞外域、跨膜区及胞质尾区。胞外域 含有3个互补决定区(CDR1-3),在胞膜外与配体相互作用。跨膜区与衔接蛋白DNAX激活蛋白12(DNAX-activating protein 12,DAP12)相互作用,而后激活包括Syk激酶、PI3K/Akt和MAPK等在内的下游信号通路,从而调控细胞的吞噬功能、炎症反应和组织修复等重要生理过程。除经典的DAP12介导的ITAM信号通路外,TREM2可以与DAP10偶联后介导YINM信号通路抑制TLR/NF-κB活性,从而调控巨噬细胞的炎症反应。胞质尾区通过跨膜结构域间接调控下 游信号通路。
TREM2依赖的信号传导广泛参与各种疾病病理生物学中的免疫炎症反应。单细胞RNA测序(scRNA-seq)显示,TREM2的表达水平与细胞功能状态高度相关。在体外培养的髓系细胞中,TREM2能够与M-CSF(macrophage colony stimulating factor)协同,驱动巨噬细胞分化,也可以负调控Toll样受体(Toll like receptor,TLR)介导的炎症反应,抑制巨噬细胞的过度活化。此外,其胞外域可被蛋白水解切割,释放可溶性TREM2(sTREM2)至血清和脑脊液中。sTREM2主要通过拮抗膜型TREM2的抗炎作用(如抑制吞噬、解除NF-κB信号抑制)以及独立激活促炎通路(如NFAT1介导的细胞因子释放)来放大炎症反应。在生理状态下,TREM2参与组织稳态维持,如影响大脑胆固醇和磷脂代 谢、皮肤毛囊维持及毛发生长抑制等;在病理状态下,TREM2信号通路成为免疫信号枢纽,如在阿尔茨海默病中,TREM2基因突变体R47H导致Aβ清除能力降低,而在肿瘤微环境中,TREM2在肿瘤相关巨噬细胞中特异性富集,影响肿瘤生长和免疫逃逸。
3.TREM2在皮肤纤维化和系统性硬化症中的作用机制
TREM2在皮肤纤维化修复过程中发挥抗纤维化,抑制瘢痕形成的作用。在系统性硬化症(systemic sclerosis,SSc)患者和博来霉素(BLM)诱导的小鼠皮肤纤维化皮损中TREM2⁺巨噬细胞显著聚集。在皮肤纤维化进程中,TREM2主要通过增强巨噬细胞与成纤维细胞的交互作用调控病变进程。研究表明,TREM2⁺巨噬细胞通过抑制TGF-β通路,拮抗肌成纤维细胞的活化和胶原蛋白的过度合成,从而发挥抗纤维化作用。而TREM2的缺失会加剧炎症反应,减慢伤口修复,如减少新生血管和促进胶原沉积。此外,TREM2⁺巨噬细胞的基因特征与胎儿皮肤巨噬细胞存在重叠类似的部分,提示其可能通过类似胎儿皮肤发育的重编程机制维持皮肤稳态。
在皮肤纤维化相关的疾病中靶向TREM2的干预治疗显示出一定的疗效。TREM2⁺巨噬细胞过继回输后显著降低BLM 诱导的小鼠皮肤厚度及减轻胶原沉积,如Ⅰ型胶原α1链(collagen type i alpha 1 chain,COL1A1)和Ⅲ型胶原 α1链(collagen type iii alpha 1 chain,COL3A1)表达下降。将工程化表达TREM2的巨噬细胞(CAR-Mφ-TREM2)通过水凝胶微孔微针(microneedles, mMNs)的方式靶向输送至瘢痕微环境后,CAR-Mφ-TREM2能够特异性识别并吞噬在瘢痕形成中起关键作用的二肽基肽酶4(dipeptidyl peptidase 4,DPP4)阳性成纤维细胞,抑制TGF-β分泌,抑制内皮细胞向促纤维化表型(如LRG1高表达状态)转化,从而减轻瘢痕严重程度。这些研究结果表明,TREM2⁺巨噬细胞及其相关干预策略在皮肤纤维化和瘢痕形成中具有重要的治疗潜力。
4.TREM2在皮肤伤口愈合和修复中的功能
4.1.TREM2在糖尿病伤口愈合中的作用
TREM2在糖尿病伤口中发挥促修复、 抑炎症的关键作用。在小鼠糖尿病伤口模型中,TREM2在伤口诱导后第3天达 到峰值表达,然后在愈合过程中逐渐下调,表明其在伤口愈合过程中发挥重要作用。在糖尿病伤口愈合过程中,TREM2主要通过两条互补途径调控病变进程:(1)驱动巨噬细胞表型转换;(2)增强巨噬细胞对成纤维细胞的信号传导。TREM2可以直接促进小鼠巨噬细胞在体外从促炎的 M1型向抗炎促修复的M2型转化。M1巨噬细胞分泌TNF-α、IL-1β、IL-6等促炎因子,激活成纤维细胞并促进胶原沉积;M2巨噬细胞则分泌IL-10、TGF-β等抗炎介质,抑制炎症并促进细胞外基质(extracellular matrix,ECM)重塑,但过度M2极化亦可导致ECM过度积聚。在机制层面,IL-4可以直接与TREM2结合,并在巨噬细胞与成纤维细 胞之间的交流中起关键作用。
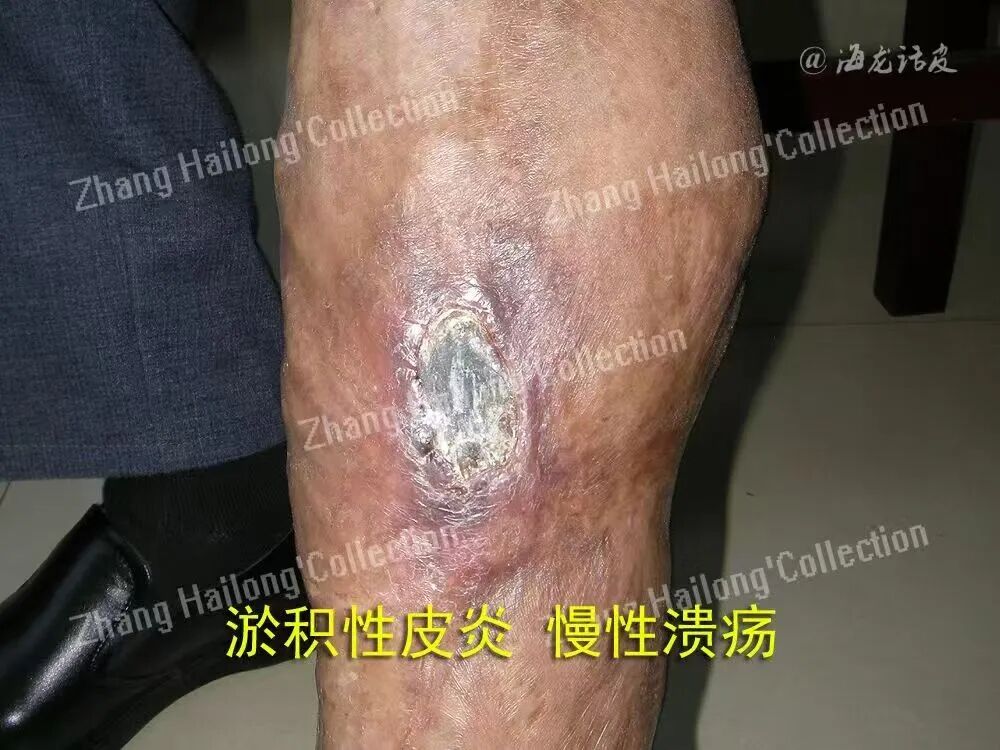
具体而言,TREM2通过与IL4结合抑制过度炎症反应、促进血管生成和胶原沉积,从而促进伤口愈合。基于上述研究,调节TREM2的含量可能具有显著的治疗潜力,在小鼠体内注射sTREM2已被证实可以抑制炎症反应,并促进糖尿病伤口的愈合。TREM2主要通过抑制炎症从而 实现对皮肤损伤的修复,在不同疾病阶段与微环境条件下,发挥不同的修复机制。在糖尿病伤口愈合的早期,TREM2会促进有序、血管伴行的修复型胶原的沉积,促进愈合。在纤维化相关的疾病中,紊乱、交联度高的胶原会导致瘢痕形成,TREM2的激活可以抑制瘢痕型胶原的形成,从而减轻瘢痕。
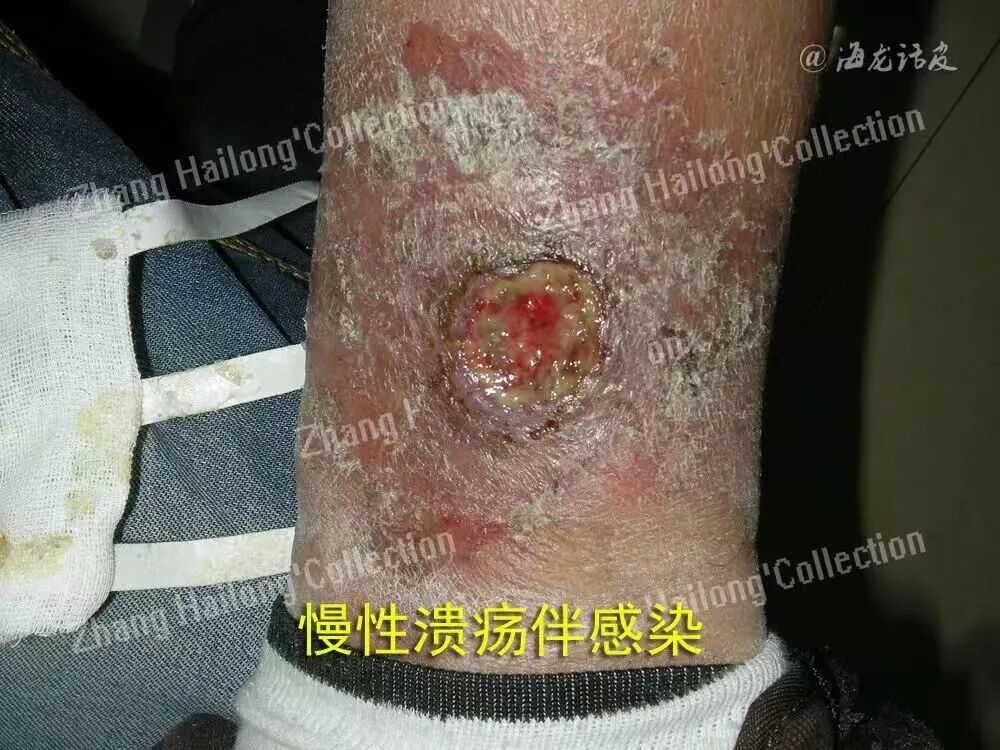
4.2.TREM2在异种皮肤移植创面愈合中的作用
在异种皮肤移植过程中,TREM2⁺巨噬细胞同样展现出促进血管生成和组织再生的机制与治疗潜力。移植后,TREM2⁺巨噬细胞被激活,上调血管生成相关因子(如VEGFA、ANGPT1)的表达,从而促进新生血管形成。在异种皮肤移植中TREM2⁺巨噬细胞分泌基质金属蛋白酶(如MMP12和 MMP13),分解胶原纤维,减轻纤维化。这些发现表明,TREM2⁺巨噬细胞在异种皮肤移植后促进组织修复与功能性皮肤结构重建。
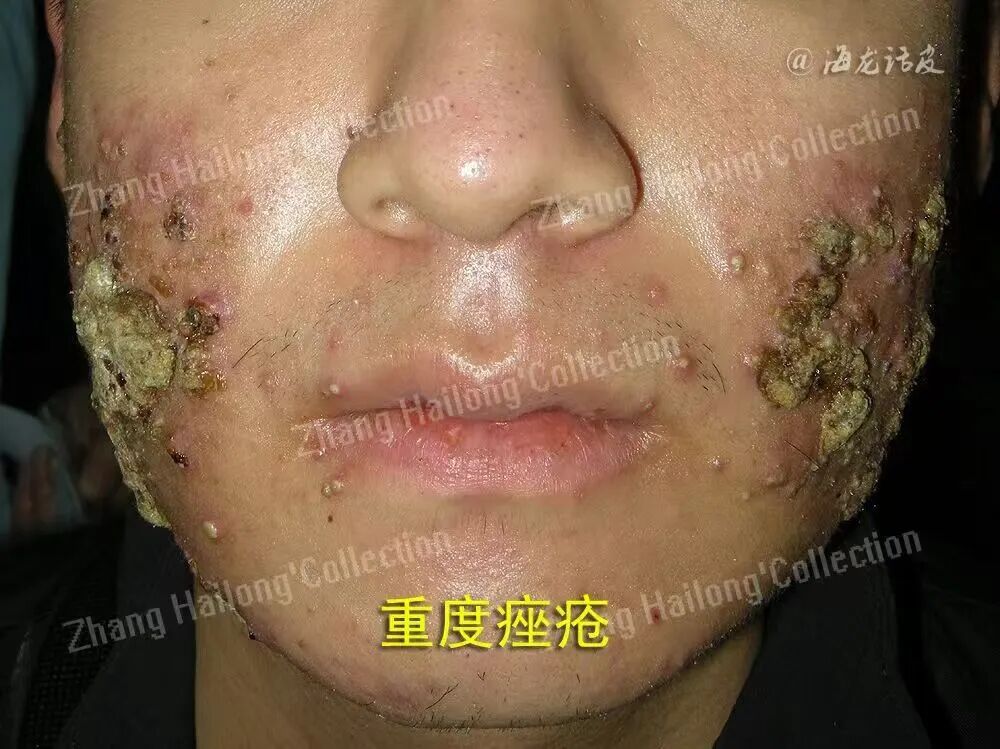
5.TREM2在痤疮中的作用
TREM2⁺巨噬细胞在痤疮病变中起致病作用。常驻的 TREM2⁺巨噬细胞通过释放颗粒蛋白前体(granulin precursor,GRN)参与炎症反应。GRN与其经典细胞表面受体分拣蛋白1(sortilin 1,SORT1)结合,进而刺激促炎细胞因子的释放,包括IL-18、CXCL2、CCL5、TNF-α、IL-6和IL-1β。这些细胞因子能够募集多种炎症细胞,诱发炎症级联反应。TREM2⁺巨噬细胞通过分泌IL-13,可以激活角质形成细胞中的IL-13RA1,导致与过度角化相关的基因(如KRT16、KRT17和FLG)表达失调,从而促进角质形成细胞的过度增殖。TREM2⁺巨噬细胞与不饱和脂质的相互作用在痤疮发病中可能也发挥重要作用,其机制类似于动脉粥样硬化中的脂质代谢过程。痤疮患者皮脂中的不饱和脂肪酸角鲨烯含量增加,角鲨烯脂质负荷使TREM2⁺巨噬细胞转化为泡沫样细胞,进一步上调TREM2蛋白水平。这些泡沫样巨噬细胞的大量聚集加剧了局部炎症反应,促使皮肤病变进一步发展。TREM2⁺巨噬细胞在痤疮病变中还表现出对痤疮丙酸杆菌(Cutibacterium acnes,C.acnes)的清除能力不足。C.acnes是痤疮发病的重要病原体之一,TREM2⁺巨噬细胞无法有效杀死该菌,从而在痤疮病变中起致病作用。
临床上常用的痤疮治疗药物过氧化苯甲酰(BPO)通过释放氧自由基拮抗该免疫抑制微环境,与TREM2信号互为拮抗。鉴于TREM2在痤疮发病中的重要作用,靶向TREM2及其相关通路(如GRN、IL-13RA1)可能成为未来痤疮治疗的新策略。通过抑制TREM2的活性或阻断其下游信号通路,有望减轻炎症反应,改善痤疮症状。
6.TREM2在皮肤肿瘤中的促肿瘤作用
6.1.TREM2在皮肤基底细胞癌中的作用
近年来,TREM2作为肿瘤相关巨噬细胞(tumor-associated macrophages,TAMs)的关键调控分子,在肿瘤免疫微环境 塑造中的作用日益受到关注。在肿瘤微环境中,TREM2主要在TAMs中表达, 并在具有免疫抑制特性的巨噬细胞群中特异性富集。在皮肤基底细胞癌(basal cell carcinoma,BCC)中,TREM2的表达具有独特的空间分布特征。通过多重成像工具与单细胞多组学技术的联合应用,研究人员发现了一种特定髓系细胞亚群——TREM2、VCAM1阳性巨噬细胞,并将其命名为皮肤癌相关髓系细胞(skin cancer-associated myeloid cells,SCAMs)。
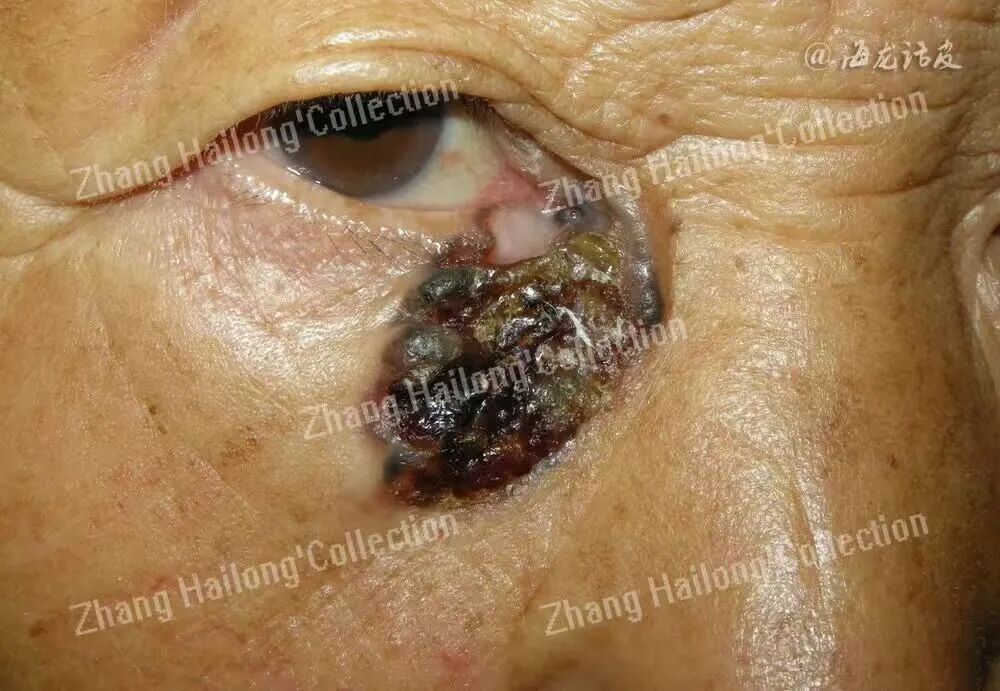
SCAMs在BCC组织中的比例与其他肿瘤接近,但显著高于正常或创伤皮肤,并且显示出较高的增殖活性。SCAMs表现出独特的基因表达谱,高表达多种促肿瘤基因,如细胞因子IL-18、趋化因子CCL18和 CXCL16。SCAMs在肿瘤组织中与肿瘤上皮细胞紧密相邻,通过分泌IL-18和CCL18,激活JAK/STAT3信号通路,促进肿瘤上皮细胞的增殖和侵袭。 此外,SCAMs还通过分泌基质金属蛋白酶(如MMP12和MMP13)分解胶原纤维,介导ECM重塑,从而有助于肿瘤的侵袭和转移。SCAMs能够在肿瘤微环境中自我增殖,维持与肿瘤上皮细胞的恒定比例。这些细胞还通过分泌免疫抑制分子(如IL-10、TGF-β)和表达免疫检查点分子(如PD-L1),抑制抗肿瘤免疫反应。靶向TREM2或SCAMs相关通路有望为BCC提供新的免疫-代谢联合干预策略。
6.2.TREM2在皮肤黑色素瘤中的作用
在皮肤黑色素瘤中,TREM2驱动TAMs形成免疫抑制微环境并与不良预后正相关。在黑色素瘤患者中,TREM2⁺TAMs在免疫治疗效果差的患者中显著富集。TREM2⁺巨噬细胞表现出免疫抑制特征,包括高表达免疫抑制分子(如IL-10、PD-L1)和低表达促炎分子(如TNF-α)。这些巨噬细胞还表现出与ECM重塑和血管生成相关的基因表达特征,这可能有助于肿瘤的侵袭和转移。Scortegagna等研究发现,在老年患者(≥70岁)和老年小鼠的黑色素瘤中,TREM2⁺巨噬细胞和GZMK⁺的CD8⁺T细胞比例增高,表示免疫系统已进入持续耗竭状态,与免疫治疗抵抗、疾病进展相关。在同一遗传背景下,年轻小鼠TREM1信号驱动肿瘤增殖,而老年小鼠TREM2信号主导肺转移。
通过检测TREM2和相关基因表达特征,可以提前预测患者对免疫治疗的反应,从而为个性化治疗提供依据。这为开发针对老年黑色素瘤患者的新型治疗方法提供了理论依据。TREM2作为皮肤黑色素瘤肿瘤微环境中潜在的免疫相关预后生物标志物具有重要意义,其在调节肿瘤免疫微环境中的关键作用和作为治疗 靶点的潜力不容忽视。虽然目前还没有TREM2相关药物应用于皮肤肿瘤,但已开展了 TREM2耗竭抗体相关的临床试验用于肿瘤研究。该研究发现靶向TREM2⁺TAMs的抗体可阻断TAM免疫抑制功能,TREM2耗竭抗体可能作为靶向药物,可诱导抗肿瘤免疫反应并减少肿瘤生长。此外,抗TREM2耗竭抗体与PD-1/PD-L1抑制剂联用显著恢复CD8⁺T细胞杀伤活性,抑制肿瘤生长。
7.结论
TREM2在皮肤性疾病中主要通过调控巨噬细胞功能发挥关键作用。在皮肤纤维化疾病中,TREM2⁺巨噬细胞通过维持皮肤稳态发挥抗纤维化保护作用。在皮肤伤口愈合过程中,TREM2通过DAP12-Syk抑制MAPK→AP-1轴,使巨 噬细胞向M2型转化,从而介导血管生成和胶原沉积,加速创面修复。在痤疮病变中,TREM2⁺巨噬细胞加剧了局部炎症反应,并且降低对C.acnes的杀伤能力。在肿瘤微环境中 TREM2通过调节TAMs功能影响肿瘤发生。这些机制表明 TREM2通过调节巨噬细胞的免疫代谢重编程和组织重塑功能,在皮肤损伤修复和纤维化疾病中发挥双重保护作用,但在痤疮与皮肤肿瘤中发挥有害作用,是肿瘤浸润巨噬细胞的关键促肿瘤标志物。
目前临床上TREM2相关的药物实验主要聚焦于阿尔兹海默症和肿瘤的治疗。研究新发现一种口服小分子TREM2抑制剂,可增强铂类化疗药物对人结肠癌的治疗效果。在FDA已批准药物中,硼替佐米和阿塔鲁仑被发现能有效抑制TAMs中TREM2的表达,从而介导免疫抑制功能。新型分子佐剂可以通过配体诱导途径调节TREM2活性,新型药物递送系统(如仿生纳米颗粒)可以靶向TREM2表现出其显著的抗胶质母细胞瘤治疗作用。虽然在皮肤肿瘤的相关研究中,有关TREM2的药物研究暂时欠缺,但一些靶向TREM2信号通路的药物可能具有治疗泛癌的效果,以及一些在神经退行性疾病中已验证的药物可能在皮肤相关疾病中也能发挥治疗效果。
TREM2在皮肤纤维化、糖尿病皮肤创面修复、异种皮肤移植创面愈合、痤疮和皮肤肿瘤等多种皮肤疾病中展现出重要作用,其机制涉及多个层面,对皮肤疾病的发生、发展和转归产生关键影响。但目前的研究仍处于探索阶段,靶向特殊疾病与特殊部位的有效递送药物仍面临严峻挑战。需要进一步深入研究TREM2的作用机制,优化治疗策略,以提高治疗效果,为皮肤肿瘤患者带来新的治疗希望。
参考文献:
1.于柯瑶,朱信霖,张克明,潘炜华,张超.TREM2在皮肤疾病领域的研究进展及应用[J/OL]中国皮肤性病学杂志. https://doi.org/10.13735.
2.Bouchon A, Hernandez-Munain C, Cella M,et al.A DAP12-mediated pathway regulates expression of CC chemokine receptor7 and maturation of human dendritic cells[J]. J Exp Med, 2001,194(8):1111-1122
3.Deczkowska A, Weiner A, Amit I.The Physiology, Pathology, and Potential Therapeutic Applications of the TREM2 Signaling Pathway[J]. Cell, 2020,181(6):1207-1217.
4.其他文献略。


