CCR:未经内分泌治疗的低级别子宫内膜样癌ESR1突变较常见,尤以NSMP亚组显著,或干扰内分泌治疗疗效
时间:2026-05-05 17:13:22 热度:37.1℃ 作者:网络

芳香化酶抑制剂(AI)用于治疗雌激素受体(ER)阳性低级别子宫内膜样癌。在乳腺癌中,ESR1突变在初诊时罕见(<5%),但在AI耐药病例中常获得性出现,被认为是内分泌治疗耐药的主要机制之一。本研究旨在评估未经内分泌治疗的子宫内膜癌标本中ESR1突变的发生率,并分析其与分子谱、ER表达及临床结局的相关性。UTOLA试验共招募147例一线化疗后缓解的晚期子宫内膜癌患者。对存档子宫内膜癌肿瘤组织进行包含ESR1在内的127个基因测序,仅评估配体结合域的热点突变。在英国基因组学数据集验证ESR1突变发生率。依据子宫内膜癌前瞻性分子风险分类器(PROMISE),将UTOLA试验中肿瘤分为POLE型、错配修复缺陷型(dMMR)、TP53异常型(TP53abn)及无特定分子谱型(NSMP)。
147例患者中137例有足够肿瘤组织用于测序。8例肿瘤检出ESR1突变(6%),包括Y537S/C/N(n=4)、L536H/P(n=2)及E380Q(n=2)。英国基因组学数据集1311例肿瘤中检出相似发生率(3.5%)。所有ESR1突变病例均为低级别子宫内膜样癌、ER阳性、孕激素受体(PR)阳性,且归为NSMP型。在转移性NSMP低级别子宫内膜样癌患者中,22%(8/37)携带ESR1突变。ESR1突变型与野生型子宫内膜癌患者接受铂类化疗后的生存结局相似(中位生存期:未达到 vs 25.3个月;P=0.114)。
ESR1突变在未经治疗的子宫内膜癌中总体罕见,但在NSMP低级别子宫内膜样癌患者中更常见,可能影响AI疗效。选择内分泌治疗时应考虑ESR1状态,且该状态应作为AI临床试验的分层因素。
研究背景
子宫内膜癌在历史上分为两类疾病:I型子宫内膜癌与肥胖及代谢综合征相关,以低级别肿瘤、高ER/PR表达、预后良好为特征;相反,II型肿瘤包含非子宫内膜样组织学类型,通常无激素受体(HR)表达,预后较差。过去十年,子宫内膜癌的发病率与死亡率持续上升。多数病例因早期诊断预后良好,5年总生存率(OS)超80%;相比之下,转移性/复发性癌患者OS率极低,5年生存率仅约15%。
子宫内膜癌的认知与诊疗取得显著进展。首先,子宫内膜癌分子分类明确了四个具有预后意义的分子亚型:POLE突变型子宫内膜癌,肿瘤突变负荷极高且预后极佳;微卫星不稳定型子宫内膜癌[MMR缺陷型(dMMR)/微卫星不稳定(MSI)],突变负荷高且对免疫检查点抑制剂高度敏感;拷贝数高型子宫内膜癌,伴频发性TP53突变,预后最差;拷贝数低型子宫内膜癌,无特定分子谱(亦称NSMP),预后中等。后续多项研究证实,可通过福尔马林固定石蜡包埋(FFPE)组织中的替代标志物,采用子宫内膜癌前瞻性分子风险分类器(PROMISE)识别出与癌症基因组图谱类似的分子分组,具有显著预后价值。重要的是,这些分子亚组还可提供部分预测价值。
NSMP型子宫内膜癌是初诊时最常见的分子亚型,包含多数低级别子宫内膜样肿瘤及大部分ER/PR表达阳性肿瘤。尽管相较于TP53突变型肿瘤病程更惰性,但该亚型仍存在显著未满足的临床需求,亟需更有效的靶向治疗策略。该亚型常检出PIK3CA、ARID1A、PTEN及CTNNB1基因的频发性体细胞突变,目前尚无经验证的匹配靶向治疗。内分泌治疗是首个获批用于ER和/或PR阳性表达子宫内膜癌患者的靶向药物,自20世纪50年代起成为子宫内膜癌的治疗选择。尽管与激素驱动的腔面型乳腺癌高度相似,但芳香化酶抑制剂(AI)的缓解率仍较低,通常低于20%,仅少数患者获得持久缓解,且缺乏精准的预测生物标志物,这种相对耐药的原因尚不明确。同样,孕激素类药物的缓解率略高,约30%,但无法转化为长期生存获益。有趣的是,ER信号通路与PI3K–Akt通路共同汇聚于细胞周期蛋白D1–CDK4/6–Rb通路。近年来,AI联合CDK4/6抑制剂在HR阳性乳腺癌中显示出显著疗效,且在子宫内膜癌的小型II期试验中展现出良好前景。鉴于子宫内膜癌发病率不断上升,且NSMP亚组缺乏有前景的靶向药物,深入理解这些肿瘤的分子背景有助于筛选更可能从内分泌治疗中获益的患者。
乳腺癌中内分泌治疗耐药的主要机制之一是获得性体细胞ESR1突变。AI治疗后乳腺癌患者中该突变检出率达36%,且相较于ESR1野生型(ESR1wt)预后更差。这些突变累及配体结合域(LBD),导致基因在无激素情况下呈现组成型转录活性,进而介导AI耐药。相比之下,原发性乳腺癌中ESR1突变罕见,检出率低于5%,但同样与内分泌治疗耐药及生存不佳相关。在子宫内膜癌患者中,多项生物标志物与内分泌治疗缓解率改善相关,包括组织学1级、子宫内膜样组织学类型、ER表达及CTNNB1突变。然而,耐药机制仍不明确且研究不足。令人关注的是,子宫内膜原发性肿瘤的全面分子谱分析显示,4%病例存在聚集于LBD的ESR1突变,且患者未接受过内分泌治疗,但研究者未将这些突变与组织学、分级或分子数据关联,亟需进一步研究。
本研究旨在探索未经内分泌治疗的存档子宫内膜癌肿瘤中ESR1突变的发生率,重点关注最适合激素治疗的子宫内膜癌亚群:低级别子宫内膜样NSMP型子宫内膜癌。UTOLA试验是一项随机II期试验,招募接受至少4周期卡铂联合紫杉醇一线化疗、且疾病无进展、稳定、部分缓解或完全缓解的晚期或转移性子宫内膜癌患者。患者随机接受奥拉帕利维持治疗或安慰剂治疗直至疾病进展。该试验未显示奥拉帕利在总体人群中带来生存获益,但在高基因组不稳定性亚组中报告显著获益。从病例报告表中提取临床病理细节,包括各中心常规检测的HR表达。肿瘤细胞ER、PR表达≥10%判定为阳性。
研究结果
患者特征:
试验招募的147例患者中,2例撤回转化研究知情同意,10例肿瘤组织不足无法进行DNA测序。最终135例子宫内膜癌肿瘤成功完成大panel测序(占队列92%)。患者中位年龄66.6岁(四分位距62.7–73.5)。队列中103例(76.3%)为子宫内膜样癌,其中69%为低级别(1级或2级),31%为高级别;26例(19.3%)为浆液性癌。76%患者ER表达≥10%,60.8%患者PR表达≥10%。基线特征总结于表1。

表1
依据PROMISE标准通过IHC/NGS完成124例患者(91.9%)的分子分类。18例(14.3%)归为dMMR,108例(85.7%)归为MMR正常型(pMMR)。69例(51.5%)存在P53表达异常,其中59例P53弥漫过表达,10例P53蛋白表达缺失;58例(43.6%)呈现野生型P53表达谱(表1)。最终18例归为dMMR(14.5%),66例归为P53abn(53.2%),40例归为NSMP(32.3%)。
ESR1突变及其临床病理特征:
135例患者中,26例个体检出28个ESR1突变。10个突变位于LBD之外(外显子1、2、3或4),1个突变有害且机制上与受体激活无关(ESR1:NM_000125:外显子8:c.1755delG:p.T585fs),7个突变意义未明。因此排除这18个突变,最终8例独特肿瘤样本检出10个致病性ESR1突变,总体队列发生率为5.9%(8/135)。这些致病性突变位于LBD四个热点:2个ESR1 E300Q突变、5个ESR1 Y537C/N/S突变、2个ESR1 L536H/P突变、1个ESR1 D538G突变。
8例ESR1突变型(ESR1mut)病例均为子宫内膜样癌,且均为低级别肿瘤(1/2级)。可获得ER/PR表达数据的7例病例中,全部ER及PR表达≥10%。分子分类方面,队列中未检出POLE突变;依据PROMISE分类,8例ESR1mut肿瘤均归为NSMP型(表2)。子宫内膜样癌中ESR1突变发生率为7.8%,NSMP型子宫内膜癌中为19%,低级别子宫内膜样NSMP型子宫内膜癌中为22.2%(图1)。生存结局方面,受限于统计学效能,ESR1mut与ESR1wt患者未检出OS差异。低级别子宫内膜样NSMP病例(n=36)中,ESR1mut患者中位OS未达到,ESR1wt患者为26.6个月[风险比4.2(0.55–31.6);P=0.133]。
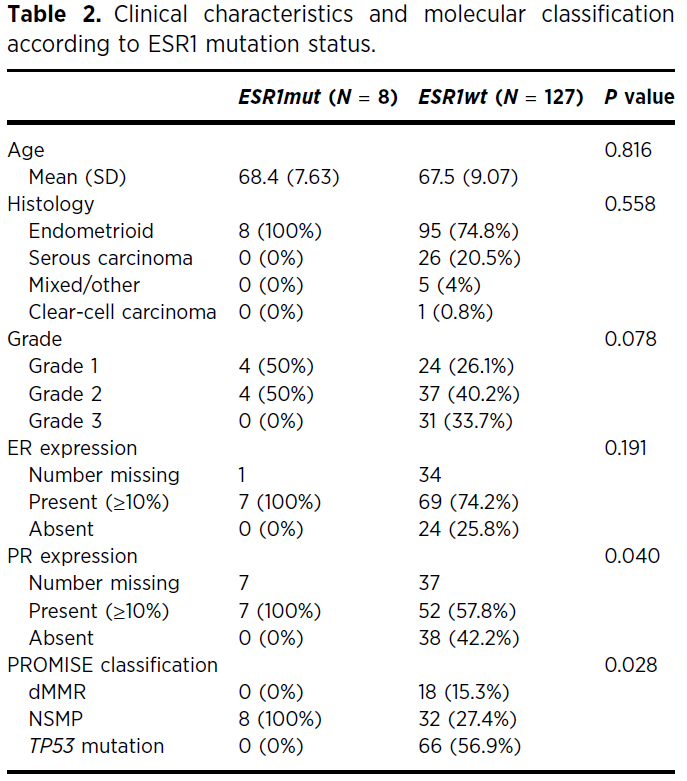
表2
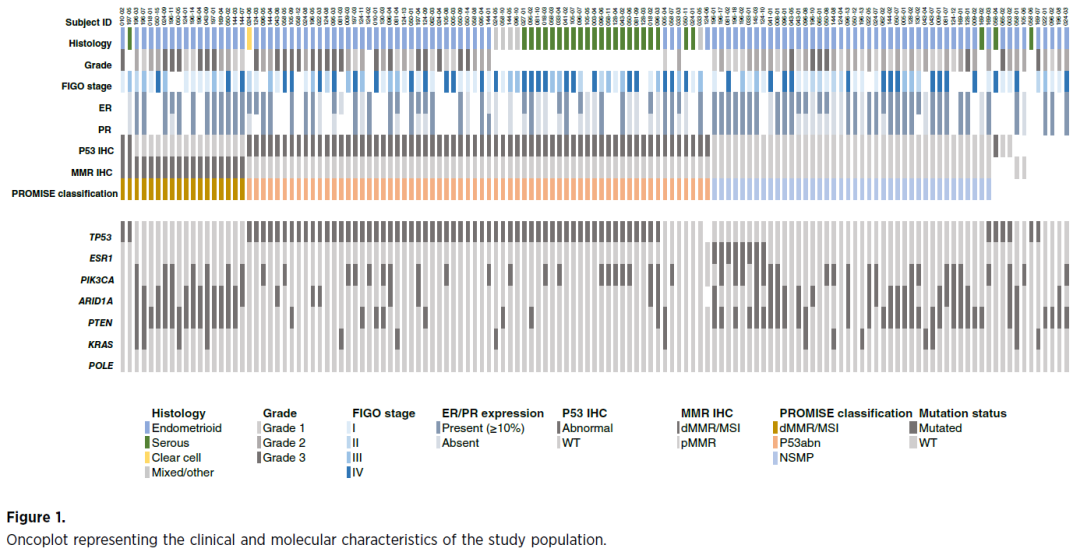
图1
P53abn亚组(n=67)中,39例为子宫内膜样癌,其中19例为低级别子宫内膜样癌。此外,TP53abn病例中67.4%为ER阳性(31/46),47.7%为PR阳性(21/44),无病例检出ESR1突变。
分子谱方面,ESR1mut病例呈现典型NSMP背景,最常见的致病性突变基因为PTEN(6/8例)、PIK3CA(5/8例)及ARID1A(2/8例)。
验证队列:
检索英国基因组学数据库以确认子宫内膜癌中ESR1突变的发生率及特征。数据库中登记1311例子宫内膜癌病例及相关外显子测序数据。患者中位年龄64岁(四分位距56–71);49.5%为子宫内膜样癌,33.7%为浆液性癌,5.4%为癌肉瘤,5.1%为透明细胞癌。子宫内膜样癌中,76.9%为低级别,23.1%为高级别。国际妇产科联盟(FIGO)分期分布为:I期51.6%、II期10.3%、III期29%、IV期9.1%。
体细胞突变方面,1311例患者中692例(52.8%)存在TP53突变,44.3%存在PTEN突变,41%存在ARID1A突变,37.1%存在PIK3CA突变,20.4%存在FBXW7突变,16.2%存在KRAS突变。最终46例检出ESR1突变(3.5%)。与UTOLA队列观察结果一致,检出的大部分突变(36/46)累及LBD,且已在乳腺癌患者中报道。具体为21个Y537C/N/S突变(58.3%)、8个L536H/R突变(22.2%)、4个G442R突变(11.1%)、3个S463P突变(8.3%)及1个V392I突变(2.8%)。
36例致病性ESR1突变病例(2.7%)中,绝大多数为低级别子宫内膜样组织学类型(80.6%);3例为高级别子宫内膜样癌,1例为癌肉瘤,2例为其他未明确组织学亚型。分子谱方面,36例ESR1mut病例中32例为TP53野生型(88.9%)。发生率方面,尽管无MMR状态数据,约6.6%低级别子宫内膜样病例检出ESR1突变。
讨论
尽管内分泌治疗长期以来被认为是HR阳性转移性子宫内膜癌耐受性良好的治疗选择,但其疗效有限,缓解率低于30%。此外,复发患者的替代治疗选择为单药化疗或帕博利珠单抗联合仑伐替尼,这类老年患者治疗毒性显著,因此亟需有效的生物标志物预测最可能从内分泌药物中获益的患者。在异质性的子宫内膜癌人群中,激素治疗最有前景的候选者是NSMP低级别子宫内膜样癌,因其高HR表达、病程惰性且与腔面型乳腺肿瘤相似。乳腺癌的研究经验可为子宫内膜癌诊疗提供参考。因此,本研究旨在探索子宫内膜癌患者中ESR1突变的发生率,重点关注低级别子宫内膜样NSMP肿瘤。
ESR1突变的获得是接受激素治疗的乳腺癌患者中报道的最重要耐药机制。AI治疗的乳腺癌病例中该突变获得率高达35%,但在未经治疗的初诊病例中罕见。相比之下,基于本研究的UTOLA队列及英国基因组学验证队列,观察到未经内分泌治疗的原发性子宫内膜癌中,ESR1突变发生率略高(3%–6%)。最重要的是,内分泌治疗最适用于低级别子宫内膜样NSMP型子宫内膜癌,本研究首次证实ESR1配体结合域激活突变在低级别子宫内膜样NSMP型子宫内膜癌中显著高发(20%),而在其他分子分型中极为罕见。该观察结果对这类患者的治疗策略具有重要意义,因为单药AI治疗大概率无法带来显著获益,应考虑替代治疗。选择性ER降解剂通过直接结合ER并灭活配体依赖及非依赖信号,具有机制优势,为其作为AI替代方案用于子宫内膜癌(包括携带ESR1突变的肿瘤)提供理论依据。同时,子宫内膜样癌中细胞周期蛋白D–Rb通路的频繁失调促进肿瘤进展,并作为旁路机制驱动内分泌耐药。在此背景下,CDK4/6抑制剂阻止Rb1磷酸化,诱导G1期细胞周期停滞,增强内分泌治疗的抗增殖作用。这为ER阳性子宫内膜癌中联合CDK4/6抑制剂与内分泌药物提供了强有力的理论依据,可同时阻断上游激素信号及下游细胞周期进程。近期多项小型临床研究在复发性子宫内膜癌中报告了良好疗效,支持该治疗方案,但仍需大型随机试验验证。
分子医学时代,子宫内膜癌异质性的认知显著提升。四个分子亚型定义了截然不同的疾病,分子分类现已成为局限性及转移性子宫内膜癌治疗算法的核心要素。NSMP亚组主要由子宫内膜样肿瘤组成,包含大部分低级别亚型,因此是最可能从激素治疗中获益的分子类别。近期Vermij及其同事证实,ER表达可进一步对NSMP子宫内膜癌患者分层,将NSMP HR阳性定义为预后良好亚组。本研究提出进一步对NSMP病例进行分子分层,在NSMP HR阳性患者中定义ESR1mut亚组,这类患者不应接受AI治疗,应优先选择他莫昔芬或ER降解剂等其他内分泌策略。本研究发现ESR1突变对低级别NSMP子宫内膜癌无预后影响,可能因为UTOLA队列接受的是化疗而非内分泌治疗。
本研究存在若干局限性,需谨慎解读结论。首先,尽管UTOLA试验人群具有临床相关性,涵盖所有组织学类型、分级及分子亚型(除极为罕见的POLE突变型子宫内膜癌),但无法代表转移性子宫内膜癌人群。入组患者需接受至少4周期铂类化疗、体力状态良好且化疗后疾病未进展,这造成显著选择偏倚,人为增加了铂类化疗获益更显著的P53abn病例数,减少了子宫内膜样病例数。英国基因组学数据库的验证研究缺乏MMR状态及POLE突变数据,是重要局限性。同时,检测单核苷酸变异的分子技术(NGS vs WGS)差异可能影响结果。此外,UTOLA队列中ESR1突变发生率更高(5.9% vs 英国基因组学数据库全人群2.7%),可能反映UTOLA试验富集了预后较差的ER阳性NSMP患者亚组,所有入组病例均为FIGO IV期或复发性疾病。尽管如此,本研究观察到ESR1突变与低级别子宫内膜样组织学类型、TP53野生型状态的关联一致,强化了既往结论。最后,研究的回顾性设计、缺乏体外机制验证及内分泌治疗缓解数据,均为准确评估子宫内膜癌中ESR1突变的临床价值带来显著局限性。
综上,ESR1突变在未经治疗的低级别子宫内膜样癌中较为常见,尤其在NSMP亚组中,近五分之一病例可检出;携带该突变的患者大概率无法从AI治疗中获益。基于该观察结果,ESR1突变状态可作为有价值的预测生物标志物,且应作为子宫内膜癌患者激素治疗相关研究的分层因素。
参考文献:
Blanc-Durand, Félix et al. “ESR1 Mutation in Endocrine Treatment-Naïve Endometrial Cancer: Prevalence, Characteristics, and Prognostic Implications, Results from the UTOLA Phase II GINECO Trial.” Clinical cancer research : an official journal of the American Association for Cancer Research vol. 32,5 (2026): 963-969. doi:10.1158/1078-0432.CCR-25-2758


