中山大学Biomaterials:三步破解顽固牙周生物膜——开发氧空位纳米系统,实现EPS降解、休眠菌激活与微生态重塑
时间:2026-05-05 17:11:19 热度:37.1℃ 作者:网络
背景介绍
牙周炎是全球第六大流行性慢性疾病,严重影响口腔健康乃至全身健康。其核心病因是龈下生物膜——一种由细菌嵌入自身分泌的胞外聚合物所形成的结构化群落。这种生物膜拥有“双重防御”:一方面,致密的EPS基质形成物理屏障,阻碍药物渗透;另一方面,生物膜深层的代谢休眠“持留菌”对抗生素高度耐受,一旦环境适宜便会迅速复苏,导致感染复发和耐药。传统机械清创和抗生素治疗难以彻底清除生物膜,且易破坏口腔微生态平衡。因此,亟需一种能同时瓦解EPS屏障、杀灭持留菌并恢复健康菌群的新型策略。
研究思路
针对这一挑战,中山大学光华口腔医学院滕伟教授与中山大学附属第一医院王琴梅研究员团队合作,开发了一种富含氧空位的多功能纳米平台——MoO₃₋ₓ/ICG。该平台将氧空位修饰的氧化钼纳米点与光敏剂吲哚菁绿结合,在近红外光照射下,可同时产生局部高温和活性氧风暴,并通过类过氧化物酶催化持续产生羟基自由基。这一协同作用不仅能够破坏EPS基质、促进超小纳米点深层渗透,还能通过热-氧化应激增加细菌膜通透性,从而“唤醒”休眠的持留菌,使其代谢活跃、恢复对抗菌药物的敏感性。随后,纳米平台彻底清除被激活的细菌,并通过重塑龈下微生物组,抑制病原菌(如红色复合体、橙色复合体),促进共生菌生长,实现从“杀灭”到“生态调节”的全周期治疗。相关内容以“Oxygen Vacancy-Rich Nanosystems Eradicate Stubborn Periodontal Biofilms by Synergistic EPS Degradation, Metabolic Activation and Microbiome Restoration”为题,发表在《Biomaterials》!

图片解析
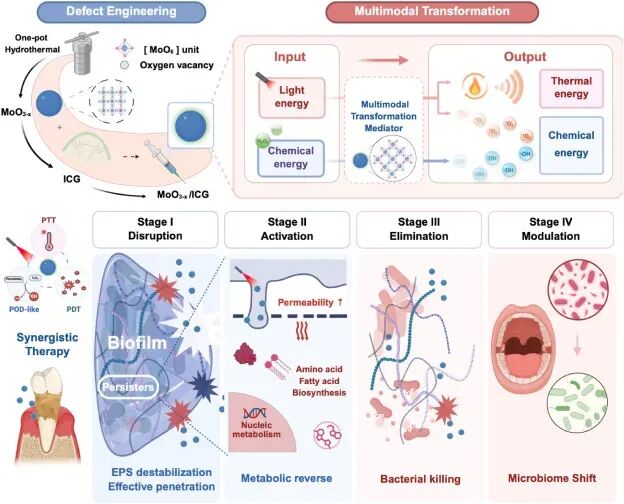
Scheme 1. 研究示意图:展示了MoO₃₋ₓ/ICG纳米平台治疗牙周生物膜的“破坏-激活-清除-调节”四步策略。在NIR照射下,纳米平台产生热和ROS,破坏EPS屏障并渗透进入生物膜深层;随后热/氧化应激增加细菌膜通透性,唤醒休眠持留菌;接着通过多种机制杀死细菌;最后重塑微生物群落,恢复健康微生态。
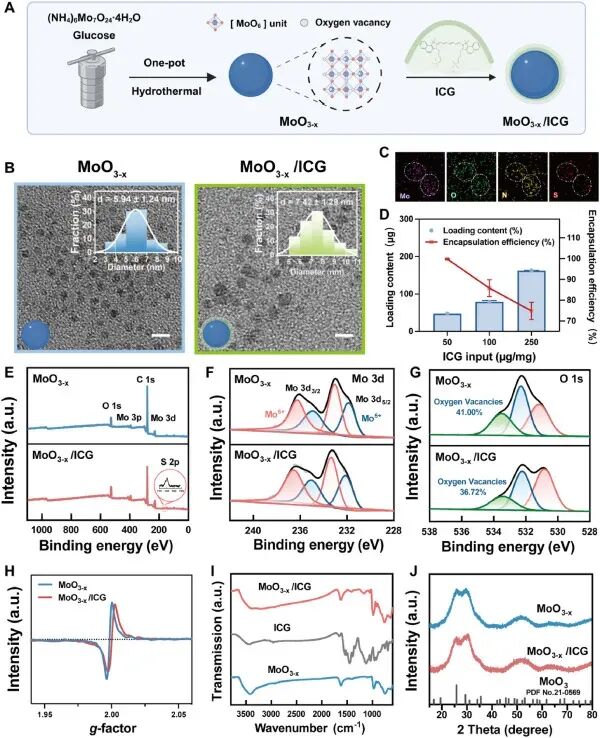
图1. MoO₃₋ₓ/ICG的合成与表征:(A) 合成示意图;(B) TEM显示纳米点粒径约7.4 nm,分布均匀;(C) 元素映射证实N、S(来自ICG)均匀分布;(D) ICG负载量测定;(E-G) XPS分析证实Mo⁵⁺/Mo⁶⁺混合价态及氧空位存在(O 1s峰531.4 eV);(H) EPR证实氧空位信号(g=2.00);(I) FTIR显示MoO₃₋ₓ与ICG之间形成氢键和共价键;(J) XRD显示无定形结构,利于催化。氧空位浓度高达41.00%,是增强光热和酶活性的关键。
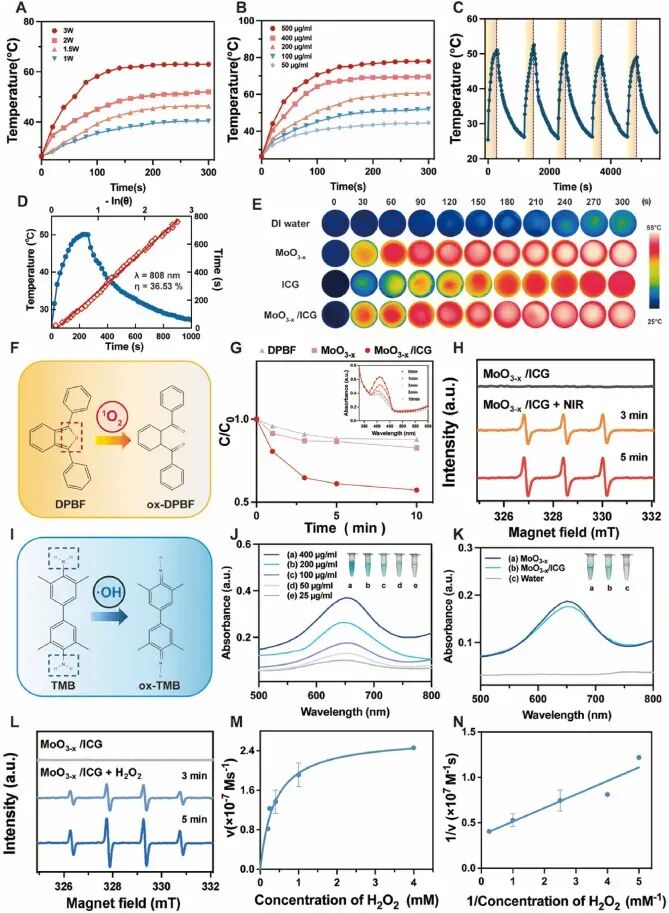
图2. 光热、光动力及类过氧化物酶活性:(A-B) 浓度和功率密度依赖的光热升温曲线;(C) 五次循环光热稳定性良好;(D) 光热转换效率:MoO₃₋ₓ为40.82%,MoO₃₋ₓ/ICG为36.53%;(E) 红外热像图证实MoO₃₋ₓ/ICG升温显著;(F-H) DPBF探针和ESR证实¹O₂生成;(I-L) TMB显色和ESR证实·OH生成(类POD活性);(M-N) 米氏动力学分析显示MoO₃₋ₓ/ICG对H₂O₂的亲和力(Km=0.37 mM)优于天然辣根过氧化物酶。该平台集PTT/PDT/POD三功能于一体。
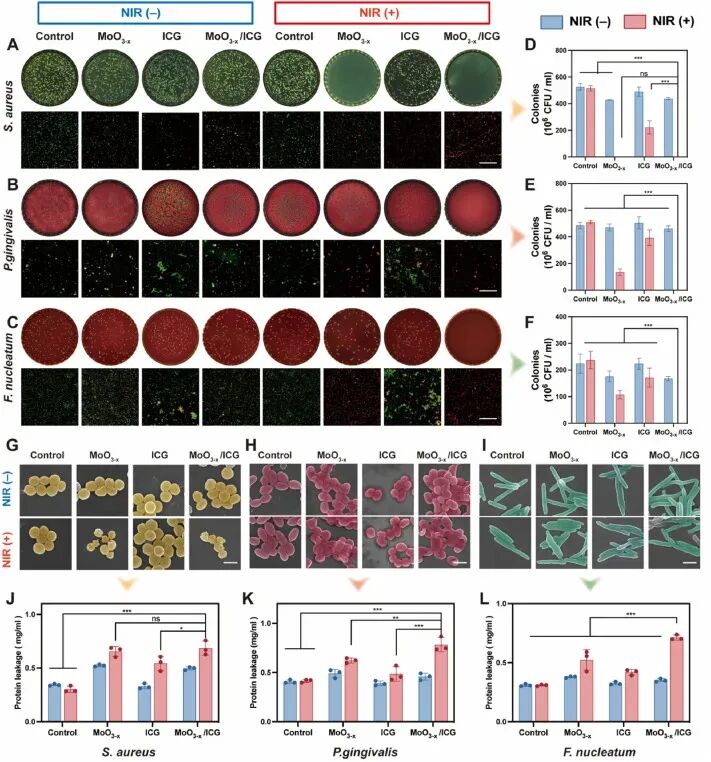
图3. 体外抗菌性能:(A-C) 平板涂布和活/死染色显示,MoO₃₋ₓ/ICG+NIR对金黄色葡萄球菌、牙龈卟啉单胞菌、具核梭杆菌的杀灭率均接近100%;(D-F) 定量分析;(G-I) SEM显示细菌膜严重破裂、内容物外泄;(J-L) 蛋白泄漏量显著增加。证明三模态协同抗菌效果卓越。
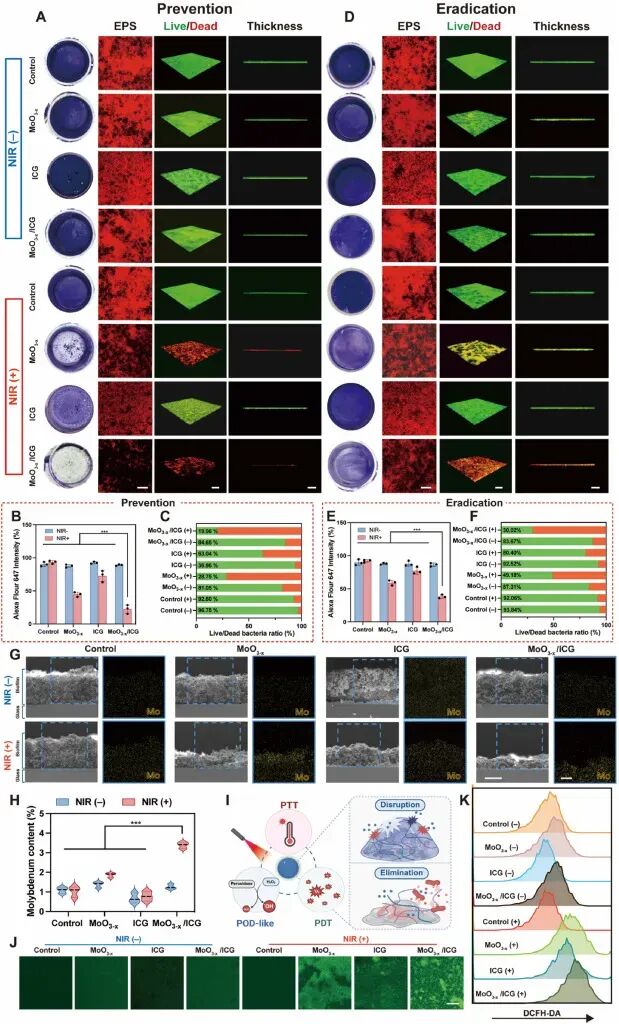
图4. 生物膜破坏与渗透:(A-C) 未成熟生物膜:结晶紫染色、EPS染色和CLSM显示,MoO₃₋ₓ/ICG+NIR显著抑制生物膜形成,EPS分泌减少,活菌比例大幅下降;(D-F) 成熟生物膜:同样处理后EPS结构塌陷、厚度减少、死菌增多;(G-H) SEM+EDS显示NIR照射后Mo元素在生物膜中含量增加3.22倍,证实纳米颗粒深层渗透增强;(I) 机制示意图;(J-K) ROS染色和流式证实NIR诱导大量ROS生成。该平台可同时预防和清除生物膜。
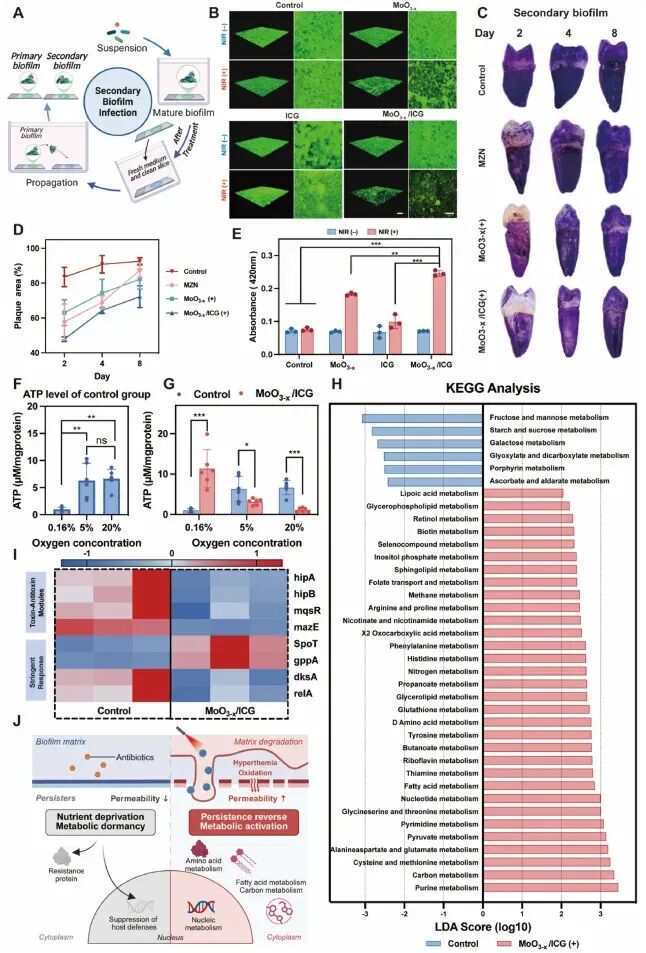
图5. 抑制二次生物膜形成及代谢激活机制:(A) 实验设计示意图;(B) CLSM显示MoO₃₋ₓ/ICG+NIR处理后远端盖玻片上二次生物膜形成最少(仅恢复32.39%);(C-D) 离体人牙模型:8天后对照组和甲硝唑组出现广泛菌斑迁移,而MoO₃₋ₓ/ICG+NIR组仍保持低覆盖;(E) 膜通透性增加2.42倍;(F-G) 不同氧浓度下ATP水平变化:厌氧条件下(模拟生物膜深层)处理后ATP水平显著升高,提示休眠菌被代谢激活;(H-I) 宏基因组分析显示处理组氨基酸/核苷酸代谢通路富集、持留相关基因(毒素-抗毒素系统)下调;(J) 机制示意图:热/氧化应激唤醒休眠菌,使其恢复药物敏感性。
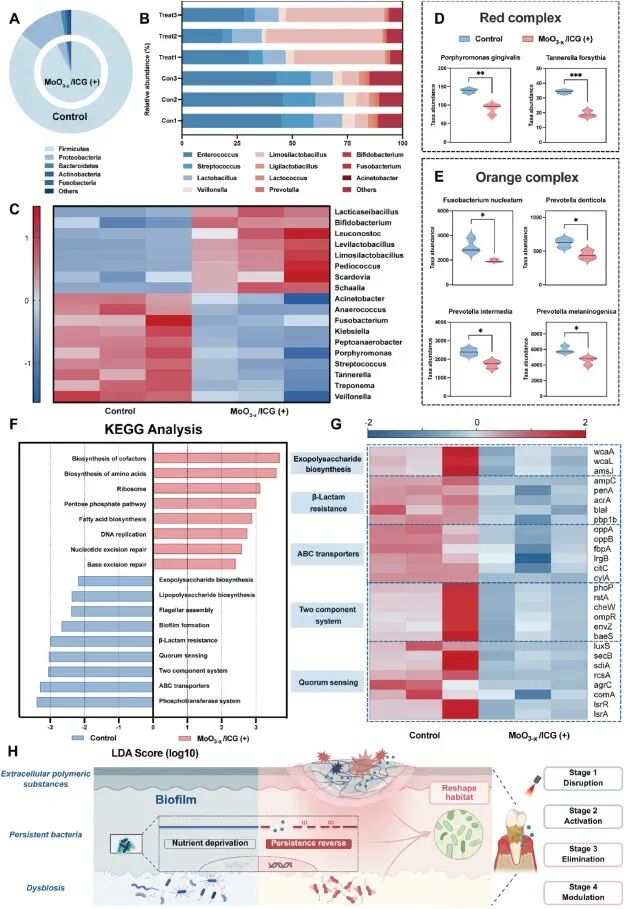
图6. 龈下微生物组重塑:(A-B) 门和属水平相对丰度;(C) 属水平热图显示MoO₃₋ₓ/ICG+NIR组中Anaerococcus、Fusobacterium、Porphyromonas等牙周病原菌减少,而乳杆菌、双歧杆菌等共生菌增加;(D-E) 红色复合体和橙色复合体病原菌丰度显著降低;(F) LEFSe分析显示处理组生物合成和应激反应通路富集;(G) EPS合成、β-内酰胺耐药、ABC转运蛋白、双组分系统、群体感应等毒力相关基因表达下调;(H) 总结“破坏-激活-清除-调节”策略。
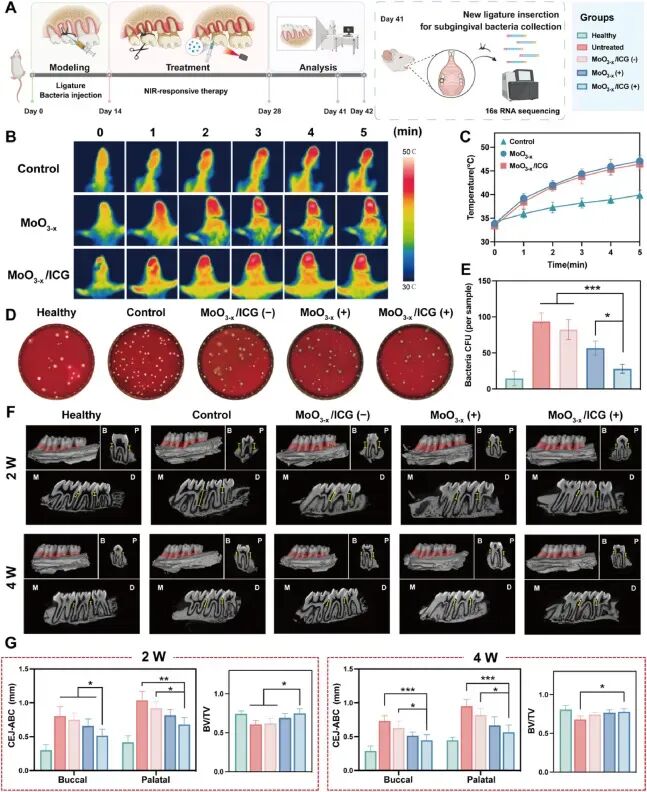
图7. 体内牙周炎治疗效果:(A) 动物模型和治疗方案;(B-C) 红外热像显示局部温度升至46-47℃;(D-E) 龈下细菌培养显示MoO₃₋ₓ/ICG+NIR组抗菌效率达83.12%;(F-G) micro-CT显示该组牙槽骨吸收最少,骨体积分数(BV/TV)最高,牙槽骨嵴顶-釉牙骨质界距离最小。
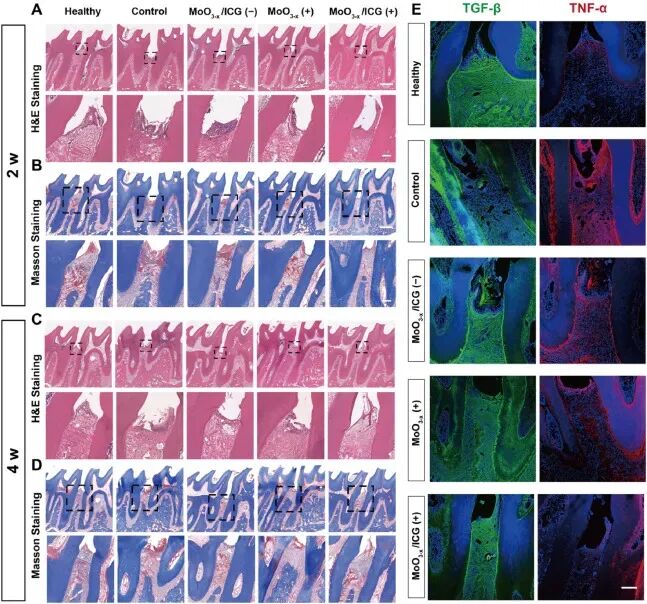
图8. 组织学与免疫荧光:(A-D) H&E和Masson染色显示MoO₃₋ₓ/ICG+NIR组炎症浸润减少、胶原纤维排列有序;(E) 免疫荧光显示TNF-α表达抑制、TGF-β表达上调,表明抗炎微环境建立。安全性评估:溶血率<2%,主要器官未见病理改变。
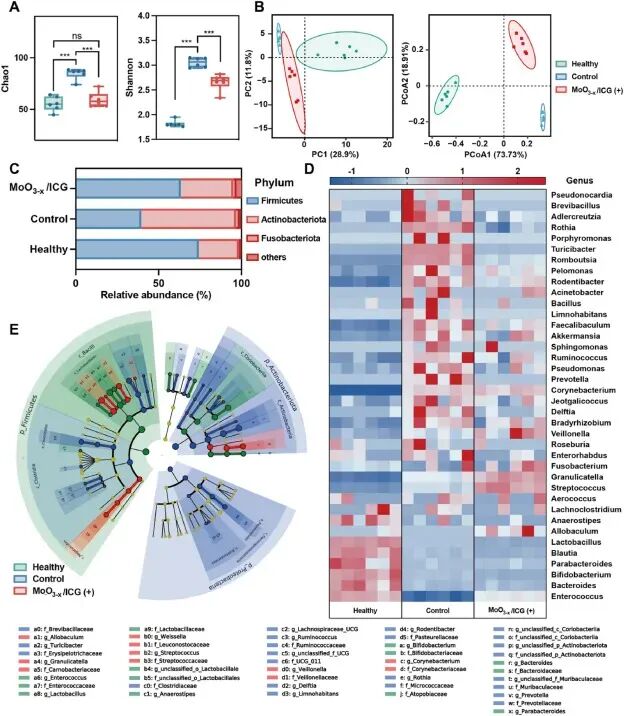
图9. 体内微生物组16S rRNA测序:(A) α多样性显示MoO₃₋ₓ/ICG(+)组Chao1和Shannon指数降低;(B) β多样性(PCA/PCoA)显示该组微生物群落结构向健康组靠近;(C-D) 门和属水平分析显示病原菌减少;(E) LEFSe鉴定差异菌群。证实该治疗能持久重塑龈下菌群,向健康状态转变。
结论
本研究成功构建了富含氧空位的MoO₃₋ₓ/ICG多功能纳米平台,该平台整合了光热治疗、光动力治疗和类过氧化物酶催化活性。在近红外光照射下,它通过“破坏EPS基质→唤醒休眠持留菌→彻底清除细菌→重塑健康微生物组”的连续策略,有效靶向牙周生物膜的整个生命周期。体外和体内实验证明,该平台不仅能高效杀灭浮游菌和生物膜内细菌,还能防止二次生物膜形成和感染复发。宏基因组和16S rRNA测序证实,治疗后的龈下微生物组中牙周病原菌(红色复合体、橙色复合体)丰度显著降低,共生菌得以恢复。该工作为顽固性牙周生物膜感染提供了一种全周期、生态调节型的新型治疗策略。
原文链接:
https://doi.org/10.1016/j.biomaterials.2026.124233


