论文解读|Jing Ma/Tianyu Zhang/Dong Liu教授团队揭示GBX2基因变异与颅面微小症的关系
时间:2026-05-05 17:09:16 热度:37.1℃ 作者:网络
颅面微小症(Craniofacial microsomia,CFM)是颅神经嵴细胞及第一、第二咽弓发育异常所致的先天性畸形。临床表现跨度大,从单纯耳廓畸形到上颌骨、下颌骨发育不全、面部不对称、眼眶发育不良均可出现。SF3B2、HOXA2、FOXI3等基因虽已被证实与CFM相关,但多数病例的遗传病因仍不清楚。GBX2编码一种对颅神经嵴细胞亚群迁移和存活至关重要的转录因子。全基因组关联研究曾将其所在区域列为CFM易感位点,但此前未报道过该基因的致病变异。
复旦大学的Jing Ma/Tianyu Zhang教授团队和南通大学的Dong Liu教授团队合作在本刊发表了题为“Pathogenic variants in GBX2 cause craniofacial microsomia”的研究快讯。该研究首次在CFM患者中检出GBX2的两个罕见错义变异。体外转录活性实验和斑马鱼功能验证表明,这些变异导致蛋白功能丧失,颅神经嵴细胞增殖受阻,进而引发CFM表型。
1. 研究方法
研究团队对201个CFM家系进行全外显子测序,筛选与表型共分离的罕见变异。在HEK-293T细胞中进行荧光素酶报告基因实验,将野生型或突变型GBX2与EEF1A1核心启动子报告质粒共转染,检测各变异的转录激活能力。同时构建斑马鱼模型,利用CRISPR干扰技术敲低gbx2表达,结合Tg(sox10:GFP) 转基因品系观察颅神经嵴细胞动态。通过共注射野生型或突变型人源GBX2 mRNA进行挽救实验,并以BrdU掺入实验检测细胞增殖。此外,利用ZESTA斑马鱼时空转录组图谱及单细胞转录组数据分析gbx2的表达模式。
2. 研究结果
研究团队在3个无亲缘关系的CFM家系中检出GBX2的两个罕见杂合错义变异:c.11C>T (p.Ala4Val) 和c.201G>C (p.Gln67His)。这两个变异均与家系内CFM表型共分离,呈常染色体显性遗传。保守性分析显示,两个位点的氨基酸在脊椎动物中高度保守(图1A–C)。
荧光素酶实验显示,与野生型相比,p.Ala4Val和p.Gln67His均显著降低EEF1A1启动子活性,提示两种变异削弱了GBX2的转录激活功能(图1E、F)。单细胞转录组数据显示,gbx2表达主要集中于神经嵴和早期咽弓谱系细胞(图1G–I)。
gbx2敲低斑马鱼胚胎在24 hpf时颅神经嵴细胞数量与对照组相当,但48 hpf时显著减少;72 hpf时出现咽弓软骨发育不全(图1J)。BrdU实验显示,gbx2敲低胚胎在24 hpf时增殖期颅神经嵴细胞显著减少(图1K)。挽救实验显示,野生型人源GBX2 mRNA可恢复颅神经嵴细胞数量和软骨形态,而两种突变型mRNA均无法挽救表型。p.Ala4Val的挽救失败尤为明显,这与携带该变异的患者临床表现更重相一致(图1J)。
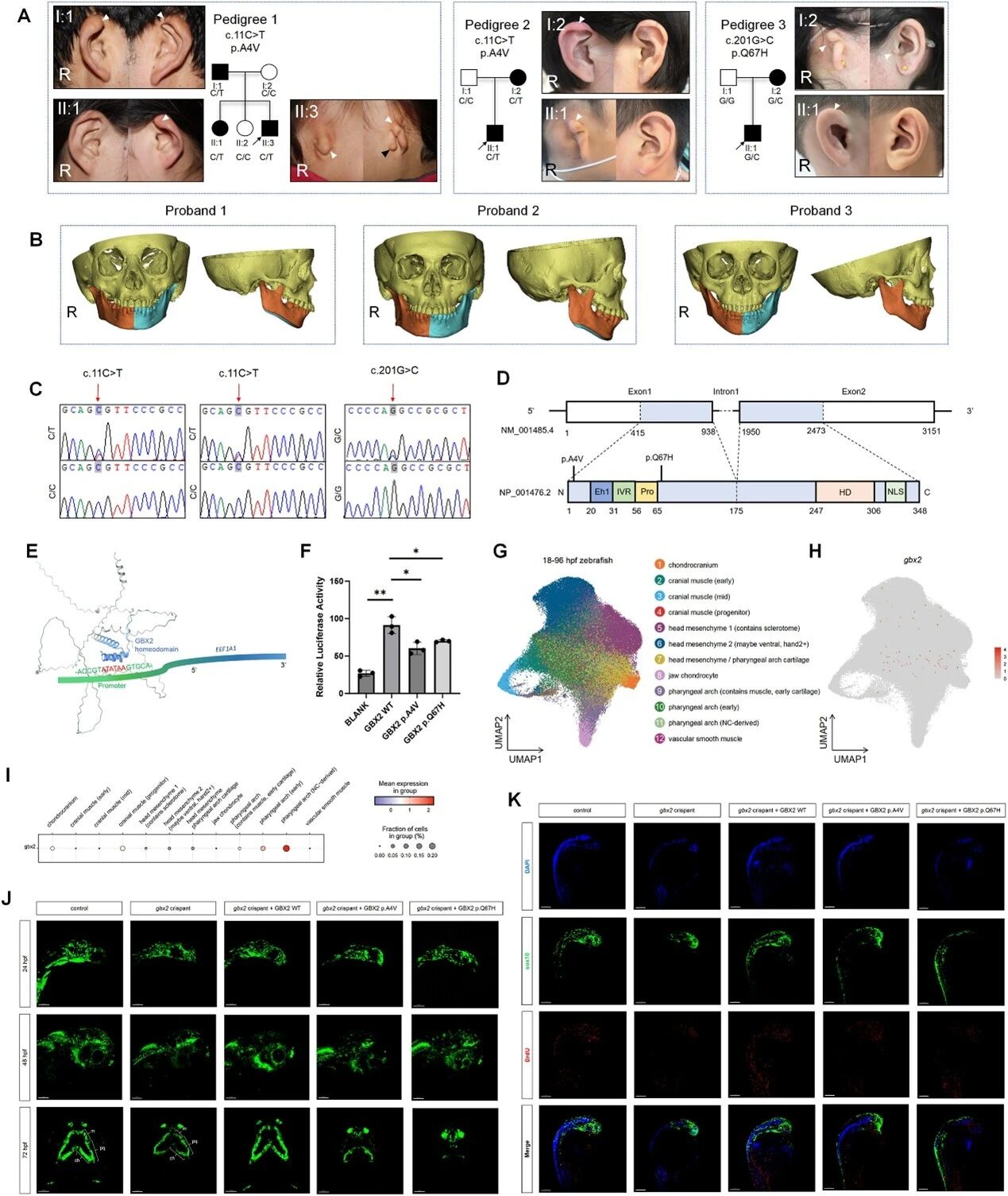
图1 GBX2的致病变异导致颅面微小症
3. 研究结论
本研究首次检出GBX2的p.Ala4Val和p.Gln67His两个错义变异。体外转录活性实验和斑马鱼功能验证证实,这些变异导致功能丧失。GBX2对颅神经嵴细胞增殖不可或缺,其功能缺失使细胞数量不足,咽弓软骨因“原料”匮乏而发育不全,最终表现为CFM。据估计,约1.5%的CFM病例可归因于GBX2变异。该研究为CFM遗传诊断提供了新靶点,也为理解颅面发育的分子机制补充了证据。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304225003034
引用这篇文章:
Yang R, Han W, Wang L, et al. Pathogenic variants in GBX2 cause craniofacial microsomia. Genes Dis. 2026;13(4):101814.


