【论著】基于弥散张量成像分析脑小血管病患者白质结构改变及其与步态障碍的相关性研究
时间:2026-05-05 17:07:57 热度:37.1℃ 作者:网络
摘要:目的采用自动纤维定量(AFQ)技术基于弥散张量成像(DTI)分析脑小血管病(CSVD)患者白质纤维束微结构改变及其与步态障碍的关系。方法前瞻性纳入2024年9月至2025年5月于徐州医科大学第二附属医院神经内科门诊就诊或住院的CSVD患者。收集患者的临床资料,包括人口统计学资料(年龄、性别、受教育年限、体质量指数)、脑血管危险因素(高血压病、糖尿病、卒中史、高脂血症、吸烟史、饮酒史)、实验室检查(总胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、脂蛋白a、空腹血糖、糖化血红蛋白、同型半胱氨酸、尿酸、肌酐)、入组后72h内蒙特利尔认知评估量表视空间执行功能评分、脑室旁白质高信号评分、深部白质高信号评分、腔隙性脑梗死、脑微出血、扩大的血管周围间隙(>10个)、脑萎缩、偶发扩散加权成像阳性、皮质微梗死、皮质表面铁沉积。入组72h内采用可穿戴运动及步态量化评估系统对所有患者进行步态分析并获取多组步态参数:基础时空参数[起立-行走测试(TUG)时间、步速、步频、行走时长、坐下时长、起立时长、步长、跨步长、支撑相、摆动相]、行走平衡性参数(步长变异度及躯干前、后、左、右倾角度峰值)、对称性参数(步长不对称性)、转向灵活参数(转向时长、转向过程角速度峰值、转向过程平均角速度)、协调性(相对平均相位差、相位协调指数、左右脚协调性)。所有患者入组72h内均完成简易体能状态量表(SPPB)评估。根据SPPB评分将所有患者分为步态正常组(SPPB评分≥10分)和步态障碍组(SPPB评分<10分);采集3.0T MRI-DTI数据,依据约翰霍普金斯大学白质纤维束图谱及路径点,将全脑流线分为20条白质纤维束,并将每条纤维束等距划分为100个节点,采用AFQ技术提取每条白质纤维束100个节点的各向异性分数(FA)、平均扩散率(MD)、轴向扩散率(AD)、径向扩散率(RD)。比较两组患者的临床资料、步态参数及影像学资料,采用偏态相关性分析探究各步态参数与各白质纤维束所有节点FA、MD、AD、RD平均值的相关性;为进一步控制混杂因素的影响,以各步态参数及SPPB评分为因变量,以与步态参数有相关性的纤维束节段FA、MD、AD、RD平均值为自变量并对自变量进行多重共线性检验,排除存在共线性[容差<0.1或方差膨胀因子(VIF)>10]的变量后采用逐步回归法进行多元线性回归分析,探究纤维束不同节段FA、MD、AD、RD平均值与各步态参数的关系。结果共纳入60例CSVD患者,男31例,女29例,年龄45~80岁,平均(64±11)岁,其中步态正常组31例,步态障碍组29例。(1)与步态障碍组比较,步态正常组患者的受教育年限更长,体质量指数更低(均P<0.05),余临床资料的组间差异均无统计学意义(均P>0.05);与步态正常组相比,步态障碍组患者的TUG时间、行走时长、步长变异度、转向时长均更高,步速、步长、跨步长、转向过程角速度峰值、转向过程平均角速度均更低(均P<0.05)。(2)步态障碍组的左侧扣带前部(节点10-20、30-35)的FA均低于步态正常组[经错误发现率(FDR)校正,均P<0.05];左下纵束前部(节点1-43、53-56)MD、左侧扣带前中部(节点12-17、29-60)RD、左下纵束前部(节点10-29)AD均高于步态正常组(经FDR校正,均P<0.05)。(3)偏态相关性分析结果显示,左侧扣带前部(节点10-20)FA平均值与转向时长(r=-0.330,P=0.027)成负相关,与转向过程角速度峰值(r=0.301,P=0.045)、转向过程平均角速度(r=0.355,P=0.017)成正相关;左下纵束前部(节点1-43)MD平均值与步速(r=-0.306,P=0.039)、步长(r=-0.344,P=0.019)、跨步长(r=-0.347,P=0.018)成负相关;左侧扣带前中部(节点29-60)RD平均值与TUG时间(r=0.326,P=0.029)、行走时长(r=0.383,P=0.009)、转向时长(r=0.512,P=0.001)成正相关,与步速(r=-0.304,P=0.042)、转向过程平均角速度(r=-0.504,P=0.001)、转向过程角速度峰值(r=-0.466,P=0.001)成负相关;左下纵束前部(节点10-29)AD平均值与步速(r=-0.354,P=0.016)、步长(r=-0.337,P=0.022)、跨步长(r=-0.347,P=0.018)、转向过程平均角速度(r=-0.341,P=0.020)成负相关,与行走时长(r=0.323,P=0.029)、坐下时长(r=0.383,P=0.009)成正相关。余步态参数与纤维束节段指标平均值均无相关性(均P>0.05)。(4)共线性分析显示,无存在共线性的变量。多元线性回归分析显示,控制混杂因素后,左下纵束前部(节点1-43)MD平均值与步长(β=-0.380,P=0.008)、跨步长(β=-0.431,P=0.002)成负相关;左下纵束前部(节点10-29)AD平均值与转向过程平均角速度成负相关(β=-0.391,P=0.007);左侧扣带前中部(节点29-60)RD平均值与TUG时间(β=0.667,P=0.002)、行走时长(β=0.387,P=0.007)及SPPB评分(β=0.413,P=0.002)成正相关,与步速(β=-0.706,P=0.013)及转向过程角速度峰值(β=-0.296,P=0.040)成负相关。余纤维束节段FA、MD、AD、RD平均值均与各步态参数及SPPB评分无相关性(均P>0.05)。结论CSVD步态障碍患者的左侧扣带前部、左下纵束前部白质微结构存在多节段损伤,且影响其步态功能。
脑小血管病(cerebral small vessel disease, CSVD)是指各种病因影响脑内小动脉及其远端分支、毛细血管及小静脉所致的一系列临床-影像-病理综合征[1]。步态障碍是CSVD患者仅次于认知障碍的第二大临床表现[2],表现为步速下降、步幅缩短及双支撑时间延长[3],可导致平衡失控,进而增加跌倒、失能、死亡等风险[4]。弥散张量成像(diffusion tensor imaging, DTI)可于CSVD常规影像学特征出现前敏感检测到白质微结构损害,其为CSVD进展的敏感标志物[5-6]。
既往采用感兴趣区分析[7]、基于体素的形态学分析[8]、基于纤维束示踪的空间统计分析[9]等方法的研究表明,CSVD患者步态障碍与胼胝体、放射冠、皮质脊髓束及上纵束等白质纤维的弥散指标异常密切相关[10]。然而有研究显示,即使CSVD患者的部分纤维束整体各向异性分数(fractional anisotropy, FA)或平均扩散率(mean diffusivity, MD)在正常范围内,其内部也可发生节段性微结构损伤[11],传统基于纤维束示踪的空间统计分析、体素分析、感兴趣区分析均将纤维束作为整体进行分析,易忽略纤维束局部变化,也无法精确定位其与临床症状同步的关键节点。自动纤维定量(automatic fiber quantification, AFQ)技术[12]可将白质纤维束细分为100个等距节段,逐点提取、分析DTI参数以探索白质纤维束局部微结构改变,其对纤维束损伤的敏感度优于基于感兴趣区、体素及纤维束示踪等常规分析方法[7-9]。本研究拟基于DTI,采用AFQ技术聚焦纤维束节段,探索CSVD伴步态障碍患者的白质纤维束微结构改变及其与步态障碍的关系。
1 对象与方法
1.1 对象
前瞻性纳入2024年9月至2025年5月于徐州医科大学第二附属医院神经内科门诊就诊或住院的CSVD患者。本研究方案经徐州医科大学第二附属医院医学伦理委员会审核批准(伦理审批号:[2024]080301)。所有患者签署了研究知情同意书。
纳入标准:(1)年龄45~80岁;(2)经3.0T MR检查确认CSVD符合以下影像学表现[13]中的至少一项:近期皮质下小梗死、可能血管源性腔隙性脑梗死、可能血管源性脑白质高信号、扩大的血管周围间隙、脑微出血、皮质表面铁沉积、脑萎缩和皮质微梗死、偶发扩散加权成像(DWI)阳性。
排除标准:(1)既往卒中后遗留肌力Ⅳ级及以下,或遗留明显共济失调或忽视;(2)合并颅内外大血管狭窄(狭窄率≥50%);(3)存在先天性智力障碍、脑外伤史及严重神经、精神疾病,有精神活性物质滥用史;(4)已被明确诊断的恶性肿瘤、重要脏器衰竭,预期寿命少于3年;(5)严重的视力(最佳矫正视力<0.3,糖尿病视网膜病变,核性白内障≥2级)或听力损害可能无法配合神经心理评估者,或存在MRI检查禁忌证;(6)有严重影响步态功能评估或临床表现为异常步态的疾病,如卒中后偏瘫、严重的腰椎病、膝关节病、帕金森病、老年性前庭病、直立性低血压等。
1.2 资料收集
收集入组患者的临床资料,包括人口统计学资料(年龄、性别、受教育年限、体质量指数)、脑血管危险因素(高血压病[14]、糖尿病[15]、卒中史[16]、高脂血症[17]、吸烟史[18]、饮酒史[18])、实验室检查(总胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、脂蛋白a、空腹血糖、糖化血红蛋白、同型半胱氨酸、尿酸、肌酐)、蒙特利尔认知评估量表视空间执行功能[19]评分。所有血液样本均在患者入组48h内空腹状态采集,视空间执行功能均在患者入组后72h内评估,以上所有实验室检查均在徐州医科大学第二附属医院完成。
1.3 步态功能评估
所有患者于入组72h内采用睿评可穿戴运动及步态量化评估系统(深圳臻络科技有限公司)进行步态分析。该设备由10个传感器、1个数据接收中心和1个上位机软件组成,将10个传感器分别放置于患者胸、腰、左右手腕、左右大腿、左右小腿及左右脚,以评估患者运动时上下肢、躯干、腰椎的客观步态变化,获取多组步态参数,包括基础时空参数[20][起立-行走测试(timed up and go test, TUG)时间、步速、步频、行走时长、坐下时长、起立时长、步长、跨步长、支撑相、摆动相]、行走平衡性参数(步长变异度及躯干前、后、左、右倾角度峰值)、对称性参数(步长不对称性)、转向灵活参数(转向时长、转向过程角速度峰值、转向过程平均角速度)、协调性(相对平均相位差、相位协调指数、左右脚协调性)。所有入组患者均于入组72h内完成简易体能状态量表(short physical performance battery, SPPB)[21]评估,评估方法:(1)平衡评估:完成并足站立10s、半串联站立10s、全串联站立10s各计1分,未坚持10s为0分;(2)步行速度评估:测量以日常速度行走4m所需时间并计算步速(m/s),步速>0.83m/s计4分,步速0.64~0.83m/s计3分,步速0.46~<0.64m/s计2分,步速<0.46m/s计1分,不能行走计0分;(3)起坐评估:双臂交叉抱于胸前,连续完成5次起坐,起坐总时间≤ 11.19s计4分,11.20~13.69s计3分, 13.70~16.69s计2分,≥16.70s计1分,不能完成计0分。TUG时间[22]评估方法:受试者从靠背椅(座高43cm)站起,以日常步速走3m越线折返,再返回坐下,所有患者重复2次TUG评估,计算2次的平均值作为最终的TUG时间。根据SPPB评分将所有患者分为步态正常组(SPPB评分≥10分)和步态障碍组(SPPB评分<10分)[4]。
1.4 影像学评估
采用美国GE Healthcare公司生产的Discovery MR750w3.0T MRI扫描仪进行全脑扫描。使用40通道头部和颈部线圈进行信号接收。DWI采用回波平面成像序列和自旋回波,参数如下:重复时间13ms,回波时间70ms,30个扩散方向,b(扩散敏感系数)=1000s/mm2,单次b=0s/mm2采集,视野为320mm×320mm×144mm,矩阵大小256×256,40层,层厚3.6mm。采集T2加权快速自旋回波、T2加权液体衰减反转恢复(FLAIR)、T1加权及磁敏感加权成像扫描,检测脑部异常。影像学评估均在患者入组后72h内完成。
1.4.1 CSVD影像学标志物采集:由2名具有5年以上脑血管病影像学诊断经验的的神经内科副主任医师在不知晓患者临床信息的情况下独立评估,意见不一致时通过协商达成一致。根据《脑小血管病MRI规范化应用专家共识》[23]基于MR评估所有CSVD患者影像学标志物,包括脑室旁白质高信号评分、深部白质高信号评分、腔隙性脑梗死、脑微出血、扩大的血管周围间隙(>10个)、脑萎缩、偶发DWI阳性、皮质微梗死、皮质表面铁沉积。
1.4.2 DTI序列预处理:所有DTI数据均在安装Ubuntu 22.04LTS操作系统的Linux工作站上完成预处理。(1)使用dcm2niix[24]转换工具将原始DICOM序列转换为NIfTI-1格式;(2)采用医学图像分析软件包(MRtrix3[25])以去除莱斯(Rician)热噪声、伪影及头动,并进行涡流校正;(3)偏置场校正:使用高级归一化工具(advanced normalization tools, ANTS)[26]进行偏置场校正;(4)张量拟合:采用牛津大学脑功能磁共振成像中心软件库[27]进行张量拟合,得到第一特征值(lambda 1,λ1)、第二特征值(lambda 2,λ2)、第三特征值(lambda 3,λ3)、FA、MD、轴向扩散率(axial diffusivity, AD)、径向扩散率(radial diffusivity, RD)图。
1.4.3 AFQ纤维束量化:将以上预处理后图像进一步导入AFQ软件中。AFQ[12]是一种能够自动识别大脑白质纤维束,并沿纤维束全长进行精细化定量分析的技术。以下操作均在Matrix Laboratory R2022b(数学计算与编程软件平台)中完成。(1)将T1结构像与前连合-后连合坐标系对齐,确保后续感兴趣区与纤维束解剖定位一致,感兴趣区共20个纤维束,分别为左(右)前丘脑辐射、左(右)皮质脊髓束、左(右)扣带、左(右)海马旁回、胼胝体主要(次要)力束、左(右)下额枕束、左(右)下纵束、左(右)上纵束、左(右)钩束、左(右)弓形束;(2)全脑纤维追踪:基于张量场进行概率流线追踪;(3)依据约翰霍普金斯大学白质纤维束图谱[28]及路径点,将全脑流线分为20条经典纤维束;(4)将异常纤维剔除,阈值参数设置如下:最大距纤维束中心距离为5mm;最大长度偏差倍数为4倍标准差;节点数为100;异常剔除迭代次数为5次;(5)在20条纤维束(每条纤维束包含100个等距节点)上提取FA、MD、AD、RD值。
1.5 统计学分析
采用SPSS 27.0软件进行统计学分析。采用Shapiro-Wilk法对计量资料进行正态性检验,符合正态分布的计量资料以x-±s表示,两组间比较采用独立样本t检验;不符合正态分布的计量资料以中位数和四分位数[M(P25,P75)]表示,两组间比较采用Mann-Whitney U秩和检验。计数资料以例(%)表示,两组间比较采用χ2检验。多重比较采用错误发现率(false discovery rate,FDR)法进行校正。采用偏态相关性分析探究各步态参数与组间比较差异有统计学意义的各白质纤维束节段所有节点FA、MD、AD、RD平均值的相关性;为进一步探究纤维束不同节段的FA、MD、AD、RD平均值与各步态参数的关系,控制年龄、性别、受教育年限、BMI、高血压病、糖尿病、卒中史、脑室旁及深部白质高信号评分、扩大的血管周围间隙等混杂因素的影响,以偏态相关性分析中与纤维束节段相关的步态参数及SPPB评分为因变量,以偏态相关性分析中与步态参数有相关性的纤维束节段FA、MD、AD、RD平均值为自变量,并对自变量进行多重共线性检验,排除存在共线性[容差<0.1或方差膨胀因子(variance inflation factor, VIF)>10]的变量,采用逐步回归法进行多元线性回归分析。以P<0.05为差异有统计学意义
2 结果
共纳入60例CSVD患者,男31例,女29例,年龄45~80岁,平均(64±11)岁,其中步态正常组31例,步态障碍组29例。
2.1 临床资料比较
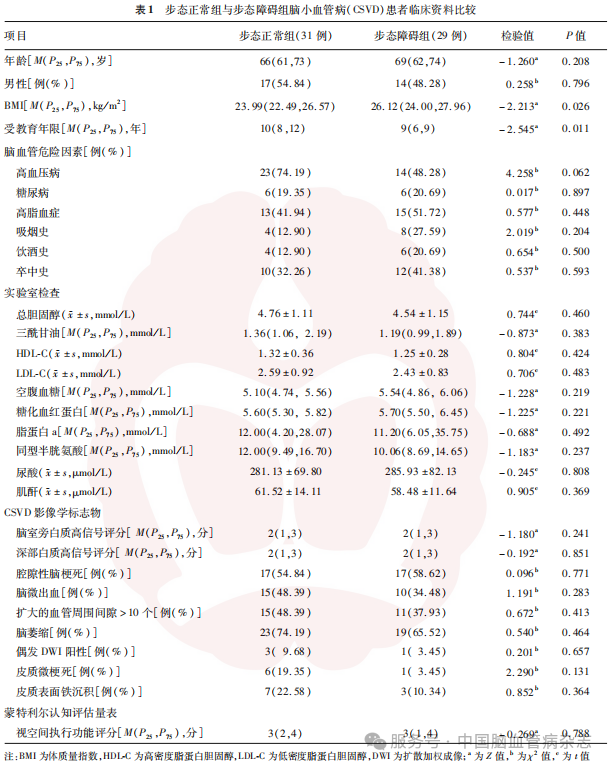
与步态障碍组比较,步态正常组患者的受教育年限更长,体质量指数更低(均P<0.05),余临床资料的组间差异均无统计学意义(均P>0.05)。见表1。
2.2 步态参数比较
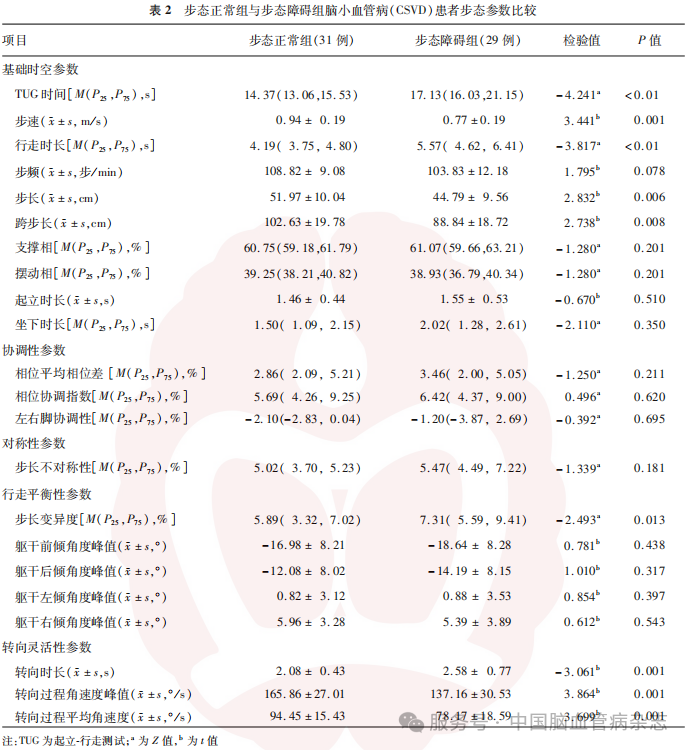
与步态正常组相比,步态障碍组患者的TUG时间、行走时长、步长变异度、转向时长均更高,步速、步长、跨步长、转向过程角速度峰值、转向过程平均角速度均更低(均P<0.05)。见表2。
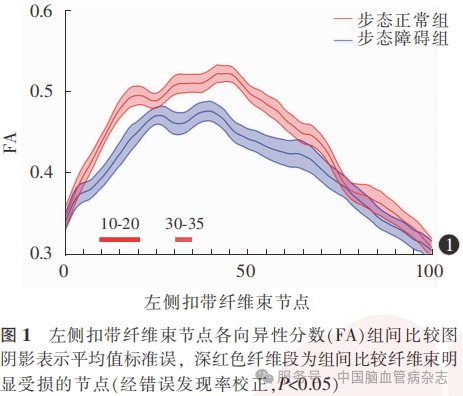
2.3 FA的组间比较
步态障碍组的左侧扣带前部(节点10-20、30-35)的FA均低于步态正常组(经FDR校正,均P<0.05),余各纤维束各节点FA的组间差异均无统计学意义(经FDR校正,均P>0.05)。见图1。
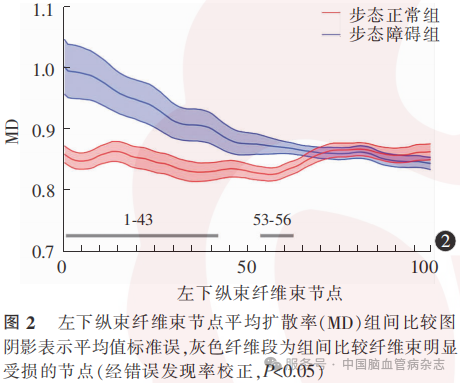
2.4 MD的组间比较
步态障碍组左下纵束前部(节点1-43、53-56)的MD高于步态正常组(经FDR校正,均P<0.05),余各纤维束各节点MD的组间差异均无统计学意义(经FDR校正,均P>0.05)。见图2。
2.5 RD的组间比较
步态障碍组左侧扣带前中部(节点12-17、29-60)的RD高于步态正常组(经FDR校正,均P<0.05),余各纤维束各节点RD的组间差异均无统计学意义(经FDR校正,均P>0.05)。见图3。
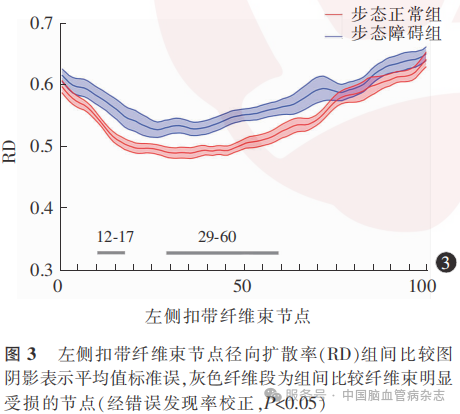
2.6 AD的组间比较
步态障碍组左下纵束前部(节点10-29)的AD高于步态正常组(经FDR校正,均P<0.05),余各纤维束各节点AD的组间差异均无统计学意义(经FDR校正,均P>0.05)。见图4。
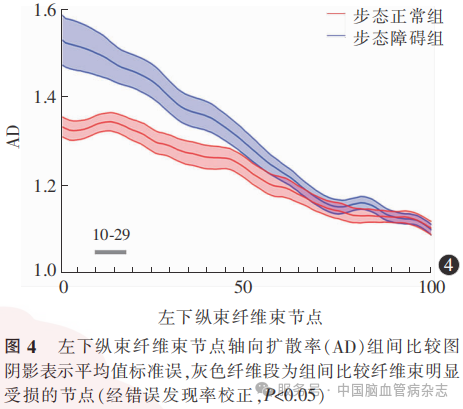
2.7 步态参数与纤维束FA、MD、AD、RD平均值的偏态相关性分析
将年龄、性别、BMI、受教育年限、高血压病、糖尿病、卒中史作为协变量,将组间比较有统计学意义的纤维束节段指标求平均值后与各步态参数进行偏态相关性分析,结果显示,左侧扣带前部(节点10-20)FA平均值与转向时长(r=-0.330,P=0.027)成负相关,与转向过程角速度峰值(r=0.301,P=0.045)、转向过程平均角速度(r=0.355,P=0.017)成正相关;左下纵束前部(节点1-43)MD平均值与步速(r=-0.306,P=0.039)、步长(r=-0.344,P=0.019)、跨步长(r=-0.347,P=0.018)成负相关;左侧扣带前中部(节点29-60)RD平均值与TUG时间(r=0.326,P=0.029)、行走时长(r=0.383,P=0.009)、转向时长(r=0.512,P=0.001)成正相关,与步速(r=-0.304,P=0.042)、转向过程平均角速度(r=-0.504,P=0.001)、转向过程角速度峰值(r=-0.466,P=0.001)成负相关;左下纵束前部(节点10-29)AD平均值与步速(r=-0.354,P=0.016)、步长(r=-0.337,P=0.022)、跨步长(r=-0.347,P=0.018)、转向过程平均角速度(r=-0.341,P=0.020)成负相关,与行走时长(r=0.323,P=0.029)、坐下时长(r=0.383,P=0.009)成正相关。余各步态参数与纤维束节段指标平均值均无相关性(均P>0.05)。
2.8 CSVD患者步态参数及SPPB评分与纤维束FA、MD、AD、RD平均值的多元线性回归分析
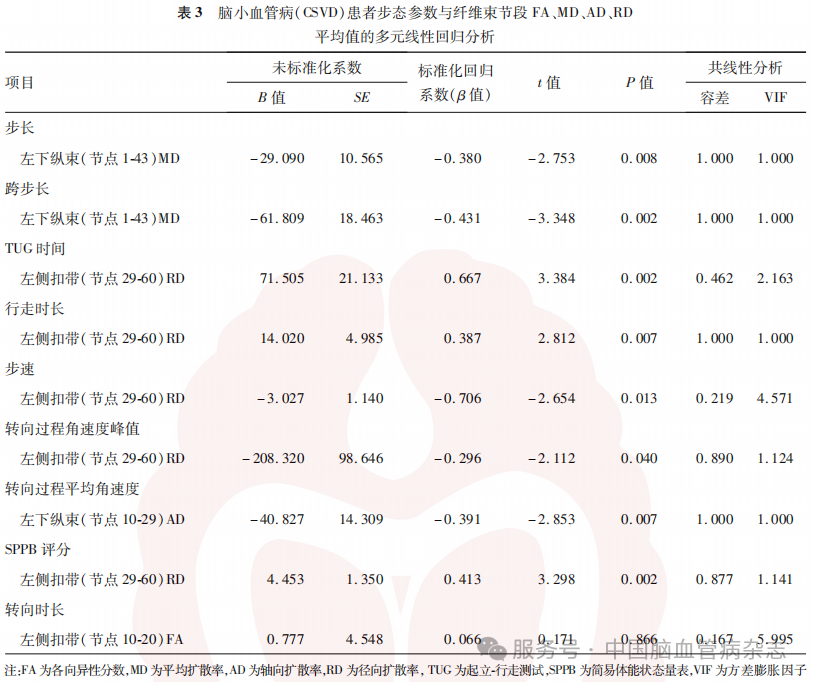
共线性分析显示,无存在共线性的变量。分别以偏态相关性分析中与纤维束节段有相关性的步态参数及SPPB评分为因变量,以偏态相关性分析中有相关性的纤维束节段FA、MD、AD、RD平均值为自变量,控制混杂因素年龄、性别、受教育年限、BMI、高血压病、糖尿病、卒中史、脑室旁白质高信号评分、深部白质高信号评分、扩大的血管周围间隙后进行线性回归分析,结果显示,左下纵束前部(节点1-43)MD平均值与步长(β=-0.380,P=0.008)、跨步长(β=-0.431,P=0.002)成负相关;左下纵束前部(节点10-29)AD平均值与转向过程平均角速度成负相关(β=-0.391,P=0.007);左侧扣带前中部(节点29-60)RD平均值与TUG时间(β=0.667,P=0.002)、行走时长(β=0.387,P=0.007)及SPPB评分(β=0.413,P=0.002)成正相关,与步速(β=-0.706,P=0.013)及转向过程角速度峰值(β=-0.296,P=0.040)成负相关。余纤维束节段FA、MD、AD、RD平均值均与各步态参数及SPPB评分无相关性(均P>0.05)。见表3。
3 讨论
Grønvik等[29]纳入1289例70岁以上社区老年人进行连续7d的可穿戴加速度计监测,根据SPPB评分分为高分(10~12分)组、中分(7~9分)组、低分(0~6分)组,结果显示,高分组老年人每日步数最多、步速最快、步行距离最长(均P<0.05),提示老年人SPPB评分越高运动能力越好。《老年人运动能力下降多学科决策模式中国专家共识(2024版)》[4]推荐可采用SPPB进行运动能力评估,以SPPB评分<10分作为运动能力下降的诊断标准(A级推荐)。参考既往研究结果,本研究根据SPPB评分将所有患者分为步态正常组(≥10分)和步态障碍组(<10分),采用新型多节点可穿戴运动及步态量化系统评估CSVD患者的步态参数,结果显示,与步态正常组患者比较,步态障碍组患者表现为步速减慢、步长缩短、转向迟缓、起立坐下时间延长、行走不稳定。为进一步了解CSVD患者纤维束损伤的特点,本研究采用概率流线追踪重建全脑白质纤维束,基于AFQ技术将纤维束等距划分为100个节点,结果显示,CSVD患者不同纤维束节段损伤可能介导了不同步态功能的下降,其白质纤维束损伤成“节段优先”模式,而非各纤维束弥漫性同步受累。
有研究认为,CSVD患者出现步态障碍主要由额叶皮质-皮质下环路受损中断引起[30],环路是由胼胝体、扣带回、额枕束、弓形束、钩束等白质纤维束连接而成[31],任何一段纤维束破坏均可能导致动作计划、启动与执行的链式失效,并增加跌倒风险[32]。Boa Sorte Silva等[33]纳入64例CSVD伴轻度认知障碍(蒙特利尔认知评估量表评分<26分,且简易精神状态检查量表评分≥20分)的老年患者的研究显示,扣带回(r=-0.30,P=0.015)、后放射冠(r=-0.26,P=0.039)和胼胝体(r=-0.26,P=0.040)的髓鞘含量降低与步态周期时间变异性增加相关,提示上述纤维束出现微结构损伤。但纤维束走行全程较长,微结构损伤可能并非同时发生[11],因此本研究将白质纤维束位点进一步细化,结果显示,步态障碍组的左侧扣带前中部(节点10-20、29-60)、左下纵束前中部(节点1-43、53-56)均出现明显微结构损害,偏态相关性分析显示,左下纵束前部(节点10-29)AD平均值不仅与步速、步长、跨步长、行走时长、转向过程平均角速度相关,且进一步线性相关性分析显示其与转向过程平均角速度成负相关;此外,偏态相关分析结果显示,左下纵束前部(节点1-43)MD平均值与步速、步长、跨步长成负相关,进一步线性回归分析显示,其与步长、跨步长成负相关,提示左下纵束前部纤维束段受损时,CSVD患者出现步长、跨步长缩短,转向过程平均角速度变慢。
下纵束是连接枕-颞叶的长联络纤维束,起自枕叶外纹状皮质,向前贯穿整个颞叶白质,止于颞叶和杏仁核-海马旁回前区[34]。该纤维束自身无独立供血动脉,血供依赖于皮质-皮质下动脉终末支,纤维束前段以大脑中动脉的颞极动脉及颞前动脉供血,后段以大脑后动脉的距状沟动脉、枕外侧动脉及颞下后动脉皮质支供血,中段为大脑后动脉颞下前、中动脉与脉络膜前动脉的分水岭区[35]。由于白质血流量低、侧支稀少,当主干动脉出现狭窄或低灌注时,下纵束可能在尚未出现梗死灶的情况下首先出现白质微结构的损伤。既往研究显示,下纵束损伤多与视觉[36]、情绪[37]、记忆[38]障碍有关,较少关注其与步态功能的关系。近年研究显示,下纵束完整性也可影响步态稳定性,一项研究纳入22例唐氏综合征患者,采用基于体素的分析方法评估白质微结构,结果显示,步时变异度[采用可穿戴运动及步态量化评估系统(GaitRite系统)自动测量连续步态周期(步时)的波动程度]与下纵束平均FA值成负相关(经多重比较校正,P<0.05)[38]。本研究多元线性回归分析显示,步态障碍组左下纵束前部出现损伤,且其与步长、跨步长、转向过程平均角速度相关,下纵束前部损伤程度越重,步长、跨步长越短,转向过程平均角速度越慢,推测下纵束易受血供降低影响而出现受损,进而影响步态功能下降。
本研究结果显示,步态障碍组的左侧扣带前中部(节点10-20、29-60)出现微结构损害,且偏态相关性分析结果显示,左侧扣带(节点10-20)FA平均值与转向时长成负相关,与转向过程角速度峰值、转向过程平均角速度成正相关,左侧扣带(节点29-60)RD平均值与TUG时间、转向时长、行走时长成正相关,与步速、转向过程平均角速度、转向过程角速度峰值成负相关,进一步线性回归分析显示,左侧扣带(节点10-20)FA平均值与转向时长成负相关,左侧扣带(节点29-60)RD平均值与TUG时间、行走时长成正相关,与步速、转向过程角速度峰值成负相关,提示左侧扣带前中部(节点29-60)损伤程度越重,步速及转向速度越慢,行走时间越长。扣带束位于扣带回深部,成“弓”形环抱胼胝体,起始至额叶亚鼻区,沿扣带回向后绕过胼胝体压部,最终止于海马旁回及钩回[39],其长纤维连接前额叶、前扣带皮质、后扣带皮质与海马结构,短纤维联络邻近顶、枕叶,构成情绪、记忆、运动调节的核心白质通道[40]。Haddad等[41]研究纳入44例轻度认知障碍(主观认知下降主诉伴客观认知损害、日常生活能力保留、排除痴呆)患者及40例认知正常(无认知下降主诉、认知筛查正常且排除痴呆)者作为对照组,采用概率性纤维追踪分析方法重建纤维束,并测量所有受试者单任务及双任务步态速度,结果显示,与对照组比较,轻度认知障碍患者的扣带回终末段FA平均值降低、RD平均值升高(均P<0.05),且该区域的FA平均值与双任务步态速度成正相关(β=0.373,P=0.001),该区域RD平均值与单任务步态速度成负相关(β=-0.374,P=0.002),提示扣带纤维束白质结构损伤与步态异常密切相关。Pappas等[42]纳入166例社区老年人(60~89岁),按照是否携带载脂蛋白E4基因和临床痴呆评定量表(0分为认知正常;0.5分为认知障碍)评估结果分为载脂蛋白E4携带组(77例;认知正常53例,认知障碍24例)、非载脂蛋白E4携带组(89例;认知正常70例,认知障碍19例),采用伪连续动脉自旋标记MRI评估脑血流,DTI评估扣带纤维束白质微结构,结果显示,与非载脂蛋白E4携带者相比,载脂蛋白E4携带者后扣带皮质脑血流降低[(46.4±9.6)ml/(100g·min)比(50.3±9.8)ml/(100g·min),P=0.002],且中介分析显示,后扣带皮质低灌注对记忆功能下降(采用听觉词语学习测试延迟回忆评估)的影响通过扣带束完整性下降(FA下降)介导(间接效应β=-0.7936, 95% CI: -124.1293~-0.1541),提示载脂蛋白E4携带者的扣带束白质灌注不足导致纤维束微结构损伤,从而出现认知功能下降。因此本研究中CSVD患者扣带前中部白质灌注不足可能是导致脑白质纤维束微结构损伤,进而影响患者步态功能的原因。
本研究存在以下局限性:(1)本研究为横断面研究,无法确定白质纤维束改变与步态障碍的因果关系,也无法观察代偿-失代偿的动态过程;(2)本研究为单中心、小样本研究,未纳入健康对照组,可能导致阈值估计偏高;(3)尽管已选择较轻、方便佩戴的可穿戴运动传感器,但设备本身存在对受试者步态干扰的可能,步态参数采集于标准化实验环境,与自然状态存在差异,且步态测试仅在静态地面进行,未加入双任务、斜坡或避障场景,可能低估真实生活中的相关风险。
综上所述,CSVD患者的白质纤维束微结构改变影响步态功能,左下纵束前部MD与步长、跨步长成负相关,其AD与转向过程平均角速度成负相关;左侧扣带前中部RD与TUG时间、行走时长成正相关,与步速、转向过程角速度峰值成负相关,其FA与转向时长成正相关,对纤维束的评估或可为CSVD患者步态障碍提供早期预警及康复靶点。


