肺癌围术期疼痛管理专家共识(2026版)
时间:2026-05-05 17:07:40 热度:37.1℃ 作者:网络
摘 要
本共识基于广泛的循证医学证据,结合改良的德尔菲法和专家会议讨论,由外科学、疼痛医学、麻醉学及肿瘤学等多学科专家团队共同制定,最终形成 14 条推荐意见。共识内容系统涵盖肺癌围术期疼痛管理的全流程,旨在规范临床疼痛管理路径,提升患者术后恢复质量并改善长期预后。本共识为肺癌围术期疼痛管理的规范化、系统化实施提供了重要指导,对改善患者术后生活质量及促进加速康复具有积极意义。
1 共识制定流程和方法
1.1 共识发起机构与专家组成员
本共识由肺癌围术期疼痛管理专家组牵头,联合胸外科、麻醉科、疼痛科、肿瘤科、精神心理科、临床药学及护理学等多学科专家共同制定。项目于 2024 年 10 月 12 日启动,先后召开 2次中期审稿会(2025 年 9 月 4、21 日),经过线上线下反复讨论与修订,于 2025 年 11 月 16 日定稿。本共识已在国际实践指南注册与透明化平台注册(注册号:PREPARE-2025CN1471)。共识制定过程遵循 2014 年《世界卫生组织指南制订手册》及 2022 年《中国制订/修订临床诊疗指南的指导原则(2022 版)》。
1.2 共识的使用者与应用的目标人群
本共识主要适用于从事肺癌围术期诊疗工作的胸外科、麻醉科、疼痛科、肿瘤科及相关护理人员。目标人群为拟接受或已接受肺癌手术的围术期患者。
1.3 证据检索和质量评价
以 perioperative pain in lung cancer、lung cancer、perioperative pain management、围术期疼痛管理、肺癌围术期疼痛、疼痛等为检索词,系统检索 PubMed、Scopus、Embase、Web of Science、Cochrane Library、中国知网、万方数据知识服务平台和维普中文期刊服务平台等数据库,检索时限均为建库至 2025 年 1 月。依据证据等级优先采纳系统评价、随机对照试验(randomized controlled trial,RCT)研究,同时参考相关的队列研究、病例对照研究、专家共识、指南及综述。最终共纳入 75 篇 RCT 及 41 篇其他相关文献。
1.4 临床问题构建和确定
本共识制定采用文献调研、临床问题提出、改良德尔菲法专家咨询、专家会议讨论及共识修订等方 法 。工作组基于文献检索结果和 PICO(population、intervention、comparison、outcome)原则提炼临床问题,设计专家咨询问卷。经过 2 轮改良德尔菲法问卷调查及 3 次专家会议讨论,将专家赞同百分比≥60% 的条目纳入共识。共识等级划分如下:基本共识(赞同率 60%~<80%)、高度共识(赞同率≥80%)。最终确定的14 条推荐意见均获专家一致认可。2 轮德尔菲法专家咨询共纳入 86 位专家,2轮问卷收回率均为 100%。
1.5 证据的评价与分级
采用GRADE(Grading of Recommendations Assessment,Development and Evaluation)系统对证据质量和推荐强度进行分级。专家投票小组基于干预措施的利弊平衡、证据质量、患者价值观与偏好以及成本效益等因素形成推荐意见(强推荐或弱推荐)。通过最多 3 轮匿名投票达成共识(共识阈值设定为≥70% 的赞同率,最低响应率为 70%)。具体分级标准见表1。

1.6 共识的传播与更新
本共识将通过学术会议、专业期刊、指南解读、专题宣讲及新媒体平台等多种渠道推广,以促进其在临床实践中的应用。计划每 3年对共识内容进行评估,并根据最新的循证医学证据和临床实践需求进行必要的更新。
2 围术期疼痛的影响因素与发生机制
2.1 围术期疼痛的定义
围术期疼痛是指患者从术前至术后康复全程可能经历的疼痛,其成因复杂,与原发疾病、手术创伤、术后并发症等有关,同时也受患者既往疼痛病史、心理状态及社会因素的影响。若围术期疼痛控制不佳,可能导致呼吸系统并发症、心血管系统并发症(血压升高、心律失常等)、免疫抑制、血糖升高、伤口愈合延迟及焦虑抑郁等心理障碍,进而影响患者的整体康复进程与长期预后[1]。围术期疼痛涵盖急性疼痛与慢性疼痛,并可表现为伤害感受性疼痛、神经病理性疼痛(neuropathic pain,NP)等多种类型[2]。临床实践中,多种疼痛类型常相互交织。因此,围术期疼痛管理需采取个体化、多模式及多学科协作的策略,综合考虑疼痛类型、强度、患者既往史及手术特点,以有效缓解患者痛苦、降低并发症风险、促进加速康复[3]。
2.2 肺癌围术期疼痛的流行病学
肺癌围术期疼痛发生率高达80%~95%,其中中重度疼痛占比超过40%[4]。疼痛不仅延缓患者术后肺功能恢复,还会增加并发症发生风险,严重影响康复进程与生活质量。急性疼痛多在术后即刻出现,常于术后6~12 h达到高峰,通常持续3~7 d后逐渐缓解;其疼痛强度存在显著的个体差异,如胸腔镜微创手术患者中重度疼痛发生率约为25.0%,而开胸手术患者可高达70.0%。此外,年轻患者痛阈相对较低,术后数字评价量表(numerical rating scale,NRS)评分通常较老年患者平均高出1.5~2.0分[5]。在术后慢性疼痛(chronic postsurgical pain,CPSP)方面,一项为期10年的单中心回顾性研究[6]显示,肺癌患者术后36个月的CPSP发生率为17.4%。值得注意的是,由于死亡、失访等因素影响,该发生率可能低于临床实际情况。即使采用创伤更小的单孔胸腔镜手术,术后3个月仍有约63.4%的患者出现CPSP[7]。
2.3 肺癌围术期疼痛的影响因素
肺癌围术期疼痛受多种因素交互影响。手术因素方面,开胸手术患者的中重度疼痛发生率显著高于胸腔镜微创手术。手术时间>3 h是CPSP的独立危险因素。患者因素方面,女性患者发生率较男性高18.0%。随着影像学技术的进步,部分术前胸部CT影像特征亦成为重要的疼痛风险预测因子。高风险因素包括:胸膜增厚或粘连、手术区域存在陈旧性炎症或纤维化,这些患者术后中重度疼痛发生率显著增加;而低风险因素为肺内病变孤立、无胸膜侵犯且胸廓结构正常[8]。心理因素方面,术前焦虑评分与术后7 d内中重度疼痛发生率呈显著正相关,且这种关联存在性别差异,女性患者焦虑对疼痛的影响强度显著高于男性,术前存在中、重度焦虑的女性患者发生CPSP的风险也显著升高[9]。年龄因素方面,年轻患者因痛阈较低,术后急性疼痛评分通常高于老年患者。基础病方面,对于合并糖尿病等基础疾病的患者,高血糖状态可能影响神经功能和组织修复,增加CPSP风险。术后因素亦不容忽视,约25.0%的患者可能出现胸腔积气或积液,当积液量超过300 mL时,会因呼吸、咳嗽等动作加剧胸膜刺激,从而加重疼痛感受[10]。
2.4 肺癌围术期疼痛的发生机制
肺癌围术期疼痛的发生由多种机制共同驱动,且各机制间存在协同效应。手术创伤是直接诱因,手术操作需切割胸壁肌肉,可能损伤肋间神经。开胸手术为保障操作空间,其组织损伤范围通常较胸腔镜手术大3~5倍,导致术后初期急性疼痛发生率可达95.0%以上,而胸腔镜手术约为70.0%[5]。神经损伤可导致疼痛信号异常传递,引发持续性刺痛、烧灼感等NP,此类疼痛对常规镇痛药物反应较差。炎症反应是围术期疼痛另一重要机制,术后6~12 h,体内肿瘤坏死因子-α(tumor necrosis factor-alpha,TNF-α)、白细胞介素-6(interleukin-6,IL-6)等炎症介质浓度可达峰值,较术前升高8~10倍。其中,开胸手术患者的炎症介质水平较胸腔镜手术患者高约50.0%,间接导致其疼痛程度更为显著[11]。
3 疼痛评估
3.1 评估时机与内容
评估时机应包括但不限于以下时点,各时点的评估侧重点有所不同,以期全面捕捉疼痛的动态变化[12-13]。具体评估时机与内容见表2。
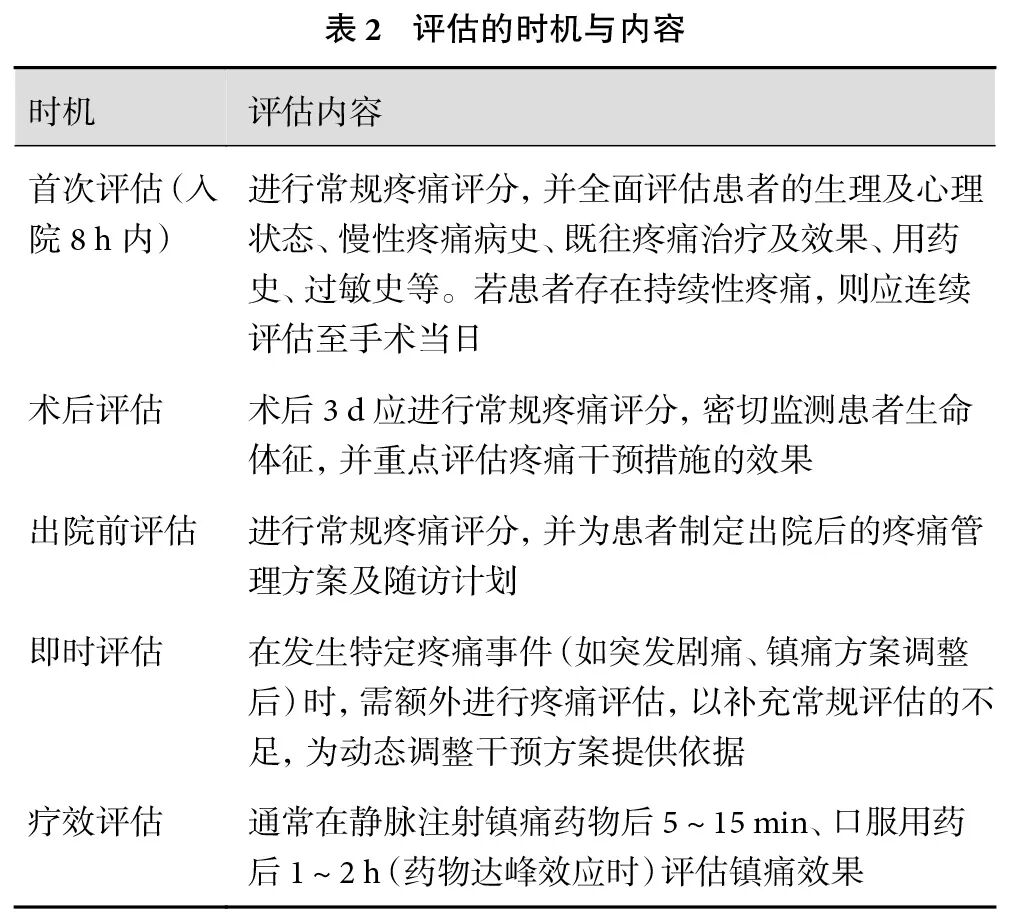
3.2 疼痛强度评估方法
疼痛评估对于判断镇痛是否充分、指导药物种类或剂量调整以及决定是否需要额外干预至关重要。推荐使用NRS(图1)、视觉模拟量表(visual analogue scale,VAS)或面部表情疼痛评分法(faces pain scale,FPS)评估疼痛强度[14-16](图2)。同时,可结合简明疼痛量表(brief pain inventory,BPI)和麦吉尔疼痛问卷(McGill Pain Questionnaire,MPQ)评估疼痛的性质、频率及其对日常生活功能的影响[17-18]。这些量表在我国成人疼痛评估中均具有良好的信度、效度和适用性。对于儿童或存在沟通障碍的患者,推荐使用易于理解和操作的FPS。
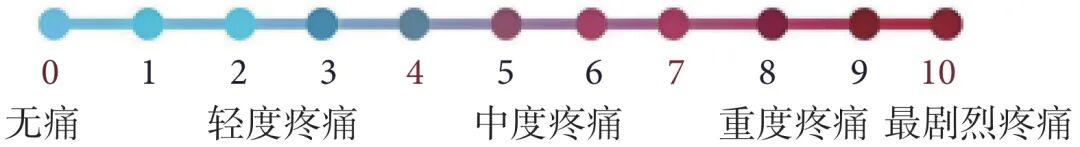
图1 疼痛数字评价量表
用 0~10 顺次 11 个数字表示疼痛从弱到强的强度等级。其中0 为无痛,10 为最剧烈疼痛,4 以下为轻度疼痛,4~7 为中度疼痛,7 以上为重度疼痛。
推荐意见1:在评估患者疼痛情况时,应考虑患者的年龄、性别、个体差异、认知功能和文化背景等,综合选择多种疼痛评估工具,以全面监测疼痛变化并准确评估治疗效果(C 级证据,强推荐)。
4 疼痛管理原则
4.1 多模式镇痛
多模式镇痛是指联合应用不同镇痛方法及作用机制的镇痛药物,通过多种给药途径,作用于疼痛发生的不同部位、时相和靶点,以实现更优的镇痛效果,同时减少单一药物的用量及其相关不良反应。该方案还可联合非药物干预措施,在确保安全的前提下,达到持续、有效的镇痛目标,是围术期镇痛管理的标准方案。
4.2 个体化疼痛治疗
患者对疼痛的感知及对镇痛药物的反应存在显著的个体差异。术后疼痛管理需综合考虑手术类型、手术部位、患者个人特征(如年龄、性别、心理状态)、疼痛程度及既往疼痛史等因素,整合口服、静脉、区域阻滞等多种技术,制定个体化的疼痛管理方案。术后需对疼痛进行准确预测与动态评估,以便及时调整治疗策略,实现最佳镇痛效果,满足患者的个体化需求。
4.3 超前镇痛
超前镇痛是指在手术切皮前即开始给予镇痛干预,旨在抑制或减弱伤害性刺激向中枢神经系统的传入,从而预防外周及中枢敏化的发生,实现对术后疼痛的早期预防和有效控制。此外,超前镇痛还有助于减轻术后躁动、改善免疫功能、减少阿片类药物用量及其相关的恶心、呕吐等不良反应。然而,当前肺癌术后镇痛的研究推荐区域神经阻滞技术及减少使用阿片类药物策略。关于药物超前镇痛的高质量 RCT 研究相对有限,尚不足以形成明确的推荐方案。未来仍需深入探讨超前镇痛的作用机制、不同药物的最佳应用时机,以进一步优化该策略。
推荐意见2:推荐根据患者个体情况,联合应用多种不同作用机制的镇痛方法,发挥协同增效作用,降低单一药物不良反应的风险,有效减轻患者疼痛,达到最佳治疗效果(C 级证据,强推荐)。
5 围术期疼痛的预防
5.1 术前预防
术前预防是管理肺癌 CPSP 的首道防线,全面细致的评估与干预至关重要。
5.1.1 心理干预
手术应激易引发患者焦虑、抑郁等负性情绪,降低疼痛阈值,加剧疼痛感知。研究[19]表明,术前焦虑是 CPSP 的危险因素,而较高的受教育水平可能降低其发生风险。对于存在心理问题的患者,应及时给予心理疏导等支持性干预,必要时请精神心理科会诊进行药物辅助治疗,以减轻患者心理负担,增强其应对手术的信心。
5.1.2 基础疾病管理
对于合并糖尿病等基础疾病的患者,高血糖状态可能影响神经功能和组织修复,增加 CPSP 风险,需制定个体化的血糖管理方案[20]。
5.2 术中预防
术中操作与麻醉管理直接影响 CPSP 的发生。
5.2.1 手术操作
推荐优先采用胸腔镜手术或机器人辅助手术等微创技术,常规腔镜手术推荐使用尽量少的切口,可采用三孔、单操作孔、单孔、乳晕旁切口等,以最大限度减少组织和神经损伤,从而降低术后疼痛的强度并缩短持续时间[21-22]。术中操作应精准,注意保护神经、血管等重要结构[23]。
5.2.2 麻醉管理
优化麻醉方案,整合区域阻滞技术,减少术中阿片类药物使用。
推荐意见3:建议优化手术切口、选择合适的手术入路和切口位置,以降低神经损伤或神经受压的风险(C 级证据,强推荐)。
5.3 术后预防
多模式镇痛是术后疼痛管理的核心,应联合使用药物治疗、物理治疗、认知行为疗法(cognitive behavioral therapy,CBT)及中医中药等不同作用机制的镇痛药物和方法,以达到最佳的镇痛效果。另外,康复措施在术后疼痛预防中也发挥着重要作用。鼓励患者术后早期活动,有助于促进血液循环、防止血栓形成,同时有助于肺复张。早期活动可显著降低术后疼痛程度,缩短住院时间,加速康复进程。
6 肺癌围术期疼痛干预策略
6.1 药物治疗
临床常用的镇痛药物主要包括非甾体抗炎药(nonsteroid anti-inflammatory drugs,NSAIDs)、对乙酰氨基酚、阿片类药物等。此外,镇静药物、抗惊厥类药物和抗抑郁药物常作为辅助镇痛药,用于治疗 NP或缓解疼痛伴随的情绪障碍。糖皮质激素通过抑制炎症反应,在特定类型的疼痛管理中亦有一定价值。
6.1.1 NSAIDs
广泛用于术后多模式镇痛。有研究[24-25]显示其使用与非小细胞肺癌(non-small cell lung cancer,NSCLC)患者的总生存期(overall survival,OS)和无进展生存期(progression-free survival,PFS)改善相关,其潜在抗肿瘤效应可能与选择性环氧化酶-2(cyclooxygenase-2,COX-2)抑制有关,但具体机制仍需前瞻性研究验证。
6.1.2 对乙酰氨基酚
常与阿片类药物或其他药物联用,增强镇痛效果。其胃肠道刺激较NSAIDs小,且不增加心血管风险。
6.1.3 弱阿片类药物
弱阿片类药物曲马多(tramadol)可与胸椎旁神经阻滞(thoracic paravertebral block,TPVB)或肋间神经阻滞(intercostal nerve block,ICNB)联合使用,减少麻醉药用量,延长镇痛时间,降低术后并发症及谵妄发生率。另由于弱阿片类药物存在的天花板效应,药物剂量增加到一定阈值后,镇痛效果不再显著提升,但不良反应仍会随剂量增加而加重,故在使用时需控制使用剂量。
6.1.4 糖皮质激素
围术期应用可减少阿片类消耗、降低心肌损伤及肺部并发症风险,促进早期活动。但需注意长期应用可能导致高血糖、骨质疏松及消化性溃疡等不良反应[26-27]。
6.1.5 抗惊厥类药物
该类药物[如加巴喷丁(gabapentin)、普瑞巴林(pregabalin)、美洛加巴林(mirogabalin)等]主要通过作用于脊髓背角神经元电压门控钙通道,减少钙离子内流,抑制神经递质释放,从而降低神经元兴奋性,是治疗 NP 的核心药物[28-30]。围术期应用可有效减轻术后疼痛、焦虑抑郁症状,改善睡眠质量,促进早期康复,故推荐其作为 CPSP的一线治疗药物[31-35]。
6.1.6 抗焦虑抑郁类药物
此类药物通过直接镇痛或间接改善情绪两种途径缓解疼痛。5-羟色胺和去甲肾上腺素再摄取抑制剂(serotonin and norepinephrine reuptake inhibitors,SNRIs)及三环类抗抑郁药(tricyclic antidepressants,TCAs)可直接抑制疼痛信号上传[36]。选 择 性 5-羟色胺再摄取抑制剂(selective serotonin reuptake inhibitors,SSRIs)则主要通过改善情绪,打破“疼痛-情绪”恶性循环。N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor,NMDAR)拮抗剂,如艾司氯胺酮(esketamine)兼具快速抗抑郁与镇痛作用。临床应依据患者具体症状选择药物,并遵循个体化给药原则。
6.1.7 阿片类
此类药物[如羟考酮(oxycodone)、氢可酮(hydrocodone)、芬太尼(fentanyl)、美沙酮(methadone)、布托啡诺(butorphanol)等]是治疗中重度癌性疼痛的基石。其常见不良反应包括便秘、嗜睡、恶心、头晕等,长期使用可导致耐受及依赖[37-38]。肿瘤学研究[39-41]提示,阿片类药物可能通过共激活表皮生长因子受体、上调细胞外信号调节激酶磷酸化等途径潜在促进肿瘤进展。回顾性研究[42]显示,术前未使用阿片类药物的肺癌患者,若术后 6 个月内持续使用,2 年全因死亡风险可能增加。无阿片类药物麻醉(如使用艾司氯胺酮等替代方案)已被证实安全有效,可降低术后恶心呕吐及远期 CPSP 发生率[43-44]。然而,Oh 等[45]的研究未发现阿片类药物用量与肺癌复发或死亡风险显著相关,结论尚存异质性。新型 G 蛋白偏向性 μ-阿片受体激动剂[如泰吉利定(tegileridine)、奥赛利定(oliceridine)等]通过选择性激活 G 蛋白通路实现镇痛,同时 β-arrestin-2 通路激活作用弱,较传统阿片类药物显著降低呼吸抑制、恶心呕吐等不良反应风险,但其在肺癌围术期的疗效与安全性需更多国内人群研究验证[46]。
常用镇痛药物的剂量与用法参见表3。
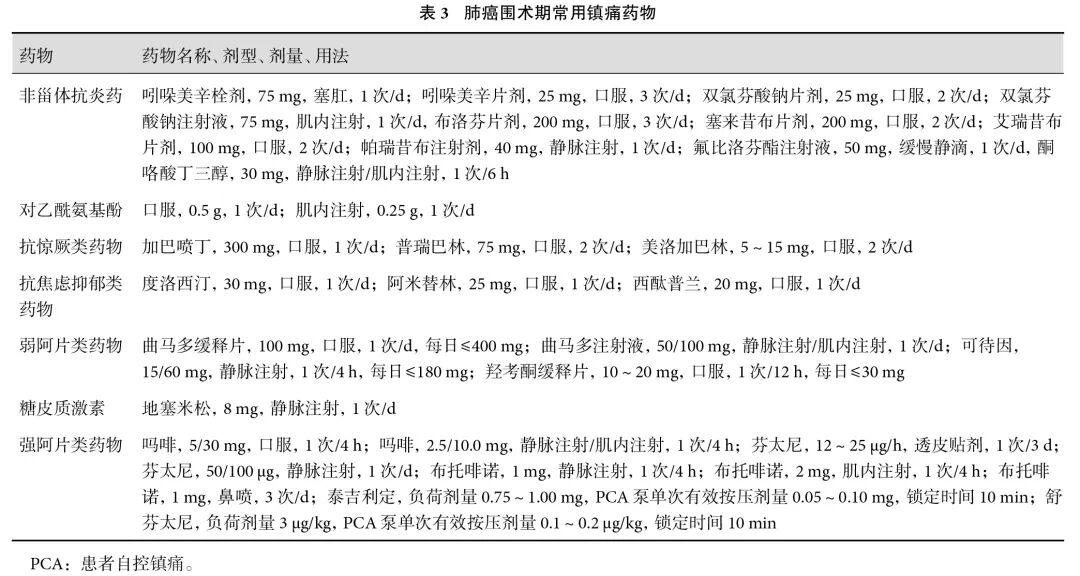
6.2 非药物治疗
6.2.1 神经阻滞技术
神经阻滞技术是胸外科手术多模式镇痛的核心组成部分,可显著降低患者术后疼痛评分、阿片类药物用量,促进呼吸功能恢复,降低肺部并发症及谵妄发生率,安全性良好[47-50]。主要技术包括区域阻滞、硬膜外阻滞(thoracic epidural analgesia,TEA)和患者自控镇痛(patient-controlled analgesia,PCA)。
区域阻滞技术目前包括ICNB、手术切口浸润性麻醉、前锯肌平面阻滞(serratus anterior plane block,SAPB)、TPVB、竖脊肌平面阻滞(erector spinae plane block,ESPB)等多种方法,并已成为胸外科手术中最为推荐的核心镇痛手段。在ICNB中,布比卡因及罗哌卡因与布比卡因的混合镇痛剂被广泛应用,镇痛效果与单独使用罗哌卡因相当,且在疼痛评分、麻醉药物使用、并发症发生率及住院时间等方面未显示出显著差异。另有研究[23, 51-55]显示新型局部麻醉药布比卡因脂质体行ICNB的镇痛效果优于传统局部麻醉药,可提供更优的静息及运动时镇痛,并显著减少PCA需求,联合星状神经节阻滞(stellate ganglion blocks,SGB)较单纯ICNB展现出更为优秀的镇痛效果。手术切口使用布比卡因脂质体对胸壁切口周围进行浸润,可有效缓解术后疼痛,促进患者早期活动,加快术后康复过程[56-58]。Zhao等[59]于2021年首次提出SAPB及其在临床中的应用,可有效减轻肺叶切除术患者的围术期疼痛,且在预防CPSP的发生方面表现出显著优势。与传统的ICNB相比,SAPB显著减少了阿片类药物的使用量,同时降低了并发症发生率[60]。研究[58,61]证实,对于胸腔镜肺叶切除术的SAPB,与罗哌卡因相比,使用布比卡因脂质体能提供更优的术后镇痛,加速患者术后康复。TPVB是肺癌患者围术期多模式镇痛的核心组分,可显著延长镇痛时间、抑制炎症与应激反应、改善呼吸力学及咳痰能力,并加速首次下床活动与出院时间[62]。多项RCT[63-64]表明,在胸腔镜肺手术中,采用布比卡因脂质体行TPVB,可显著延长术后镇痛持续时间,改善患者恢复质量。胸腔镜引导的TPVB在操作便捷性、首次穿刺成功率、阻滞覆盖范围及镇痛质量方面均优于超声引导的TPVB[65]。ESPB是一种新型的区域麻醉技术,于2016年首次被描述,具有操作简便、并发症风险低等优势,其适用范围广,可用于多种手术的术后镇痛[66]。多项研究[67-69]提示ESPB在安全性和镇痛效果方面优于TPVB及SAPB,而对于胸腔镜肺切除术前的ESPB,与传统局部麻醉药盐酸布比卡因相比,使用布比卡因脂质体能在术后提供具有临床意义的镇痛效果,并显著减少阿片类药物使用。
推荐意见4:术中应根据手术类型选择相应的区域神经阻滞技术作为多模式镇痛的核心措施。具体方案可以包括:① 胸腔镜直视下于 T2~T10每肋间使用罗哌卡因或布比卡因脂质体行肋间神经阻滞或椎旁神经阻滞。若无法在直视下完成阻滞,推荐采用超声联合 CT 进行实时引导,尤其适用于解剖复杂、肥胖(体重指数≥30 kg/m2)或存在脊柱畸形的患者,以提升穿刺精准性与安全性(B 级证据,强推荐)。② 关胸前沿手术切口使用布比卡因脂质体浸润注射(C 级证据,强推荐)。③ 使用罗哌卡因或布比卡因脂质体进行前锯肌平面阻滞作为首选的筋膜平面阻滞技术(B 级证据,强推荐)。④ 术侧单次或连续给予罗哌卡因、或单次给予布比卡因脂质体行胸椎旁神经阻滞作为首选的神经阻滞方案;若存在椎旁神经阻滞禁忌,可使用罗哌卡因或布比卡因脂质体行竖脊肌平面阻滞(B 级证据,强推荐)。
TEA与PCA是胸外科术后疼痛管理的重要组成部分。TEA可为胸段至腰段脊神经支配区域的手术提供持续、有效的术后镇痛。研究[70-72]表明,与全身性阿片类药物静脉镇痛相比,TEA在促进胃肠功能恢复、降低疼痛评分以及减少术后并发症方面具有优势。尽管TEA被视为术后镇痛的“金标准”,但其常见不良反应如低血压、尿潴留等,可能与加速康复外科(enhanced recovery after surgery,ERAS)路径的目标存在冲突。近年大样本回顾性研究[73]进一步显示,与区域神经阻滞相比,硬膜外麻醉在术后3~6个月的长期镇痛药物处方率方面未展现出显著优势。因此,临床决策应更侧重于其对患者循环稳定性的影响及其与ERAS路径的契合度。PCA作为一种以患者为中心的镇痛模式,其核心在于将部分镇痛药物控制权交予患者,以适应个体代谢差异和疼痛感知变化,实现更灵活的疼痛控制。自20世纪90年代引入我国以来,PCA已在术后疼痛管理中广泛应用,并在癌痛、分娩镇痛及慢性疼痛治疗中展现出重要潜力[74]。PCA常用途径包括静脉自控镇痛(patient-controlled intravenous analgesia,PCIA)和硬膜外自控镇痛(patient-controlled epidural analgesia,PCEA)。PCIA以阿片类药物为基础,可实现快速镇痛滴定;PCEA则经硬膜外导管给予局部麻醉药或联合阿片类药物,镇痛效果明确且具有节段性特点,但需注意留置导管可能带来的硬膜外血肿、感染等风险。综上,对于不宜行区域神经阻滞或拟行开胸手术的患者,可考虑采用TEA或PCA进行术后镇痛。然而,在胸腔镜手术中应用时,应审慎评估其与ERAS路径的潜在冲突[75]。
推荐意见5:对于无法行区域阻滞的患者、开胸手术及手术时长预计>3 h 的患者,建议行硬膜外阻滞或患者自控镇痛,但需权衡不良反应与加速康复路径之间的冲突(B 级证据,强推荐)。
6.2.2 神经调控治疗
神经调控治疗是一种通过电、磁、化学等物理或生物手段调节神经系统功能活动,以改善或恢复神经功能异常的治疗技术。常用方法包括经皮神经电刺激(transcutaneous electrical nerve stimulation,TENS)、磁刺激(magnetic stimulation,MS)、射频治疗 (radiofrequency therapy,RFT)和脊髓电刺激植入术(spinal cord stimulation,SCS)等。在 MS 治疗中,经颅磁刺激(transcranial magnetic stimulation,TMS)可能通过促进突触可塑性产生长期镇痛效应[76]。研究[77]对大脑运动区施加 10 Hz 的高频 TMS 对慢性神经性疼痛患者具有镇痛作用。外周磁刺激(peripheral magnetic stimulation,PMS)的相关研究结果尚存异质性。一项回顾性研究[78]显示,部分患者在 3个月时疼痛显著减轻,阿片类药物用量亦有所减少。然而,一项Meta分析[79]指出,PMS对术后急性期(2 个月内)疼痛可能有效,而对 6 个月及 12 个月时的持续性疼痛、阿片消耗量及不良事件均无显著影响。此外,尽管有病例报告[80]显示SCS用于 NSCLC开胸术后疼痛可获得多方面理想效果,但目前仍缺乏RCT证据支持其广泛应用。
6.2.3 认知行为模式疗法
在肺癌围术期疼痛管理中,心理因素对疼痛的感知、表达及应对具有重要影响。焦虑、抑郁、恐惧等负性情绪可显著加重患者术后疼痛感受,因此,系统化的心理干预是疼痛管理的重要组成部分。CBT 作为一种结构化的非药物干预手段,能够有效调节患者对疼痛的感知、应对方式和情绪反应。研究[81-83]表明,CBT 通过纠正患者对疼痛的不良认知、缓解患者术前焦虑与抑郁状态、减少阿片类药物使用,有效减轻术后疼痛强度,预防慢性疼痛发生,从而提升患者生活质量并促进术后康复。
6.2.4 物理治疗
物理治疗是术后快速康复路径的重要组成部分,其常用方法包括冷疗法、热疗法、超声治疗、矫正治疗等。在肺癌围术期疼痛管理中,其不仅是药物镇痛的有效补充,更是实现个体化、精准化疼痛管理的关键环节,具有缓解术后疼痛、改善术后肺功能、增强患者活动能力、预防相关并发症及促进患者整体康复进程等作用[84–85]。
6.2.5 中医中药治疗
中医中药治疗作为补充与替代医学的重要组成部分,在肺癌围术期疼痛管理中具有独特价值。其通过整体调理、活血化瘀、行气止痛、扶正祛邪等作用机制,能够有效缓解术后疼痛、改善临床症状、减少镇痛药物依赖,有效促进患者康复[86–87]。
推荐意见6:推荐将神经调控治疗、认知行为模式疗法、物理治疗及中医中药治疗纳入围术期多模式镇痛方案,以协同增强镇痛效果,改善患者焦虑情绪,促进康复(C 级证据,强推荐)。
6.3 围术期护理管理策略
随着 ERAS 理念的普及及“无痛舒适化”医疗模式的推广[88–89],护理人员在肺癌围术期疼痛管理中的角色已由传统的疼痛评估与医嘱执行者,转变为集评估、决策、干预、宣教与随访于一体的核心执行者。新模式强调以患者为中心,将预防性镇痛、多模式镇痛等理念贯穿于围术期全程,旨在实现精准化、个体化的疼痛管理,提升患者舒适度与满意度。
护理人员应确保疼痛评估准确、连续、系统,规范执行多模式镇痛方案,并为患者及家属提供循证导向的个体化疼痛教育。术前疼痛宣教是提升患者认知与依从性、奠定疼痛管理成效的关键环节。护理人员须在术前完成患者生理与心理全面评估,开展个体化访谈[90]。针对焦虑、抑郁、恐惧等负性情绪对术后疼痛感知的放大效应,应进行系统心理状态筛查。通过有效沟通,以耐心、温和的态度消除患者及家属对疼痛的认知误区,缓解术前焦虑,增强医患信任。宣教内容应结合患者年龄、文化背景、职业及语言习惯进行个性化设计,并采用宣传手册、视频资料、移动应用程序等多模态途径,确保信息传递高效、易懂[91]。具体宣教项目及内容要点见表4。
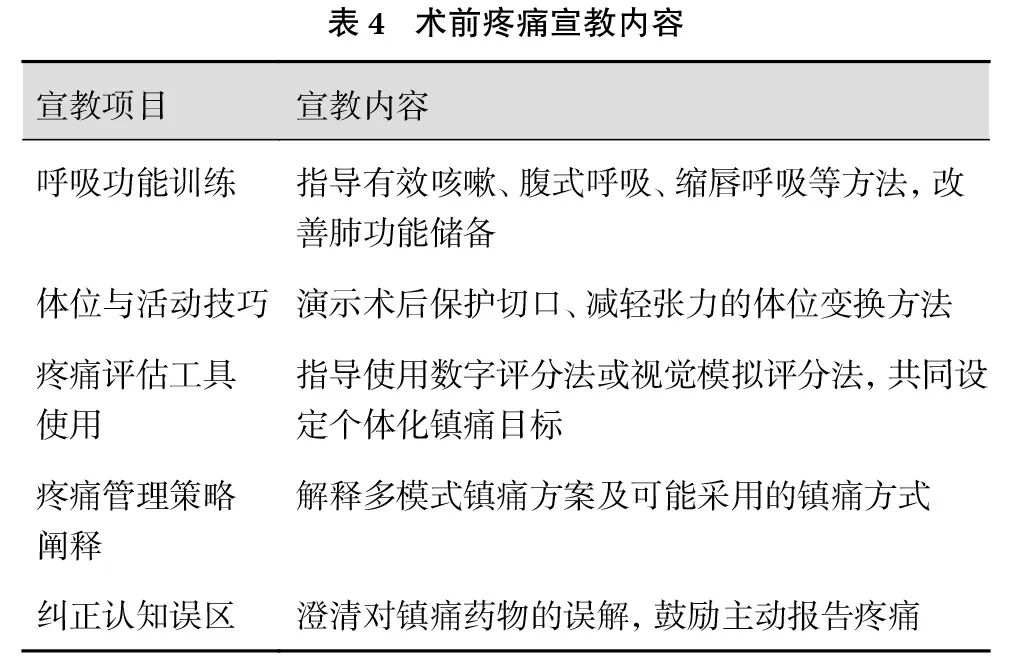
推荐意见7:术前对患者进行全面的心理状态评估,并提供系统化、个体化的疼痛管理宣教,内容涵盖呼吸功能训练、疼痛评估工具使用、镇痛目标设定及镇痛方案解读。术后需加强镇痛措施落实的指导与不良反应监测(C 级证据,强推荐)。
6.4 胸腔引流管管理策略
胸腔引流管是肺癌术后管理胸腔积液、积气等并发症的标准装置。20世纪前,临床多采用“双管策略”(前上管排气、后下管排液,管径28~32 F),该策略虽兼顾排气与排液,但术后疼痛显著。20世纪末以来,RCT[92-98]证实,肺叶切除术后采用16 F或更细规格,如8~10 F的单管引流,在引流效果相当的基础上可显著减轻疼痛,因而“单管、细径、早拔”逐步成为胸外科引流新标准。随着非气管插管麻醉与自主呼吸麻醉技术的发展,无管化技术应运而生。该技术通过避免气管插管、机械通气、胸腔引流管及导尿管留置,简化手术流程,减少术后不适,加速康复[99]。自2011年首例非插管胸腔镜肺叶切除术报道以来,无管化技术适用范围已扩展至几乎所有肺部术式,甚至包括支气管成形、肺移植等复杂手术,尤其适用于重症肌无力、双侧肺手术、困难气道或边缘肺功能等特定患者。多项研究[100-107]证实,无管化技术通过减少肌松药的使用,加快患者术后呼吸功能与活动能力的恢复,降低全身并发症与炎症细胞因子水平,从而减少胸腔引流及对肋间神经的压迫损伤,显著减轻术后疼痛,改善患者手术体验,加快术后康复,缩短住院时间。目前,该技术常与ICNB、胸椎旁阻滞、胸段硬膜外麻醉或喉罩全身麻醉等多模式镇痛策略联合应用,已成为围术期疼痛管理的重要组成部分。
推荐意见8:术后根据患者情况可选择较细口径引流管,置入合适深度,并在无漏气证据时尽早拔除,以降低引流管相关疼痛(A 级证据,强推荐)。
推荐意见9:对于体重指数<30 kg/m2、无广泛胸内粘连的肺楔形或亚肺叶切除患者,可以由经验丰富的外科与麻醉科团队开展无管胸腔镜手术,通过避免留置胸腔引流管减轻术后疼痛(B级证据,强推荐)。
7 术后慢性疼痛
CPSP 是影响肺癌患者术后生活质量的重要因素,其规范管理是围术期疼痛管理的核心环节之一。
7.1 定义与临床表现
7.1.1 定义
CPSP 的诊断需满足国际疼痛协会的核心定义,即手术后出现的手术区域疼痛,持续时间超过 3 个月,且排除其他病因(如晚期恶性肿瘤、全身疼痛综合征、系统感染等)[108]。本共识结合微创肺部手术特点,对 CPSP 定义予以进一步明确,须涵盖以下要素:(1) 排除其他可能引起慢性疼痛的疾病;(2)疼痛性质可为新发疼痛、原有疼痛加剧、无症状期后显现或由急性术后疼痛迁延演变而来;(3)疼痛范围涵盖手术区域及其相关神经支配区域;(4)疼痛持续时间至少为 1 个月。
系统性综述[109]表明,胸外科术后CPSP多表现为NP。我国的《神经病理性疼痛诊疗专家共识》[110]及《周围神经病理性疼痛诊疗中国专家共识》[111]均明确指出,CPSP 属于由周围神经损害所致的周围性神经病理性疼痛(peripheral neuropathic pain,PNP)。2021年发布的《慢性手术后疼痛的专家共识》[112]进一步强调了神经损伤在CPSP发生中的关键作用。本共识采纳上述观点,将 PNP 作为微创肺部手术 CPSP 的核心病理机制,为临床诊疗提供明确依据。
7.1.2 临床表现
微创肺部手术后的 CPSP 常为混合性疼痛,但以 NP 为主要表现。患者可出现自发性疼痛、痛觉过敏(对正常刺激反应增强)、异常疼痛(非伤害性刺激诱发疼痛)以及感觉异常(如麻木、刺痛、烧灼感等)[113]。临床表现具有显著个体差异性。疼痛部位多位于胸部,尤其是手术切口邻近区域,但亦可放射至相应神经支配范围。除疼痛外,患者常伴有呼吸急促、胸闷及局部皮肤麻木等症状。疼痛多为持续性,可导致生活质量显著下降,并常引发焦虑、抑郁等情绪障碍,以及入睡困难、早醒、睡眠质量差等睡眠障碍。严重者可能出现活动受限,甚至影响劳动能力[114]。
7.2 评估与诊断
CPSP 的诊断需结合患者主诉、临床观察及客观评估工具,以实现量化评估与精准诊断。辅助检查手段主要包括:(1)神经电生理学检查:有助于明确神经损伤的部位与程度,并为预后判断提供参考;(2)红外热层析成像:可通过检测局部温度变化,辅助评估疼痛程度与治疗反应;(3)高分辨率 CT:手术侧胸膜明显增厚伴强化提示胸膜粘连及慢性疼痛风险[115];见表5。

推荐意见10:伤口愈合情况是诊断 CPSP 的必要条件,而局部皮肤颜色变化、肿胀水肿、肌肉紧张度、疤痕形成及感觉异常等,可作为辅助诊断的参考指标(C 级证据,强推荐)。
推荐意见11:神经电生理学、红外热成像等辅助检查,可作为评估 CPSP 的重要手段,以提升诊断的全面性与可靠性(C 级证据,强推荐)。
7.3 治疗原则与方案
胸外科 CPSP 应遵循“从无创到有创、从低风险到高风险”的阶梯化治疗原则,以实现精准镇痛并最大限度降低治疗相关风险。
7.3.1 无创治疗
药物治疗:以 NSAIDs[如布洛芬(ibuprofen)、艾瑞昔布(imrecoxib)、塞来昔布(celecoxib)]为核心,若存在 NP 成分(如刺痛、麻木),应加用抗惊厥药物及抗焦虑抑郁药物。
非药物治疗:对合并焦虑情绪的患者,可应用CBT,通过调整患者对疼痛的认知与行为反应,降低疼痛感知。
7.3.2 MS与神经阻滞技术
若一线治疗效果不佳,且疼痛严重影响生活质量,可使用 MS治疗或采取以超声引导下的局部神经阻滞为主要手段,包括 ICNB、胸壁局部浸润阻滞的微创介入治疗,通过注射局部麻醉药直接阻断疼痛信号传导。
7.3.3 神经调控治疗与鞘内药物输注系统
适用于经一、二级治疗后疼痛仍控制不佳,且严重影响睡眠、情绪的顽固性病例。神经调控治疗窗口可适当前移,以尽早改善患者生活质量。常用方式包括(1)脉冲射频:尤其适用于影像学(高频超声或 MR 神经成像)提示明确神经形态异常(如神经增粗、神经瘤形成或被疤痕包裹)的患者。推荐在CT 引导下进行,以精准调节神经兴奋性,缓解疼痛且不导致神经热损伤;(2)SCS:通过植入电极刺激脊髓神经,阻断疼痛信号上传;(3)鞘内药物输注系统:鞘内镇痛所需药物剂量更低、疗效更佳,适用于其他方法无效或晚期癌痛患者。
推荐意见12:推荐加巴喷丁、美洛加巴林等抗惊厥类药物作为 CPSP 的一线治疗药物。注意用药剂量的阶梯调整及停药步骤,以减少不良反应与戒断症状(A 级证据,强推荐)。
推荐意见13:CPSP 患者,尤其伴有 NP 成分者,推荐使用区域神经阻滞技术作为重要治疗手段(B级证据,强推荐)。
推荐意见14:顽固性肺部 CPSP 患者,可考虑神经调控治疗,如磁刺激、脉冲射频或脊髓电刺激植入术等方法(B 级证据,强推荐)。
8 肺癌围术期疼痛诊治全流程
肺癌围术期疼痛管理应贯穿术前、术中及术后全阶段,形成系统化、个体化的诊疗路径。
8.1 术前阶段
应全面评估患者年龄、性别、心理状态、既往疼痛史、用药史、过敏史、认知功能及治疗期望等因素,并进行充分的疼痛知识宣教。对存在术前疼痛、阿片类药物耐受、有慢性疼痛史等高危因素者,建议术前即开始预防性镇痛。
8.2 术中阶段
根据手术部位、创伤程度、切口数量、手术时间(如是否>3 h)等因素,选择适宜的镇痛技术,具体方案参见图3。

图 2 面部表情疼痛评分法的疼痛分级
0 为无痛,2 为有点痛,4 为轻微疼痛,6 为疼痛明显,8 为疼痛严重,10 为疼痛剧烈。
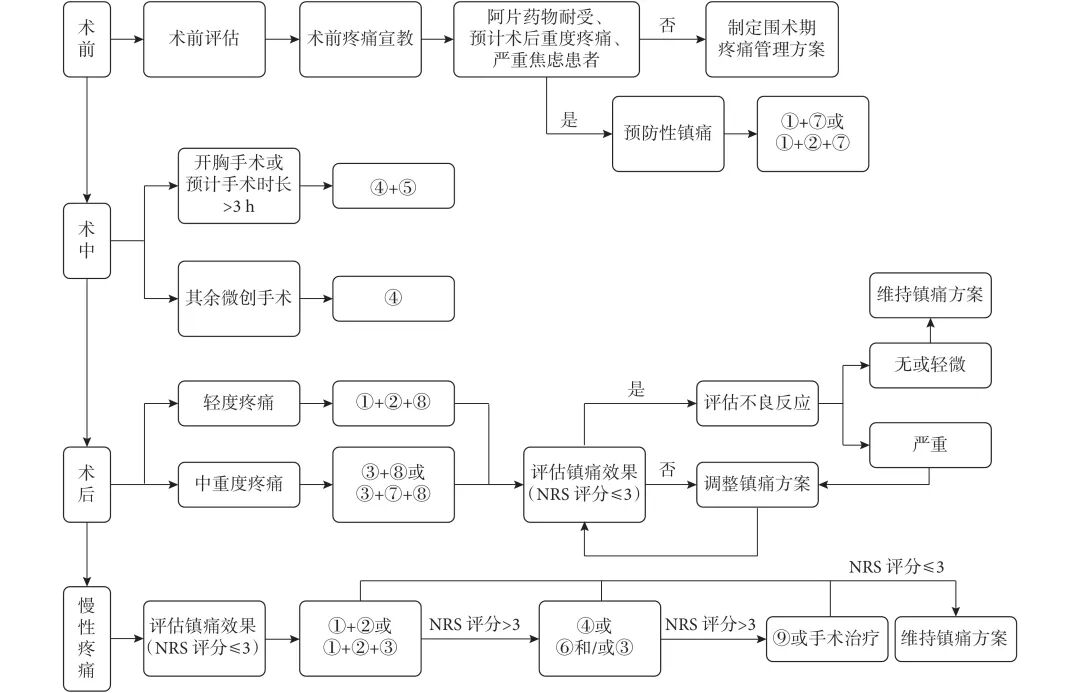
图 3 肺癌围术期疼痛管理策略选择参考
NRS:数字评价量表;① 为对乙酰氨基酚或非甾体抗炎药类药物,② 为抗惊厥及抗焦虑抑郁类药物,③ 为阿片类药物,④ 为区域神经阻滞技术,⑤ 为硬膜外阻滞或患者自控镇痛技术,⑥ 为神经调控治疗,⑦ 为认知行为疗法,⑧ 为物理治疗及中医中药治疗,⑨ 为鞘内药物输注系统。
8.3 术后阶段
密切评估疼痛程度,按时、按阶梯给予镇痛治疗,并积极防治 CPSP。
9 总结与展望
本共识作为国内首部专注于肺癌围术期疼痛管理的专家共识,旨在通过规范临床路径,改善患者术后生存质量与长期预后。共识系统阐述了围术期疼痛的定义、病因、影响因素、评估方法、管理原则及多种治疗策略,并重点突出了围术期疼痛的诊断与处理。结合中国医疗实践特点,本共识倡导多模式镇痛、个体化治疗及综合管理方案,详细介绍了常用镇痛药物的作用机制、使用规范与不良反应,同时肯定了非药物疗法在疼痛管理中的价值。
然而,当前肺癌围术期疼痛管理仍存在若干待解决的关键问题,如超前镇痛的最佳时机与机制尚未明确,阿片类药物长期应用对预后的影响仍有争议,非药物疗法的有效性与适用人群需进一步验证,围术期疼痛的防治尚缺乏国际统一的标准化方案。展望未来,期望通过更多高质量的临床研究与实践探索,持续优化肺癌围术期疼痛管理策略,最终为患者提供更加安全、高效、舒适的医疗服务。
利益冲突 无。
本共识计划书见本刊网站电子版补充材料。
制订专家组名单
牵头专家(按姓氏拼音排序):陈椿(福建医科大学附属协和医院胸外科);樊碧发(中日友好医院疼痛科);何建行(广州医科大学附属第一医院胸外科);支修益(首都医科大学宣武医院胸外科)
执笔专家:崔飞(广州医科大学附属第一医院胸外科);张弘浩(广州医科大学附属第一医院胸外科);贾一帆(武汉大学人民医院疼痛科);郑斌(福建医科大学附属协和医院胸外科);杨汉宇(广州医科大学附属第一医院麻醉科)
专家组成员(按姓氏拼音排序):车国卫(四川大学华西医院胸外科);陈昶(上海肺科医院胸外科);陈椿(福建医科大学附属协和医院胸外科);陈克能(北京大学肿瘤医院胸外科);陈莹(广州医科大学附属第一医院胸外科);陈友伟(香港大学深圳医院麻醉科);樊碧发(中日友好医院疼痛科);高立梅(广州医科大学附属第一医院胸外科);高阳(中南大学湘雅医院胸外科);耿国军(厦门大学附属第一医院胸外科);何建行(广州医科大学附属第一医院胸外科);何正富(浙江大学医学院附属邵逸夫医院胸外科);侯建彬(安阳市肿瘤医院胸外科);胡坚(浙江大学医学院附属第一医院胸外科);黄刚(河北医科大学第三医院胸外科);雷迁(四川省人民医院麻醉科);李鹤成(上海交通大学医学院附属瑞金医院胸外科);李辉(首都医科大学附属北京朝阳医院胸外科);李维(武汉大学人民医院疼痛科);李文雅(中国医科大学附属第一医院胸外科);李小飞(空军军医大学唐都医院胸外科);李水清(北京大学第三医院疼痛科);廖思达(广州医科大学附属第一医院麻醉科);刘辉(广州医科大学附属第一医院麻醉科);刘洪生(北京协和医院胸外科);刘云(宜昌市中心人民医院胸外科);罗洞波(新疆医科大学附属肿瘤医院胸外科);罗宏伟(高新医胸科医院胸外科);马建群(哈尔滨医科大学附属肿瘤医院胸外科);毛宁(重庆医科大学附属永川医院胸外科);邱斌(中国医学科学院肿瘤医院胸外科);石英(上海市浦东新区人民医院疼痛科);邵丰(南京市胸科医院胸外科);邵文龙(广州医科大学附属第一医院胸外科);陶高见(南京鼓楼医院疼痛科);唐元章(广州医科大学附属第一医院疼痛科);王仁峰(复旦大学附属中山医院厦门医院胸外科);王永(中国医科大学航空总医院疼痛科);韦海涛(河南大学淮河医院胸外科);吴卫兵(江苏省人民医院胸外科);冼磊(广西医科大学第二附属医院胸外科);谢广伦(河南省肿瘤医院疼痛科);许华(上海中医药大学附属岳阳中西医结合医院疼痛科);薛涛(东南大学附属中大医院胸外科);杨力宝(三明市第二医院放疗科);杨立强(首都医科大学宣武医院疼痛科);叶济世(武汉大学人民医院疼痛科);张昊(徐州医科大学附属医院胸外科);张淼(徐州市中心医院胸外科);张敏(重庆医科大学附属第一医院胸外科);张清(广州医科大学附属第一医院胸外科);张力为(新疆医科大学第一附属医院胸外科);张双平(山西省肿瘤医院胸外科);张奕(漳州市医院胸外科);赵国芳(宁波市第二医院胸外科);赵军(苏州大学附属第一医院胸外科);支修益(首都医科大学宣武医院胸外科);朱全(江苏省人民医院胸外科);邹慧超(哈尔滨医科大学附属肿瘤医院疼痛科)
审核组成员(按姓氏拼音排序):陈昶(上海肺科医院胸外科);车国卫(四川大学华西医院胸外科);陈克能(北京大学肿瘤医院胸外科);胡坚(浙江大学医学院附属第一医院胸外科);李辉(首都医科大学附属北京朝阳医院胸外科);李鹤成(上海交通大学医学院附属瑞金医院胸外科);薛涛(东南大学附属中大医院胸外科)
秘书组成员(按姓氏拼音排序):弓磊(天津医科大学肿瘤医院食管肿瘤科);郭文巍(广州医科大学附属第一医院胸外科);黄丹霞(广州医科大学附属第一医院胸外科);黄广磊(福建医科大学附属协和医院胸外科);何荣琦(泉州市第一医院肿瘤外科);贾强(武汉大学人民医院疼痛科);刘高峰(联勤保障部队第 988 医院胸外科);李力(北京协和医院胸外科);李颖娴(广州医科大学附属第一医院胸外科);刘志恒(深圳市第二人民医院麻醉科);单汉民(浙江医院疼痛科);宋兰(北京协和医院放射科);孙学军(大连医科大学第一附属医院麻醉科);王博(武汉大学人民医院胸外科);徐卉(同济医学院附属同济医院麻醉科);闫万璞(北京大学肿瘤医院胸外科);闫亚飞(武汉大学人民医院疼痛科);赵晋波(第四军医大学附属唐都医院胸外科);张境浩(广州医科大学附属第一医院疼痛科);占新庆(南平市第一医院胸外科);郑志民(晋江市医院胸外科)
参考文献略。


