7月龄胆道闭锁女婴治疗后反复胆管炎难控制?WES检出线粒体DNA 3243A>G突变探明病因
时间:2026-05-05 17:04:56 热度:37.1℃ 作者:网络
Kasai手术(肝门空肠吻合术)后发生的胆管炎会导致胆道闭锁(BA)患者预后不良。本文报告一例胆道闭锁儿童患者,在接受Kasai手术后出现复发性胆管炎,后续检测发现其携带线粒体DNA(mtDNA)3243 A>G突变。本病例患者为一名 7 月龄女婴,2 月龄时出现黄疸、粪便颜色异常和尿液色深等症状,据此诊断为高胆红素血症。肝胆动态显像提示为胆道闭锁,该诊断经腹部超声检查及腹腔镜探查得到证实。患婴接受了Kasai手术,术后第 19 天出院。但后续出现反复发作、治疗抵抗的胆管炎,因此再次入院。鉴于患者复杂的临床病程,在取得知情同意后进行了基因检测,结果显示存在致病性mtDNA 3243位点(A>G)变异。由于病情严重,患婴在Kasai手术后 5 个月接受了肝移植手术。本文报告了一例以复发性胆管炎为表现的mtDNA 3243 A>G突变罕见病例,提示线粒体功能障碍可能持续诱发炎症。本病例凸显了识别胆道闭锁患者中线粒体突变的重要性,因为这类突变对患者预后具有关键影响。对于伴有复发性胆管炎的胆道闭锁患者,全面的基因评估可能使其获益。
背 景
胆道闭锁(BA)的特征是病因不明的闭塞性胆管病,以及胆管进行性纤维硬化,最终导致严重胆汁淤积、肝纤维化和肝硬化。尽管Kasai肝门肠吻合术及其他围手术期管理策略已有所改进,但许多胆道闭锁患者仍需接受肝移植才能实现长期生存。胆管炎是接受Kasai肝门肠吻合术的患者最常见的并发症,发生率为 30%-70%,通常在术后第一年内发作,尤其多见于术后前 6 个月。多项研究已证实,胆管炎是Kasai术后胆道闭锁患者预后不良的危险因素。
肝脏组织是糖异生、甘油三酯氧化、脂肪酸分解、氨基酸脱氨基与转氨基,以及绝大多数血浆蛋白合成等多种关键代谢过程的主要发生场所。肝细胞内线粒体含量极其丰富,平均每个细胞含有 1000 个线粒体,占细胞总体积的 18%。线粒体突变会对肝细胞造成严重损伤,进而可能影响众多必需的细胞过程。最新研究表明,在非酒精性脂肪性肝病和肝衰竭中,线粒体损伤以及线粒体DNA(mtDNA)的释放,可能会引发炎症小体激活和全身炎症反应。线粒体DNA第 3243 位核苷酸发生腺嘌呤到鸟嘌呤的替换(m.3243 A>G)会影响亮氨酸转运RNA(UUR)基因,已证实会导致多种临床症状,包括线粒体肌病、脑病、乳酸性酸中毒和卒中样发作。该突变会改变转运RNA的加工过程和稳态水平,导致氨基酸错误掺入,进而可能影响炎症通路。本文在此报告一例因胆道闭锁接受Kasai手术后出现复发性胆管炎的患者,其携带mtDNA 3243A>G突变。
病 例
患婴女,7 月龄,2 月龄时,其母亲发现患婴出现黄疸、粪便颜色异常的症状,遂前往当地诊所就诊。首次入院后完善了肝功能全套检查,结果显示总胆红素(TBIL)升高至 114.21 μmol/L,直接胆红素(DBIL)升高至 60.92 μmol/L;同时尿常规提示胆红素2+。随后行肝胆动态显像检查:注射显像剂后 10 分钟内肝脏显影,放射性示踪剂分布均匀;双肾及膀胱也均显影,且膀胱显影随时间推移进行性增强。但 24 小时后观察到肠道内无放射性示踪剂分布,高度提示胆道闭锁诊断。为寻求进一步治疗,患婴被转诊至首都医科大学附属北京儿童医院。患婴整体状况尚可,但存在明显巩膜黄染,皮肤呈棕褐色,粪便为奶油状灰白色。入院后血液检查结果显示,γ-谷氨酰转肽酶水平升高至 578.8 U/L,总胆红素为 127.47 μmol/L,直接胆红素为 92.35 μmol/L(图1)。腹部超声检查提示胆总管显示不清;空腹状态下腹部超声可见胆囊大小为 1.5×0.3×0.4 cm,壁厚 0.25 cm,形态僵硬,内壁不规则。母乳喂养后约 2 小时复查超声,胆囊大小及形态均无变化,支持胆道闭锁诊断。行超声弹性成像检查,在肝右叶随机选取多个位点测量组织弹性,所得平均弹性值为 12.1 千帕(kPa)。
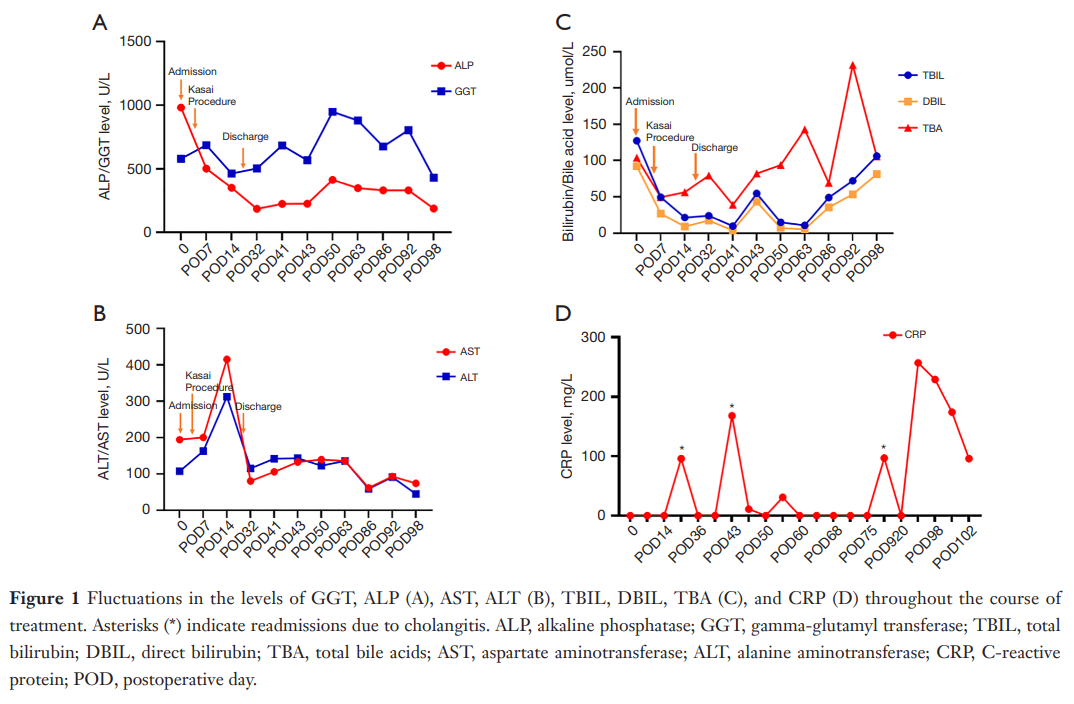
▲图1 治疗过程中 GGT、ALP (A)、AST、ALT (B)、TBIL、DBIL、TBA (C) 和 CRP (D) 水平的波动情况;星号 (*) 表示因胆管炎再次入院
患婴接受了腹腔镜探查手术,腹腔镜直视下可见肝脏肿大,呈棕褐色,伴结节样改变,表面毛细血管增粗,类似蜘蛛痣表现,胆囊细小、发育不良,呈条索状,位于肝裂内。因肝脏体积较大,腹腔镜下无法完成胆道造影,应家属要求,行开腹手术,即Kasai手术,术中采集肝组织、切除的胆囊及肝门部纤维块样本,送病理检查。病理报告显示重要结果如下:肝脏的组织学特征符合肝外胆道梗阻所致的早期胆道纤维化,Ishak分级为 4 级,免疫组化分析显示巨细胞病毒(CMV)阴性,胆管上皮细胞角蛋白7(CK7)阳性,特殊染色结果显示过碘酸-希夫(PAS)染色、Masson染色阳性,铜染色阴性,网状纤维染色阳性;胆囊发育不良;肝门部纤维块标本为少量纤维组织,特征为散在分布的小管腔,内衬扁平上皮,管状结构周围可见淋巴细胞浸润,提示存在炎症反应,此外可见神经丛增生肥大,管周区域伴壁厚不均的血管。术后患婴接受预防性抗生素治疗以预防胆管炎,静脉输注美罗培南(20 mg/kg/次,每 8 小时 1 次),持续 2 周,后续序贯口服头孢地尼分散片与复方磺胺甲恶唑片,每 2 周交替给药,治疗后患婴粪便颜色加深,尿液颜色变浅,皮肤及巩膜黄染逐渐消退。术后 19 天,随访血生化检查显示γ-谷氨酰转肽酶为 463.7 U/L,总胆红素为 21.5 μmol/L,直接胆红素为 9.05 μmol/L(图1),患婴出院。尽管初期症状改善,但术后 3 个月内患婴仍出现复发性胆管炎,先后 3 次再次入院。住院期间完善了全面的诊断评估:连续监测C反应蛋白(CRP)水平(图1D),提示持续炎症反应,峰值达 257 mg/L;发热(体温 ≥38.5℃)发作时采集外周血培养,经 120 小时孵育后均无细菌生长。每次住院均经验性启动静脉美罗培南(20 mg/kg,每 8 小时 1 次)治疗,前两次发作时,发热于 72 小时内消退,患婴体温正常后出院。但最后一次住院期间,患婴持续高热(>39℃)且CRP水平进行性升高,遂升级治疗方案,加用氟康唑(覆盖真菌感染)及静脉免疫球蛋白(IVIG),尽管采取上述干预措施,临床症状仍无改善,随后加用利奈唑胺覆盖疑似耐药病原体,但炎症标志物仍持续升高。此外,超声弹性成像评估的肝脏弹性值持续升高,达 42.0 kPa,提示肝纤维化进展,术后第 77 天行磁共振胰胆管造影,显示肝内胆管扩张(图2)。
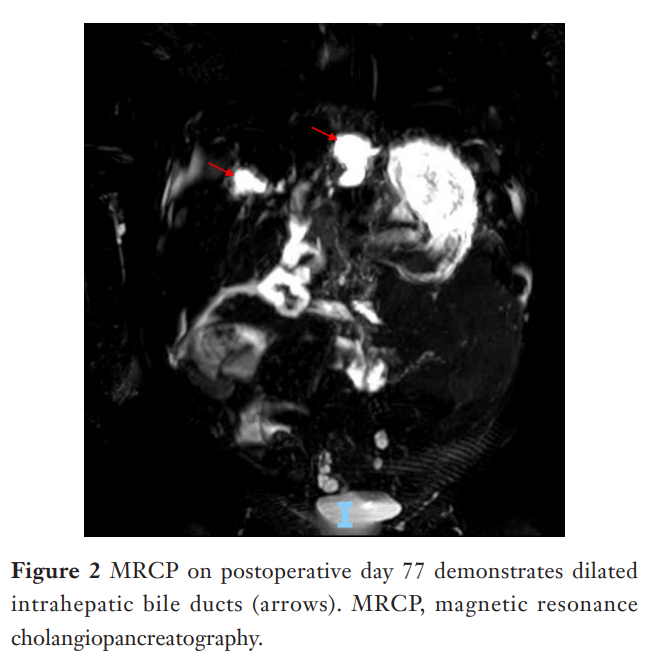
▲图2 术后第77天进行的磁共振胰胆管造影(MRCP)显示肝内胆管扩张(箭头所示)
鉴于患婴复杂的临床病程,在取得知情同意后,采用全外显子测序(WES)进行了遗传学检测,结果显示线粒体DNA第 3243 位存在致病性变异(A>G),突变丰度为 9195/(9195+2432)(79.08%)。家系谱系分析显示,患者母亲的同一位点突变丰度为 3931/(3931+21076)(15.72%)(图3)。由于肝脏疾病进展且胆管炎无法得到控制,患婴在初次手术后 5 个月于外院接受了肝移植手术。患者术后恢复顺利,在 20 月龄的末次随访时情况保持稳定。
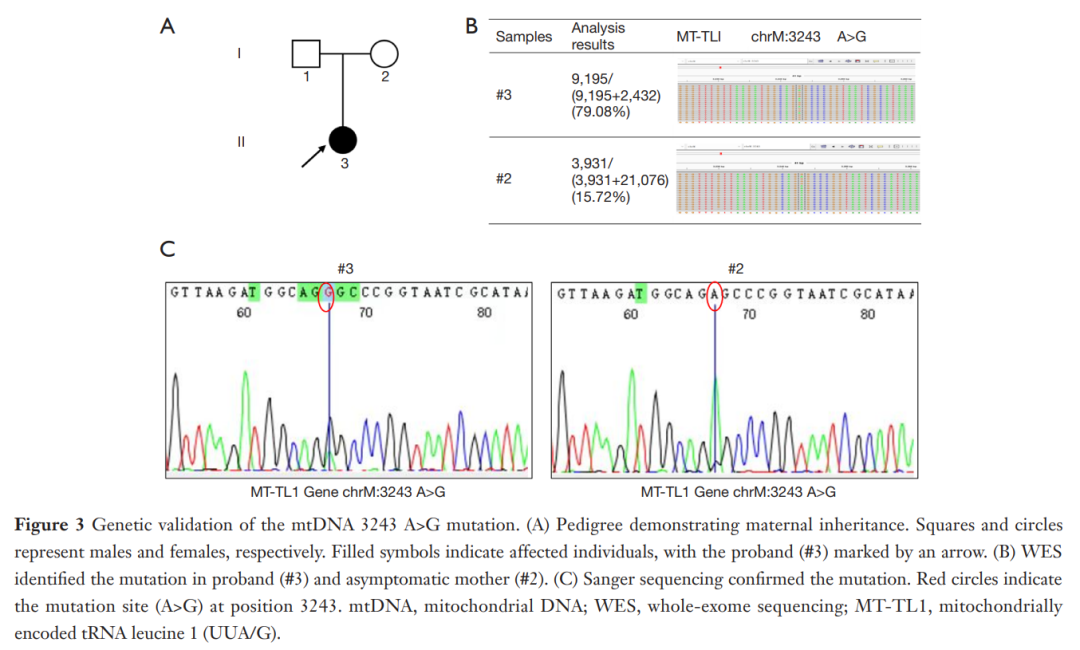
▲图3 线粒体DNA 3243 A>G突变的遗传验证
讨 论
胆管炎仍是胆道闭锁患者接受Kasai手术后的主要并发症,大量研究证实其对患者的长期预后具有关键影响。反复发作的胆管炎会加快肝纤维化进展,最终成为肝移植的重要指征。尽管术后胆管炎影响重大,但这类发作的根本原因目前仍未完全阐明。
本文报告了首例携带mtDNA 3243 A>G突变、伴复发性胆管炎的胆道闭锁患者病例。mtDNA 3243 A>G突变发生于亮氨酸转运RNA(UUR)二氢尿嘧啶环的保守核苷酸位点,最常与线粒体脑病、乳酸性酸中毒和卒中样发作(MELAS)相关。mtDNA 3243 A>G突变的表型表达具有高度异质性,已在多种疾病中被检出,包括2型糖尿病伴耳聋综合征、进行性眼外肌麻痹、VACTERL综合征、膜性肾病、结肠癌、急性胰腺炎及肝衰竭等。在所有这类突变和多态性中,仅少数能与已知的表型效应建立关联。一项纳入 151 名携带mtDNA 3243 A>G突变患者的 6 年前瞻性研究发现,这些患者的表型差异极大,其中57例无法与任何已知表型对应,被归入“其他”组别。在确诊为多呼吸链酶缺陷的儿童中,50%(100 例中的 50 例)存在mtDNA耗竭,其中 64%(50 例中的 32 例)的患者自新生儿期起就出现严重肝脏受累。值得注意的是,其中半数病例的潜在突变仍未明确,提示存在更多的遗传异质性。另一项研究对 3 名急性肝衰竭患儿进行了全外显子测序,结果显示MPV17、SERAC1和NOTCH2基因存在致病突变,尽管这些患者没有出现与这些基因改变相关的典型临床表现。基于既往研究结果,罕见遗传因素可能是部分患者急性肝衰竭的诱因,通过下一代测序技术进一步探索或可发现新的线粒体表型。本例患者携带的该突变,提示其可能与Kasai术后复发性胆管炎的发病机制相关。
胆道闭锁的炎症和纤维化过程涉及胆管损伤与胆管细胞凋亡,最终可导致肝纤维化、肝硬化,甚至终末期肝病。失调的炎症反应是胆道闭锁病程中的关键因素,会驱动疾病进展、恶化预后。线粒体功能障碍是包括酒精性肝病(ALD)、非酒精性脂肪性肝病(NAFLD)、肝纤维化和药物性肝损伤在内的多种肝脏疾病的核心诱因,但胆道闭锁中肝线粒体功能障碍的具体机制目前仍不明确。胆道闭锁中的线粒体功能障碍可能源于毒性胆汁酸蓄积,后者会诱导氧化应激、加剧炎症反应,进而造成细胞损伤,包括细胞衰老和线粒体功能异常。线粒体在三磷酸腺苷(ATP)生成、活性氧(ROS)产生、信号传导、胞质钙离子转运及凋亡调控中发挥关键作用。mtDNA突变会扰乱细胞能量转导,损害肝脏能量代谢,进而影响肝脏再生能力和炎症应答能力。Koh等在胆道闭锁患者中发现了34种常见的mtDNA蛋白编码基因非同义变异,全面的三维结构分析显示,这些突变位于呼吸链复合物I至V的关键区域,参与亚基组装、质子转运和超复合物组装过程。值得注意的是,胆道闭锁患者的慢性肝损伤程度和肝功能异常与肝衰竭程度密切相关,提示mtDNA突变可能加重肝病,是胆道闭锁相关病理的潜在基础机制。Nakajima等发现,接受Kasai肝门肠吻合术和肝移植的胆道闭锁患者中,细胞衰老和mtDNA损伤进展与临床分期相关,可作为肝移植的参考指标。Lane等在与原发性线粒体疾病无关的严重肝衰竭病例中观察到线粒体功能障碍,在因各种原因接受肝移植评估的 45 名患者中,9 例为胆道闭锁患者,其中 20%-50% 存在不同程度的线粒体改变,但这些改变在胆道闭锁发病机制中的作用仍不明确,可能与肝细胞功能障碍的特定阶段相关,而胆道闭锁患者白细胞中mtDNA拷贝数较低也支持这一点,提示存在炎症和继发性mtDNA损伤。此外,mtDNA拷贝数降低也与胆道闭锁、严重纤维化、黄疸及肝功能异常的风险升高相关。值得注意的是,本例患者检出了与多种线粒体疾病和肝脏病变相关的mtDNA 3243 A>G突变,提示线粒体功能障碍与Kasai术后复发性胆管炎之间可能存在关联,尽管导致该患者表型的确切机制仍不明确。未来研究需通过实验模型和大规模队列验证mtDNA 3243 A>G突变的功能影响,以明确其临床意义。此外,尽管全外显子测序结果显示,本例患者的核基因中未发现具有临床意义的致病性单核苷酸变异(SNVs)或大片段拷贝数变异(CNVs),但检出了大量意义未明的变异(VUS),后续研究需进一步验证这些变异,以明确其在疾病中的潜在作用。
综上,本病例报告揭示了胆道闭锁、复发性胆管炎与mtDNA 3243 A>G突变之间的罕见关联。本文研究结果表明,该突变引发的线粒体功能障碍可能是Kasai术后复发性胆管炎的诱因之一。这凸显了对伴复发性胆管炎的胆道闭锁患者进行基因评估,尤其是线粒体突变筛查的重要性。全面的基因分析有助于深入了解疾病进展,为个体化治疗提供指导。
参考文献:
Sun, Jie#; Zhang, Yanan#; Sun, Dayan; Huang, Jinshi. MtDNA 3243 A>G mutation and recurrent cholangitis after Kasai procedure in biliary atresia: a case report. Translational Pediatrics 14(3):p 522-528, March 31, 2025. | DOI: 10.21037/tp-2024-592


