【协和医学杂志】基于机器学习的老年原发性膜性肾病预后预测模型构建
时间:2026-05-05 17:02:53 热度:37.1℃ 作者:网络
原发性膜性肾病(PMN)是成人原发性肾病综合征中最常见的病理类型,其发病率在老年人群中呈逐年上升趋势[1-3]。随着全球人口老龄化的加剧,老年PMN的临床管理已成为肾脏病学领域面临的严峻挑战。与中青年患者相比,高龄不仅是PMN预后不良的独立危险因素[4-5],更常伴随复杂的临床管理难题。
老年PMN患者常合并高血压、糖尿病及心血管疾病等慢性疾病,并伴有器官功能减退及免疫衰老等生理特点[6-8]。这些病理生理特征导致老年患者对免疫抑制治疗的耐受性差,感染等并发症发生率更高,且完全缓解率及肾脏长期存活率均显著低于年轻群体[9-13]。因此,如何在避免过度治疗所致医源性损伤与积极干预以延缓肾衰竭之间取得平衡,成为老年PMN管理的核心难点。实现这一平衡的关键在于,早期、精准识别出预后不良的高危个体。
然而,目前经典的PMN预后预测工具,如基于蛋白尿和肾功能的多伦多风险评分,多源于混合年龄队列[14]。在多数预测模型中,年龄通常仅作为一个线性协变量纳入分析[15-18]。这种处理方式难以体现老年患者群体的复杂特征:例如,年龄与肾功能下降之间可能存在非线性交互关系,且老年患者面临更高的竞争性死亡风险(非肾脏原因导致的死亡)以及独特的代谢背景。现有通用模型往往难以捕捉这些老年特异性风险特征,导致其在老年亚组中的预测效能不足。尽管近年来针对抗磷脂酶A2受体(PLA2R)抗体等生物标志物的研究增多,但目前仍缺乏基于真实世界数据、整合“临床-生化-病理”多维度特征的老年PMN预后预测模型。
为此,本研究旨在整合肾穿刺活检时多维度临床病理信息,构建适用于老年PMN患者的预后预测模型,以实现对疾病的早期精准分层,进而指导临床医生制定个体化的免疫治疗方案及随访策略。
1 资料与方法
1.1 研究对象
本研究为单中心回顾性队列研究,纳入2010年1月1日至2022年12月31日于中山大学附属第一医院经肾穿刺活检确诊为PMN的老年患者。
纳入标准:(1)经肾穿刺活检确诊为PMN;(2)年龄≥60岁;(3)估算的肾小球滤过率(eGFR)>15 mL/(min·1.73 m2)。
排除标准:(1)继发性膜性肾病(如肿瘤、风湿免疫性疾病、感染、遗传及药物/毒物等继发因素所致膜性肾病);(2)随访期间未发生终点事件,且随访时间<12个月(截至2024年12月30日)。
本研究已通过中山大学附属第一医院伦理委员会批准(审批号:No.[2024]846),并遵循《赫尔辛基宣言》。
1.2 数据收集及预处理
通过电子病历系统收集患者人口学信息及基线临床病理资料,并通过门诊病历系统或电话随访获取患者的治疗反应及肾功能预后信息。所有基线资料均为肾穿刺活检时获取,不包含任何随访数据。病理学指标由2名经验丰富的病理科医师独立评估肾活检标本。肾小球损伤通过球性硬化比例、节段硬化比例、新月体比例以及有无肾小球囊粘连评估。
肾小管间质损伤方面,根据病变程度对小管萎缩及间质纤维化进行半定量分级,间质纤维化具体分为无、轻度、中度、重度;肾小管损伤严重程度按受累面积占比(0,0~5%,5%~25%,25%~50%,50%~100%)进行分类;肾脏免疫病理染色强度按阴性、1+、2+、3+和>3+分级记录。
人口学资料及肾穿刺活检时的实验室检查结果亦被收集,并使用CKD-EPI公式估算eGFR;连续性变量保留原始数值,所有非等级计数资料均按“有/无”二分类记录。为降低变量间的共线性,采用平均动脉压(舒张压+1/3×收缩压)综合反映血压水平,并使用血清总蛋白(TP)综合反映血清蛋白水平。
为降低数据缺失导致的潜在偏倚,本研究剔除了缺失值比例超过25%的变量。此外,小管性蛋白尿指标[如尿α1微球蛋白、尿β2微球蛋白(β2-MG)]与肾功能预后密切相关,具有重要临床价值[19]。尽管该组指标在部分早期入组患者中未作为常规检查项目,缺失率略高于25%(附件1),但由于其缺失主要源于检测时期的临床实践差异,而非患者病情严重程度,性质接近随机缺失,仍予以保留。随后,采用基于R语言mice包中的分类回归树(CART)插补方法对缺失数据进行多重插补。
1.3 结局事件定义
本研究的主要观察终点定义为复合肾脏不良结局或死亡,包括:
1 进展至终末期肾病(ESRD),定义为eGFR 持续低于15 mL/(min·1.73 m2) 超过3个月,或开始规律透析/肾移植;
2 肾功能显著恶化,定义为eGFR较基线水平下降≥50%;
3 全因死亡。
此外,临床疗效评估参照KDIGO指南标准[20],具体定义如下:
1 完全缓解(CR),24 h尿蛋白定量<0.3 g/d且血清白蛋白>35 g/L;
2 部分缓解(PR),24 h尿蛋白定量<3.5 g/d且较基线水平下降>50%。
1.4 模型构建、评估、解析及应用
本研究采用基于随访时间分层的随机拆分方法,按7:3比例将数据集划分为训练集和验证集。首先,为从95个初始临床特征中筛选出最稳健的预测因子,本研究在训练集中采用最小绝对收缩和选择算子(LASSO)回归进行变量筛选;其次,基于随机生存森林(RSF)模型输出的变量重要性排序,选取重要性排名前20位的变量(附件2)。综合上述算法结果,并结合既往文献报道及变量的临床意义[16-17,19,21-25],最终确定候选自变量集合。随后,采用 Spearman 秩相关分析降低变量多重共线性对模型稳定性的影响(对于相关系数 | r |>0.5的变量,保留与终点事件相关性更强的变量)。
本研究最终共纳入23个自变量用于初始模型构建,包括:性别、年龄、合并高血压、合并糖尿病、eGFR、尿素、TP、二氧化碳结合力(CO2 CP)、载脂蛋白B与载脂蛋白A1比值(ApoB/ApoA1)、血小板计数(PLT)、活化部分凝血活酶时间(APTT)、纤维蛋白原(Fbg)、血清免疫球蛋白G(IgG)、血清补体3(C3)、血清补体C4、尿糖、24 h尿蛋白定量、β2-MG、尿免疫球蛋白G/尿白蛋白比值(uIgG/ALB)、肾小球节段硬化比例、肾小球囊粘连、肾小球C3沉积强度及肾小管萎缩程度。
在训练集中,采用惩罚 Cox 比例风险回归模型进行建模,采用5折交叉验证确定最优正则化参数,基于23个自变量构建初始模型。根据自变量平均绝对SurvSHAP(t)(Time-Dependent Survival Shapley Addi-tive Explanations,时间依赖性生存SHAP解释)值从低到高逐步剔除,构建简约预测模型,并在验证集中对模型进行独立性能验证,根据验证集Harrell一致性指数(C-index,简称C指数)和受试者工作特征曲线下面积(AUROC)的变化趋势,选择最终模型。模型性能评价包括:
1 模型区分度,采用C指数评估总体区分度,计算时间依赖性AUROC及精确率-召回率曲线下面积(AUPR)评估模型在关键时间点的判别能力;
2 模型校准度,通过绘制校准曲线及计算Brier评分评价模型预测风险与实际观察风险的一致性;
3 临床实用性,采用决策曲线分析(DCA)评估模型在不同风险阈值下的临床净获益。
基于最终模型,分别计算每例患者在3年、5年及10年时间点发生终点事件的预测风险概率。在训练集中,采用约登指数(Youden index)确定各时间点对应的风险阈值。随后,将这些时间特异性阈值分别应用于训练集和验证集,对患者进行风险分层。最后,通过Kaplan-Meier(KM)生存分析,评估模型在不同随访时间点(3年、5年、10年)的风险区分能力,并将模型转化为简易计算器便于临床应用。研究设计流程图详见图1。
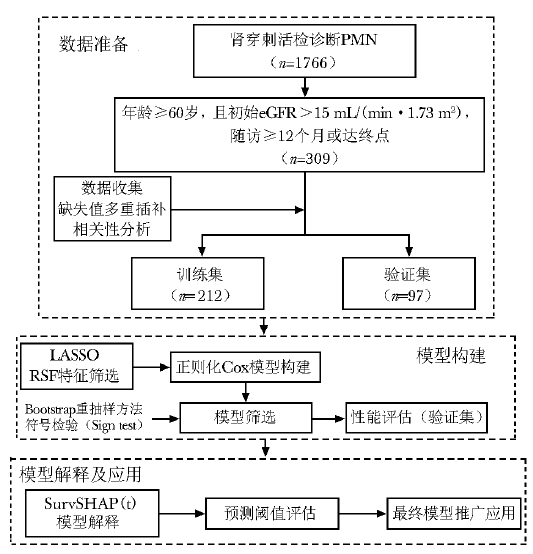
图1 研究设计流程图
注:PMN:原发性膜性肾病;eGFR :估算的肾小球滤过率;LASSO:最小绝对收缩和选择算子;RSF:随机生存森林
1.5 样本量估算
本研究基于预后模型构建的样本量估算原则。考虑到数据集中主要终点发生率为38.2%,基于事件每变量(EPV)至少需10~15例的要求,计划在惩罚性Cox回归模型中纳入不超过10个候选预测因子,至少需100~150例终点事件。本研究最终收集到118例终点事件,基本满足模型稳定性对事件数的需求(EPV=8~12)。
1.6 统计学处理
本研究采用R软件(v4.3.0)进行统计分析。符合正态分布的连续变量以均数±标准差表示,不符合正态分布的连续变量以中位数(四分位数)表示。分类变量以频数(百分数)表示。所有检验均为双侧检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 研究人群的基线特征
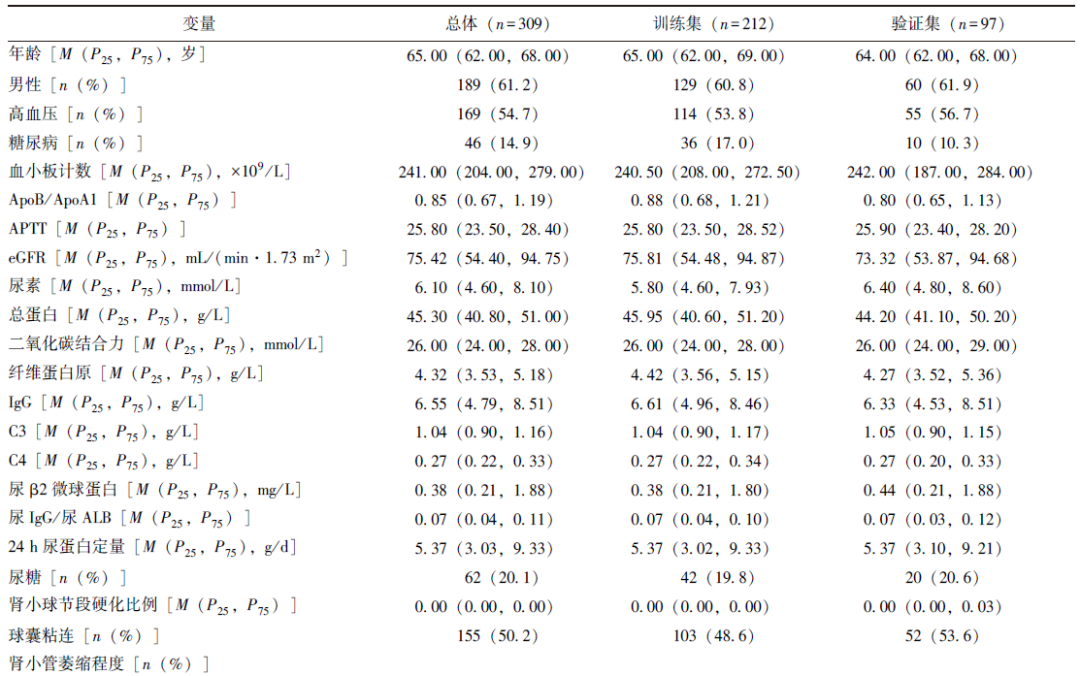
本研究共纳入309例老年PMN患者,中位年龄为65.00(62.00,68.00)岁,其中男性占61.2%(189/309)。合并症方面,54.7%(169/309)的患者合并高血压,14.9%(46/309)合并糖尿病。中位随访时间为47.00(25.00,89.00)个月,随访期间,38.2%(118/309)的患者发生终点事件。按7:3的比例将患者随机划分为训练集(212例)和验证集(97例)。其中,训练集有74例(34.9%)发生终点事件,验证集有44例(45.4%)发生终点事件,总体人群、训练集与验证集基线特征分布见表1。
表1 总体人群、训练集与验证集基线特征

2.2 最终模型的筛选与验证
在基于原始模型中各变量的平均绝对 SurvSHAP(t) 值(附件3)进行逐步变量剔除,构建老年PMN患者不良结局(ESRD/eGFR下降≥50%/死亡)最优预测模型的过程中,当纳入变量数减至8个时,训练集C指数出现明显转折点;而变量数多于8个时,C指数趋于稳定(图2A)。
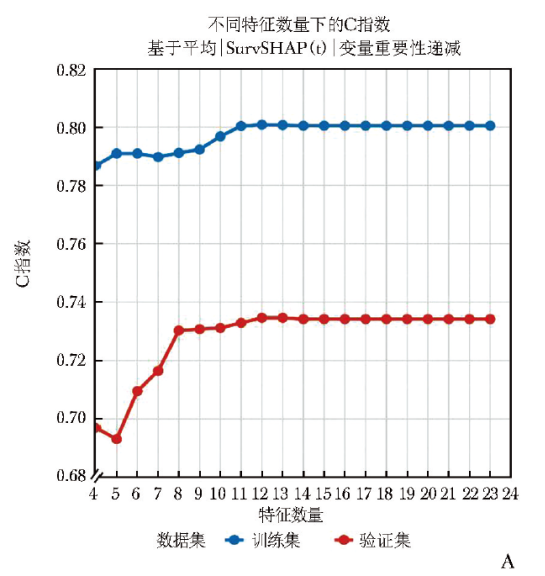
图2 逐步变量递减过程中模型性能指标的变化:A. 训练集与验证集C指数
AUROC:受试者工作特征曲线下面积;AUPR:精确率-召回率曲线下面积
综合考量模型简洁性与预测效能,含9个变量的模型表现最优。与包含全部23个变量的初始模型相比,该9变量模型保持了相当的区分能力(ΔC指数=-0.003,P=0.664)(附件4)。此外,该模型在AUROC、AUPR及Brier评分方面均表现优异(图2B~2D),提示其在精确度和校准度方面亦有优势。
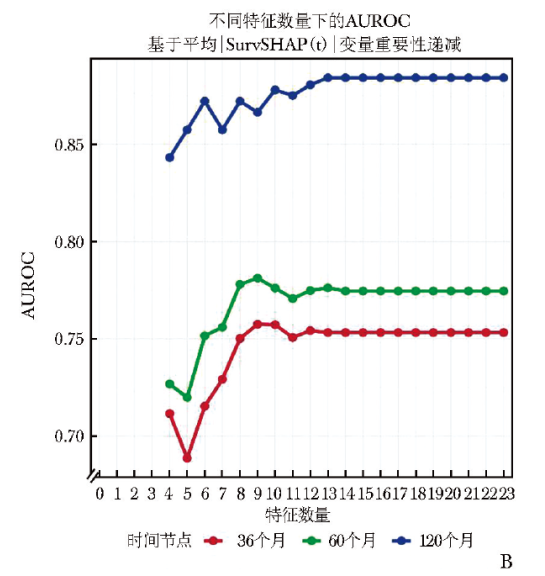
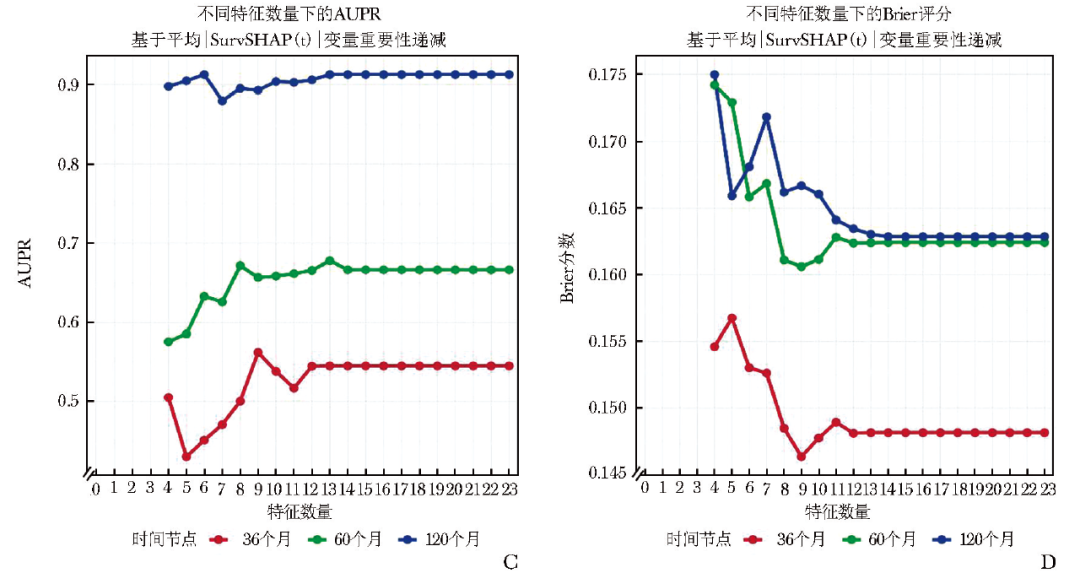
图2 逐步变量递减过程中模型性能指标的变化:B.验证集AUROC;C.验证集AUPR;D.验证集Brier评分
AUROC:受试者工作特征曲线下面积;AUPR:精确率-召回率曲线下面积
在验证集中,该9变量模型展现出稳定的预测性能:C指数为0.731(95% CI:0.652~0.797);时间依赖性AUROC在36个月、60个月和120个月分别为0.758(95% CI:0.614~0.901)、0.781(95% CI:0.646~0.916)和0.866(95% CI:0.740~0.993)(图3A)。
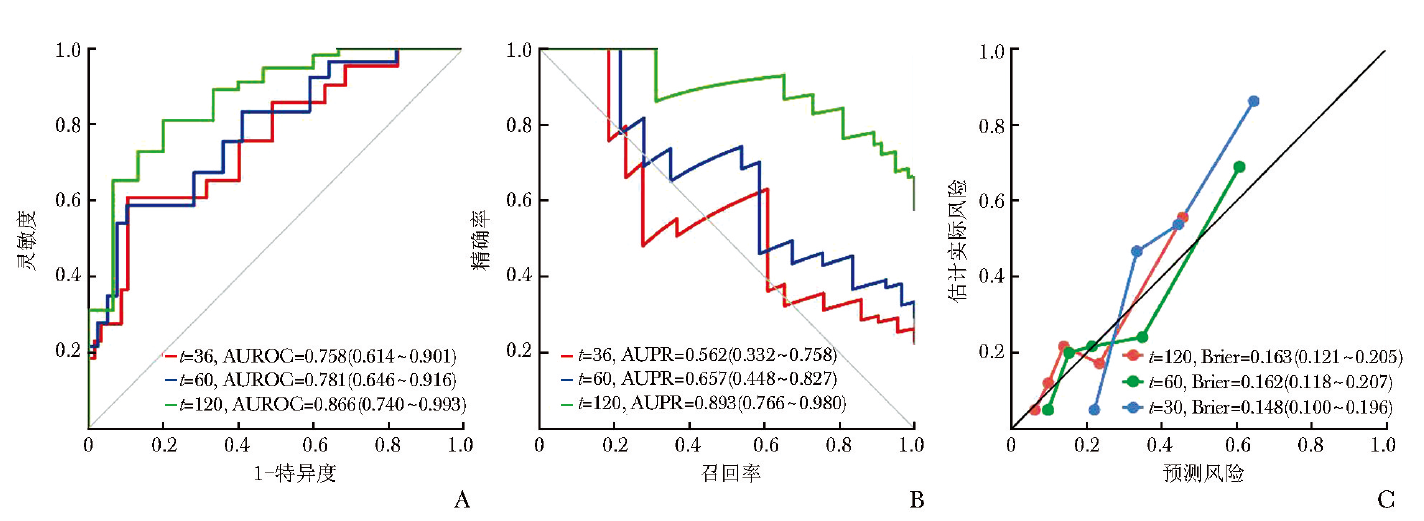
图3 最终模型在验证集36个月、60个月及120个月时间点的预测性能
A.AUROC;B.AUPR;C.校准曲线
决策曲线分析进一步证实,该模型在3年、5年及10年的预测时间窗内均具有显著的临床净获益(图3D~3F),提示其具备良好的临床转化潜力。
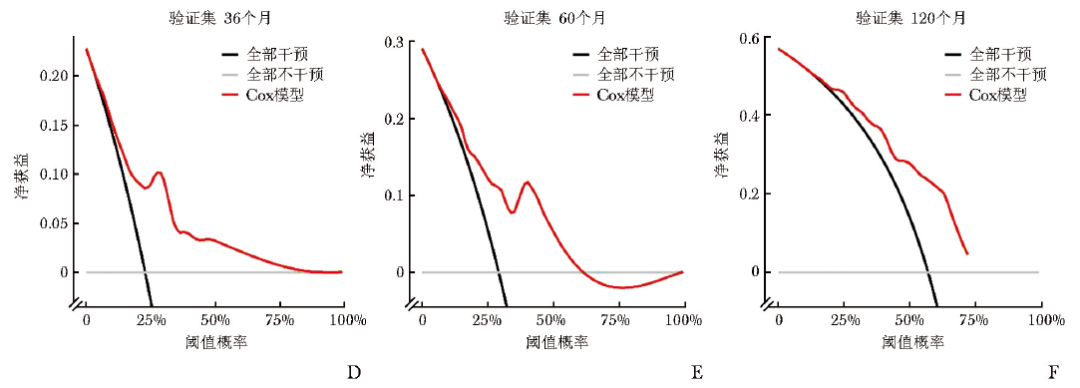
图3 最终模型在验证集36个月、60个月及120个月时间点的预测性能
D.决策曲线分析(36个月);E.决策曲线分析(60个月);F.决策曲线分析(120个月)
模型在训练集中同样表现出良好的预测效能(附件5)。基于上述结果,最终选定包含9个变量的模型用于后续分析。最终纳入的预测因子包括:eGFR、TP、肾小球囊粘连、肾小球节段硬化比例、尿糖、Fbg、尿素、年龄及APTT。
2.3 模型解释
为提升模型可解释性,本研究采用SurvSHAP(t)方法来解释最终模型的输出,从特征层面的全局解释和个体层面的局部解释来解析最终的模型。
全局解释:计算每个变量对预测模型的贡献度来实现模型的可解释性。采用SurvSHAP(t)值评估各特征对模型的贡献度,并按降序排列展示,其中eGFR、TP、肾小球囊粘连、尿糖以及肾小球节段硬化比例对模型的贡献度排名前五位(图4A、B)。
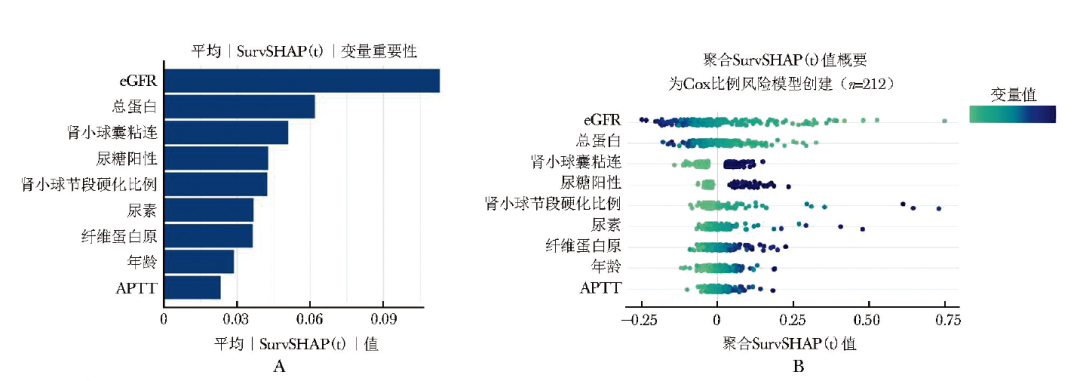
图4 基于SurvSHAP(t)方法的全局模型解释
A.基于平均|SurvSHAP(t)|的全局特征重要性排序图;B.聚合SurvSHAP(t)特征重要性点图
注:肾小球囊粘连、尿糖为二分类变量,赋值:0.00=阴性,1.00=阳性; APTT:同表1;eGFR:同图1
此外,聚合SurvSHAP(t)依赖图(图4C)展示了单个特征对模型输出的影响,其中 SurvSHAP(t)值>0 表示该特征对终点事件风险呈正向贡献(增加风险)。
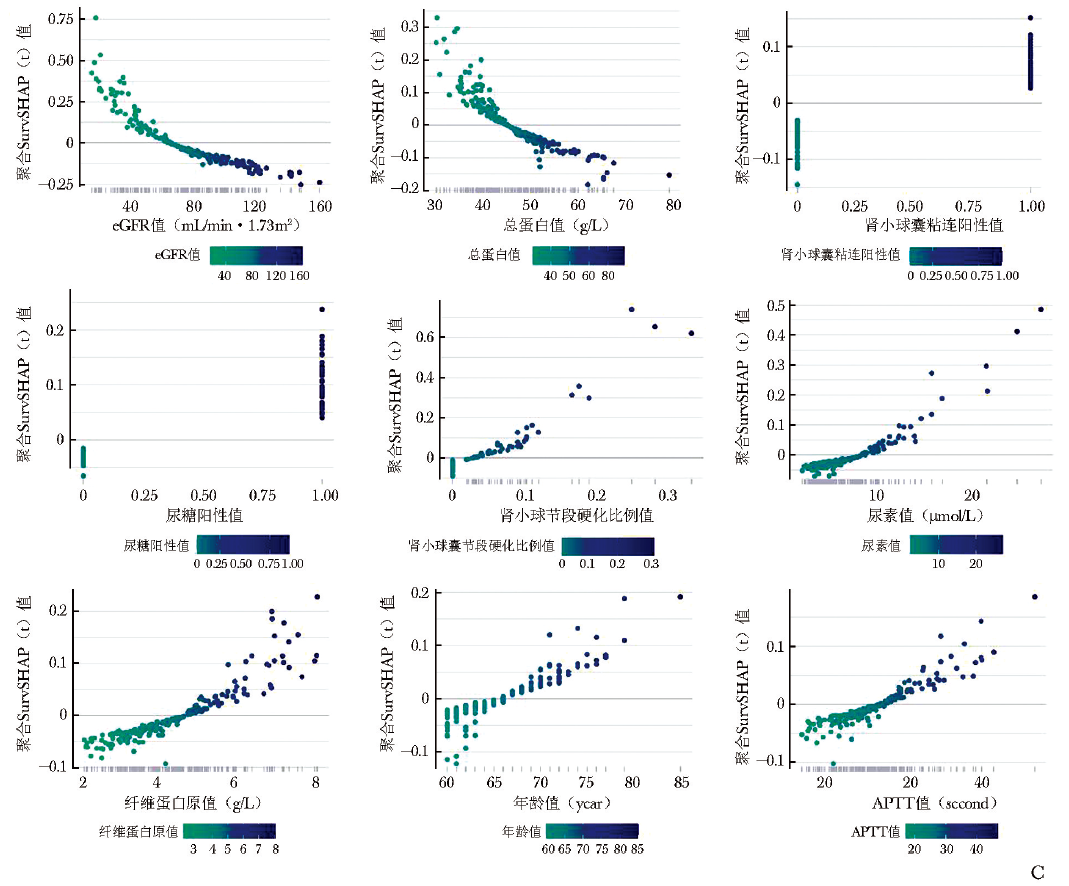
图4 基于SurvSHAP(t)方法的全局模型解释
C.聚合SurvSHAP(t)依赖图
注:肾小球囊粘连、尿糖为二分类变量,赋值:0.00=阴性,1.00=阳性; APTT:同表1;eGFR:同图1
例如,eGFR<65.5 mL/(min·1.73 m2)、TP<45.3 g/L、肾小球节段硬化比例 > 2.9%,以及年龄 > 66岁,均表现为SurvSHAP(t)值呈正值,提示这些因素达到或超过上述阈值时,患者发生终点事件的风险增高。
局部解析:为展示模型在个体层面的预测能力,图5呈现了2例代表性患者的局部解析结果。图5A为1例高风险患者:模型预测其3年、5年及10年发生终点事件的概率分别为55.18%、72.34%及95.74%,该患者在随访25个月时实际发生终点事件。对其预测贡献最大的危险因素包括肾小球节段硬化比例(33.33%)、肾小球囊粘连以及初始eGFR<65.5 mL/(min·1.73 m2)。图5B则为另一例低风险患者:模型预测其3年、5年及10年发生终点事件的概率分别为7.81%、12.22%及27.39%,该患者随访至109个月仍未发生终点事件。
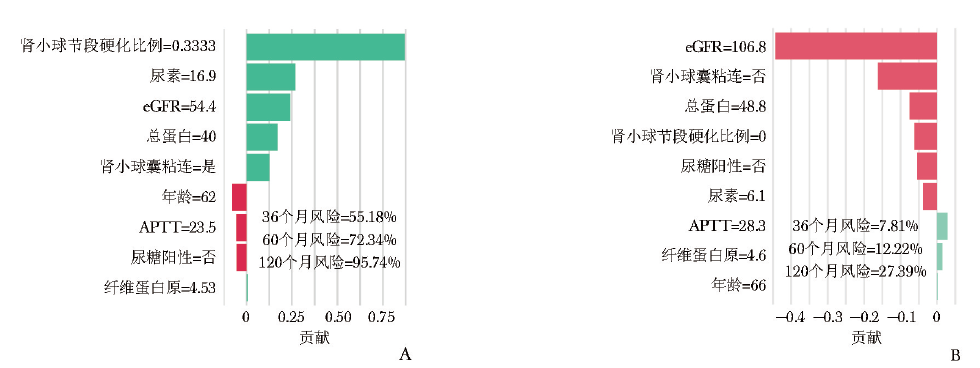
图5 模型解释及应用
A.1例高风险患者的危险因素贡献(随访25个月发生终点事件);B.1例低风险患者的危险因素贡献(随访109个月时未发生终点事件);
2.4 模型应用
基于训练集,采用约登指数确定模型在3年、5年及10年预测终点事件的概率阈值,分别为18.46%、25.74%和47.73%。这些阈值实现了敏感性与特异性的最佳平衡,据此可将患者分为“预测模型阳性”(高风险)与“预测模型阴性”(低风险)两组。在验证集中,基于上述阈值划分的两组患者预后存在显著差异(图5C),验证了风险分层策略的可靠性。
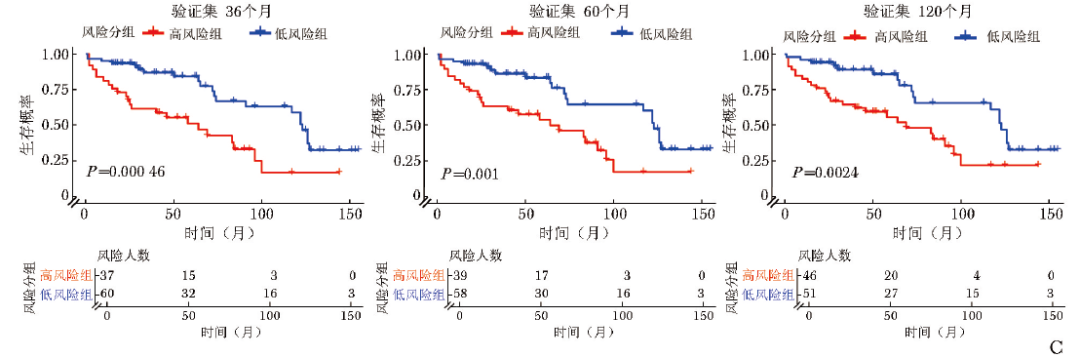
图5 模型解释及应用
C. 基于3、5、10年风险阈值(分别为18.46%、25.74%、47.73%)将验证集患者分为高、低风险组,KM分析发现各时间点高风险组预后均较差
为便于临床应用,笔者将最终模型部署为网页版简易计算器(图5D)。用户输入9项预测特征(eGFR、TP、肾小球囊粘连、肾小球节段硬化比例、尿糖、Fbg、尿素、年龄、APTT)后,即可自动预测个体患者在3年、5年及10年发生终点事件的发生风险,为临床决策提供量化支持。
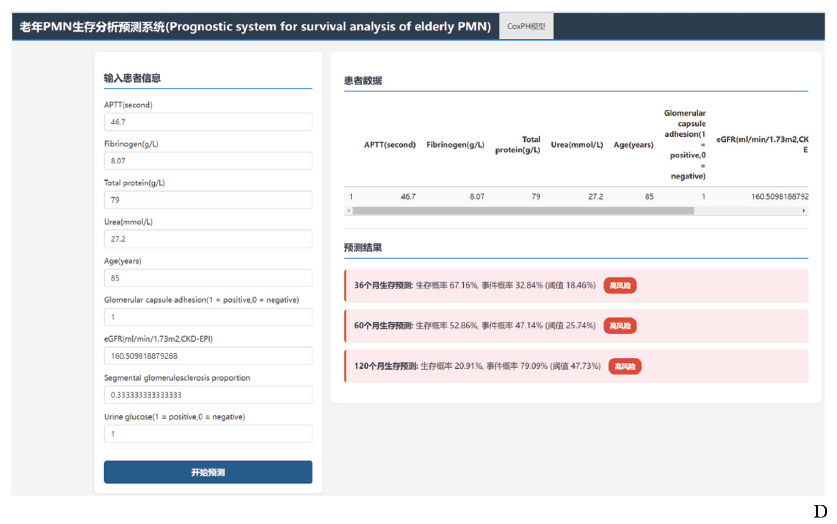
图5 模型解释及应用
D. 将该预测模型构建为简易网页计算器用于临床应用
3 讨论
随着人口老龄化,老年PMN发病率逐渐增加[1-3],是老年肾病综合征最主要的病理类型。老年PMN因其特有的病理生理学特点,其预后评估和治疗决策面临更大的不确定性。本研究首次基于机器学习算法,整合肾穿刺活检时的基线“临床-生化-病理”多维度信息,构建并验证了专门针对60岁以上老年PMN患者的长期预后预测模型。
模型纳入的9个常规临床指标包括eGFR、TP、肾小球囊粘连、尿糖、肾小球节段硬化比例、Fbg、尿素、年龄及APTT,均为肾穿刺活检时易于获取的基线数据,无需随访资料。该模型可实现在肾穿刺活检时即刻对患者的远期预后进行个体化预测,具有高度临床实用性和可操作性。
模型C指数为0.731(95% CI:0.652~0.797),在短期及长期时间窗内均具有良好预测性能,其3年、5年及10年的AUROC值分别达到0.758、0.781和0.866,临床净获益在3年、5年及10年的预测时间窗内均得到决策曲线分析证实,为老年PMN患者的风险分层和个性化管理提供了便捷、科学的潜在工具。
本研究的主要优势在于首次针对老年PMN这一特殊人群开发了专用的预后预测工具。与既往基于全年龄段人群的经典模型(如Ponticelli风险评分[26])或基于PLA2R抗体的预测工具[27]不同,本模型单独对老年患者预后进行预测,充分考虑了老年患者特有的临床背景,如合并症负担、免疫衰老导致的治疗反应差异[7],以及与年龄相关的竞争死亡风险[4]。这些因素在混合年龄模型中被简化为线性协变量,可能无法准确捕捉老年患者预后的非线性复杂关联。
另外,KDIGO指南将随访6个月的蛋白尿缓解情况作为危险分层和启动免疫治疗的关键依据[20]。然而,对于老年患者而言,6个月的观察期可能错过最佳干预时机或予以过度免疫治疗。本研究基于肾穿刺活检时的基线资料即可早期预测个体预后,为临床医生制订个体化、及时的干预策略提供了潜在工具。例如对模型预测阳性患者,可在肾活检时即制订个性化免疫治疗方案,增加随访频率,关注并预防感染及心血管并发症。
本研究纳入的预测因子具有明确的病理生理学意义。既往研究多强调肾小管间质纤维化在PMN疾病进展中的作用[28],本研究发现除基线eGFR这公认的强预测因子外,肾小球节段硬化比例以及反映肾小球活动性炎症的肾小球球囊粘连对预后的影响较间质纤维化权重更高。既往研究提示,肾小球节段硬化及eGFR是公认的肾脏预后强预测指标[14,28-29],而肾小球球囊粘连与肾小球节段硬化反映了足细胞损伤后肾实质不可逆的持久性损伤的病变,与PMN患者更低的治疗缓解及更差的肾功能显著相关[25],提示老年PMN肾脏代偿性能力减弱,一旦出现肾小球损伤,更易跨越“不可逆损伤”阈值,肾小球炎症的控制对改善PMN预后具有重要意义。
值得注意的是,本研究发现凝血相关指标(Fbg、APTT)及代谢指标(尿糖、尿素)是老年PMN预后的重要预测因子。老年PMN患者因高龄、肾病综合征及卧床等因素,常处于高凝状态。高Fbg水平不仅增加了血栓栓塞并发症的发生风险,还可能通过诱发肾内微血栓形成及内皮细胞损伤,加速肾小球硬化进程,这与此前研究提出的“炎症-凝血-内皮损伤”在慢性肾脏病进展中的作用机制相符[30]。同时,尿糖的纳入不仅反映了糖尿病这一常见合并症的负面影响,高尿糖还可能提示肾小管重吸收功能受损(即使在血糖正常时),反映了老年患者更为脆弱的肾小管功能储备。
在方法学上,本研究采用的LASSO回归联合RSF策略,从多维临床病理资料中筛选出与终点事件真正相关的因素。针对机器学习模型“黑箱”属性导致的临床应用障碍,本研究使用SurvSHAP(t)分析解析变量对模型及个体的贡献,使临床医生能够直观理解为何某些蛋白尿尚可但伴有高凝和肾小球硬化的老年患者会被判定为极高危人群,从而支持更积极或更审慎的治疗决策。与关注短期蛋白尿缓解的模型不同,本研究将全因死亡纳入复合终点。既往队列研究表明,老年PMN患者面临的主要威胁往往来自心血管事件或感染导致的死亡,而非单纯的肾衰竭[31-32]。本模型在预测5年及10年长期结局方面表现优异(AUROC>0.78),提示其不仅能预警尿毒症风险,更能识别出那些处于“生理脆弱期”的高危个体,从而指导医生在关注免疫治疗的同时,强化对心血管风险及感染并发症的综合管理。
本研究存在一定局限性:(1)本研究为单中心回顾性设计,尽管进行了内部随机验证,但模型的外推性仍需多中心、大样本的前瞻性队列研究进一步证实;(2)本研究训练集的212例患者,74例(34.9%)达终点事件,EPV为8.2,略低于传统推荐的10,尽管模型在独立验证集中表现良好,但对机器学习来说,该样本量可能无法使机器学习模型达到最佳训练状态,未来需基于更大样本及终点事件建立更加稳健的预测模型;(3)受限于研究跨度(2010—2022年),早期患者缺乏基线抗PLA2R抗体数据,导致该指标未被纳入。
值得注意的是,在老年人群中,反映器官累积损伤的指标(肾小球节段硬化及球囊粘连等肾小球不可逆性损伤、eGFR)对长期预后的决定权可能高于免疫学指标。然而,抗PLA2R抗体滴度与病情活动度密切相关[20],未来的研究应致力于构建整合新型血清学标志物[如抗PLA2R及抗1型血栓反应蛋白结构域7A(THSD7A)抗体等]、遗传易感因素及老年综合评估指标的前瞻性动态预测模型。
4 小结
综上所述,本研究开发的老年PMN预后预测模型在内部验证数据集中具有良好的区分度、校准度及临床解释性。该模型强调了慢性病理损伤、高凝状态及代谢负荷在老年PMN进展中的关键作用,填补了该领域针对老年亚组专用预测工具的空白,具有重要的潜在临床转化价值,未来需通过多中心、更大样本量的前瞻性队列研究对模型的外推性进行进一步验证。
参考文献
[1]Xu X, Wang G B, Chen N, et al. Long-term exposure to air pollution and increased risk of membranous nephropathy in China[J]. J Am Soc Nephrol, 2016, 27(12): 3739-3746.
[2]McGrogan A, Franssen C F M, De Vries C S. The incidence of primary glomerulonephritis worldwide: a systematic review of the literature[J]. Nephrol Dial Transplant, 2011, 26(2): 414-430.
[3]Qian Q, Nasr S H. Diagnosis and treatment of glomerular diseases in elderly patients[J]. Adv Chronic Kidney Dis, 2014, 21(2): 228-246.
[4]Krakowska-Jura K, Kler A N, Wajerowska W, et al. Prognostic factors of proteinuria remission in primary membranous nephropathy[J]. J Clin Med, 2025, 14(9): 2880.
[5]Wu M Q, Chen Y H, He Z X, et al. Spontaneous remission in primary membranous nephropathy: mechanisms, predic-tive factors, and implications for personalized management[J]. Front Immunol, 2025, 16: 1651810.
[6]Lu R J, Wang E K, Benayoun B A. Functional genomics of inflamm-aging and immunosenescence[J]. Brief Funct Genomics, 2022, 21(1): 43-55.
[7]Zhang L X, Wang F, Wang L, et al. Prevalence of chronic kidney disease in China: a cross-pal survey[J]. Lancet, 2012, 379(9818): 815-822.
[8]Coresh J, Selvin E, Stevens L A, et al. Prevalence of chronic kidney disease in the United States[J]. JAMA, 2007, 298(17): 2038-2047.
[9]Yokoyama H, Yamamoto R, Imai E, et al. Better remission rates in elderly Japanese patients with primary membranous nephropathy in nationwide real-world practice: The Japan Nephrotic Syndrome Cohort Study (JNSCS)[J]. Clin Exp Nephrol, 2020, 24(10): 893-909.
[10]Tan J X, Luo X Y, Yang J Q, et al. Clinicopathological characteristics and risk factors in elderly patients with biopsy-proven IgA nephropathy[J]. Ren Fail, 2022, 44(1): 1027-1037.
[11]Kim Y, Yoon H E, Chung B H, et al. Clinical outcomes and effects of treatment in older patients with idiopathic membranous nephropathy[J]. Korean J Intern Med, 2019, 34(5): 1091-1099.
[12]Liang J X, Hao W K, Xia F X, et al. Clinicopathological features and outcome in elderly patients with idiopathic membranous nephropathy[J]. Ren Fail, 2023, 45(1): 2212081.
[13]Yamaguchi M, Ando M, Yamamoto R, et al. Patient age and the prognosis of idiopathic membranous nephropathy[J]. PLoS One, 2014, 9(10): e110376.
[14]Cattran D C, Pei Y, Greenwood C M, et al. Validation of a predictive model of idiopathic membranous nephropathy: its clinical and research implications[J]. Kidney Int, 1997, 51(3): 901-907.
[15]Liu L L, Wang H T, Zhao B, et al. Nomogram to predict the progression of patients with primary membranous nephropathy and nephrotic syndrome[J]. Int Urol Nephrol, 2022, 54(2): 331-341.
[16]Hu X F, Xu J, Wang W, et al. Combined serologic and genetic risk score and prognostication of phospholipase A2 receptor-associated membranous nephropathy[J]. Clin J Am Soc Nephrol, 2024, 19(5): 573-582.
[17]Wen L, Li Q Q, Cheng G Y, et al. Prognostic value of serum complement cleavage factor Bb in idiopathic membranous nephropathy and establishment of nomogram model[J]. Sci Rep, 2024, 14(1): 27266.
[18]Liang Y F, Li Q, Zou Z H, et al. A dynamic prediction model for renal progression in primary membranous nephropathy[J]. Int J Med Sci, 2024, 21(7): 1292-1301.
[19]Oto O A, Demir E, Mirioglu S, et al. Clinical significance of glomerular C3 deposition in primary membranous nephropathy[J]. J Nephrol, 2021, 34(2): 581-587.
[20]Kidney Disease: Improving Global Outcomes (KDIGO) Glomerular Diseases Work Group. KDIGO 2021 clinical practice guideline for the management of glomerular diseases[J]. Kidney Int, 2021, 100(4S): S1-S276.
[21]Cattran D C, Reich H N, Beanlands H J, et al. The impact of sex in primary glomerulonephritis[J]. Nephrol Dial Transplant, 2008, 23(7): 2247-2253.
[22]Hou J, Cheng Y L, Hou Y, et al. Lower serum and higher urine immunoglobulin G are associated with an increased severity of idiopathic membranous nephropathy[J]. Ann Clin Lab Sci, 2019, 49(6): 777-784.
[23]Gan W Y, Zhu F, Zeng X R, et al. The association between serum complement 4 and relapse of primary membranous nephropathy: a multicenter retrospective cohort study[J]. Front Med (Lausanne), 2024, 11: 1451677.
[24]Lu W J, Gong S H, Li J, et al. Clinicopathological features and prognosis in patients with idiopathic membranous nephropathy with hypertension[J]. Exp Ther Med, 2020, 19(4): 2615-2621.
[25]Van Damme B, Tardanico R, Vanrenterghem Y. Adhesions, focal sclerosis, protein crescents, and capsular lesions in membranous nephropathy[J]. J Pathol, 1990, 161(1): 47-56.
[26]Ponticelli C, Zucchelli P, Passerini P, et al. A randomized trial of methylprednisolone and chlorambucil in idiopathic membranous nephropathy[J]. N Engl J Med, 1989, 320(1): 8-13.
[27]Hoxha E, Harendza S, Zahner G, et al. An immunofluorescence test for phospholipase-A2-receptor antibodies and its clinical usefulness in patients with membranous glomerulonephritis[J]. Nephrol Dial Transplant, 2011, 26(8): 2526-2532.
[28]Troyanov S, Roasio L, Pandes M, et al. Renal pathology in idiopathic membranous nephropathy: a new perspective[J]. Kidney Int, 2006, 69(9): 1641-1648.
[29]Stangou M J, Marinaki S, Papachristou E, et al. Histolo-gical grading in primary membranous nephropathy is essential for clinical management and predicts outcome of patients[J]. Histopathology, 2019, 75(5): 660-671.
[30]Gupta J, Mitra N, Kanetsky P A, et al. Association between albuminuria, kidney function, and inflammatory biomarker profile in CKD in CRIC[J]. Clin J Am Soc Nephrol, 2012, 7(12): 1938-1946.
[31]Choi J Y, Chin H J, Lee H, et al. Idiopathic membranous nephropathy in older patients: clinical features and outcomes[J]. PLoS One, 2020, 15(10): e0240566.
[32]Von Groote T C, Williams G, Au E H, et al. Immunosuppressive treatment for primary membranous nephropathy in adults with nephrotic syndrome[J]. Cochrane Database Syst Rev, 2021, 11(11): CD004293.


