Front.aging neurosci-阿尔兹海默病小鼠模型海马CA1 N-甲基-D-天冬氨酸受体功能缺陷和突触可塑性
时间:2021-12-14 16:01:58 热度:37.1℃ 作者:网络
 阿尔茨海默病(AD)是一种进行性神经系统疾病,其特征是学习和记忆功能受损,产生认知功能障碍。AD患者海马体积缩小,特别是海马CA1区是AD是受损最严重的区域之一,可作为辅助检查区域,提高AD诊断的准确性。N-甲基-D-天冬氨酸受体(NMDARs)是主要的配体门控谷氨酸受体,对神经元发育、突触可塑性和兴奋性毒性至关重要。淀粉样蛋白 β (Aβ) 是AD的病理标志之一,直接干扰神经元的NMDAR功能。来自宁波大学医学院的研究团队研究了AD模型动物海马CA1 N-甲基-D-天冬氨酸受体功能缺陷和突触可塑性的神经病理生理学的改变。
阿尔茨海默病(AD)是一种进行性神经系统疾病,其特征是学习和记忆功能受损,产生认知功能障碍。AD患者海马体积缩小,特别是海马CA1区是AD是受损最严重的区域之一,可作为辅助检查区域,提高AD诊断的准确性。N-甲基-D-天冬氨酸受体(NMDARs)是主要的配体门控谷氨酸受体,对神经元发育、突触可塑性和兴奋性毒性至关重要。淀粉样蛋白 β (Aβ) 是AD的病理标志之一,直接干扰神经元的NMDAR功能。来自宁波大学医学院的研究团队研究了AD模型动物海马CA1 N-甲基-D-天冬氨酸受体功能缺陷和突触可塑性的神经病理生理学的改变。

研究结果
1、APPS1/PS1小鼠6/8月龄认知功能受损情况
通过Y迷宫、新位置识别(NLR)和新物体识别(NOR)测量小鼠认知功能情况。结果表明,在 Y 迷宫中,4月龄APP/PS1小鼠与年龄匹配的WT小鼠没有差异,6月龄和8月龄APP/PS1小鼠表现出自发交替减少,NOR中鉴别指数降低。结果说明,APP/PS1小鼠在6个月大时表现出工作记忆和长期识别记忆受损,在8个月大时表现出空间识别记忆受损。利用巴恩斯迷宫以进一步验证 APP/PS1 小鼠的认知功能障碍。在4月龄的WT和APP/PS1小鼠中,没有观察到统计学上的显着差异(图 1C-E)。在 6月龄的小鼠中,APP/PS1小鼠在目标象限中花费的时间减少(图 1G),与 WT小鼠相比,在逃逸潜伏期中没有观察到差异。8个月大的APP/PS1小鼠在训练阶段的第3天和第4天逃逸潜伏期都减少(图 1I),在目标象限中花费的时间减少了(图1J),与WT小鼠相比,错误数量有所增加(图 1K)。这些结果与NLR测试的结果一致,表明APP/PS1小鼠的记忆任务表现有进行性下降,这也与海马体密切相关。 图1 4、6和8月龄的WT和APP/PS1小鼠的Barnes迷宫表现
图1 4、6和8月龄的WT和APP/PS1小鼠的Barnes迷宫表现
2、6月龄的消暑运动活动减少,8月龄的小鼠CA1 LTP受损
6 个月大的 APP/PS1 小鼠在新环境中的运动活动减少,但未发现活动性和认知能力之间存在显着相关性。作者检查了相同年龄的APP/PS1小鼠的侧支CA1 锥体神经元突触的LTP,与对照小鼠相比,8月龄的APP/PS1小鼠CA1区域的LTP显着降低。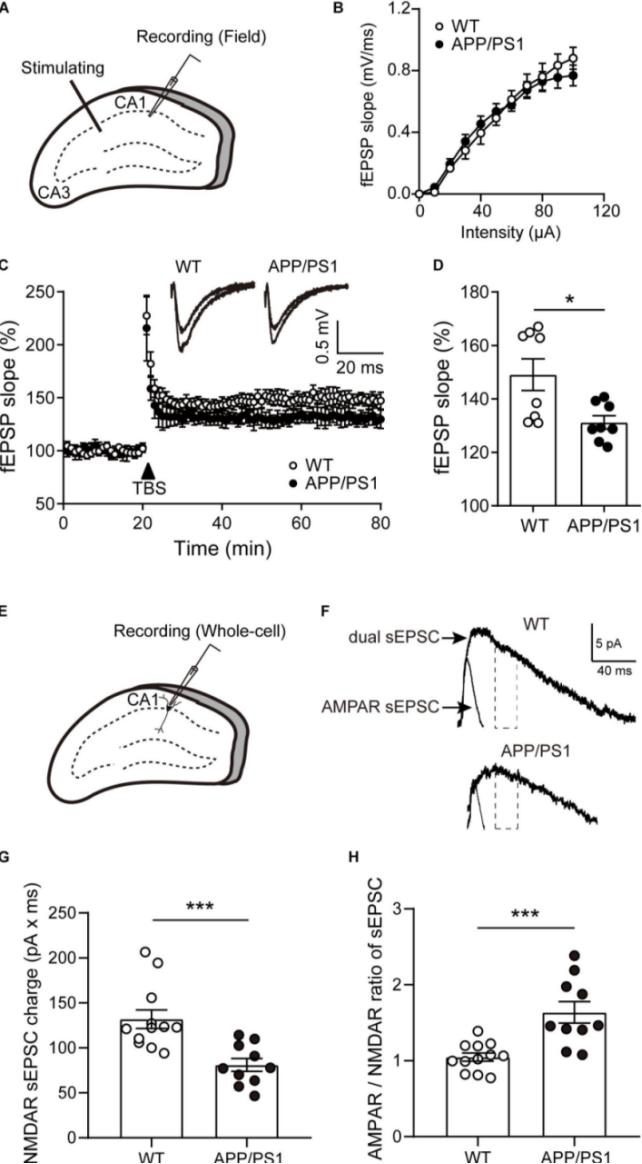 图2 8月龄APP/PS1小鼠CA1锥体神经元LTP和NMDAR sEPSC
图2 8月龄APP/PS1小鼠CA1锥体神经元LTP和NMDAR sEPSC
3、8月龄小鼠神经改变情况
8月龄的APP/PS1小鼠CA1锥体神经元N-甲基-D-天冬氨酸受体电流降低,AMPAR sEPSCs 与NMDAR sEPSCs 的比例显着增加。此外,小鼠锥体神经元的形态复杂性和树突棘降低,海马中N-甲基-D-天冬氨酸受体亚基和相关突触蛋白的表达水平降低。 综上,认知功能障碍是AD最显著的症状,通常先有一段时间的轻度认知障碍 (MCI)。与之前的报道一致,作者证实了认知功能随着APP/PS1小鼠年龄的增加而恶化,包括工作记忆、短期空间记忆、长时识别记忆和空间学习记忆。这些认知任务主要反映依赖海马体的学习和记忆能力。结果提示,8月龄的APP/PS1小鼠的海马功能异常。 海马CA1区突触可塑性指标的长时程增强与空间学习和记忆密切相关,CA1区LTP降低常见于以认知功能障碍为特征或伴有认知功能障碍的疾病,例如 AD、精神分裂症和抑郁症。许多形式的LTP的引发需要NMDAR激活,可塑性的减弱或增强主要受通过NMDAR流入的Ca 2+动力学控制。越来越多的证据表明,AD中NMDAR相关的突触异常,这与作者的结果一致,即海马CA1中NMDAR介导的sEPSC减少,会使APP/PS1小鼠的突触可塑性受损。 蛋白质印迹实验显示APP/PS1小鼠海马CA1中NR2A和NR2B的表达水平降低。这些结果表明NMDAR介导的sEPSC的减少可能是由于特定受体亚基的低表达造成的。此外,在 APP/PS1小鼠的海马CA1中观察到PSD95和SNAP25的表达水平降低,下调的PSD95表达可能是APP/PS1小鼠树突棘密度降低的原因。 图3 认知障碍机制示意图
但是作者的研究存在一些局限性,比如对受体亚基蛋白表达的检测和电生理研究并没有区分NMDAR的位置(突触内部或外部),这需要更细致的研究来确定疾病进展过程中NMDAR 功能的动态变化,并区分AD模型中突触和突触外NMDAR的变化,需要进一步研究NMDAR 功能障碍的破坏性影响,以开发更有效的针对AD机制的靶向治疗。
图3 认知障碍机制示意图
但是作者的研究存在一些局限性,比如对受体亚基蛋白表达的检测和电生理研究并没有区分NMDAR的位置(突触内部或外部),这需要更细致的研究来确定疾病进展过程中NMDAR 功能的动态变化,并区分AD模型中突触和突触外NMDAR的变化,需要进一步研究NMDAR 功能障碍的破坏性影响,以开发更有效的针对AD机制的靶向治疗。
参考文献
Le Xu, Yiying Zhou, Linbo Hu, Hongde Jiang, Yibei Dong, Haowei Shen, Zhongze Lou, Siyu Yang, Yunxin Ji, Liemin Ruan and Xiaoqin Zhang,Deficits in N-Methyl-D-Aspartate Receptor Function and Synaptic Plasticity in Hippocampal CA1 in APP/PS1 Mouse Model of Alzheimer’s Disease,Front. Aging Neurosci., 30 November 2021,https://doi.org/10.3389/fnagi.2021.772980 编译作者: 原代美少女 (Brainnews创作团队) 校审: Simon (Brainnews编辑部)- END -




