BTK抑制剂治疗CLL,心血管毒性的管理策略
时间:2025-02-04 12:10:12 热度:37.1℃ 作者:网络
BTK抑制剂(BTKi)和BCL-2抑制剂等靶向治疗已成为慢性淋巴细胞白血病(CLL)的主要治疗手段,以前使用的免疫化疗已大部分被BTK抑制剂或BCL-2抑制剂单药联合CD20单克隆抗体联合使用所取代,无论是作为一线治疗还是在疾病复发时。BTKi最常见的不良反应(AE)包括疲劳、瘀伤、感染、血液学异常和心血管异常。虽然治疗期间的AE通常为轻度的(1级和2级),但部分患者会出现3级和4级AE,需要额外的医疗手段和/或暂时或永久停药。
《Blood Reviews》近日发表综述,分析了CLL治疗中与BTKi相关的心血管效应,以及对出现心血管毒性的患者进行的多学科管理,特别关注与伊布替尼和新一代BTKi(阿可替尼、泽布替尼和匹妥布替尼[pirtobrutinib])相关的心血管风险数据和策略,包括房颤、高血压、室性心律失常、猝死、心力衰竭、出血和缺血并发症(卒中和心肌梗死)。该综述覆盖了新兴证据,涉及血液学生物标志物、 心脏毒性机制和治疗干预,将血液学和心脏病学联系起来,以增强理解并指导全面的预防和管理策略。现由AI整理主要内容,个别细节稍作修改,如需参考敬请查阅原文。

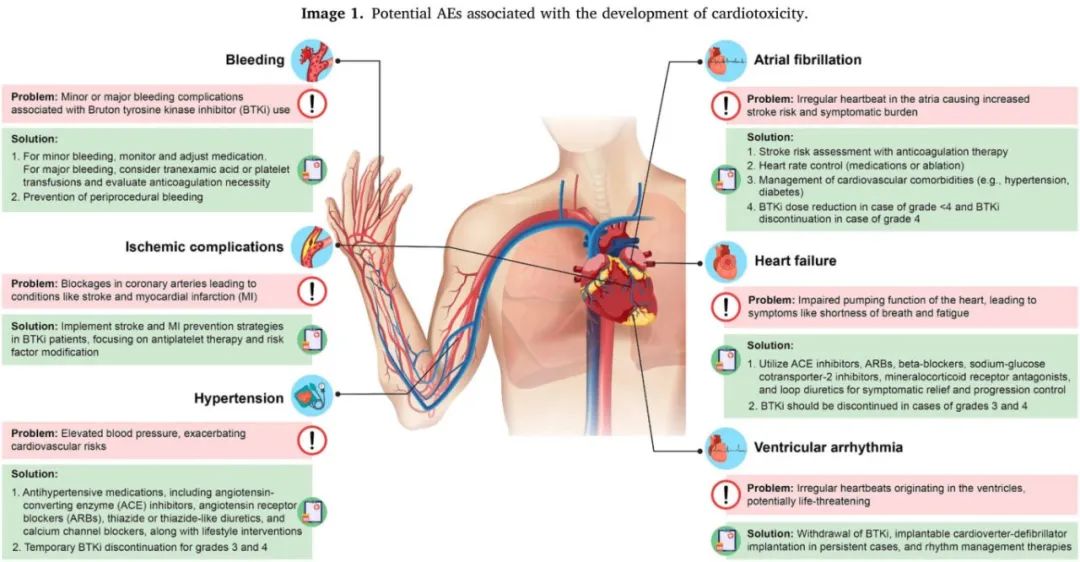
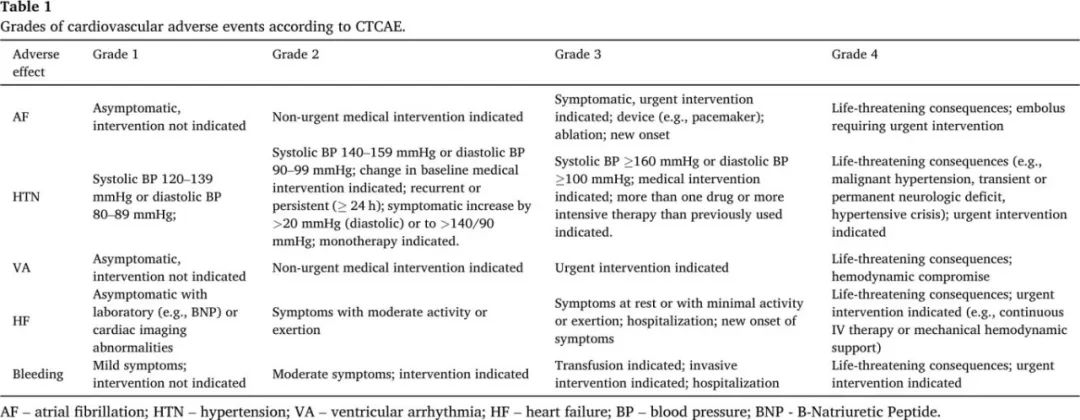
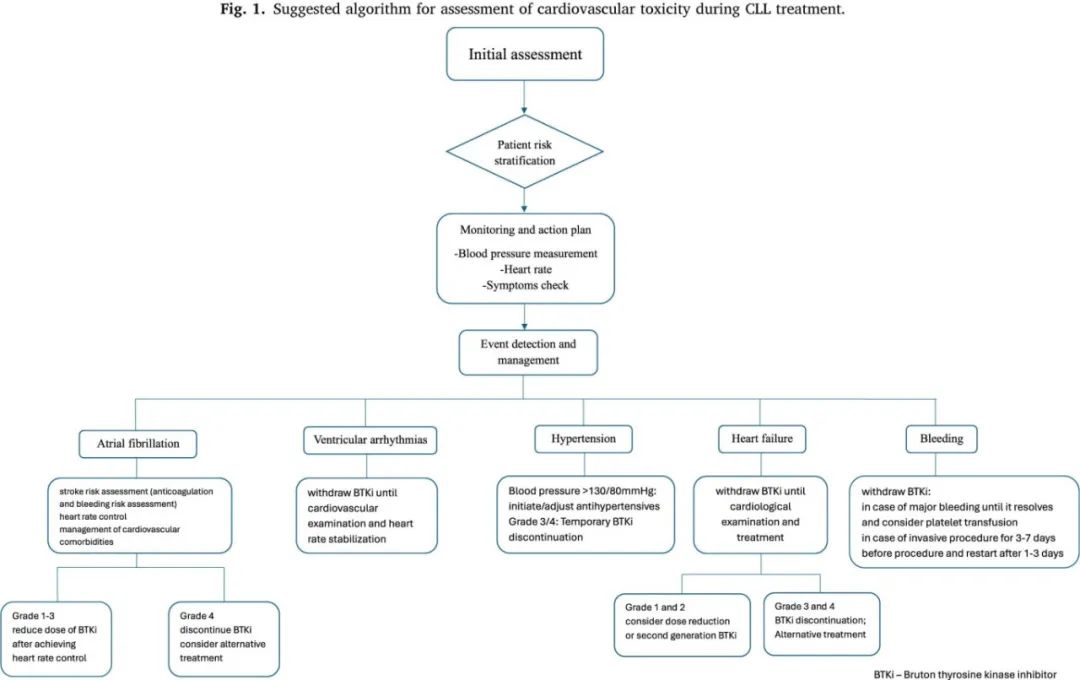
与心脏毒性发展相关的潜在AE见图1。根据不良事件通用术语标准(CTCAE)分级的心脏毒性相关AE见表1。
2. 房颤
2.1.发病率
房颤是BTKi治疗中最常见的AE之一,接受伊布替尼治疗的患者中发病率高达16%。房颤发作的中位时间为伊布替尼开始后5-7个月。与非使用患者相比,使用伊布替尼的患者房颤风险增加4倍。与伊布替尼相比,阿可替尼引起的房颤较少(9.4% vs. 16%),但多于化疗免疫治疗(8% vs. 3%)。泽布替尼也与较低的房颤发病率相关(5.2% vs 13.3%)。
2.2. 房颤的管理
管理房颤包括评估卒中风险(抗凝和出血风险评估)、心律控制和心血管合并症的管理,包括生活方式的改变。中风风险通常使用CHA2DS2VASc评分估计。抗凝治疗建议用于评分≥2的男性和评分≥3的女性。出血风险的评估也很重要,HAS-BLED评分常用于临床环境。BTKi治疗相关的出血似乎与抑制胶原和糖蛋白VI(GPVI)下游调节的强效抗血小板效应有关。在考虑BTKi诱导的房颤的抗凝治疗时,应评估CHA2DS2VASc和HAS-BLED评分。如果CHA2DS2VASc评分高于HAS-BLED评分,则应给予抗凝治疗。对于接受伊布替尼治疗的患者,直接口服抗凝药(DOAC)是首选(利伐沙班和阿哌沙班优于达比加群酯),因为它们更易管理且与其他药物的相互作用较少。
2.3. CLL治疗后的房颤管理
BTKi治疗期间出现的房颤可能会影响未来的CLL管理。值得注意的是,根据CTCAE确定房颤的等级很重要,因为目前的建议要求4级房颤患者永久停用BTKi。对于较低等级的AE,建议继续BTKi治疗并充分管理房颤。对于因新发≤3级房颤而停用伊布替尼的患者,可以在房颤控制后继续使用伊布替尼,剂量减少至每天280mg。对于不耐受伊布替尼的患者,尤其是有房颤的患者,转用替代BTKi(阿可替尼或泽布替尼)是一个有前景且有效的策略。
3. 高血压
3.1. 机制和发病率
高血压是BTKi的已知AE,定义为治疗出现或现有高血压恶化。根据临床研究,它是最常见的3级AE之一,发病率在14%到28%之间。与化疗免疫治疗相关的高血压相比,伊布替尼和泽布替尼似乎具有相似的BTKi相关高血压风险,而阿可替尼的风险较低。
3.2. 高血压的管理
在所有接受BTKi治疗的患者中,应常规监测血压,并及时治疗血压升高,因为不受控制的高血压是其他心血管疾病的风险因素。BTKi相关的高血压应根据一般指南进行管理,特别注意合并症和药物相互作用。初始治疗包括使用四大类抗高血压药物中的一种:血管紧张素转换酶抑制剂、血管紧张素受体阻滞剂、噻嗪类或噻嗪类样利尿剂和钙通道阻滞剂。如果单药治疗无法控制血压,则应添加其他药物以实现正常血压。应避免使用非二氢吡啶类钙通路阻滞剂(如维拉帕米和地尔硫卓),因为它们与BTKi有主要的药物相互作用。
3.3. 高血压管理后的CLL治疗
在大多数BTKi相关的高血压病例中,不需要停用伊布替尼治疗。对于3级或4级事件,应暂时停用伊布替尼;然而在毒性降至1级或患者完全恢复后,可以安全地继续使用伊布替尼,并考虑减少剂量。如果3级或4级高血压复发,可以考虑转用二代BTKi,而未能充分控制血压应给予替代CLL治疗。
4. 室性心律失常(VA)和猝死
4.1. 机制和发病率
最初没有数据显示VA与BTKi治疗之间存在关联,然而随着BTKi的进一步使用,VA被认为是一个潜在的AE。接受伊布替尼治疗的患者中VA的发病率为每1000人年6.0-7.9例,猝死更为罕见。与非BTKi治疗相比,伊布替尼与VA的发病率增加有关。有数据表明,阿可替尼也与VA有关,相对风险为8.2,表明可能存在BTKi类效应。
4.2. VA的管理
未检测到的VA可能潜在致命,导致猝死,从而强调了及时识别和治疗这种情况的重要性。与BTKi相关的VA应根据指南进行治疗。对于药物诱导的心律失常,建议停用致病药物。对于在停药后仍存在生命危险的VA的患者,应考虑植入心脏复律除颤器。
4.3. VA管理后的CLL治疗
VA是猝死的可预防原因,应监测接受BTKi治疗的患者。患者应在BTKi开始前被告知VA的潜在风险,并在治疗期间评估心悸、头晕和晕厥。对于有VA史、左室射血分数降低或猝死家族史的患者,应采用多学科方法权衡BTKi的利弊。如果风险高于潜在获益,应考虑替代CLL疗法。在BTKi相关的VA发作后,应停用BTKi,直到进行心血管检查并稳定心律。
5.心力衰竭
5.1. 机制和发病率
心力衰竭可以作为多种抗癌剂的并发症出现,主要是系统化疗对心肌的直接损伤。最初未观察到心力衰竭与BTKi治疗之间的相关性,然而进一步分析和随访显示,2-5%的接受BTKi治疗的患者出现了心力衰竭,主要是迟发性。与BTKi治疗相关的其他心血管毒性一样,心力衰竭可能由于PI3K/Akt通路的抑制导致纤维化、钙转运不足和心肌细胞死亡。
5.2. 心力衰竭的管理
在开始BTKi治疗前,血液学家应了解心血管合并症和发生心血管毒性的潜在风险。对于已诊断为心肌病和左室射血分数降低的患者,应谨慎使用BTKi,并考虑为高风险患者选择替代CLL治疗。接受BTKi治疗且有心力衰竭症状(如呼吸困难、下肢水肿、心跳加快或不规律、咳嗽)的患者应立即转诊心脏病学家。BTKi相关的心力衰竭治疗应根据标准指南进行,包括启动ACE抑制剂或血管紧张素受体阻滞剂、β受体阻滞剂,可能还有SLGT2抑制剂和矿物皮质激素受体拮抗剂。对于有液体潴留的心力衰竭患者,首选袢利尿剂(如呋塞米、布美他尼和托拉塞米)。
5.3.心力衰竭管理后的CLL治疗
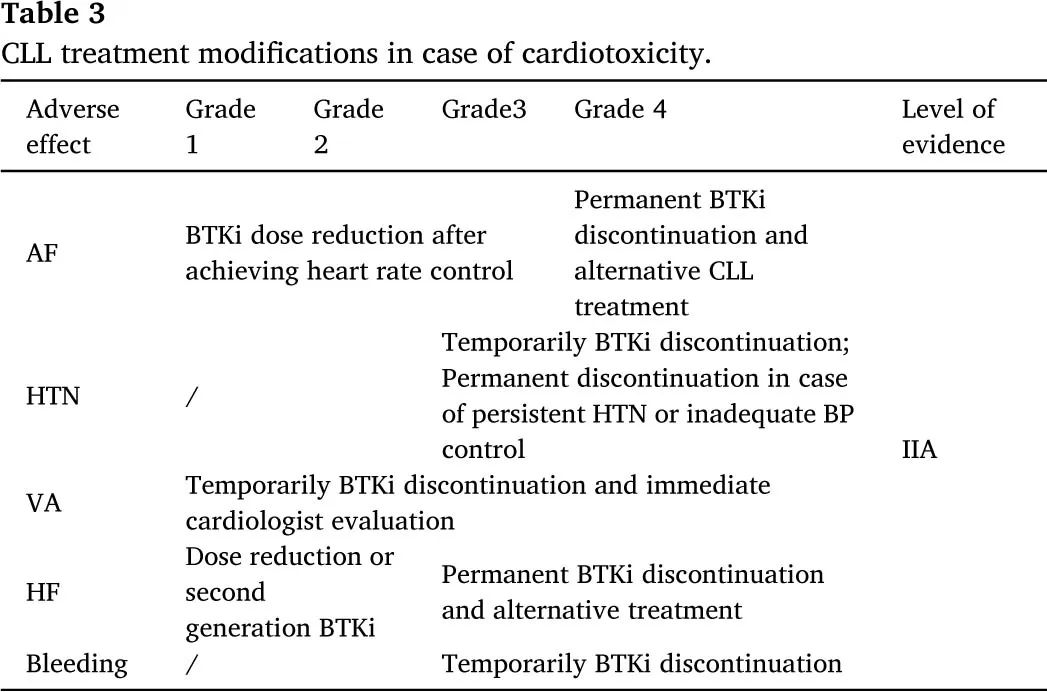
根据CTCAE,需要住院和紧急医疗护理的症状性心力衰竭(HF)归类为3级,而威胁生命和血流动力学不稳定的情况则归类为4级。对于低级别HF,如果与启动的心血管治疗有不可接受的药物相互作用,则需要暂时停药或减少剂量。然而在BTKi相关心力衰竭和患者心脏状况稳定后,进一步的CLL治疗应采用多学科方法。对于3级和4级HF,建议使用替代治疗;而对于1级或2级HF,则应考虑减少伊布替尼的剂量或使用二代BTKi。
6.出血
6.1. 机制和发病率
早期临床研究表明,BTKi治疗期间出血率增加,包括胃肠道出血、硬膜下血肿和血尿。在后期试验中,接受伊布替尼治疗的患者中高达50%出现出血,其中大多数为1级和2级(自发性瘀伤或紫癜);3级出血占5%。与接受化疗的对照组相比,伊布替尼增加了出血的发生率。接受BTKi治疗的患者与对照组相比,重大出血的相对风险约为1.66。在接受抗血小板或抗凝治疗的BTKi治疗患者中,重大出血的发生率分别为2.5%和3.2%。上述风险与抗凝剂或抗血小板治疗的一般报告风险相符。与伊布替尼一样,阿可替尼的使用也增加相对于化疗免疫治疗的出血发生率。BTKi抑制对血小板功能和止血的影响尚不清楚。正常的血小板聚集和粘附依赖于von Willebrand因子和胶原蛋白,这由糖蛋白1b和GPVI促进。据认为,伊布替尼通过抑制血小板受体下游的两个激酶BTK和TEC(非目标活性)来引起出血。在X连锁无丙种球蛋白血症患者中,由于TEC对不活跃BTK的补偿,出血风险并未增加。在体外研究中,伊布替尼抑制X连锁无丙种球蛋白血症患者的血小板聚集。其他体外研究显示,伊布替尼在富含血小板的血浆中抑制了GPVI信号传导,而阿可替尼则没有。除了GPVI,伊布替尼还通过BTK和TEC抑制C型凝集素样受体2的信号传导,导致血小板粘附后的不稳定性。此外,CLL患者的血小板功能障碍是由于ADP和胶原蛋白介导的血小板功能下降。作为BTKi治疗的特异性不良反应,出血的发生率在治疗6个月后下降,这可能是由于疾病得到了控制。
6.2.出血的管理
轻微出血,如瘀伤和紫癜,并不提示潜在的重大出血;因此不需要治疗这些不良反应,BTKi应继续不间断使用。对于大出血,应暂时停用BTKi,可能需要血小板输注,因为与BTKi相关的医源性血小板功能障碍,无论血小板计数如何。建议使用氨甲环酸治疗BTKi相关大出血。
6.3.出血后的CLL治疗
出血是BTKi治疗的常见不良反应;大多数患者经历1级或2级出血,不需要停药或减少剂量。对于大出血,应暂时停用BTKi,直到出血解决。已经接受抗血小板或抗凝治疗的BTKi治疗候选者应在BTKi启动前重新评估治疗指征,考虑出血的风险。BTKi与抗凝剂和抗血小板剂的联合使用增加了重大出血的风险。应考虑为一些患者提供替代CLL治疗,特别是需要双重抗血小板治疗的患者。为了防止围手术期出血,伊布替尼应在重大侵入性手术前7天停用,小手术前3天停用。伊布替尼可以在手术后1-3天在手术止血良好的患者中重新开始。对于紧急、非计划的手术,无法及时停用伊布替尼,需要血小板输注。
7. 缺血性并发症:卒中和心肌梗死
7.1. 机制、发病率和管理
房颤(AF)是缺血性卒中的已知原因,也是BTKi治疗中最明确的心脏不良反应。因此,预防卒中是治疗BTKi相关房颤的主要目标之一。房颤患者的卒中风险为0.2-12.2%,在恶性疾病患者中会进一步增加。虽然卒中可能发生在伊布替尼治疗期间,但它似乎是一种罕见的不良反应,仅在之前的回顾性研究中观察到少数患者(1.6%的BTKi治疗患者)。在一项针对老年患者的伊布替尼治疗研究中,卒中风险增加了1.9倍。在接受阿可替尼和泽布替尼治疗的患者中,卒中未被识别为不良反应。伊布替尼治疗患者卒中的潜在机制包括炎症反应增加、氧化应激和PI3K/Akt信号通路抑制。急性心肌梗死(MI)是BTKi治疗的潜在缺血性并发症。在接受CLL治疗的患者中,接受伊布替尼治疗的患者相对于其他治疗选择风险增加了1.86倍,相对于未治疗风险增加了2.83倍。预防卒中和心肌梗死是治疗其他心血管BTKi不良反应的主要策略。控制血压、管理房颤以及充分的抗凝或抗血小板治疗,以及控制其他风险因素,如高脂血症和糖尿病,对预防卒中和心肌梗死至关重要。对于心肌梗死或卒中的病例,应停用伊布替尼,直到心肌梗死和卒中治疗完成。房颤患者的卒中预防策略包括评估CHA2DS2VASc评分。对于男性评分≥2,女性评分≥3的患者,应在评估出血风险后启动抗凝治疗。对于双重或三重抗凝或抗血小板治疗的病例,应提供替代CLL治疗。
8.心包疾病及BTKi罕见或未被认识的心脏毒性?
心包疾病是肿瘤患者中常见且严重的并发症,表现为急性心包炎、心包积液或缩窄性心包炎。它与肺癌、乳腺癌、淋巴瘤、白血病、胃肠道肿瘤和黑色素瘤最为相关,由疾病本身或化疗、免疫治疗和放疗引起。在接受伊布替尼治疗的患者中,心包炎和心包积液是罕见的并发症,只有少数病例与其他心血管不良反应一起报告,或作为孤立事件发生。在有限的临床试验数据中,352名接受伊布替尼联合利妥昔单抗(IR)治疗的患者中有7名(2.0%)经历了心包事件,包括心包积液和心包填塞。一项全面的心血管事件荟萃分析显示,心包积液(0.5%)和心包炎(0.4%)的风险较低。药物警戒数据显示,心包积液81例,心包炎24例,心包填塞16例,心包出血14例。然而,及时识别至关重要,因为这些情况可能进展为危及生命的心包填塞。BTKi增加心包积液风险的机制涉及抑制血小板衍生生长因子受体β和Src家族酪氨酸激酶,两者都在调节内皮通透性和间质组织压力中发挥作用。急性心包炎的管理通常涉及大剂量非甾体抗炎药,但在BTKi治疗的患者中,其使用可能加剧抗血小板效应,因此选择使用秋水仙碱和类固醇。可以考虑暂时停用伊布替尼,快速减少类固醇剂量,并长期使用秋水仙碱以缓解症状。对于不耐受伊布替尼的患者,可以考虑切换到第二代BTKi,以减少心脏交叉反应。对于中度或重度症状、血流动力学不稳定、心包填塞或对治疗无反应的心包积液,首选治疗方法是心包穿刺术。如果可能,BTKi应在手术前3-7天停用;如果不行,应考虑血小板输注。扩展的现实世界数据对于进一步评估接受BTK抑制剂治疗的患者中心包事件的频率、风险因素和结果至关重要。
9.非共价BTK和心脏毒性
匹妥布替尼是一种高选择性的非共价可逆BTK抑制剂,与BTK的结合比其他激酶选择性高300倍,减少了非目标毒性的潜在风险,并能克服共价BTKi使用中可能产生的耐药机制。匹妥布替尼表现出增强的选择性,仅抑制4种激酶中的50%以上,而伊布替尼和泽布替尼分别抑制22种和6种激酶。最初,它于2023年1月获批用于治疗复发或难治性套细胞淋巴瘤,并于2023年12月获批用于治疗复发/难治性CLL。匹妥布替尼在复发/难治性CLL患者中的安全性和有效性在临床试验中得到确定。匹妥布替尼的高度选择性可能解释了大多数之前导致患者停用共价BTKi的不良反应的低复发率,除了中性粒细胞减少和感染。匹妥布替尼最常见的不良反应是感染(71%)、出血(42.6%)和中性粒细胞减少(32.5%)。与BTKi通常相关的不良反应相对较少:14.2%的患者出现高血压,3.8%的患者出现房颤或房扑。在另一项试验中,房颤发生在不到1%的患者中,为2级,与患者病史相关,而非匹妥布替尼使用。在这项研究中,30名患者中只有2名在切换到匹妥布替尼后出现复发,表明房颤与共价BTKi的关联。在类似的研究中,9名因出血停用共价BTKi的患者中,没有人经历≥3级复发。也没有观察到突发心脏死亡或室性心律失常。与其它BTKi一样,匹妥布替尼结合TEC和CSK激酶,增加出血风险。一项研究表明,匹妥布替尼的非目标抑制不会导致不可逆的血小板功能障碍。这种对血小板功能的可逆影响可能解释了匹妥布替尼使用中观察到的相对较低的出血发生率。匹妥布替尼是心血管合并症患者以及不耐受伊布替尼、阿可替尼或泽布替尼患者的潜在选择,提供了共价BTKi的替代方案。进一步涉及未治疗患者、长期和现实世界数据的研究应提供更多的见解。
10. 心脏毒性监测和CLL治疗的建议
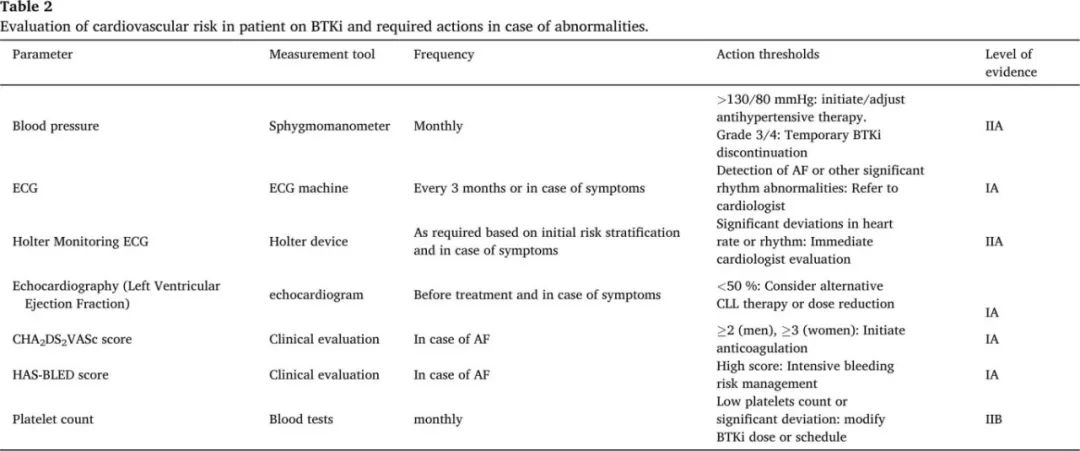
考虑到接受BTKi治疗的患者发生心血管不良反应的风险,血液学家应在治疗前和治疗期间评估心血管风险并采取预防措施。在BTKi治疗前应获取病史(包括心律失常、高血压、家族中突发死亡史和合并用药)。CLL患者通常被认为是脆弱的,因为存在需要持续治疗的合并症,通常涉及多药治疗,这增加了药物误用和药物相互作用的潜在风险。定期重新评估合并治疗对于管理与CLL特异性治疗的潜在药物相互作用和有效解决不良反应至关重要。应进行额外的心血管检查,包括血压测量、心电图(ECG)和超声心动图,以及左心室射血分数测量。还应教育患者关于心血管不良反应的潜在症状。有突然心悸、呼吸困难、胸痛、水肿、不明原因的晕厥或血压升高的患者应转诊给心脏病专家进行紧急心脏评估。在BTKi治疗期间,应反复进行心血管评估,包括每月评估心血管症状和血压测量,每3-6个月进行一次心电图检查,如有症状或不良反应则进行超声心动图检查。根据结果,可以考虑进行额外的检查,包括24小时Holter心电图或心脏磁共振成像。
11. 未来考虑
为了推进CLL的靶向治疗,必须关注几个关键领域。首先,需要进一步研究以阐明与BTKi和其他靶向治疗相关的心脏毒性的潜在机制。此外,迫切需要开发更安全的BTKi,这些BTKi在保持疗效的同时减少心血管副作用。根据个体患者档案(包括遗传、生活方式和合并症因素)制定CLL治疗的增强策略,对于最小化不良反应至关重要。加强多学科管理方法,纳入血液学家和心脏病专家,可以显著改善CLL患者的心血管并发症管理。最后,长期研究监测接受BTKi和其他靶向治疗的患者的心血管健康和总体结果,将为优化未来治疗方案提供宝贵的见解。
12. 结论
应教育患者关于BTKi治疗的潜在不良反应,包括心血管不良反应的体征和症状,以及何时寻求紧急医疗护理。对于疑似与BTKi相关的心脏毒性,应由血液学家和心脏病专家评估风险-效益比,以确定是否可以安全继续CLL治疗。进一步的分析应提供更多关于不同BTKi在毒性发展背景下的比较和优势的数据。
参考文献
Sofija Kozarac et al., Blood Reviews, https://doi.org/10.1016/j.blre.2025.101268


