关键突破 | 乙肝新药临床试验,这几点值得深思!
时间:2025-02-03 12:08:33 热度:37.1℃ 作者:网络
现行抗病毒药物治疗慢性乙型肝炎(CHB)的主要目标是实现功能性治愈,即停药后24周,血清HBV DNA持续<定量下线(LLOQ,<10 IU/ml),HBsAg消失(<0.05 IU/ml),伴或不伴抗-HBs阳转。
随着对各种机制和药物靶点的探索不断深化,许多针对乙型肝炎病毒(HBV)生命周期和免疫系统的新药研发取得显著进展,北京大学医学部的庄辉院士作了《关于乙型肝炎新药临床试验的几点思考》报告。肝胆相照平台特将该报告的精华部分整理成文,以飨读者。
一、在研乙型肝炎新药临床试验的主要治疗终点
目前,功能性治愈被广泛认为是CHB抗病毒治疗的主要终点。为什么功能性治愈是目前在研乙型肝炎(乙肝)新药临床试验的主要终点呢[1-3]?
首先,完全治愈(彻底治愈),即消除ccCDNA和整合的HBV DNA是一个理想状态,但目前很难达到。一方面没有消除cccDNA和整合的HBV DNA的新药;另一方面也缺乏商品化和标准化检测cccDNA和整合的HBV DNA的试剂。
目前部分治愈的定义已修订为:停药后24周,血清HBsAg持续<100 IU/ml,HBV DNA持续<定量下限(<10 IU/ml)。但部分治愈患者于停药后再活动发生率为15%~40%,因此,不能作为治疗终点,只能作为功能性治愈的中间终点。
▼ 功能性治愈是指在有限疗程的抗病毒治疗后:
① 血清HBV DNA持续低于定量下限(LLOQ,<10 IU/ml);
② 肝脏生化学指标恢复正常;
③ HBeAg阴转或血清学转换;
④ 确证HBsAg消失(即检测2次,间隔24周,HBsAg<0.05 IU/ml);
⑤ 有或无抗-HBs阳转。
▼ 在我国,功能性治愈又称临床治愈。CHB患者获得功能性治愈表示:
① HBV复制被抑制;
② 病毒抗原产生被抑制;
③ 宿主对HBV特异性免疫应答恢复。
历届AASLD-EASL联席会议对功能性治愈的定义如表1所示[4]。
表1. 历届AASLD-EASL联席会议对功能性治愈的定义
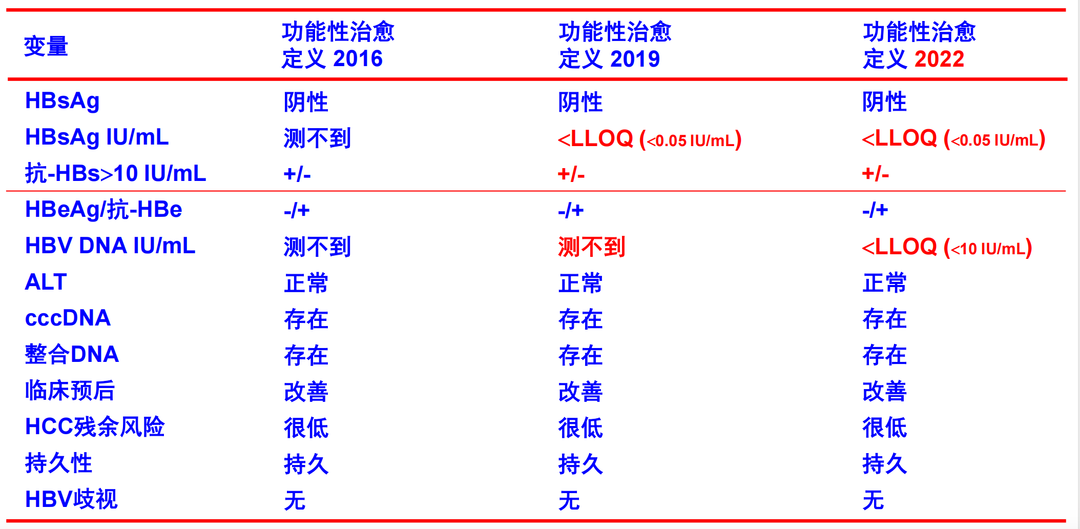
既往将CHB的治疗终点定为理想终点(停药后获得持久的HBsAg消失,可伴或不伴抗-HBs阳转)、满意终点(停药后获得持续的病毒学应答和ALT复常,HBeAg阳性患者同时伴有HBeAg血清学转换)和基本终点(抗病毒治疗期间维持病毒学应答)。这些治疗终点曾在2012年欧洲肝病学会指南和我国慢性乙型肝炎防治指南(2015年版)提及,但已不再应用。目前一致认为功能性治愈是在研乙肝新药临床试验的主要治疗终点。
二、乙型肝炎新药临床试验的主要评价指标
CHB治疗的主要目标是:提高存活率,减少肝硬化、肝脏失代偿、原发性肝细胞癌(HCC)和肝病相关死亡。但到达这些临床终点需要几十年,因此,不适用于新药临床试验的治疗终点。
▼ 临床试验一直将替代指标作为临床试验的评价指标,主要包括:
① 生化学:ALT复常;
② 病毒学:HBV DNA低于定量检测下限;
③ 血清学:HBsAg消失,伴或不伴抗-HBs阳转、HBeAg消失伴或不伴抗-HBe阳转;
④ 组织学:炎症和纤维化改善。
所有这些替代指标中,HBsAg消失最为重要[5],因为HBsAg消失表示HBV DNA复制和病毒蛋白表达被抑制、宿主对HBV特异性免疫恢复,而且,HBsAg消失还与停药后临床预后持续改善有关。与单独HBV DNA抑制比较,HBsAg消失者的HCC和肝脏失代偿发生率较低,特别是肝硬化患者。而且HBsAg有标准化的、普遍应用的检测试剂可供使用。
目前,血清HBV RNA和HBcrAg新的生物标志物作为乙肝新药临床试验的评价指标价值有限。
▼ HBV RNA检测:
① 无标准化试剂;
② 无可供选择的试剂;
③ 如引物设计不合理,可检出HBV RNA和HBV DNA,不完全是pgRNA。
④ 当血清HBV DNA水平低时(<3 log IU/ml),该检测试剂的灵敏度较低。
血清HBcrAg检测试剂对血清HBV DNA水平低和HBeAg阴性CHB者灵敏度较低。
此外,该2个生物标志物的下降与临床预后改善的关联尚未被证实。因此,世界卫生组织2024年版指南指出,目前该2个生物标志物的检测试剂尚处于科研使用阶段。
三、乙肝新药的临床试验的结果
近年来,许多CHB抗病毒治疗的新药或治疗策略取得了显著的进展[6, 7]。在研的乙肝治疗新药见图1和图2。
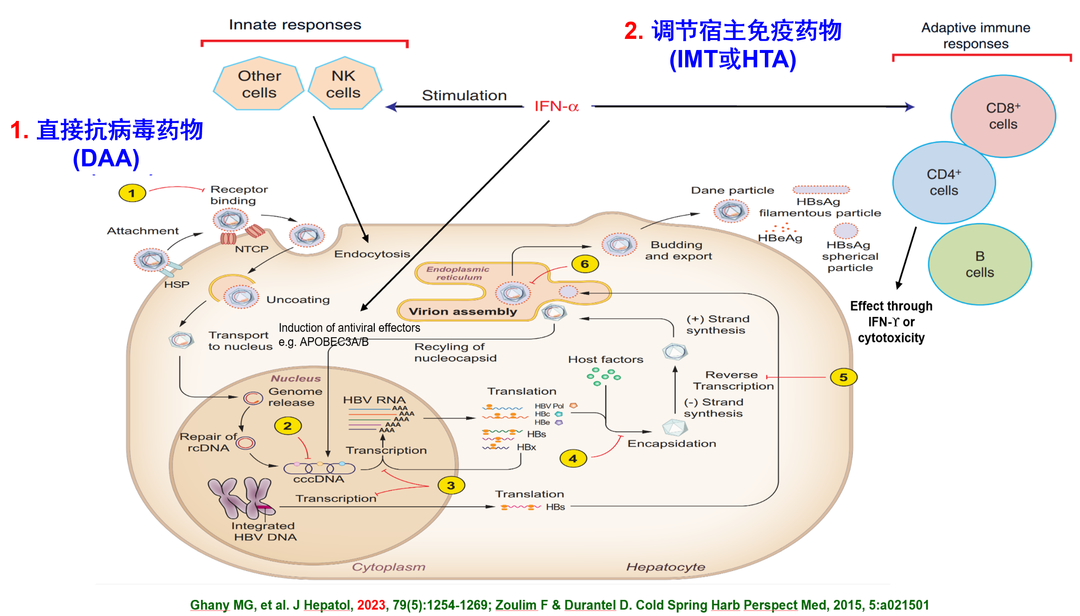
图1 在研乙肝新药及其作用靶点
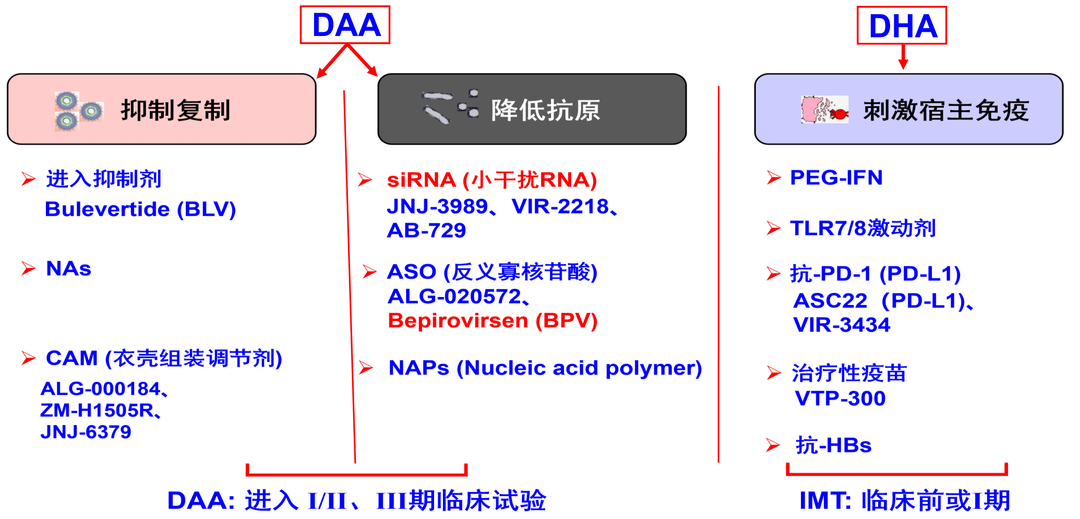
图2. 进入不同期临床试验的乙肝新药
由表2可见,目前完成临床试验2b并进入III期临床试验的药物为反义寡核苷酸(ASO)Bepirovirsen(BPV),此药可使部分CHB患者获得临床治愈。siRNA 2期临床试验表明,治疗48周,停药后24周,无1例CHB获得HBsAg消失。
表2. 乙肝新药的临床试验结果
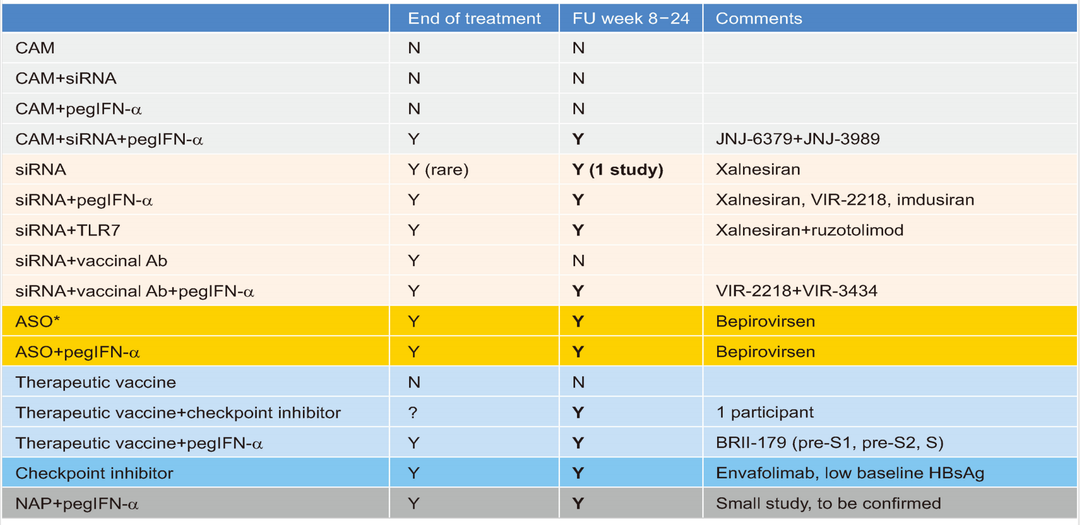
2024年6月,亚太消除病毒性肝炎工作组对乙肝抗病毒新药的功能性治愈进行了荟萃分析,包括15种新药19项研究,临床试验对象为无肝硬化的CHB患者。
▼ 研究结果显示:
① 新型抗病毒治疗在达到预期治疗终点(包括功能性治愈和HBsAg减少)方面效果有限;
② 没有表现出优于NA治疗对照组;
③ HBsAg的消失和下降通常不持久。这可能与新药疗效欠佳或者由于临床试验设计欠佳有关。
Bepirovirsen(BPV)是Ionis Pharmaceuticals 和 GSK合作开发用于CHB治疗的一款反义寡核苷酸(ASO),靶向所有HBV RNA,包括HBV信使RNA和前基因组RNA。
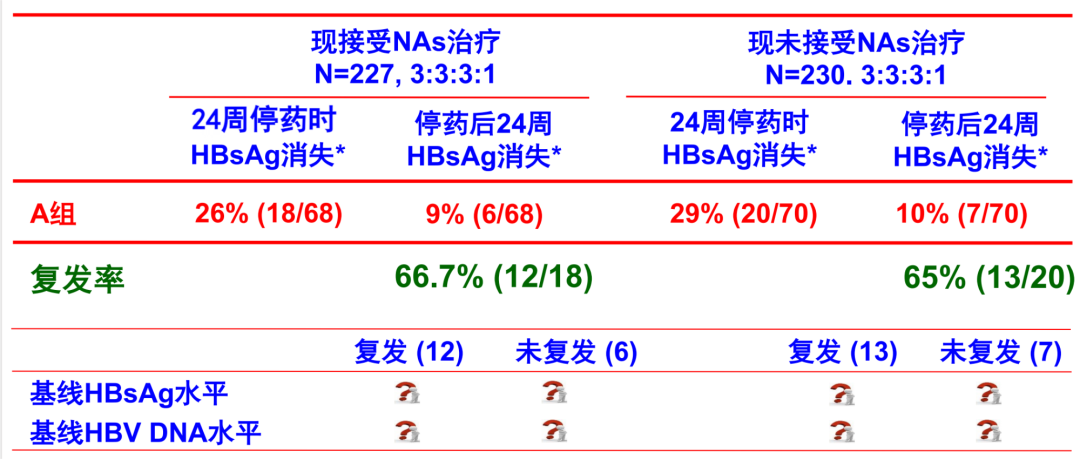
研究人员进行了一项2b期试验(B-Clear)[8],旨在评估接受持续核苷(酸)类似物(NAs)治疗或不接受NAs治疗的CHB患者,接受12周和24周BPV治疗的疗效和安全性。主要终点是BPV治疗结束24周后达到HBsAg <0.05 IU/ml 和 HBV DNA < 20 IU/ml 患者的比例。结果如表3所示。
表3. B-Clear试验结果
BPV还报告了IIb期、多中心、随机、开放的B-Together研究,对BPV和Peg-IFN序贯治疗能否提高BPV疗效进行了评估。结果显示,使用BPV治疗24周后,基线HBsAg≤3000 IU/ml的患者中有51%实现了HBsAg清除;基线HBsAg≤1000 IU/ml的患者中,有65%实现了HBsAg清除(图3)。但BPV序贯PegIFN治疗24周,未能有效维持患者HBsAg消失率。停药24周,基线HBsAg<1000 IU/ml患者的HBsAg消失率仅为24%,复发率为63.6%(7/11)。
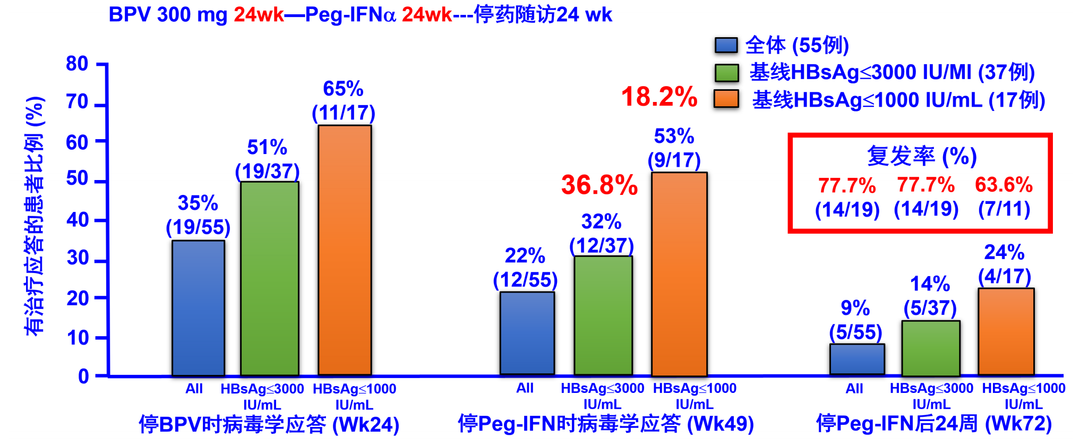
图3. B-Together研究结果
▼ BPV 2b临床试验结果提示:
① BPV短期疗效较好,基线HBsAg<1000 IU/ml患者治疗24周,HBsAg消失率可达65%,但停药后复发率高,说明疗效持续时间短;
② 被选患者基线HBsAg和HBV DNA水平相对较高,可能需选基线HBsAg和HBV DNA水平较低的患者;
③ BPV 24周疗程短,需要延长疗程;
④ 需与NAs和/或Peg-IFN联合治疗。
四、乙肝新药临床试验的设计
选择符合优势人群标准的CHB患者,对乙肝新药临床试验的设计尤为重要。经NAs治疗的优势人群,加用Peg-IFN治疗,基线HBsAg水平与治疗48周时HBsAg清除率的关系如图4所示。基线HBsAg水平>500 IU/ml患者的HBsAg清除率较低。
此外,与巩固治疗<12周患者比较,巩固治疗12~24周或>24周患者的功能性治愈率高、HBsAg复阳率低(图5)。确证HBsAg消失患者持久性高。所谓确证HBsAg消失者,是指于停药后24周,重复检测HBsAg仍<0.05 IU/ml者(图6)。
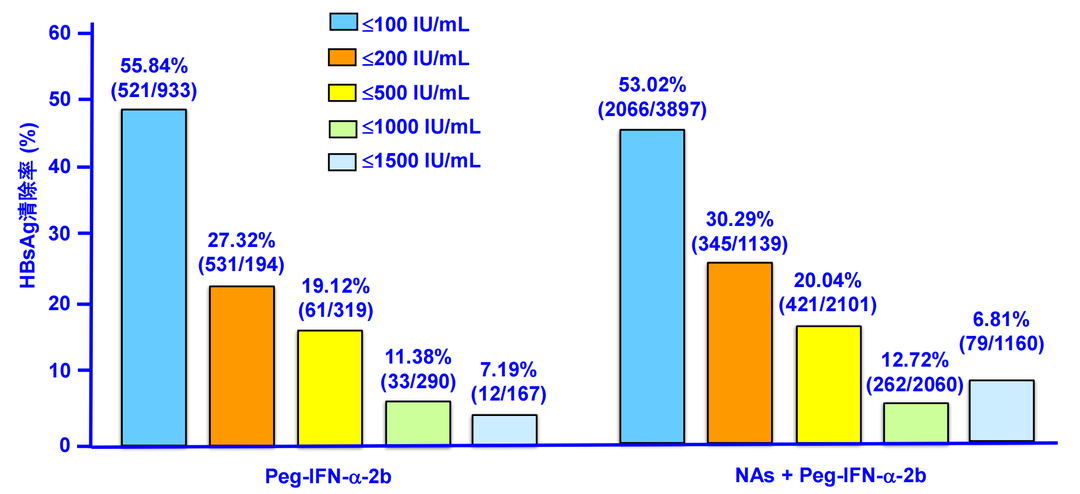
图4. 基线HBsAg水平与治疗48周时HBsAg清除率
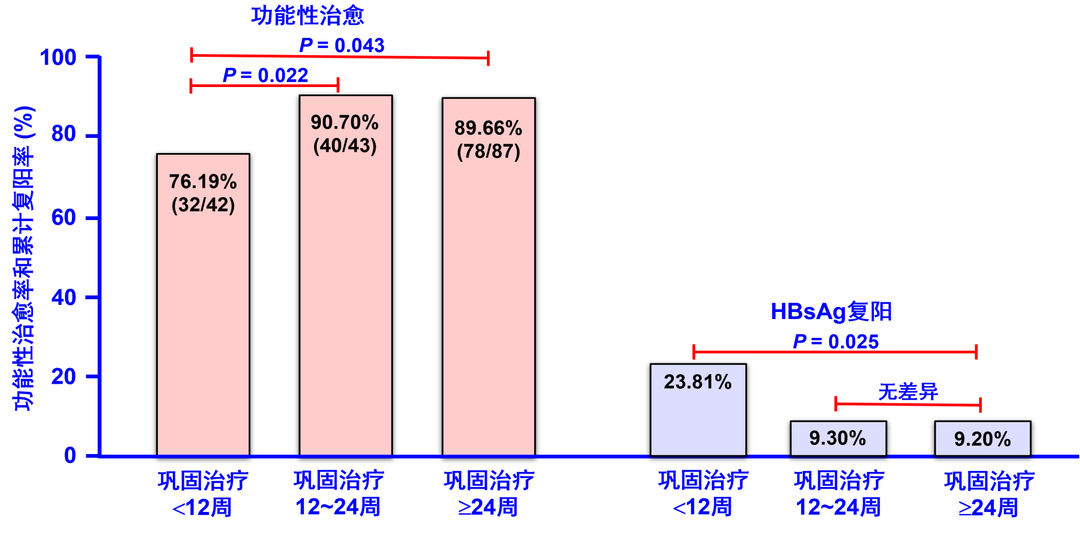
图5. 巩固治疗时间与功能性治愈率和HBsAg复阳率
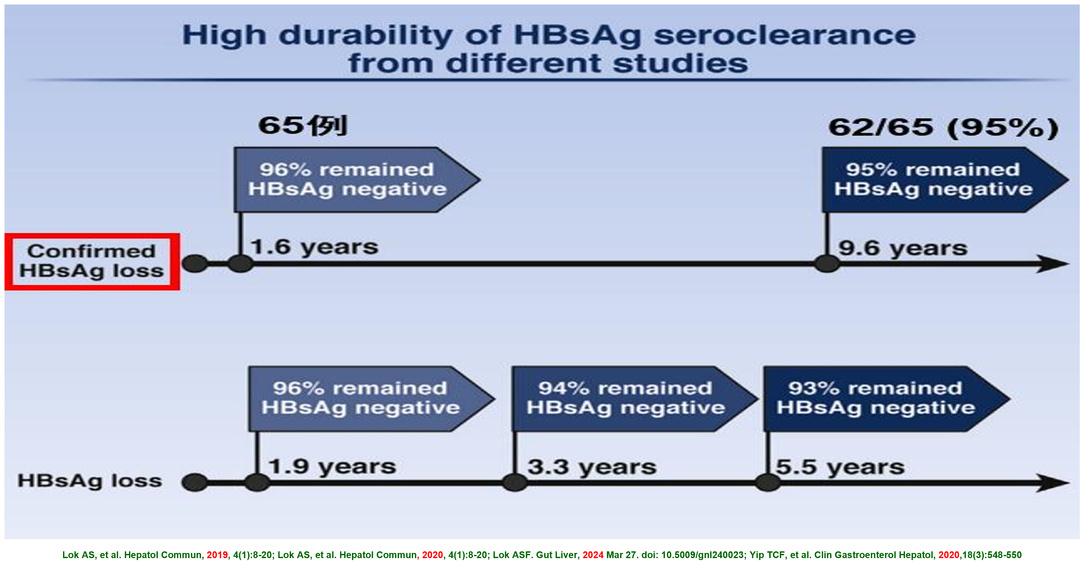
图6 确证HBsAg消失患者的HBsAg复阳率低
因此,为提高目前在研乙肝新药的功能性治愈率,可借鉴NAs加用Peg-IFN治疗策略的临床试验设计,如:
① 研究对象可根据新药疗效,设定入组临床试验CHB患者的基线HBV DNA和HBsAg水平;
② 延长治疗时间;
③ 与NAs或Peg-IFN联合治疗;
④ 确证HBsAg消失(即检测2次,间隔24周,2次均<0.05 IU/ml);
⑤ HBsAg消失后巩固治疗至少24周等。
五、总结
① 乙肝新药临床试验的主要终点是功能性治愈。
② 乙肝新药临床试验的主要评价指标是生化学、病毒学、血清学、组织学,其中以HBsAg持续消失最重要。
③ 需要进一步完善乙肝新药的临床试验设计,使乙肝新药早日上市。
参考文献
[1] Ghany MG, Buti M, Lampertico P, Lee HM, Faculty A-EH-HTEC. Guidance on treatment endpoints and study design for clinical trials aiming to achieve cure in chronic hepatitis B and D: Report from the 2022 AASLD-EASL HBV-HDV Treatment Endpoints Conference. J Hepatol, 2023, 79(5):1254-1269.
[2] Cornberg M, Lok AS, Terrault NA, Zoulim F, Faculty E-AHTEC. Guidance for design and endpoints of clinical trials in chronic hepatitis B - Report from the 2019 EASL-AASLD HBV Treatment Endpoints Conference (double dagger). J Hepatol, 2020, 72(3):539-557.
[3] Lok AS, Zoulim F, Dusheiko G, Ghany MG. Hepatitis B cure: From discovery to regulatory approval. Hepatology, 2017, 66(4):1296-1313.
[4] Lok ASF. Toward a Functional Cure for Hepatitis B. Gut Liver, 2024 Mar 27. doi: 10.5009/gnl240023;
[5] Yip TC, Wong VW, Lai MS, et al. Risk of hepatic decompensation but not hepatocellular carcinoma decreases over time in patients with hepatitis B surface antigen loss. J Hepatol, 2023, 78(3):524-533.
[6] Fanning GC, Zoulim F, Hou J, Bertoletti A. Therapeutic strategies for hepatitis B virus infection: towards a cure. Nat Rev Drug Discov, 2019, 18(11):827-844.
[7] Roca Suarez AA, Testoni B, Zoulim F. HBV 2021: New therapeutic strategies against an old foe. Liver Int, 2021, 41 Suppl 1:15-23.
[8] Yuen MF, Lim SG, Plesniak R, Tsuji K, Janssen HLA, Pojoga C, et al. Efficacy and Safety of Bepirovirsen in Chronic Hepatitis B Infection. N Engl J Med, 2022, 387(21):1957-1968.


