【衡道丨病例】病理诊断——宫颈大细胞神经内分泌癌
时间:2025-01-22 12:09:15 热度:37.1℃ 作者:网络
病史介绍
患者女性,46岁,因“绝经后阴道流血半年,阴道分泌物增多1+月”入院。
外院:子宫颈异常密度肿块,考虑宫颈癌。
HPV检测示:HPV18型阳性。
外院活检示:“宫颈赘生物”考虑腺癌。
胸部CT示:未见结节。
组织病理活检
大体观:
送检全子宫带双侧附件,体积12cm×8cm×4cm,宫颈内口见一灰白色肿物,体积4cm×2cm×1cm,表面粗糙,溃烂,切面灰白,质稍硬,似侵及宫颈管壁内1/2,局部似累及阴道壁,肉眼未见宫颈管内口累及,宫腔与双附件未见肿瘤。
镜下观:
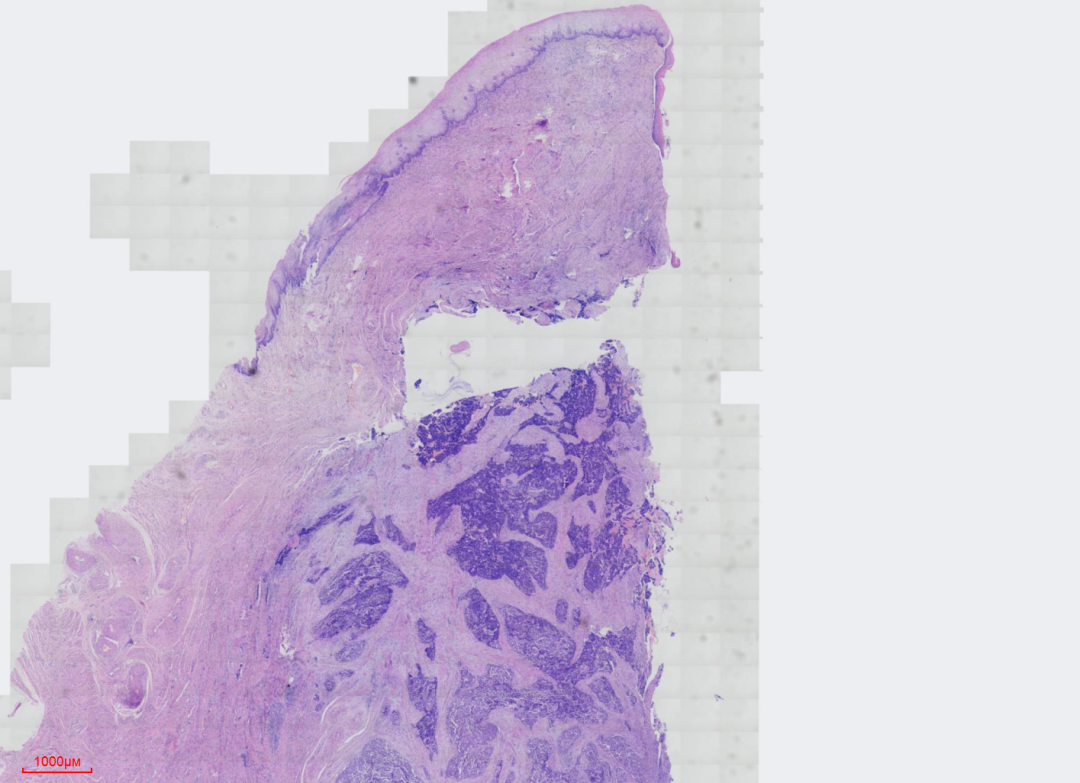
图1 低倍镜下,可见肿瘤组织位于宫颈鳞状上皮以下,未累及表面鳞状上皮组织,肿瘤组织呈浸润性生长,大部分区域呈巢团状生长模式,也可以呈片状生长模式。
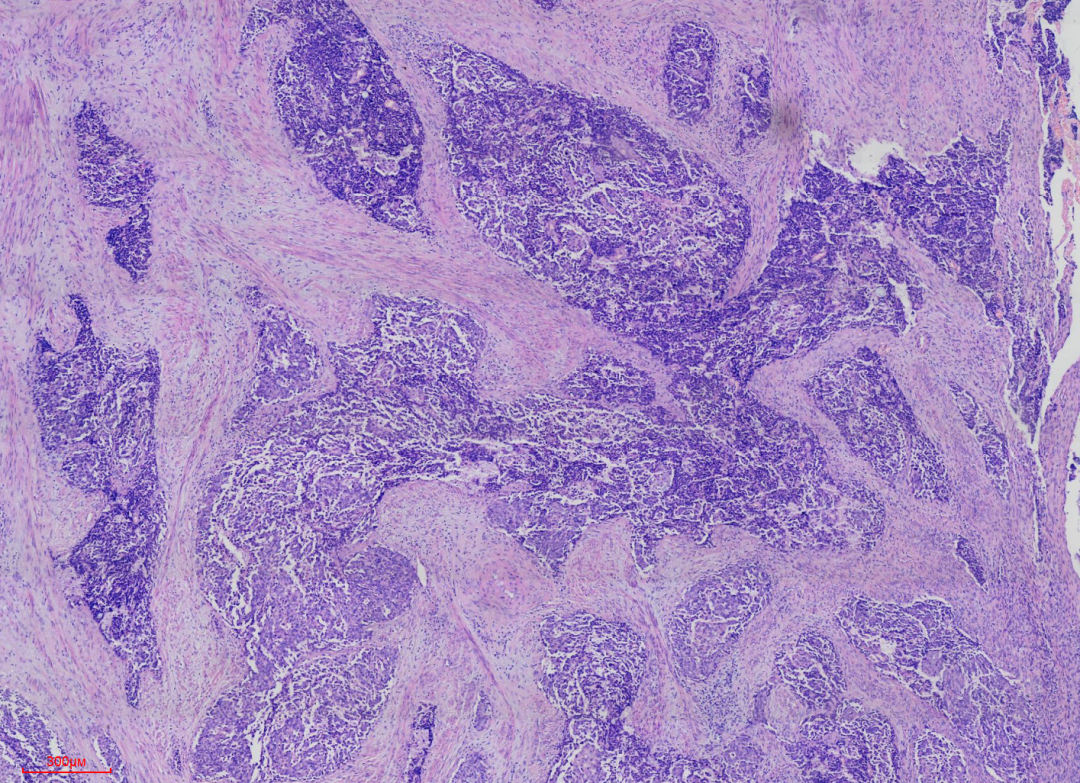
图2 40倍镜下浸润性肿瘤组织呈巢片状生长,周围间质显示较明显的纤维化,肿瘤组织中央可以有坏死区域。
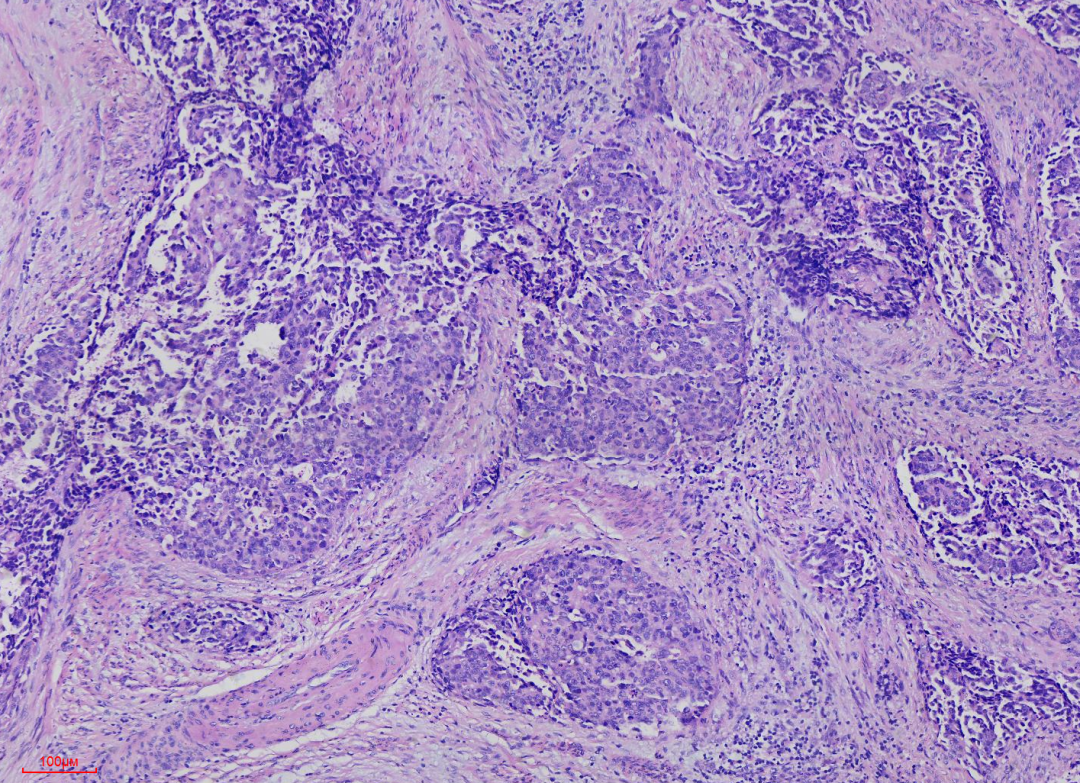
图3 100倍镜下见肿瘤细胞异型性较明显,细胞增大较明显,细胞之间大小有差异,大部分区域瘤细胞胞质较多,细胞核染色呈粗颗粒状,核形状不规则。
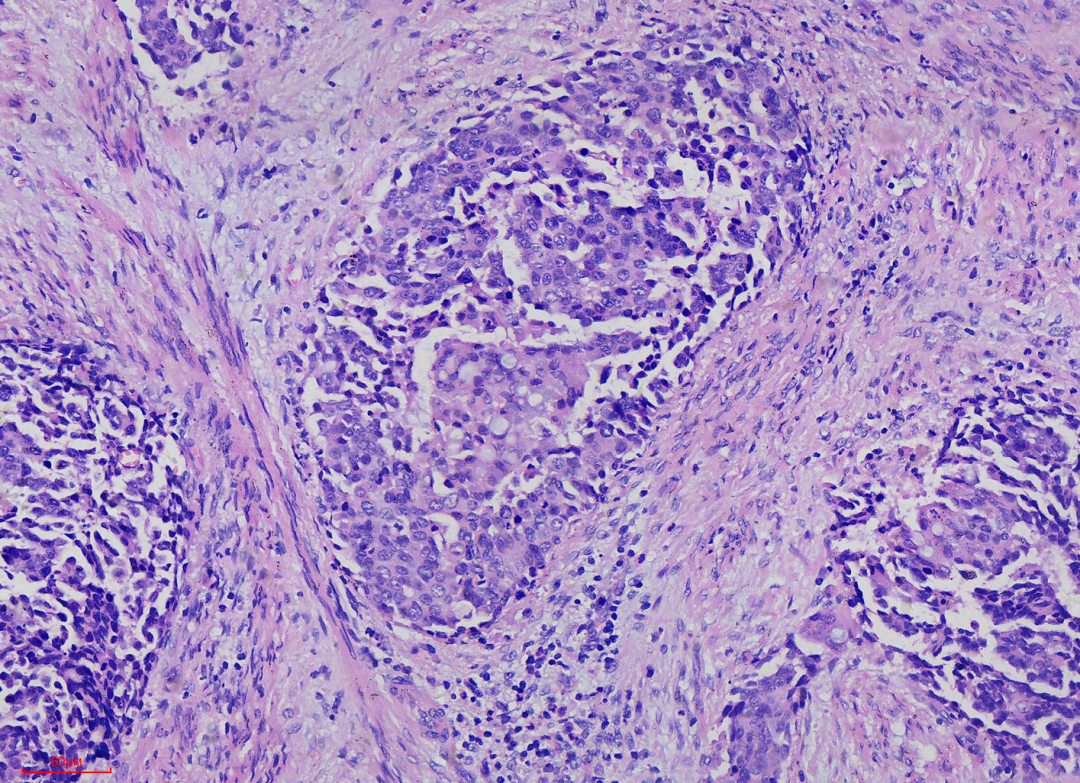
图4 200倍镜下见肿瘤细胞异型性较明显,细胞增大,细胞大小不等,肿瘤细胞可见明确细胞质,细胞核染色较深、呈粗颗粒状,核形状不规则,大细胞肿瘤组织中央可见少许似印戒样的粘液细胞。
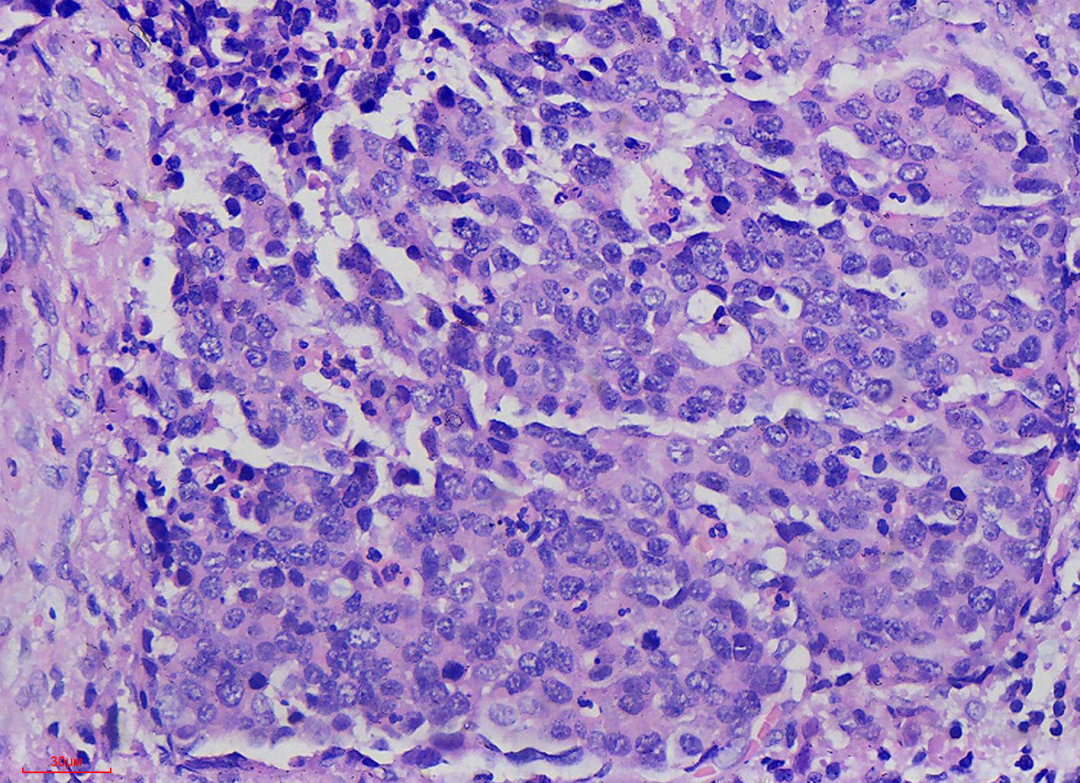
图5 400倍镜下见肿瘤细胞呈圆形,细胞异型性明显,细胞核染色较深、呈粗颗粒状,核形状不规则,部分细胞可见明显核仁,核分裂可见。
免疫组化
免疫组化阳性指标:
CK-P(+);P16(弥漫强+);SYN(+);CD56(+);CGA(+);TTF1(少许+) ;Ki-67(约90%);P53(异常过表达) ;CEA(印戒样粘液细胞+);CK7(印戒样粘液细胞+) ;Stathmin(+++,约50%);BRG-1(+);CAM5.2(核旁点状+)。
免疫组化阴性指标:
P63、 ER、 PR、 P40、 CK20 、P504S。
特殊染色:
大细胞中央印戒样粘液细胞显示:AB(+)、PAS(+)。
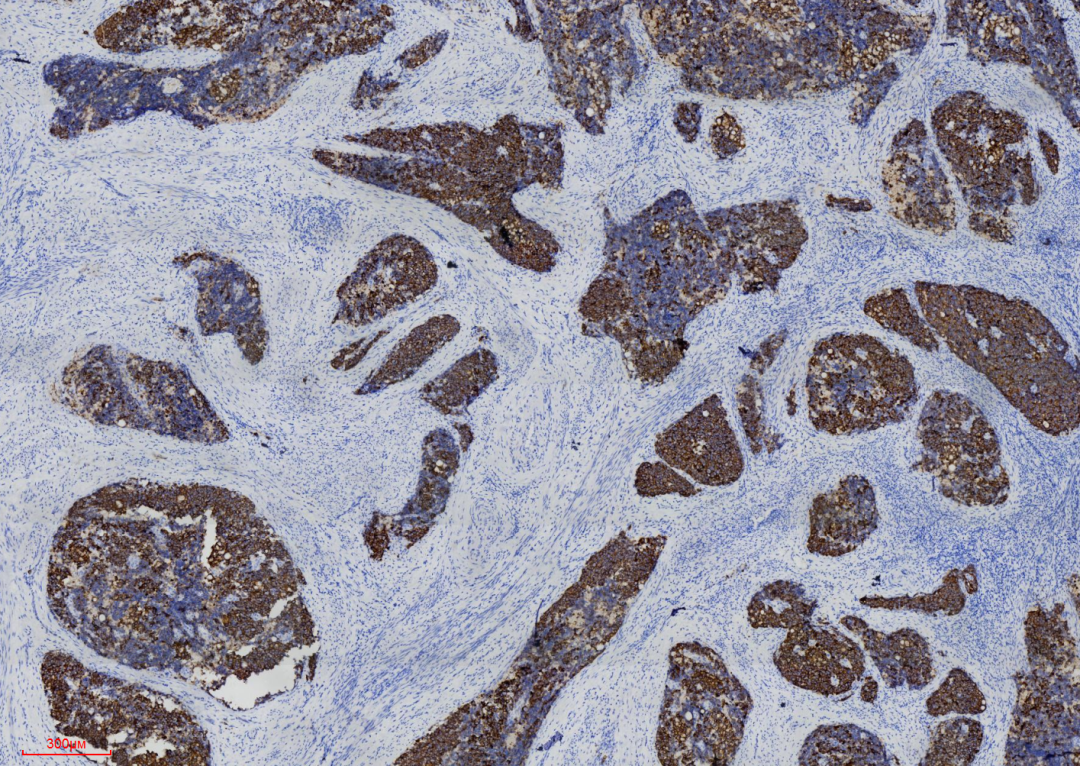
图6 显示免疫组化上皮来源标记物CK-P阳性,阳性方式呈核旁颗粒状。
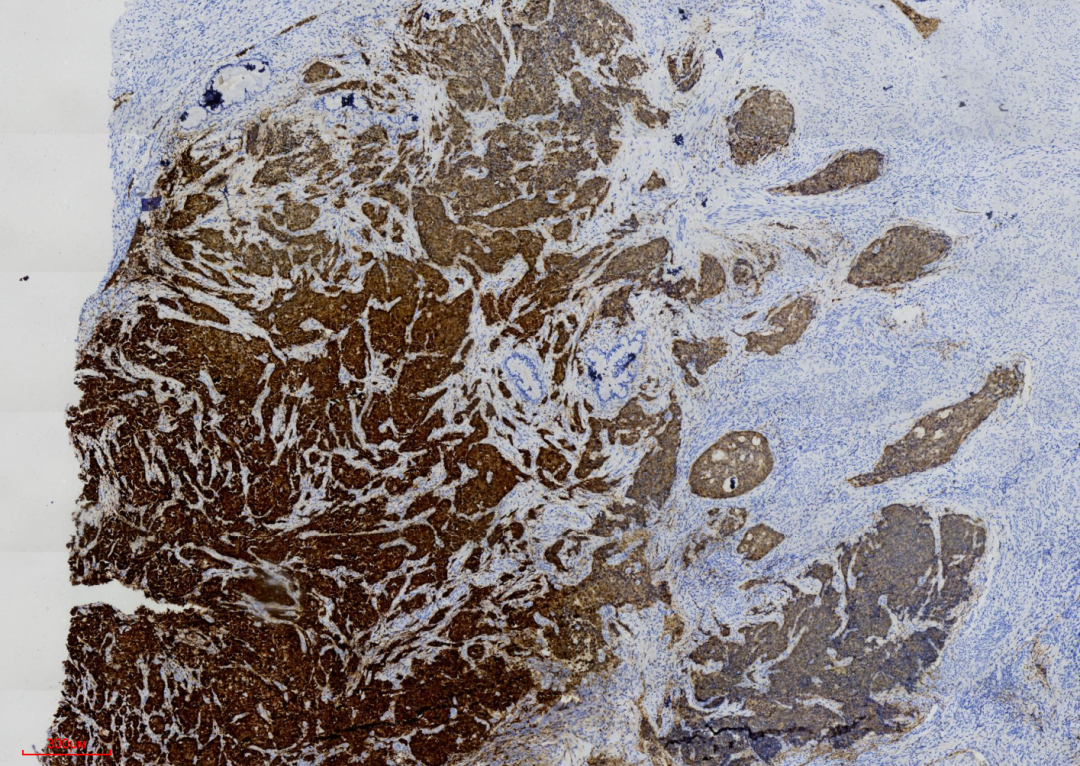
图7 显示免疫组化P16呈现弥漫强阳性表达。
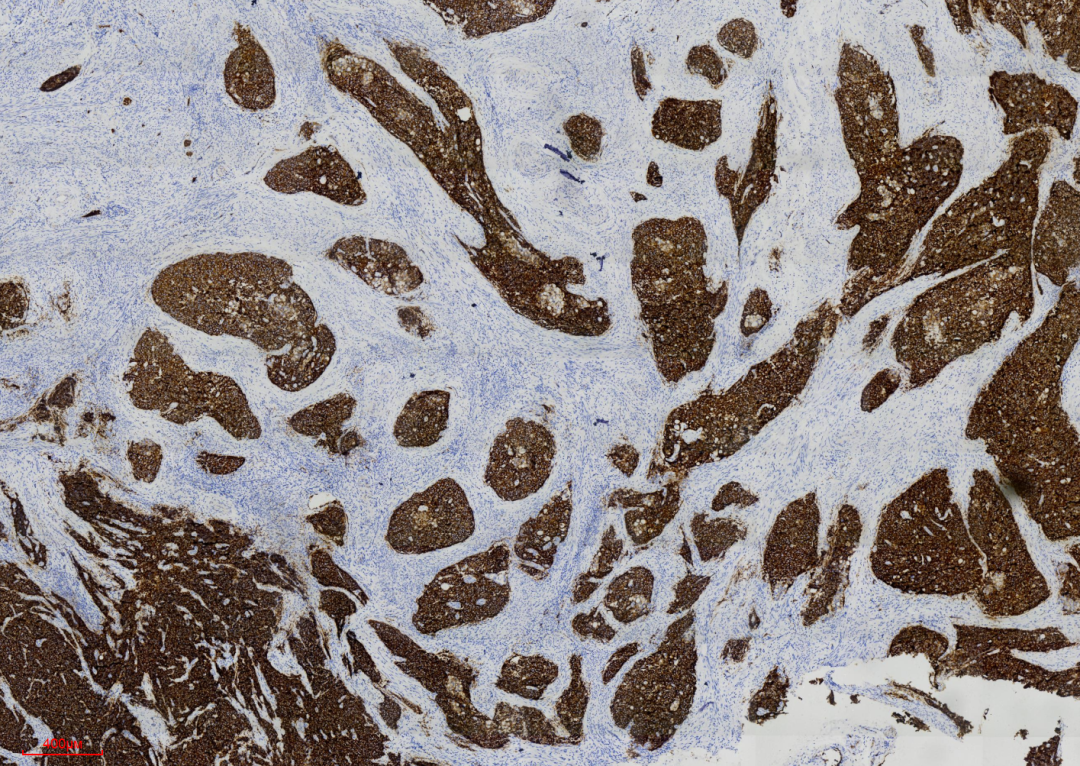
图8 显示免疫组化SYN呈现弥漫强阳性表达。
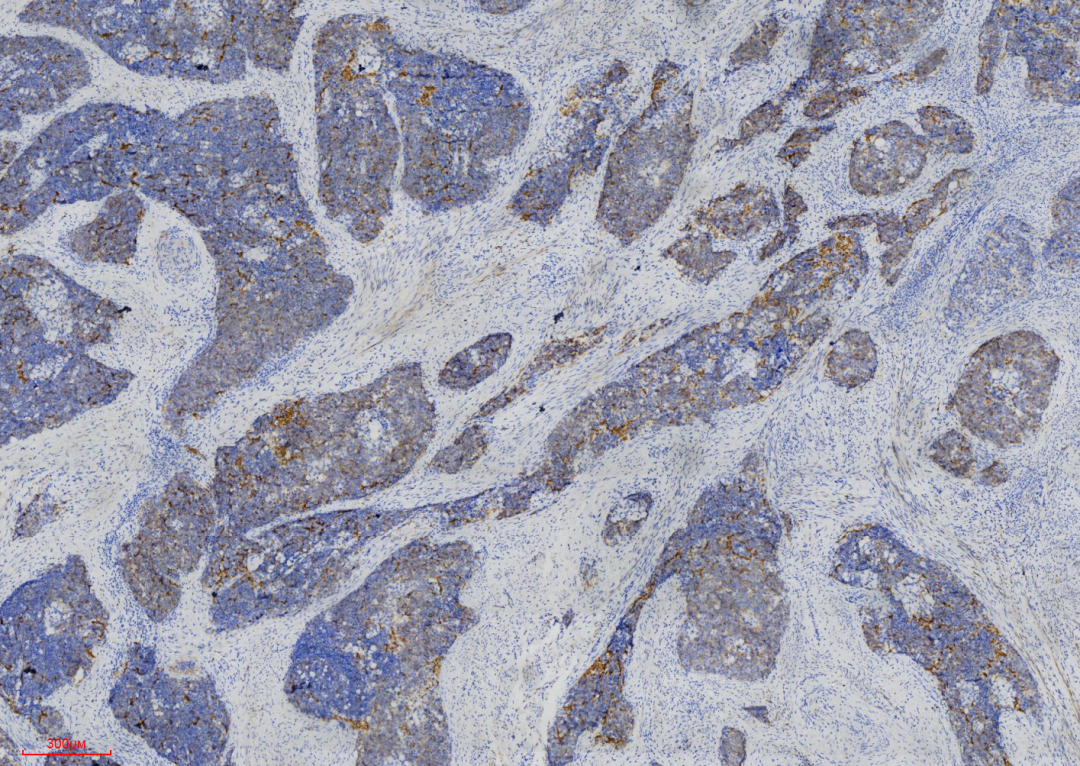
图9 显示免疫组化CD56呈现阳性表达。
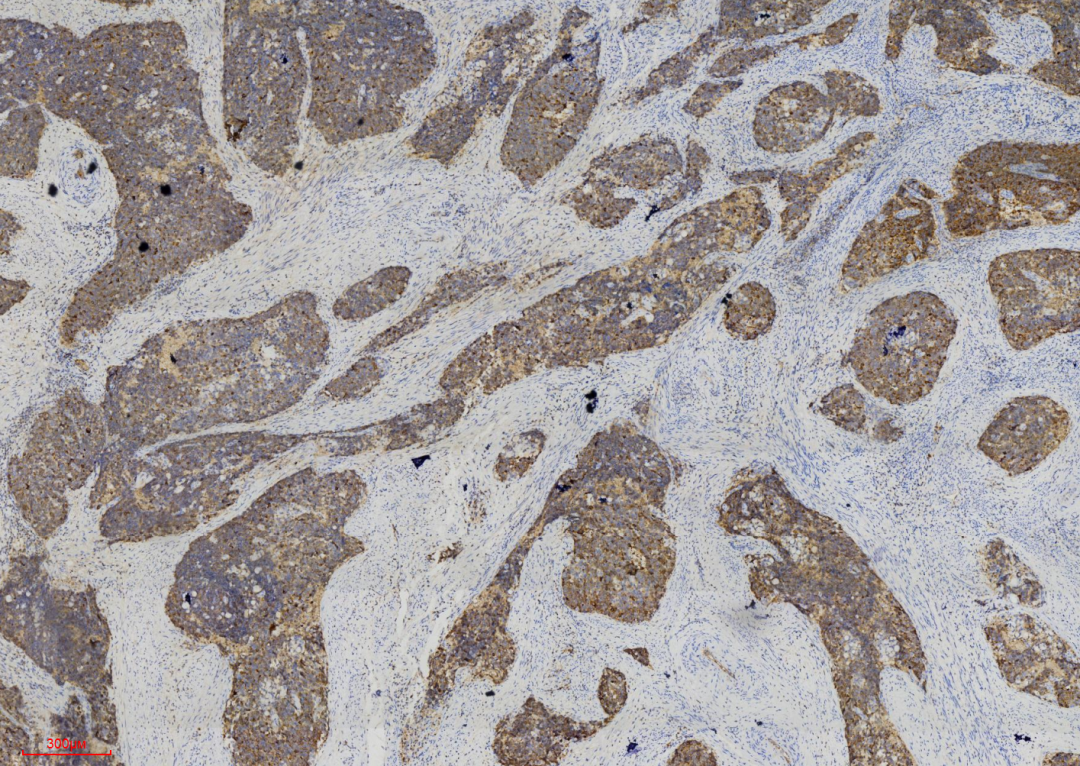
图10 显示最具特异性的神经内分泌标记物CGA呈现阳性表达。
病理诊断
大细胞神经内分泌癌,可见少量腺癌(约占2%),肿瘤最大径4cm,肿瘤浸润深度<1/2宫颈间质,累及宫颈阴道壁,可见脉管内癌栓,阴道壁切缘及宫腔未见癌组织。
术后6个月上腹部增强CT:考虑肝内、多发胸腰椎体及部分附件、以及所见双肺多发转移瘤。
讨论
概述
神经内分泌肿瘤(Neuroendocrine Neoplasms,NEN)是由弥漫性分布的神经内分泌细胞引起的一系列恶性肿瘤组成。NEN最常见的位置是胃肠道(62-70%),其次是气管支气管系统(25%)。子宫颈原发的神经内分泌癌(neuroendocrine cervix carcinoma,NEC)罕见,占宫颈癌的1.4-2%。NEC与同病期鳞癌、腺癌相比生物学行为表现出更高的侵袭性,初诊时多为进展期,其疾病进展、转移、复发及死亡风险均较高,预后差。
发病机制
目前关于NTC起源尚有争议,主要研究观点如下:宫颈黏膜内含有的少量嗜银细胞,具有向神经内分泌分化并产生多肽激素,并可进一步恶变为神经内分泌肿瘤。起源于子宫颈的全能干细胞。也有认为起源于宫颈腺上皮下的储备细胞,而这一观点能够很好的解释同时伴发的鳞癌或腺癌。但发病机制还需进一步研究探索。
分类分级
1997年美国病理学会提出了NEC的标准化术语 ,基于Ki-67指数、有丝分裂指数和坏死等肿瘤特征确定为四类: 小细胞神经内分泌癌、大细胞神经内分泌癌、典型类癌和非典型类癌。2020年WHO第5版女性生殖器官肿瘤分类中将子宫颈神经内分泌肿瘤分为低级别神经内分泌肿瘤(neuroendocrine tumour,NET)和高级别神经内分泌癌(neuroendocrine carcinoma,NEC),此外还有混合性神经内分泌-非神经内分泌肿瘤。虽然NET和NEC在神经内分泌相关免疫组化标记物(Syn、CgA、CD56)表达方面无明显差异,但在生物学和临床结局方面差异较大。

在NECC中,小细胞神经内分泌癌最多见,约占80%,其次是大细胞神经内分泌癌约占12%,其他组织学类型如未分化神经内分泌肿瘤约占8%。
宫颈大细胞神经内分泌癌病变特点
LCNEC因复发率高,易发生早期转移,具有高度侵袭性,其预后极差。原发性LCNEC是少见的高度恶性肿瘤,发病率占宫颈恶性肿瘤0.087%-0.900%,发病年龄为21-94岁。临床LCNEC的原发部位多见于肺、喉及胃等部位,原发宫颈者国内外文献中罕见报道。
临床表现
宫颈LCNEC临床表现与其他类型宫颈癌无异,主要表现为阴道不规则出血、流液和不规则的肿块。因肿瘤一般弥漫性浸润间质,而不侵犯宫颈黏膜上皮,致使宫颈细胞学检查多为阴性而漏诊,阴道镜下也无特异性表现。临床上很少出现典型的神经内分泌症状,临床生化检查也无特异性的激素类标记物。Embry等人报道40%的LCNEC患者存在转移,常见的转移部位为肺和肝,其他转移部位还包括肾上腺、骨等。
镜下形态学特征
肿瘤分化差,常有器官样分化,典型的排列为梁状或者索样,也可以呈片状,但边缘有栅栏状形态,并常见地图样坏死灶。
肿瘤细胞大小相对较一致,通常中等或较大,无序重叠簇拥在一起,细胞核直径是正常的3-5倍,呈圆形或椭圆形泡状,可含有神经内分泌细颗粒,常可见1-3个明显的嗜酸性核仁。
胞质中等或较丰富,嗜酸性。腺性分化不少见,一组研究发现,约66%的LCNEC 合并原位腺癌,25%合并腺癌。
免疫组化
最常用的神经内分泌标志物是嗜铬粒蛋白A(CGA)、突触素(SYN)、CD56和神经元特异性烯醇化酶(NSE)。除HE染色观察形态学外,CGA是大细胞神经内分泌癌的特异性标志物,而在小细胞NEC的阳性率33%~100%。嗜铬粒蛋白是最特异的标志物,但敏感度不高。大多数子宫颈高级别神经内分泌癌p16染色呈弥漫性阳性。
鉴别诊断
①SCNEC:NTC最常见类型,需重点鉴别。后者肿瘤细胞的细胞质稀少,核浓染,在镜下主要表现为细染色质呈细颗粒状,无核仁或核仁不清晰,CgA免疫标记物阳性率较低。
②转移性大细胞癌:需结合临床病史及影像学检查排除。
③低级别神经内分泌肿瘤:尤其活检标本挤压后易误诊,而后者Ki-67增殖指数高表达。
④小细胞非角化型鳞癌或基底细胞样鳞癌:肿瘤细胞小,癌巢中央出现角化或单个细胞角化,弥漫表达鳞癌标记P63、P40及CK5/6等,而神经内分泌标记物阴性。
⑤淋巴瘤、恶性黑色素瘤等。
病理分期
NECC的分期遵循国际妇产科联盟(FIGO)子宫颈恶性肿瘤分期系统,影像学和病理学证据参与肿瘤分期,影像学评估选择CT、MRI和PET成像。



