GLP-1RA真实世界研究成果在国际期刊发表,聚乙二醇洛塞那肽为糖尿病肾病患者带来多重受益,且可改善脂质水平
时间:2024-08-08 18:00:25 热度:37.1℃ 作者:网络
近日,一项关于GLP-1受体激动剂(GLP-1RA)治疗糖尿病肾病(DKD)患者的真实世界研究成果在国际期刊《糖尿病,代谢综合症和肥胖》(Diabetes, Metabolic Syndrome and Obesity)上发表。研究发现,孚来美®(聚乙二醇洛塞那肽)相比其它GLP-1RA类药物,胃肠道反应和低血糖发生率均更低,具有安全性优势;且治疗6个月能够显著改善轻中度DKD患者的血糖、血压、血脂和体重,有助延缓肾脏疾病进展,给患者带来多重获益[1]。

DKD是继发于糖尿病的一种慢性肾脏疾病,是糖尿病的主要并发症,也是最严重的并发症之一[2]。约有 30%–40% 的糖尿病患者伴有DKD[3],是导致终末期肾病(ESRD)的主要原因[4]。GLP-1RA除了具有降糖作用之外,还具有降压、减重和调节脂质等作用[5]。多项心血管结局试验已表明,GLP-1RA具有心脏和肾脏的双重获益,能够减少2型糖尿病患者肾脏不良事件风险[6]。然而,关于GLP-1RA治疗DKD患者的真实世界研究却很有限。
这项单臂、回顾性、真实世界研究共纳入了364例接受GLP-1RA治疗至少6个月的患者,其中包括利拉鲁肽49例,司美格鲁肽52例,度拉糖肽104例,聚乙二醇洛塞那肽159例。42%为女性,平均年龄52.1岁,基线糖化血红蛋白(HbA1c)8.6%,基线BMI 27.8 kg/m2。治疗前后收集实验室测量数据,包括血糖、血脂、血压、尿微量白蛋白与肌酐比值(UACR)、24 小时尿蛋白和估算肾小球滤过率(eGFR)。主要终点是治疗 6 个月时的HbA1c水平[1]。
一、GLP-1RA带来降糖、减重、降压、降脂多重获益,且显著减少尿蛋白并改善肾功能[1]
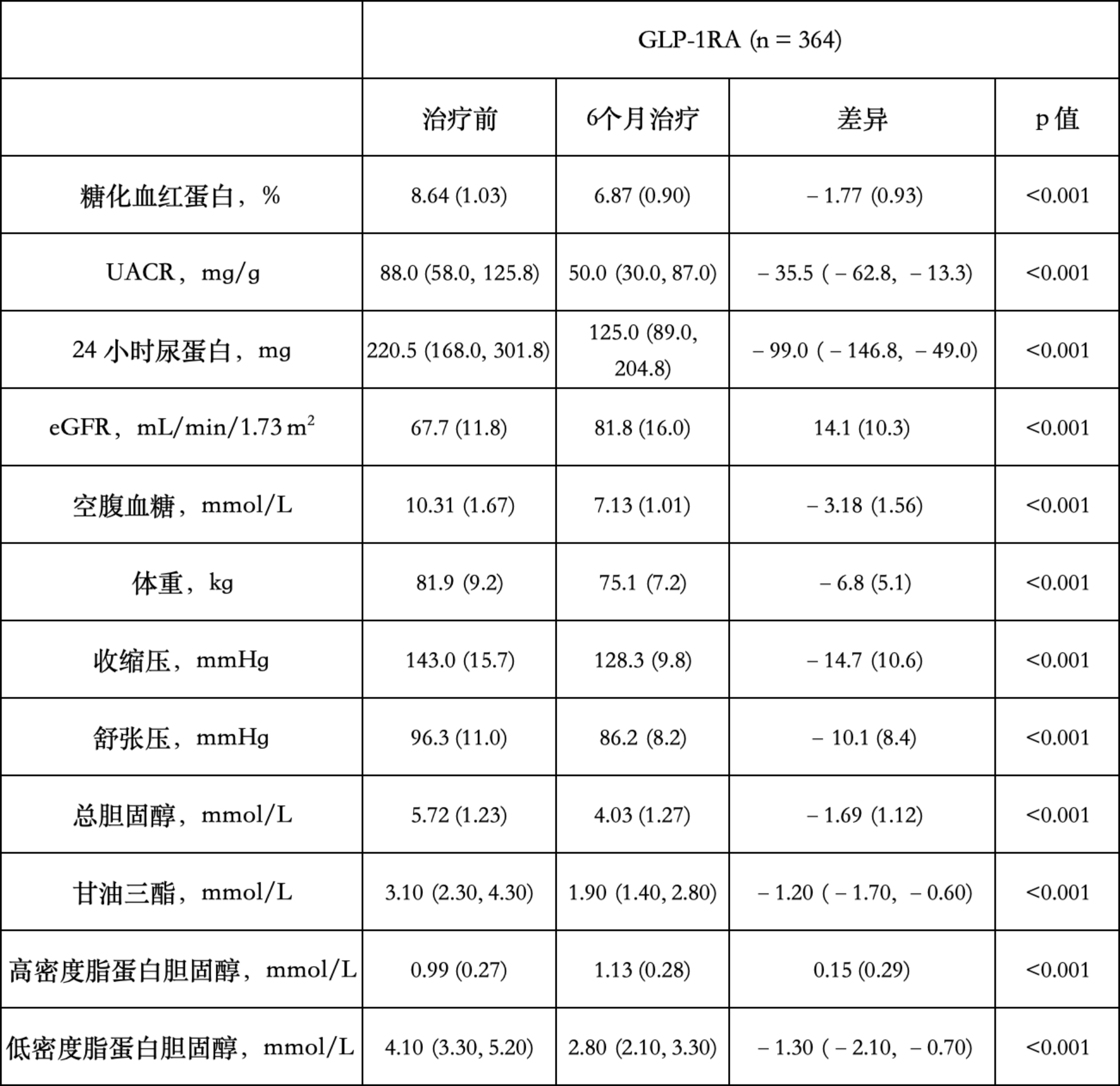
GLP-1RA治疗6个月后,平均HbA1c水平显著下降1.77% (p<0.001),同时UACR降低了40.3%。此外,24小时尿蛋白和eGFR也显著改善(均 p<0.001)。与基线相比,患者的空腹血糖、体重、收缩压 (SBP)、舒张压 (DBP)、总胆固醇 (TC)、血糖、甘油三酯 (TG)、高密度脂蛋白、胆固醇 (HDL-C) 和低密度脂蛋白胆固醇 (LDL-C)均有显着改善(均p < 0.001)(表1)。
表1.使用 GLP-1RA治疗6 个月的指标变化
二、聚乙二醇洛塞那肽的胃肠道反应和低血糖发生率均更低,更具安全性优势[1]
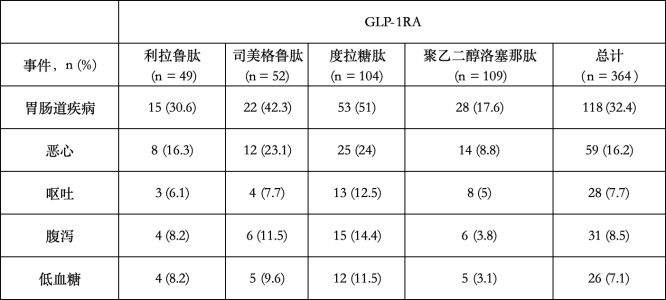
研究显示,尽管使用聚乙二醇洛塞那肽治疗的患者数量最多(44%,159/364),但其胃肠道反应的总发生率(17.6% vs 30.6%~51%)和低血糖发生率(3.1% vs 8.2%~11.5%)均低于其它GLP-1RA。胃肠道反应中的恶心(8.8% vs 16.3%~24%)、呕吐(5% vs 6.1%~12.5%)、腹泻(3.8% vs 8.2%~14.4%)发生率也均低于其它GLP-1RA(表2)。
表2. 治疗期间胃肠道不良反应及低血糖情况
三、无论是否使用ACEi/ARB类肾保护药,GLP-1RA均能降低蛋白尿,且越早使用获益越明显[1]
血管紧张素转换酶抑制剂(ACEi)或血管紧张素受体拮抗剂(ARB)类药物是最常用的肾保护药物,已被KDIGO指南推荐治疗糖尿病且合并高血压和蛋白尿的患者[7]。值得注意的是,本研究中有59.3% 的患者在基线时服用ACEi或ARB类药物,这些患者在接受GLP -1RA治疗后UACR降低了41.5%;而在那些未服用ACEi或ARB类药物的患者中,GLP-1RA治疗后UACR依然降低了35.8%。这提示GLP-1RA能够独立于ACEi或ARB降低蛋白尿。
亚组分析表明,病程<10年的患者相比病程≥10年的患者,HbA1c水平(p<0.001)、UACR(p=0.036)和 eGFR(p<0.001)改善更为明显,这提示越早开始GLP-1RA治疗的患者,血糖及肾功能的改善越明显。
结语
既往曾有随机对照研究证实了聚乙二醇洛塞那肽对轻中度DKD患者的疗效与一线的SGLT2抑制剂达格列净相当,且具有改善脂质水平的额外获益[8]。这项真实世界研究则再次证实了聚乙二醇洛塞那肽能够为轻中度DKD患者带来降糖、降压、减重、改善血脂、改善肾功能和延缓肾脏进展等多重获益,且在安全性上更具优势,胃肠道反应和低血糖发生率低将有助改善患者的生活质量并提高依从性,聚乙二醇洛塞那肽的多重获益和安全性优势将为DKD患者带来更优的治疗选择。
参考文献:
1. Ying Liu et al. Real-world clinical effectiveness of glucagon-like peptide-1 receptor agonist on mild-to-moderate diabetic kidney disease in patients with type 2 diabetes: a retrospective, single-arm clinical trial.Diabetes, Metabolic Syndrome and Obesity 2024:17 2913–2921.
2. Mohandes S, Doke T, Hu H, et al. Molecular pathways that drive diabetic kidney disease. J Clin Invest. 2023;15;133:e165654.
3. Bonner R, Albajrami O, Hudspeth J, et al. Diabetic kidney disease. Prim Care. 2020;47:645-659.
4. Mima A, Nomura A, Fujii T. Current findings on the efficacy of incretin-based drugs for diabetic kidney disease: a narrative review. Biomed Pharmacother. 2023;165:115032.
5. Ard J, Fitch A, Fruh S, et al. Weight loss and maintenance related to the mechanism of action of glucagon-like peptide 1 receptor agonists. Adv Ther. 2021;38:2821-2839.
6. Caruso I, Cignarelli A, Giorgino F. Heterogeneity and similarities in GLP-1 receptor agonist cardiovascular outcomes trials. Trends Endocrinol Metab. 2019;30:578-589.
7. Kidney Disease: Improving Global Outcomes Diabetes Work, G. KDIGO 2022 clinical practice guideline for diabetes management in chronic kidney disease. Kidney Int. 2022;102:S1-S127.
8. Cao Y, Cao S, Zhao J, Zhao J, Zhao Y and Liu Y (2024) Efficacy and safety of polyethylene glycol loxenatide in treating mild-to-moderate diabetic kidney disease in type 2 diabetes patients: a randomized, open-label, clinical trial.Front. Endocrinol. 15:1387993.


