抑郁症患者使用舍曲林应关注CYP2C19基因检测,代谢表型对治疗结局具有显著影响
时间:2026-05-05 17:02:26 热度:37.1℃ 作者:网络
由于个体基因变异,部分患者对初始抗抑郁药物无反应。本研究旨在探讨特定基因多态性与抗抑郁药物疗效的关联,并在基因检测指导下提高治疗的准确性与有效性。对 2022 年 1 月至 2024 年 12 月随县人民医院的病历进行回顾性筛选,应用排除标准后共纳入 202 例携带 CYP2C19 基因的抑郁症患者。根据基因代谢类型分为三组:快代谢组(A 组,n=65)、中间代谢组(B 组,n=94)、慢代谢组(C 组,n=43)。三组均接受舍曲林治疗,疗程 6 周。观察指标包括汉密尔顿抑郁量表(HAMD)评分;药物起效时间;有效率和缓解率;临床总体印象改善量表(CGI-I)评分;神经递质因子 5-羟色胺(5-HT)、γ-氨基丁酸(GABA)和脑源性神经营养因子(BDNF)水平;不良事件发生率;以及莫里西药物依从性量表-8(MMAS-8)评分。
用药前三组患者基线数据具有可比性(p>0.05)。与 A 组、B 组相比,C 组患者 HAMD 评分下降更显著(均 p<0.05),应答率与缓解率更高(均 p<0.05);三组中 C 组药物起效时间更短(均 p<0.05),CGI–I 评分改善更显著(均 p<0.05),神经递质因子 5-HT、GABA、BDNF 上调更突出(均 p<0.05)。不良事件发生率方面,C 组最高,A 组最低(10.8% vs 24.5% vs 41.9%)。与其他组相比,B 组 MMAS-8 评分升高更显著(均 p<0.05)。
代谢表型对携带 CYP2C19 基因的抑郁症患者舍曲林治疗结局具有显著影响。三组中,C 组治疗疗效更佳,但不良事件发生率升高、用药依从性降低;A 组疗效相对较差;B 组依从性更优。临床实践中,可依据 CYP2C19 代谢分型实施个体化治疗,以提高疗效、减少不良事件并降低医疗负担。
研究背景
抑郁症作为全球高发且危害深远的精神障碍,已成为严重威胁人类心理健康的公共卫生问题。世界卫生组织数据显示,全球约有 3.22 亿人罹患抑郁症,其发病率逐年上升,发病年龄日趋年轻化。在中国,抑郁症患病率已达 3.4%,且随着社会竞争加剧、生活节奏加快,这一数字持续攀升。值得注意的是,不同人群抑郁症患病率存在显著差异,例如青少年抑郁障碍患病率达 7.4%,沉重的学业压力与社交障碍是主要诱因;女性产后抑郁发生率约 13.1%~16.6%,与激素水平波动及角色适应不良密切相关;老年人群因慢性病、孤独等因素,抑郁症患病率超 20%,空巢老人抑郁检出率接近非空巢老人的两倍。抑郁症不仅导致患者出现情绪低落、兴趣减退、思维迟缓等核心症状,还常伴随睡眠障碍、食欲改变、躯体不适等躯体症状,严重时可引发自伤、自杀等极端行为,给患者自身、家庭及社会带来沉重负担。从社会功能来看,抑郁症患者工作能力显著下降,缺勤率高于健康人群,工作效率降低,许多患者因病被迫辞职或调整岗位;家庭生活中,患者情绪问题易引发家庭矛盾,导致婚姻关系紧张、亲子关系疏离,抑郁患者家庭普遍存在不同程度的情感沟通障碍,单亲家庭患者对子女成长负面影响尤为显著。
当前抑郁症治疗仍面临诸多挑战,现有治疗方案以药物治疗为核心,辅以心理治疗、物理治疗等手段。但在药物选择上,多依赖临床医生经验判断,缺乏精准指导依据。由于个体基因差异显著,不同患者对同一抗抑郁药物的疗效与耐受性往往存在极大差异。因此,探索精准治疗策略以提升抑郁症治疗的有效性与安全性,成为精神病学领域亟待解决的紧迫问题。随着分子生物学与基因组学技术的快速发展,基因检测技术在临床医学中应用日益广泛,为抑郁症个体化管理提供了全新视角与策略。基因检测通过分析患者基因序列,可识别与药物代谢、疗效相关的基因变异,进而预测患者对特定药物的反应,为临床医生制定个体化治疗方案提供科学依据。CYP450 酶系统作为人体内重要的药物代谢酶系统,在抗抑郁药代谢中发挥关键作用,CYP2C19 是 CYP450 家族重要成员,参与多种抗抑郁药代谢,其基因多态性可显著影响药物在体内的代谢速度与血药浓度,进而影响药物疗效与不良事件发生。近年来,全基因组关联研究已定位 200 余个与抑郁症易感性及药物反应相关的基因位点,CYP2C19、CYP2D6 等药物代谢基因研究较为成熟,临床验证检测准确率达 80%。2025 年精神病学药物基因组学检测专家共识明确推荐,对使用选择性 5 - 羟色胺再摄取抑制剂(SSRIs)的患者进行 CYP2C19 基因检测,以优化治疗方案。舍曲林作为常用 SSRI 类药物,因疗效确切、安全性高,广泛用于抑郁症治疗,尤其在青少年及老年抑郁症患者中应用普遍。但临床实践发现,舍曲林在不同患者中的治疗效果差异显著,部分患者疗效显著,部分患者疗效不佳或出现明显不良事件。研究表明,CYP2C19 基因多态性可能是导致这一差异的重要原因。CYP2C19 存在多种等位基因变异,根据代谢功能可分为快代谢、中间代谢、慢代谢等不同表型,不同代谢表型患者对舍曲林的代谢能力不同,导致药物体内暴露量差异,进而影响治疗效果与不良事件风险。
本研究对携带 CYP2C19 基因的患者进行分组研究,系统分析不同代谢表型患者经舍曲林治疗后各项指标的差异,旨在阐明 CYP2C19 基因多态性对舍曲林治疗效果的影响,为抑郁症个体化治疗提供新策略与新方法。本研究结果有望为改善抑郁症患者治疗效果、降低疾病社会影响提供积极价值。
研究方法
筛选 2022 年 1 月至 2024 年 12 月三年间随县人民医院收治的抑郁症患者病历。本研究主要目的为明确 CYP2C19 基因多态性对舍曲林治疗效果的影响。研究流程图(图 1)显示,初始筛选 212 例患者,应用排除标准后保留 207 例;数据分析阶段因病历数据缺失排除 5 例,最终 202 例纳入回顾性对比分析,根据等位基因差异分为三组:快代谢组(A 组,n=65)、中间代谢组(B 组,n=94)、慢代谢组(C 组,n=43)。本研究初始筛选 212 例患者,应用排除标准后纳入 207 例,其中 5 例数据缺失,最终分析 202 例,A、B、C 组分别为 65 例、94 例、43 例。纳入标准:(1) 符合《国际疾病分类第 11 版》抑郁症诊断标准;(2) 年龄 18~60 岁;(3) 病历记录完成至少 6 周舍曲林治疗;(4) 入院前 2 周内未使用抗抑郁药或抗精神病药,入院后接受抗抑郁治疗;(5) 具备 CYP2C19 基因型检测数据。排除标准:(1) 既往诊断为难治性抑郁症;(2) 合并严重躯体疾病:存在剧烈疼痛(VAS≥7 分)、呼吸困难(呼吸频率显著增快 > 30 次 / 分,伴三凹征或发绀)、大出血(如消化道大出血,短时间失血量超 1000mL,导致低血压休克)、昏迷等严重症状者;(3) 现存或既往有影响药物吸收、分布、排泄的疾病(如胃切除术);(4) 器质性疾病;(5) 孕妇、哺乳期女性及计划 2 个月内妊娠女性;(6) 合并其他精神疾病;(7) 研究药物过敏史或滥用史;(8) 存在自杀意念或行为;(9) 个人或家族癫痫史;(10) 智力障碍;(11) 近 2 个月内参与任何临床试验。
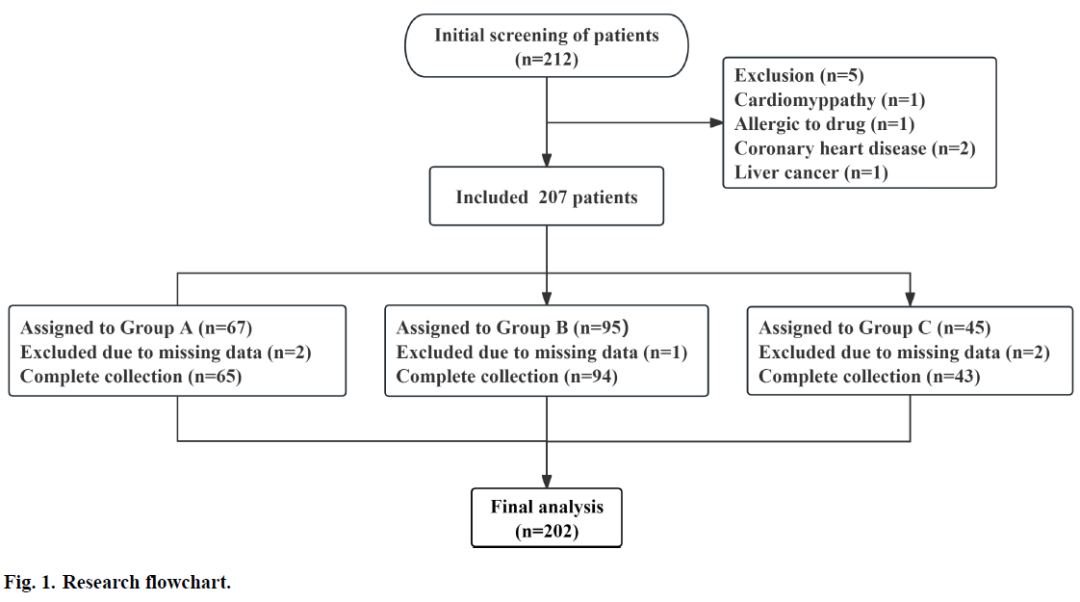
图1
采用抗凝管采集空腹外周静脉血,检测 CYP2C19 基因型。根据检测结果将患者分为三种代谢表型组:快代谢者:携带 CYP2C19 *1/*17 或*17/*17 基因型;中间代谢者:携带 CYP2C19 *1/*1、*1/*2、*1/*3、*2/*17、*3/*17 基因型;慢代谢者:携带 CYP2C19 *2/*2、*3/*3、*2/*3 基因型。最终 A 组(快代谢)65 例,B 组(中间代谢)94 例,C 组(慢代谢)43 例。
根据病历记录,所有患者初始给予盐酸舍曲林25mg / 日。A、B、C 组剂量范围分别为 75~150mg / 日、25~75mg / 日、25~50mg / 日,药物剂量依据临床常规治疗剂量,符合《中国抑郁障碍防治指南(2024 版)》剂量推荐框架。观察期 6 周,整个临床观察期内不联合使用其他抗抑郁药、抗精神病药、心理治疗或物理治疗。
汉密尔顿抑郁量表(HAMD)是临床评估抑郁症状的常用工具,17 项版本(HAMD-17)应用最广泛。HAMD-17 包含 17 项症状条目,各条目按症状严重程度分级,多数条目采用 0~4 分或 0~2 分评分,总分越高提示抑郁越严重。分级标准:总分 <7 分无抑郁症状;7~17 分轻度抑郁;18~24 分中度抑郁;>24 分重度抑郁。以治疗期间 HAMD 评分较基线首次下降≥20% 为起效时间判断标准,提示药物对患者产生初始疗效。应答定义为治疗 6 周后 HAMD 评分较基线下降≥50%,提示患者抑郁症状显著改善,符合该标准患者占总人数比例为应答率。缓解定义为治疗 6 周后 HAMD 评分≤7 分,提示患者抑郁症状基本消失,达到该状态患者占总人数比例为缓解率。临床总体印象 - 改善量表(CGI–I)是精神科临床研究常用标准化评估工具,包含临床总体印象 - 严重程度(CGI–S)与 CGI–I 两个核心维度,其中 CGI–I 聚焦治疗后患者病情较基线的改善程度,是评估疗效的关键主观指标。CGI–I 采用 7 级评分法,量化从 “明显恶化” 到 “明显改善”,评分越低提示改善程度越好。Morisky 用药依从性量表 - 8(MMAS-8)是评估患者用药依从性的常用工具,尤其适用于高血压、糖尿病、抑郁症等慢性疾病患者依从性评估。量表包含 8 个条目,均以 “是”“否” 作答,聚焦患者药物治疗期间的行为表现,全面反映依从性水平。所有条目得分相加,总分 0~8 分,得分越高提示用药依从性越好。
研究结果
患者基线数据比较:
收集并分析本回顾性队列患者基线数据,包括年龄、体重指数(BMI)、性别、受教育程度、就业状况、婚姻状况、饮酒史、吸烟史、抑郁病程、本次发作病程、首次住院次数、住院时长、抑郁严重程度,结果见表 1。三组数据交叉比较显示,上述基线指标差异均无统计学意义(均 p>0.05),提示三组患者具有高度可比性,可进行结局指标比较。
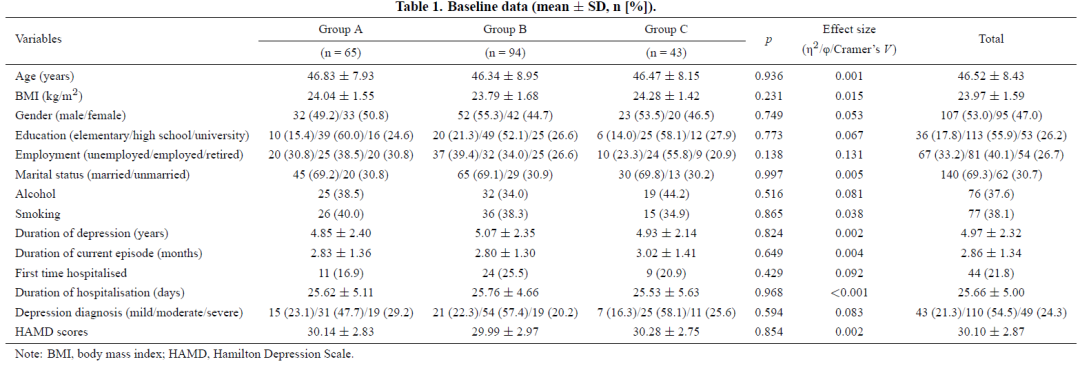
表1
患者 HAMD 评分比较:
三组 HAMD 评分比较结果见表 2。用药前三组 HAMD 评分无显著差异(p=0.854);用药后三组 HAMD 评分均显著下降(均 p<0.05)。用药后组间比较显示,B 组、C 组 HAMD 评分下降幅度显著大于 A 组(B 组 vs A 组 p=0.038;C 组 vs A 组 p<0.001),C 组下降幅度显著大于 B 组(p=0.032)。提示用药后三组患者抑郁状态均改善,其中 C 组改善最佳,B 组次之,A 组最差。
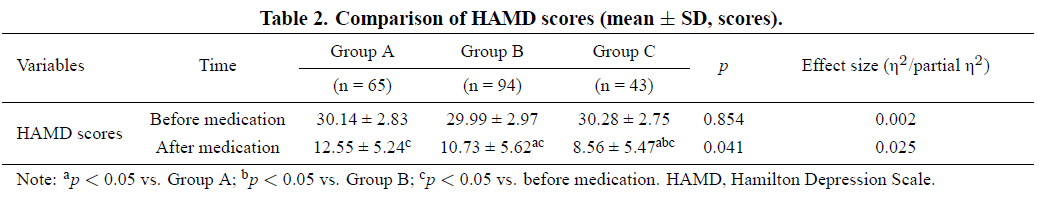
表2
药物起效时间比较:
三组舍曲林治疗 6 周后起效时间见表 3。A 组起效时间 12.83±3.36 天,B 组 11.72±3.32 天,C 组 10.05±3.52 天。三组起效时间比较显示,B 组、C 组起效时间短于 A 组(B 组 vs A 组 p=0.025;C 组 vs A 组 p<0.001),C 组起效时间短于 B 组(p=0.008)。提示不同 CYP2C19 代谢表型患者舍曲林起效时间存在差异,C 组起效最快,A 组最慢,B 组介于两者之间。
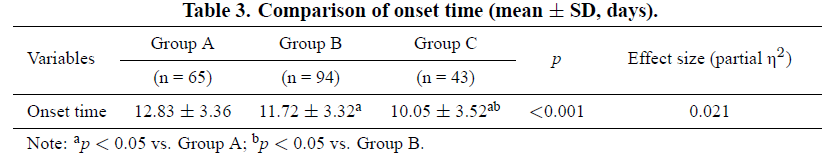
表3
患者应答率与缓解率比较:
三组药物应答率与缓解率汇总比较结果见表 4。A 组应答率 38.5%、缓解率 30.8%;B 组应答率 55.3%、缓解率 42.6%;C 组应答率 74.4%、缓解率 62.8%。B 组应答率、缓解率高于 A 组(应答率 p=0.037;缓解率 p=0.034);三组中 C 组应答率(C 组 vs A 组 p<0.001;C 组 vs B 组 p=0.033)与缓解率(C 组 vs A 组 p<0.001;C 组 vs B 组 p=0.028)最高。提示舍曲林治疗下,三种 CYP2C19 代谢表型中,C 组应答与缓解最快,A 组最慢,B 组介于两者之间。
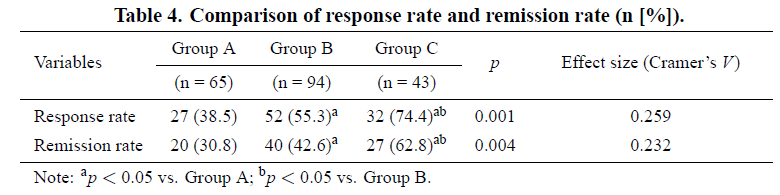
表4
患者 CGI–I 评分比较:
CGI 量表总体改善维度评分结果见表 5。用药前三组 CGI–I 评分无差异(p=0.831);用药后三组均显著改善(均 p<0.05)。三组中 C 组 CGI–I 评分最低(C 组 vs A 组 p<0.001;C 组 vs B 组 p=0.021),B 组 CGI–I 评分仅低于 A 组(p=0.036)。提示不同 CYP2C19 代谢表型舍曲林疗效比较中,C 组疗效改善最显著,A 组较 B 组、C 组改善更差。
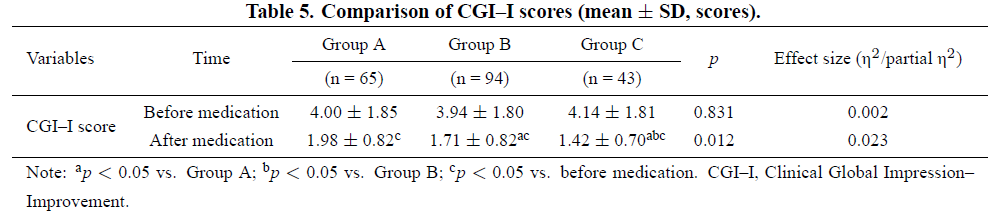
表5
患者神经递质与神经营养因子比较:
患者病历中神经递质因子 5-HT、GABA 及神经营养因子 BDNF 数据统计分析结果见表 6。用药前三组 5-HT、GABA、BDNF 浓度无显著差异(5-HT p=0.106;GABA p=0.197;BDNF p=0.677);用药后三组三项指标浓度均显著升高(均 p<0.05)。用药后组间比较显示,与 A 组相比,B 组、C 组 5-HT(B 组 vs A 组 p=0.022;C 组 vs A 组 p<0.001)、GABA(B 组 vs A 组 p=0.015;C 组 vs A 组 p<0.001)、BDNF(B 组 vs A 组 p=0.030;C 组 vs A 组 p<0.001)浓度显著更高,且 C 组三项因子浓度升高幅度显著大于 B 组(5-HT p=0.026;GABA p=0.022;BDNF p=0.005)。提示舍曲林可改善患者神经元功能,进而缓解抑郁情绪;三种 CYP2C19 代谢表型中,慢代谢表型舍曲林治疗效果最佳,快代谢表型疗效较中、慢代谢表型更差。
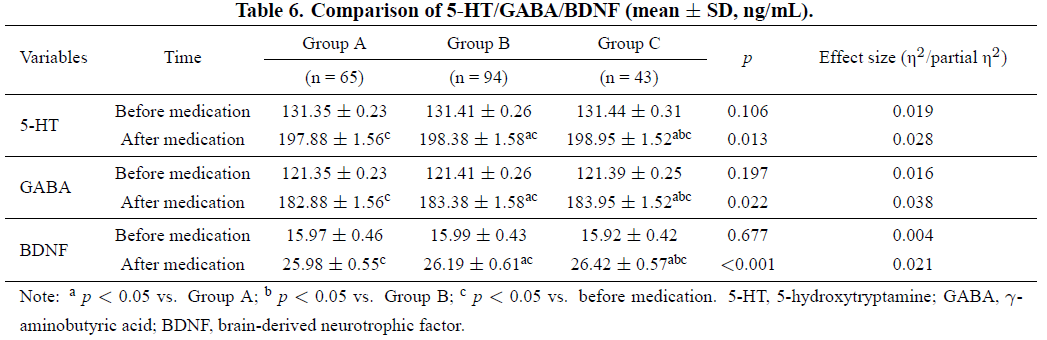
表6
药物不良事件发生率比较:
三组患者不良事件发生情况见表 7。A 组胃肠道反应 3 例、神经系统反应 2 例、性功能障碍 2 例,不良事件总例数 7 例,发生率 10.8%;B 组胃肠道反应 11 例、神经系统反应 8 例、性功能障碍 4 例,总例数 23 例,发生率 24.5%;C 组胃肠道反应 9 例、神经系统反应 6 例、性功能障碍 3 例,总例数 18 例,发生率 41.9%。三组不良事件发生比较显示,A 组发生率最低,C 组最高(A 组 vs B 组 p=0.030;A 组 vs C 组 p<0.001;B 组 vs C 组 p=0.039)。此外,B 组胃肠道不良事件发生率最高(p=0.033),三组神经系统反应、性功能障碍差异无统计学意义(p=0.188,p=0.625)。提示不同 CYP2C19 代谢表型患者接受舍曲林治疗时,A 组不良事件发生率最低,C 组最高,B 组介于两者之间。
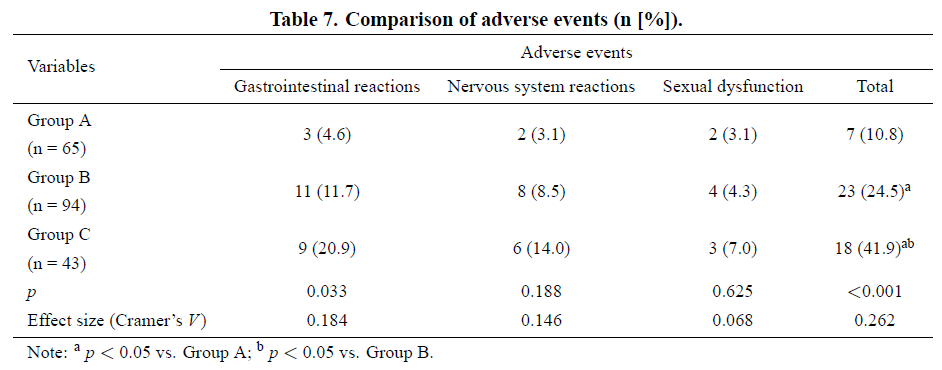
表7
患者 MMAS-8 评分比较:
采用 MMAS-8 评分评估治疗期间用药依从性,结果见表 8。用药前三组依从性评分无显著差异(p=0.469);用药后三组依从性评分均显著升高(均 p<0.05),提示舍曲林治疗缓解患者抑郁情绪,提升用药依从性。此外,B 组 MMAS-8 评分升高幅度显著大于 A 组、C 组(B 组 vs A 组 p=0.011;B 组 vs C 组 p=0.032),A 组与 C 组 MMAS-8 评分无显著差异(p=0.929)。三组比较结果提示,舍曲林可改善患者抑郁情绪、提高用药依从性,其中 B 组依从性改善最显著,A 组与 C 组依从性改善无显著差异。
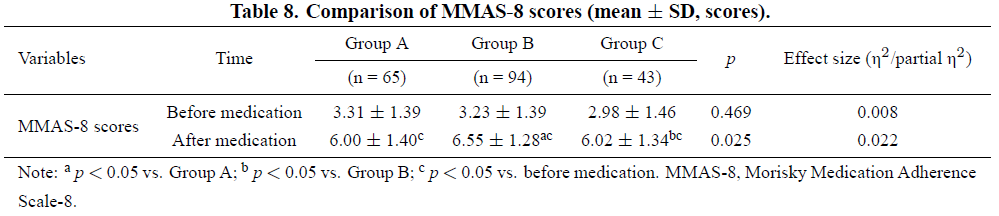
表8
讨 论
抑郁症作为全球高发精神障碍,其治疗长期以来是精神病学领域的重点与难点。当前治疗方案多依赖经验用药,但个体基因差异显著,导致部分患者对初始药物无反应,不仅延误治疗时机,还增加患者痛苦与医疗负担。在此背景下,探索精准治疗策略成为突破抑郁症治疗瓶颈的关键。CYP450 酶系统作为肝脏主要药物代谢酶系统,对药物体内转化至关重要,其中 CYP2C19 是 CYP450 家族关键成员,已证实其基因多态性与多种药物代谢效率密切相关。CYP2C19 基因位于 10 号染色体 q24.2 区,目前已发现多种等位基因变异。不同基因型酶活性差异显著,可进一步将人群分为快代谢、中代谢、慢代谢者。深入研究 CYP2C19 代谢表型对舍曲林治疗效果的影响,为抑郁症个体化治疗提供重要理论依据与实践参考。
严等人在中国汉族人群中开展的大规模研究发现,CYP2C19 慢代谢、中代谢组舍曲林血药浓度较正常代谢组升高,且舍曲林抗抑郁转换率较正常代谢组显著提高,该研究结果与本研究一致。本研究中,与 A 组、B 组相比,C 组 HAMD 评分下降更显著,应答率与缓解率更高,药物起效时间更短,CGI–I 评分改善更显著,这与 CYP2C19 不同等位基因相关。快代谢表型患者携带 CYP2C19 基因野生型等位基因,酶活性高,药物代谢分解快,服用舍曲林后药物在体内快速代谢,难以维持有效治疗血药浓度,进而影响治疗效果。相反,慢代谢表型患者多携带 CYP2C19 基因功能缺失等位基因,酶活性显著降低,药物体内代谢缓慢,血药浓度易升高并维持高水平;中代谢表型患者 CYP2C19 酶活性介于快、慢代谢组之间,药物代谢速度中等。
5-HT 是重要中枢神经递质,在调节情绪、睡眠、食欲等生理过程中发挥关键作用。大量证据表明,抑郁症患者 5-HT 功能降低,突触间隙 5-HT 浓度下降,这一现象被认为是抑郁症发病的关键机制。舍曲林作为 SSRI 类药物,主要通过抑制神经元对 5-HT 的再摄取,提高突触间隙 5-HT 浓度,发挥抗抑郁作用。本研究结果显示,舍曲林治疗后 C 组患者 5-HT 上调更显著,这与患者体内高舍曲林血药浓度密切相关。因 CYP2C19 酶活性低,舍曲林体内代谢缓慢,可持续抑制 5-HT 再摄取,使突触间隙 5-HT 水平显著升高,有效缓解抑郁症状。相反,A 组患者舍曲林代谢快、血药浓度低,对 5-HT 再摄取抑制作用弱,5-HT 上调程度相对较低,这是该组疗效不佳的重要原因。GABA 是中枢神经系统主要抑制性神经递质,具有镇静、抗焦虑、抗惊厥等作用。研究表明,抑郁症患者脑内 GABA 水平降低、GABA 介导的神经传递受损,可能与抑郁症状发生密切相关。舍曲林除作用于 5-HT 系统外,还可通过增加 GABA 释放或减少其代谢调节 GABA 神经元功能,提高突触间隙 GABA 浓度,发挥抗抑郁作用。本研究中,C 组 GABA 上调较其他组更显著,与其高舍曲林血药浓度相关。高浓度舍曲林可有效激活 GABA 神经元,促进 GABA 合成与释放,同时抑制 GABA 降解,使突触间隙 GABA 浓度显著升高,增强抑制性神经传递,缓解患者焦虑紧张情绪,改善抑郁症状。A 组因舍曲林血药浓度低,对 GABA 系统调节作用弱,GABA 上调程度低。BDNF 是公认的关键神经营养因子,对神经元生长、分化、存活与修复至关重要,是维持神经系统正常功能与可塑性的必需物质。BDNF 可促进神经元再生与突触形成,改善神经可塑性,进而帮助缓解抑郁症状、预防疾病复发。本研究结果显示,C 组患者 BDNF 上调较其他组更显著,因 C 组高舍曲林血药浓度可有效刺激 BDNF 合成与释放。舍曲林可能通过激活丝裂原活化蛋白激酶等相关信号通路,促进 BDNF 基因表达,提高 BDNF 水平。BDNF 水平显著升高可促进海马等脑区神经元再生与突触重塑,改善神经可塑性,增强抗抑郁效果,使 C 组患者临床结局更优。
药物不良事件是影响患者治疗依从性与疗效的重要因素。本研究中,C 组药物不良事件发生率最高,这与慢代谢表型患者舍曲林血药浓度高密切相关。血药浓度升高可能导致药物在体内蓄积,进而升高恶心、呕吐、头晕、失眠等药物不良事件风险。这些不良事件不仅导致患者躯体不适,还可能降低治疗信心,导致治疗依从性下降。相反,A 组药物不良事件发生率最低,因快代谢表型患者药物代谢快、血药浓度低,减少了不良事件发生。此外,B 组 MMAS-8 评分升高较其他组更显著,提示中代谢表型患者治疗依从性改善更明显,因 B 组治疗期间血药浓度维持在相对稳定的治疗范围,不良事件发生率低,患者耐受性好,能坚持用药方案,保持良好治疗依从性。慢代谢组抑郁症患者存在临床矛盾:疗效最佳,但不良事件发生率最高、用药依从性最差。其核心机制为基因型导致舍曲林代谢酶活性缺失或显著降低,药物体内暴露量增加、消除半衰期延长。高药物浓度虽能充分抑制 5-HT 再摄取、上调 GABA 与 BDNF 水平,实现更佳疗效,但舍曲林不良事件呈剂量依赖性,高药物蓄积直接升高胃肠道反应、头晕等不良事件风险。持续不良事件体验降低患者治疗信心,引发自行减量、漏服等行为,最终导致用药依从性下降。临床医生可通过基因型指导个体化剂量调整、不良事件分层干预、全程用药管理,平衡疗效与安全性,解决上述矛盾。
本研究未直接检测患者血浆舍曲林浓度,当前对疗效差异机制的解释仍基于 CYP2C19 基因功能与药代动力学已知理论的间接推断,缺乏血浆药物浓度直接数据支持。这一结果被认为与 CYP2C19 基因独特的等位基因特征相关。推断主要依据:快代谢者携带 CYP2C19 基因野生型等位基因,编码高活性代谢酶,可快速催化舍曲林生物转化。根据药代动力学基本原理,此类患者服用标准剂量舍曲林后,药物在体内快速代谢清除,血浆药物浓度难以维持在持续有效的治疗窗内,这可能是疗效不佳的关键原因。相反,慢代谢者多携带 CYP2C19 基因功能缺失等位基因,此类等位基因突变导致代谢酶活性显著降低甚至完全失活。根据药物代谢理论逻辑,酶活性下降直接减慢舍曲林体内代谢速度,药物可达到高血浆浓度并维持较长时间,这种相对稳定的高血浆药物浓度状态,可能是慢代谢组疗效好、起效快的核心机制。中代谢者通常为 CYP2C19 基因杂合基因型,结合野生型与功能缺失等位基因,代谢酶活性恰好介于快、慢代谢者之间,因此药物代谢速度与推断血浆药物浓度水平也介于两组之间,这种中间状态与该组患者观察到的中等疗效指标水平逻辑相符。未来研究应进一步纳入血浆药物浓度检测指标,形成完整数据链,为不同代谢表型患者疗效差异提供直接确凿的机制证据,同时为基于代谢表型制定精准舍曲林剂量方案提供依据。
尽管本研究得出相关结果,但仍存在以下局限性:即使进行协方差分析,仍存在混杂因素;回顾性设计、单中心小样本、未设置 CYP2C19 *1/*1 组,降低结果可靠性与普遍性,影响代谢表型描述准确性;仅探讨 CYP2C19 与舍曲林的关联,观察期 6 周不足以评估长期疗效。未来研究应采用大样本多中心前瞻性设计,探索多基因 - 抗抑郁药交互作用构建预测模型,延长观察期评估长期结局,结合临床 / 环境因素制定个体化方案。
CYP2C19 代谢表型对携带该基因的抑郁症患者舍曲林治疗疗效具有显著影响。应重视基因检测在抑郁症个体化治疗中的应用,依据患者 CYP2C19 代谢基因型制定合理治疗方案,提高疗效、减少不良事件、降低医疗负担。同时,未来需开展更深入研究,持续完善个体化治疗策略,为抑郁症患者提供更优质高效的医疗服务。
“抑郁症个性化用药基因检测”项目,覆盖上文提到的CYP2C19*2(c.681G>A)、CYP2C19*3(c.636G>A)和CYP2C19*17(c.-806C>T),可指导舍曲林等个体化用药,检测样本需要外周血(EDTA管,2ml)或口腔拭子(≥2支),报告周期为4-5个自然日。

参考文献:
Li, Shichao et al. “Exploring the Effect of Genetic Testing on Personalised Treatment Plans for Depression.” Actas espanolas de psiquiatria vol. 54,1 (2026): 28-41. doi:10.62641/aep.v54i1.2098


