华中科技大学/武汉纺织大学合作,最新Nature Microbiology:肠道细菌竟能“制造药物”,逆转儿童脓毒症
时间:2026-05-05 17:05:10 热度:37.1℃ 作者:网络
在全球范围内,脓毒症依然是儿童死亡的重要原因之一,尤其是在5岁以下人群中占据极高比例。尽管抗生素和支持治疗已成为临床常规手段,但其疗效往往有限,难以解决肠道菌群失衡与免疫紊乱等根本问题。与此同时,胆汁酸作为调控肠道屏障、炎症反应和免疫功能的重要分子,其在脓毒症中的作用逐渐受到关注,但具体机制仍不清晰。如何在复杂的“肠道菌群—胆汁酸”网络中找到关键调控因子,成为当前亟待突破的科学难题。
今日,华中科技大学宁康教授、刘欣教授联合武汉纺织大学朱泉霏教授通过整合代谢组学与宏基因组学数据,首次系统揭示了一种由肠道共生菌产生的硫酸化胆汁酸——DCA-3S,在儿童脓毒症中的关键作用。研究不仅发现该分子可作为高准确度的诊断标志物,还通过动物和类器官实验证实其能够显著改善肠道屏障、抑制炎症反应,从而缓解脓毒症进程。这一发现颠覆了“胆汁酸硫酸化仅发生于肝脏”的传统认知,并为脓毒症的早期诊断与干预提供了全新思路。相关成果以“Sulfated bile acid produced by a human gut commensal alleviates paediatric sepsis in mice”为题发表在《Nature Microbiology》上,Xiang Liu, Haobo Zhang, Yan-Zhen Wang, Xinyu Tu, Jiejie Wen为共同第一作者。

从胆汁酸谱入手:锁定关键分子
研究首先对儿童脓毒症患者与健康对照的胆汁酸进行系统分析。在整体水平上,主成分分析清晰地将两组人群区分开来(图1a),提示胆汁酸代谢在疾病状态下发生显著改变。进一步差异分析发现,多种胆汁酸水平显著变化,其中一类“硫酸化胆汁酸”尤为突出(图1b)。在众多候选分子中,DCA-3S表现最为亮眼。通过机器学习模型筛选,该分子成为最重要的预测因子(图1c、1d),其诊断准确性在独立验证队列中依然保持较高水平。同时,相关性分析显示,DCA-3S水平与CRP、IL-6等炎症指标密切相关(图1e),暗示其不仅是“标志物”,更可能参与疾病调控过程。
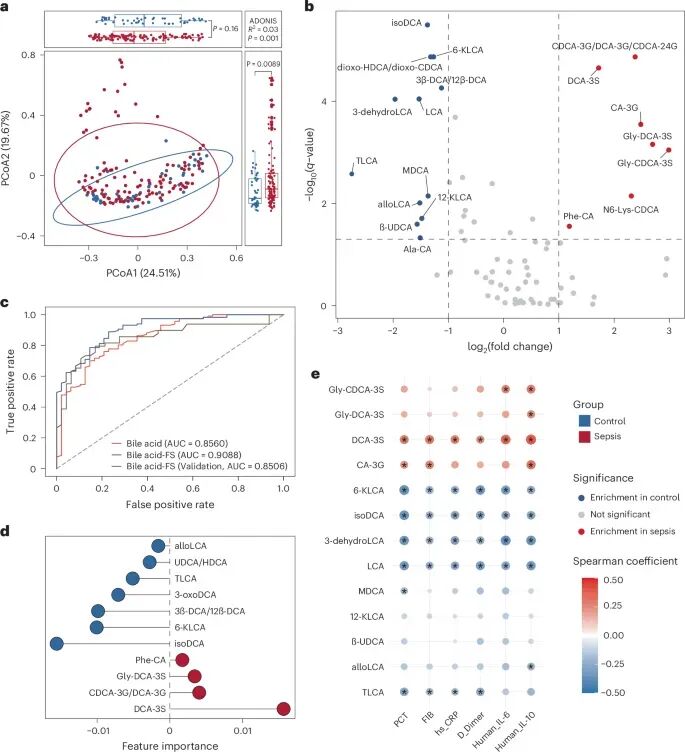
图1:胆汁酸谱分析发现DCA-3S在脓毒症中显著升高,并具有高诊断价值。
肠道菌群失衡:幕后推手浮出水面
既然胆汁酸发生显著变化,那么谁在“操控”这一过程?研究将目光转向肠道菌群。结果显示,脓毒症患儿的菌群多样性显著下降(图2a),群落结构也发生明显分离(图2b),提示肠道生态系统整体紊乱。在具体菌群层面,Enterococcus属显著富集,而多种有益菌则明显减少(图2c)。进一步分析发现,在物种层面,乳糖肠球菌在脓毒症患者中显著升高(图2d)。基于菌群构建的诊断模型同样具有较高准确性(图2e–2g),而将菌群与胆汁酸信息结合后,诊断能力进一步提升,提示两者之间存在紧密联系。
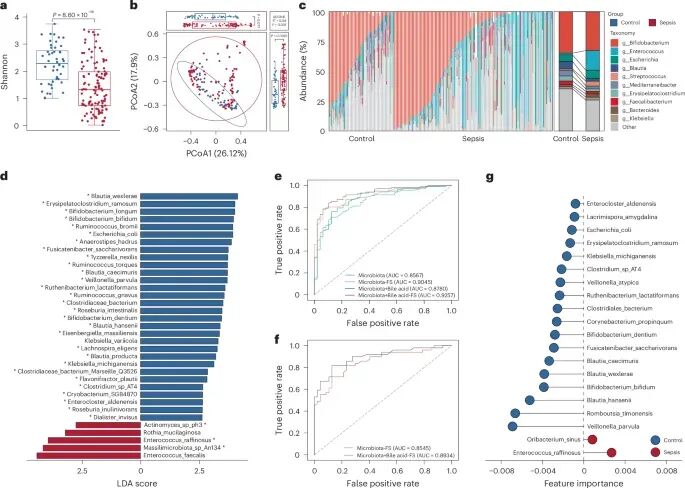
图2:脓毒症患儿肠道菌群严重失衡,Enterococcus显著富集。
关键桥梁:DCA-3S连接菌群与疾病
接下来,研究深入探讨菌群与胆汁酸之间的关系。分析显示,菌群多样性与胆汁酸丰富度呈显著正相关(图3a),说明两者在系统层面高度耦合。更重要的是,乳糖肠球菌的丰度与DCA-3S水平呈显著正相关(图3b),并通过网络分析进一步揭示其与炎症指标之间的关联(图3c)。中介分析则给出了关键证据:DCA-3S在菌群与脓毒症之间起到了“桥梁”作用(图3d)。换句话说,这种胆汁酸是菌群影响疾病的重要媒介。
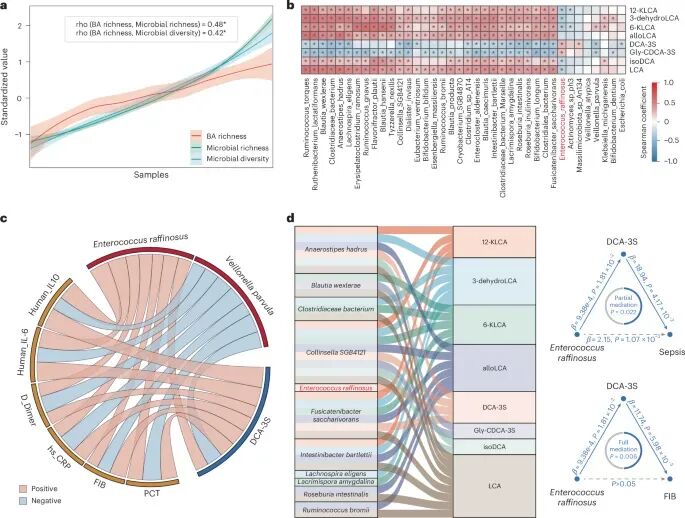
图3:DCA-3S在菌群与脓毒症之间发挥关键中介作用。
谁在生产DCA-3S?答案出乎意料
传统观点认为,胆汁酸的硫酸化主要发生在肝脏。但实验结果却完全颠覆了这一认知。研究通过体外培养与同位素示踪发现,多种肠道细菌可以将DCA转化为DCA-3S(图4a、4b)。在27种分离菌株中,有15种具备该能力,其中乳糖肠球菌的效率最高(图4c、4d)。时间序列实验显示,该分子在培养过程中持续积累(图4e),证明其确为细菌主动合成产物。更关键的是体内实验结果:DCA-3S主要存在于肠道,而在肝脏几乎检测不到(图4f–4h)。即便人为提高肝脏底物浓度,其生成量仍极低。这一发现明确指出:肠道微生物才是DCA-3S的主要来源。
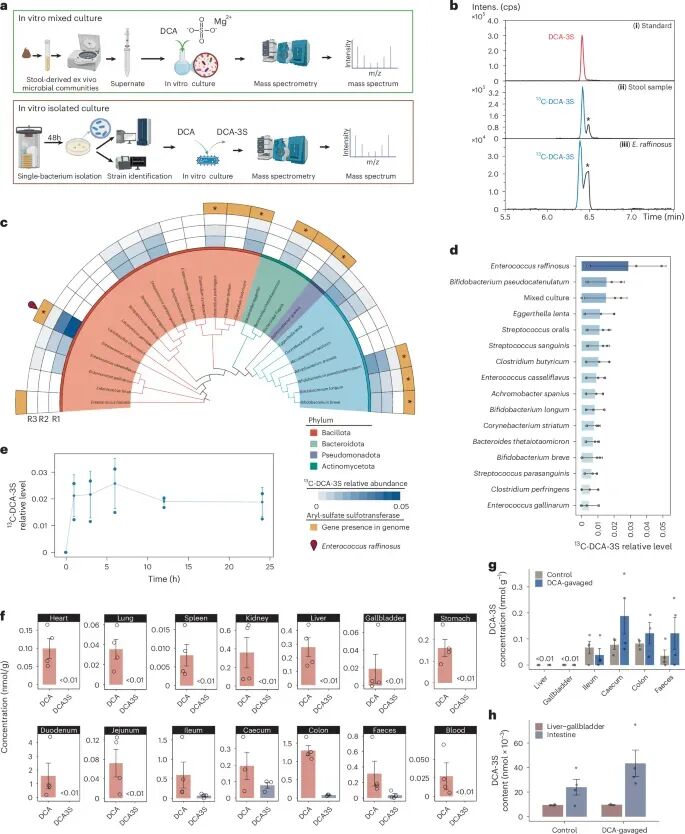
图4:肠道细菌,尤其是E. raffinosus,是DCA-3S的主要生产者。
不只是标志物,更是“治疗因子”
既然DCA-3S与疾病密切相关,它是否能直接干预脓毒症?研究在小鼠模型中给出了肯定答案。在治疗实验中,补充DCA-3S显著降低炎症指标CRP和PCT(图5e、5f),并改善肠道结构损伤(图5b–5d)。同时,菌群多样性得到部分恢复(图5g、5h),说明其对微生态具有调节作用。更令人振奋的是预防实验:提前给予DCA-3S可显著降低脓毒症严重程度(图5m、5n),并减少炎症细胞浸润(图5j–5l)。这意味着,该分子不仅能“治病”,还可能用于“防病”。
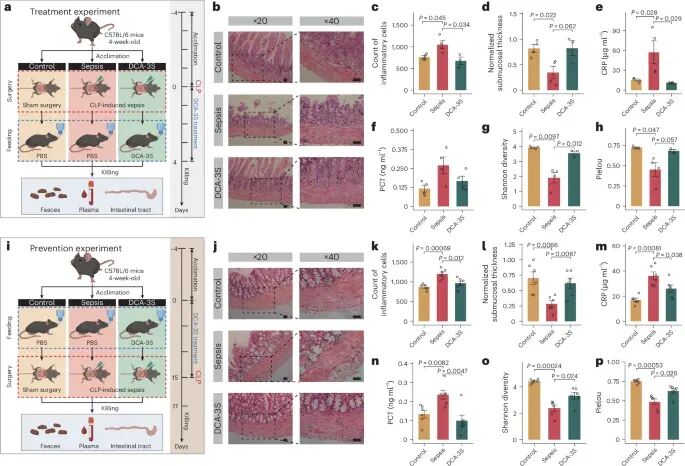
图5:补充DCA-3S可显著缓解并预防小鼠脓毒症。
作用机制揭秘:修复肠道屏障
在类器官模型中,研究进一步解析了DCA-3S的作用机制。结果显示,该分子显著降低肠道通透性(图6b),有效阻止“肠漏”现象。分子层面上,DCA-3S增强紧密连接蛋白CLDN4表达(图6c、6d),减少细胞凋亡(图6e),并促进上皮细胞增殖与分化(图6f–6h)。在健康模型中也观察到类似趋势(图6i–6n),说明其具有普遍的保护作用。进一步机制研究表明,DCA-3S通过激活FXR信号通路发挥作用,从而调控细胞更新与炎症反应。
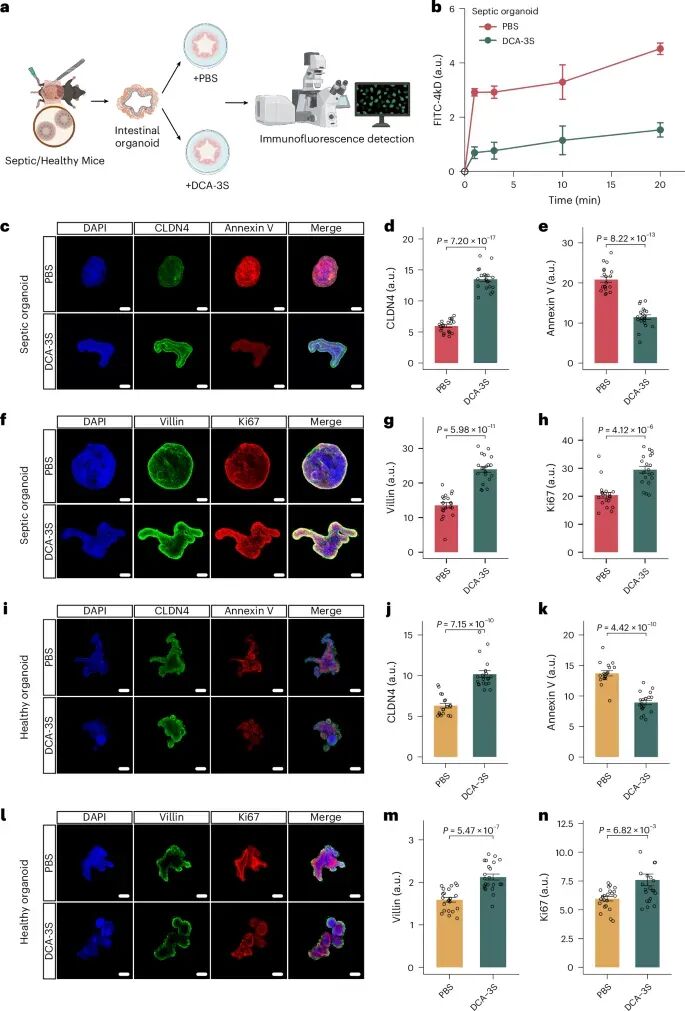
图6:DCA-3S通过增强肠道屏障功能发挥保护作用。
小结
这项研究从“肠道菌群—胆汁酸—宿主”的复杂网络中,精准锁定了一个关键分子DCA-3S,不仅揭示了其来源与机制,还验证了其治疗潜力。更重要的是,它打破了胆汁酸代谢的经典认知,为理解微生物与宿主互作提供了全新视角。未来,DCA-3S有望发展为脓毒症的早期诊断标志物及干预手段。当然,其在人群中的安全性与有效性仍需进一步临床验证。但可以预见,这一发现将推动脓毒症治疗从“对症支持”迈向“精准调控”的新阶段。
原文链接:
https://www.nature.com/articles/s41564-026-02351-1


