BLOOD:PP2A是在急性髓系白血病中通过 c-Myc/p21 轴决定细胞命运的可治疗靶向驱动因素
时间:2021-11-28 08:03:27 热度:37.1℃ 作者:网络
急性髓系白血病(AML)是一种进展迅速的恶性肿瘤,其特征是造血功能成熟异常,细胞增殖不受控制,患者整体预后较差。细胞分化失调是急性白血病发生的标志,磷酸酶在癌症中被广泛抑制,但传统上与分化无关。
在此,国外一样研究团队发现蛋白磷酸酶 2A (PP2A) 的沉默直接有助于急性髓系白血病 (AML) 的分化阻滞。基因表达和大规模细胞计数分析表明,PP2A 激活调节细胞周期和转录调节因子,这些调节因子对终末髓系分化进行编程。
细胞系取自美国型培养集输和德国微生物细胞培养集输,从患者的单采或骨髓(BM)抽吸物中获得原发性AML细胞,使用10%的胎牛血清培养(0.5-1x106细胞/ml);谷酰胺约2毫米;青霉素(100 116 U/ml);链霉素(100 g/ml) ,并补充IL3, GM-CSF和SCF。同样培养AML细胞系,不添加补剂。
通过annexin-V-FITC和碘化丙啶检测细胞凋亡。在共培养实验中用annexin-V PE和7-AAD检测细胞存活率。在流式细胞实验中染色结合表面标记物对活细胞进行门控。对小鼠骨髓中AML细胞谱系进行检测,采用抗体组合(CD3、Gr1、CD11b、B220 和ter119)并进行相关的同型对照。进行分析。
使用与遗传方法并行的新型药理剂 OSU-2S,研究团队发现PP2A驱动的AML成熟依赖于c-Myc下调,这意味着恶性造血中一个关键的决定点。c-Myc在正常造血过程中受到严格调控和未能关闭Myc会阻碍小鼠的终末髓系分化,并导致AML。
图1:PP2A介导OSU-2S反应的细胞死亡

图2:PP2A介导对OSU-2S的基因表达变化
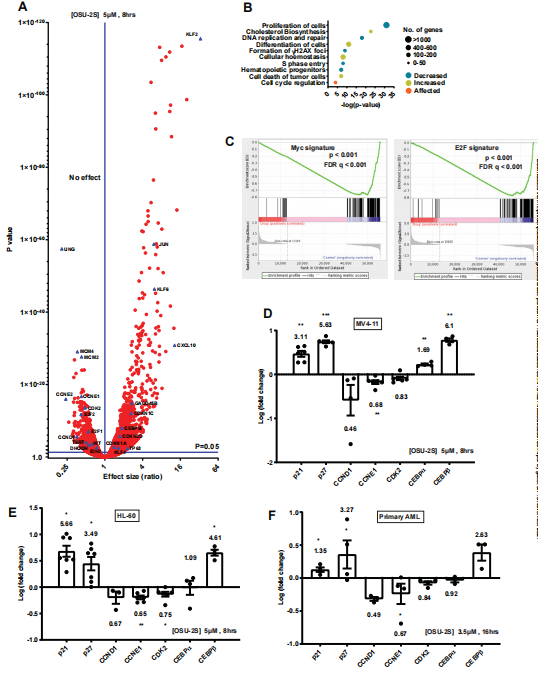
他们还发现PP2A激活逆转c-Myc介导的成熟阻断促进AML的终末分化。考虑到c-Myc在90%的AML中过表达,并在各种驱动突变的下游被激活,PP2A介导的Myc降解可以诱导不同AML亚群的分化。
与此相一致的是,OSU-2S在原发性AML中显示出了强大的活性,具有不同的突变/细胞遗传学特征。Myc介导的分化阻滞和去分化在多种其他癌症的发病机制中也很重要,包括乳腺癌伯基特淋巴瘤77和胰腺肿瘤。尽管Myc在癌症中存在广泛的失调,但其靶向仍然具有挑战性。因此,OSU-2S介导的PP2A介导的Myc控制具有潜在的治疗动力。
图3:PP2A介导对OSU-2S反应的细胞周期阻滞
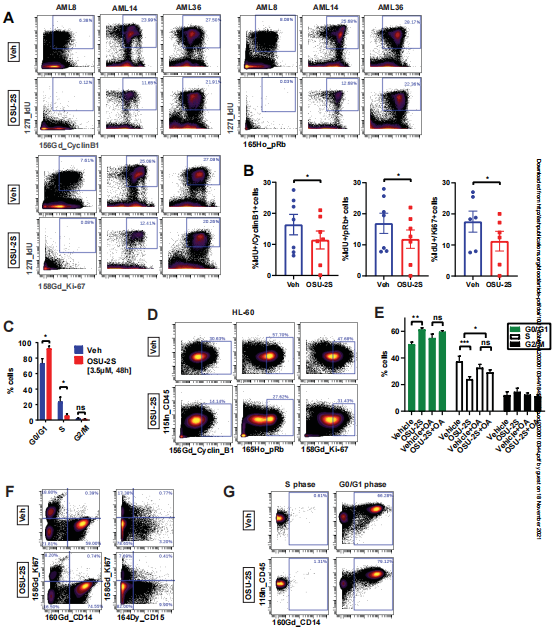
图4:在Tet2-/-Flt3ITD突变的小鼠AML模型中,OSU-2S诱导成熟并延长存活期。
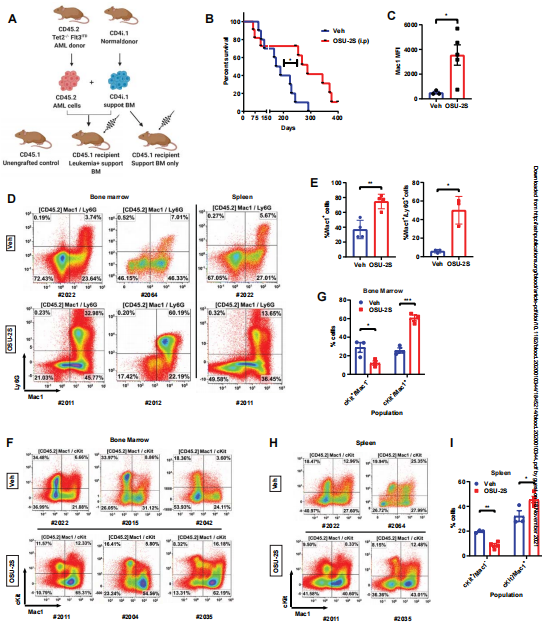
最后,他们证明 PP2A 激活减少白血病起始干细胞,增加白血病原始细胞成熟,并提高体内鼠 Tet2-/-Flt3ITD/WT 和人 AML 模型的总体存活率。
图5:PP2A的激活降低了体内和体外的干性。
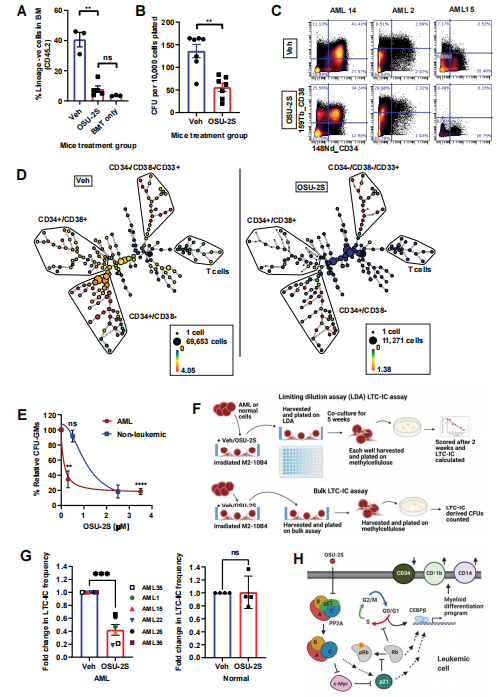
总而言之,他们的研究结果将 PP2A/c-Myc/p21 轴确定为 AML 分化/增殖转换的关键调节因子,可以在具有失调成熟命运的恶性肿瘤中进行治疗。研究确定了磷酸酶在癌细胞命运中的肿瘤抑制作用,并为AML和其他磷酸酶活性受抑制的恶性肿瘤的靶向治疗提供了一个框架。
原始出处:
Goswami S,Mani R,Nunes J,et al.PP2A is a therapeutically targetable driver of cell fate decisions via a c-Myc/p21 axis in Acute Myeloid Leukemia.[J].Blood,1970,:.


