Front Oncol:安罗替尼(Anlotinib)治疗中国复发或转移性宫颈癌患者中的有效性和安全性
时间:2021-11-03 19:01:35 热度:37.1℃ 作者:网络
宫颈癌(CC)是最常见的妇科癌症之一,在全球女性发病率和死亡率中排名第四。二线或以上治疗的应答率相对较低,为15% - 30%,复发或转移性CC的应答持续时间较短。VEGF抑制剂贝伐珠单抗(Bevacizumab)于2014年获美国食品和药物管理局批准,联合化疗用于复发或晚期CC患者。安罗替尼(Anlotinib)是一种新型口服多靶点酪氨酸激酶抑制剂(TKI),靶向VEGFR、血小板衍生生长因子受体(PDGFR)、成纤维细胞生长因子受体(FGFR)、c-Kit等靶点。一项针对晚期非小细胞肺癌的III期试验证实了安罗替尼的有效性和安全性。然而,安罗替尼尚未在复发或转移性晚期CC患者中进行评估。因此,复旦大学团队开展了一项II期研究,以评估安罗替尼在复发或难治性CC患者中的有效性和安全性。相关结果发表在Frontiers in Oncology杂志上。

研究纳入经组织学证实复发或转移的晚期CC患者。患者每日早餐前口服安罗替尼12 mg,服用2周,休息1周(每3周(21天)为一个周期)。安罗替尼口服直到疾病进展、患者自行退出、不耐受毒性或死亡。根据实体肿瘤疗效评价标准,主要终点为客观缓解率(ORR),次要终点包括疾病控制率(DCR)、无进展生存期(PFS)、总生存期(OS)和安全性。
2018年9月至2019年11月,共筛查46例患者,其中41例复发性晚期CC患者入选本研究。中位年龄53岁(范围:42 - 64岁)。组织学结果显示,82.9%(34/41)患者为鳞状细胞癌,14.6%(6/41)为腺癌,2.4%(1/41)为其他类型。40例(97.6%;40/41)的ECOG PS评分为0,仅有1例患者(2.4%;1/41)患者ECOG PS评分为1。初诊FIGO分期中,I期4.9% (2/41),II期61.0% (25/41),III期19.5% (8/41),IV期14.6%(6/41)。所有患者既往至少接受过两种治疗。26例(63.4%;26/41)曾接受过两次以上的治疗。
在16个月的随访期间,10例(24.4%)患者确认对治疗有应答,其中6例(14.6%)患者持续反应。缓解时间发生在2.3个月。安罗替尼治疗的患者中位PFS为3.2个月(95% CI: 0.4 - 5.9),中位OS为9.9个月(95% CI: 5.7-11.8)。
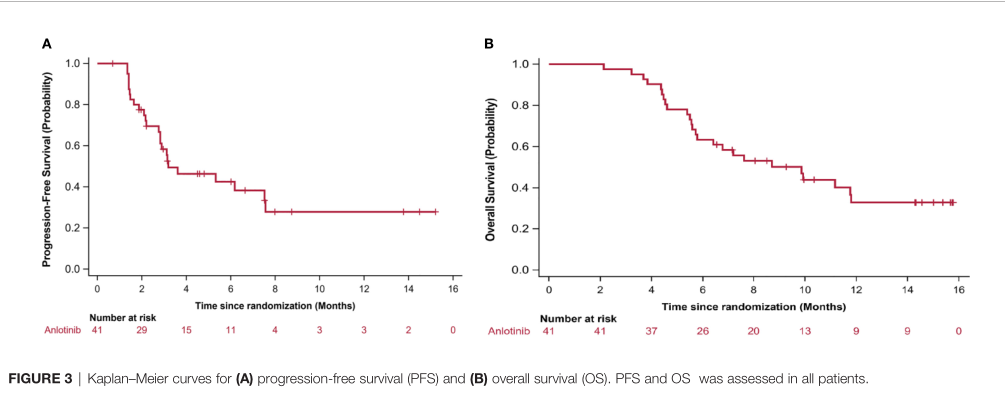
PFS和OS
对40例(40/41)患者进行治疗反应评估。无患者达到CR, 10例(24.4%)患者达到PR。ORR为24.4% (95% CI: 12.4-40.3)。SD有14例(34.2%),PD 16例(39.0%)。DCR为58.5% (95% CI: 42.1-73.7)。

疗效评估
对临床病理特征分层的ORR亚组分析显示,所有亚组中均有肿瘤的退缩,各亚组ORR与总体一致。

亚组ORR分析
所有患者都经历了AEs。大多数AEs为1级或2级。最常见的不良事件是贫血(29.3%)、手足综合征(26.8%)、淋巴细胞减少(24.4%)、尿白细胞阳性(22%)、疲劳(19.5%)和血尿(17.1%)。高级AEs(3级)包括尿白细胞阳性(9.8%)、血尿(4.9%)和高血压(2.4%)。没有患者有4级AEs。没有发生与治疗有关的死亡。

不良事件
综上,研究表明,这是第一个评估安罗替尼在中国复发或转移性宫颈癌患者中的有效性和安全性的研究。安罗替尼在这些患者中产生了持久的临床反应,安全性可控。
原始出处:
Zhu J, Song C, Zheng Z, Xia L, Chen Y, Ke G and Wu X (2021) Anlotinib in Chinese Patients With Recurrent Advanced Cervical Cancer: A Prospective Single-Arm, Open-Label Phase II Trial. Front. Oncol. 11:720343. doi: 10.3389/fonc.2021.720343


