ESMO Open:在抗肿瘤治疗的癌症患者中,BNT162b2冠状病毒2019信使RNA疫苗接种后体液免疫应答降低
时间:2021-10-11 11:02:08 热度:37.1℃ 作者:网络

背景:癌症患者患严重2019冠状病毒病(COVID-19)的风险更高。然而,COVID-19疫苗对正在接受治疗的癌症患者的安全性和有效性尚不清楚。
患者和方法:在这项介入前瞻性多队列研究中,对接受化疗、免疫治疗、靶向或激素治疗的实体肿瘤患者,每隔21天给予启动和加强剂量的BNT162b2 covid19疫苗,以及接受利妥昔单抗或异基因造血干细胞移植后的血液学恶性肿瘤患者。评估疫苗安全性和有效性(直到加强后3个月)。一段时间后(直到增强剂28天后)随访抗严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)受体结合域(RBD)抗体水平,并在增强剂28天后分析体外SARS-CoV-2对武汉野生毒株的50%中和滴度(NT50)。
结果:局部和全身不良事件(AEs)大多为轻到中度(只有1%-3%的患者经历严重的AEs)。局部性而非全身性的AEs在加强剂量后发生更频繁。197例癌症患者加强疫苗接种后28天,化疗组RBD结合抗体滴度和NT50较低(234.05 IU/ml [95% CI) 122.10-448.66]和24.54 (95% CI 14.50-41.52)。与健康个体相比[分别为1844.93 IU/ml (95% CI 1383.57-2460.14)和122.63 (95% CI 76.85-195.67)],不论化疗周期中接种疫苗的时机如何。在接受美罗华治疗的血液科患者中,抗体反应极低;只有2例患者的RBD结合抗体滴度达到50%,对症状性SARS-CoV-2感染具有保护作用(< 200iu /ml),只有1例患者的NT50高于检测限。在研究期间,5名癌症患者检测出SARS-CoV-2感染阳性,其中一名接受美罗华治疗的患者出现严重的COVID-19,导致住院2周。
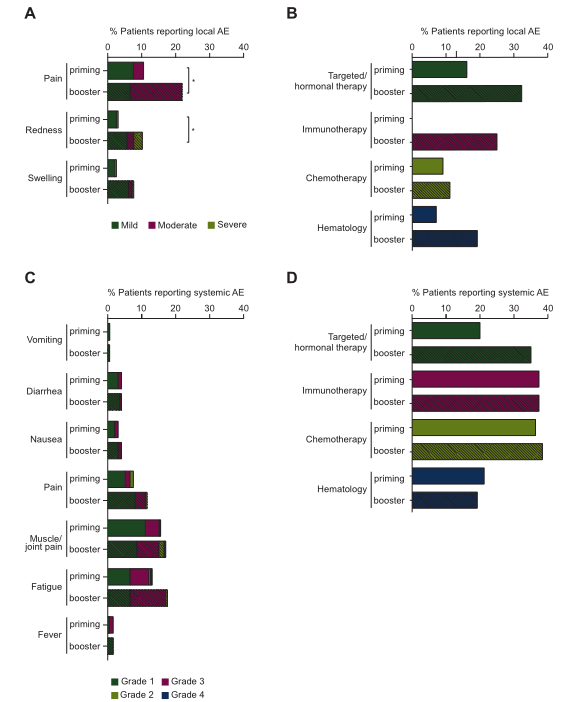
图1 在启动和加强BNT162b2疫苗接种后7天内报告了局部和全身不良事件(AEs);从所有研究队列中汇集而来的(A)局部和(C)系统性不良反应,并以总研究人群的百分比表示(接种疫苗为200人,加强接种为197人)。(C)局部和系统的不良反应是从所有研究队列中汇集而来的,并以总研究人群的百分比表示(接种疫苗为200人,加强疫苗为197人)。为了显示不同研究队列之间不良反应发生率的差异,报告不良反应的患者的比例以该队列中患者数量的百分比表示(第一剂疫苗:血液学队列,41;靶向/激素治疗队列,n=80;化疗队列,n=63;免疫治疗队列,n=16;第二疫苗剂量:血液学队列,n=41;靶向/激素治疗队列,n=80;化疗队列,n=80;免疫治疗队列,n=16;第二疫苗剂量:血液学队列,n=41;靶向/激素治疗队列,n=80;化疗队列,n=63;免疫治疗队列,n=16;第二疫苗剂量:血液学队列,n=41;靶向/激素治疗队列,n=80;化疗队列,n=16(B和D)。开放条表示第一次接种疫苗后报告的不良反应,而虚线表示第二次接种疫苗后报告的不良反应。使用McNemar检验和BonferroniHolm校正进行了两种疫苗接种之间的比较,报告了队列数(n?4)以及不同的局部AE(n=3)和全身性AE(n=7)的数量:*P<0.05
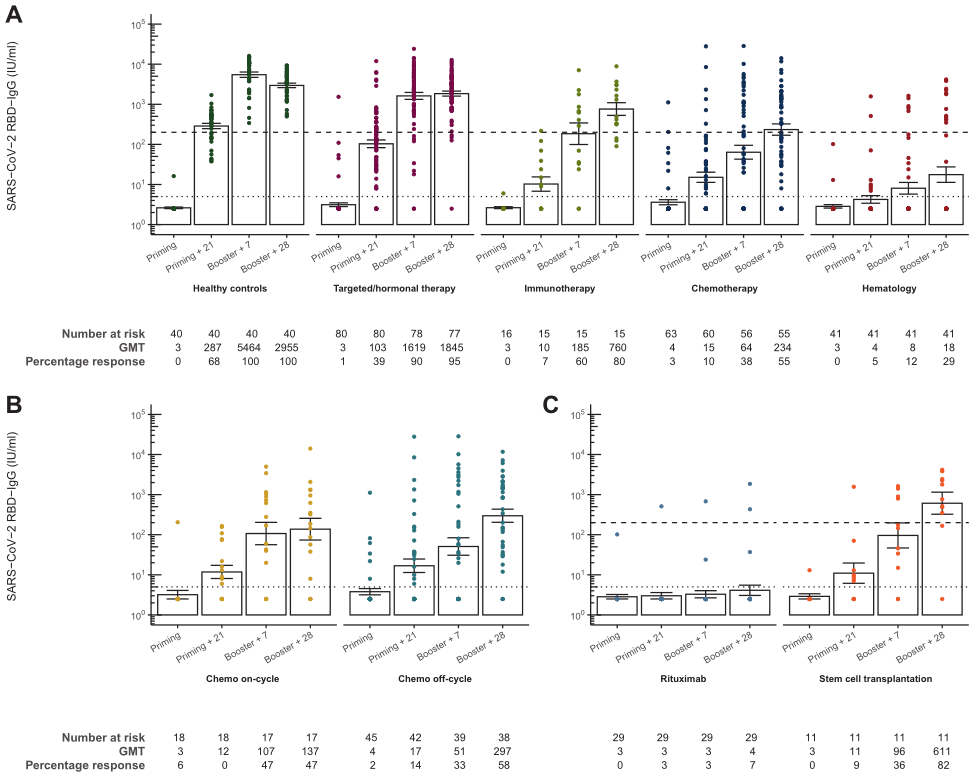
图2 BNT162b2疫苗给药后产生的严重急性呼吸综合征冠状病毒2(SARS-CoV-2)抗RBD抗体应答;病毒中和试验,中和滴度为50%(NT50),定义为SARS-CoV-2(2019nCoV-Italia-INMI1株,编号008V-03893,第5代)感染井中50%中和的样品稀释度(倒数滴度)。(A)在体外,不同实验组的SARS-CoV-2对野生型武汉株的NT50在加强剂量后28天。(B)SARS-CoV-2、抗RBD免疫球蛋白G(IgG)与NT50之间的相关性,定量下限(LLQ)以上的所有值均用回归直线表示。(2)SARS-CoV-2、抗RBD免疫球蛋白G(IgG)与NT50的相关性。给出了NT50的几何平均滴度(GMT),虚线表示LLQ。对于NT50,低于LLQ的值被归结为1/10 LLQ。I表示标准误差

图3 严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)在接种BNT162b2疫苗后产生中和抗体反应;病毒中和试验,中和滴度为50%中和滴度(NT50),定义为SARS-CoV-2(2019nCoV-Italia-INMI1株,编号008V-03893,第5代)感染井中50%中和的样品稀释度(倒数滴度)。(A)在体外,不同实验组的SARS-CoV-2对野生型武汉株的NT50在加强剂量后28天。(B)SARS-CoV-2、抗RBD免疫球蛋白G(IgG)与NT50之间的相关性,定量下限(LLQ)以上的所有值均用回归直线表示。(2)SARS-CoV-2、抗RBD免疫球蛋白G(IgG)与NT50的相关性。给出了NT50的几何平均滴度(GMT),虚线表示LLQ。对于NT50,低于LLQ的值被归结为1/10 LLQ。I表示标准误差
结论:BNT162b2疫苗在积极治疗的肿瘤患者中耐受性良好。然而,免疫的癌症患者的抗体反应被延迟和减弱,主要是在接受化疗或利妥昔单抗的患者中,导致突破性感染。
原文出处:
Peeters M, Verbruggen L, Teuwen L,et al,Reduced humoral immune response after BNT162b2 coronavirus disease 2019 messenger RNA vaccination in cancer patients under antineoplastic treatment.ESMO Open 2021 Sep 08;6(5)


