AM:青岛科技大学朱之灵/复旦大学杨冬琴合作研究利用机器学习辅助实现治疗溃疡性结肠炎纳米酶的高通量筛选
时间:2025-01-27 12:08:48 热度:37.1℃ 作者:网络
溃疡性结肠炎(UC)是一种慢性胃肠道炎症性疾病,患病率不断上升。由于UC症状的反复发作和难以治疗,现有治疗药物无法满足患者需求。
2025年1月12日,青岛科技大学朱之灵、复旦大学杨冬琴共同通讯在Advanced Materials在线发表题为“Machine Learning-Assisted High-Throughput Screening of Nanozymes for Ulcerative Colitis”的研究论文。该研究提出了一种机器学习辅助的高通量筛选策略,以加速发现用于UC治疗的高效纳米酶。使用机器学习模型量化和预测治疗需求,包括抗氧化特性、酸稳定性和zeta电位,通过高通量筛选评估肠道屏障修复效果和生物安全性等不可量化的属性。
特征显著性分析、确定独立性筛选和稀疏运算符符号回归揭示了材料特征与治疗需求之间的高维结构-活性关系。SrDy2O4具有高稳定性、低毒性、靶向能力和活性氧(ROS)清除能力,通过稳定线粒体膜电位来减少ROS的产生,降低细胞质中的细胞色素C水平,并抑制肠上皮细胞凋亡。与葡聚糖硫酸钠盐处理的模型组相比,SrDy2O4治疗小鼠的结肠长度和体重明显改善。转录组和16SrRNA测序分析表明,SrDy2O4促进肠道有益细菌的生存,减少致病菌,从而有效恢复肠道微生物群平衡。此外,SrDy2O4能够进行X射线成像,且没有副作用。

溃疡性结肠炎(UC)是一种慢性胃肠道炎症性疾病,其特征是肠粘膜反复或长期炎症,发病率在全球范围内有所上升。溃疡性结肠炎的临床表现包括肠道和肠外症状,大约三分之一的UC患者会出现外周关节炎、原发性硬化性胆管炎和结节性红斑等肠外症状。最常见的肠道症状包括血便和腹泻。尚不清楚UC的发病机制,但主要是由肠道免疫反应失调、肠道菌群变化、遗传易感性和环境因素共同作用引起的。UC难以治愈,主要治疗目标是诱导和维持临床和内镜缓解。UC的药物治疗已经从早期使用5-氨基水杨酸(5-ASA)类似物、糖皮质激素和免疫抑制剂治疗发展到最新的生物制剂。尽管在过去十年中观察到生物制剂的临床治疗缓解率有所提高,但长期治愈率仍是一个重大挑战。此外,生物制剂需要较长的给药间隔且价格昂贵,给患者带来了巨大的经济负担。因此,迫切需要开发新型、低成本的UC治疗药物。
纳米酶是一类具有类似酶催化活性的纳米材料,由于其独特的物理化学性质以及出色的生物降解性和生物相容性,在生物医学领域显示出相当大的潜力。可以通过表面改性和成分替换进行优化纳米酶,以实现在肠道特定区域的靶向递送,同时避免药物释放过程中对身体其他部位产生不必要的副作用。此外,由于纳米酶具有多种类酶催化活性,其可以同时发挥抗炎、抗氧化和免疫调节作用。因此,纳米酶在功能上优于传统的生物材料和纳米材料,为溃疡性结肠炎等炎症性疾病提供了理想的治疗方法。然而,由于材料系统的局限性和复杂的UC微环境,这些纳米酶的治疗效果达不到临床预期。
理想的纳米酶应在肠道微环境中具有几个关键特性,如生物相容性、靶向性、稳定性和催化活性。纳米酶的生物相容性及其对肠道微生物群的影响是生物医学应用中两个关键而复杂的因素。生物相容性确保纳米酶与宿主细胞安全共存,同时考虑其与免疫系统的相互作用。理想情况下,纳米酶应表现出低毒性和免疫原性,以防止快速清除和炎症反应。此外,纳米酶的表面特性和降解产物会显著影响其生物相容性。纳米酶通过影响肠道微生物的新陈代谢、生长和群落结构来间接影响宿主健康。鉴于肠道微生物群的多样性及其生态相互作用的复杂性,评估纳米酶对各种微生物的影响至关重要。设计整合多种类酶活性同时精确调节其物理化学性质的纳米酶仍具有挑战性。从本质上讲,纳米酶的设计应确保每种活性的高效表达和相互协同作用,解决活性和稳定性之间的权衡,并优化生物相容性和细胞摄取。传统设计方法缺乏精确性,以及实验结果与模型预测之间的差异显著增加了开发高效UC治疗纳米酶的复杂性。
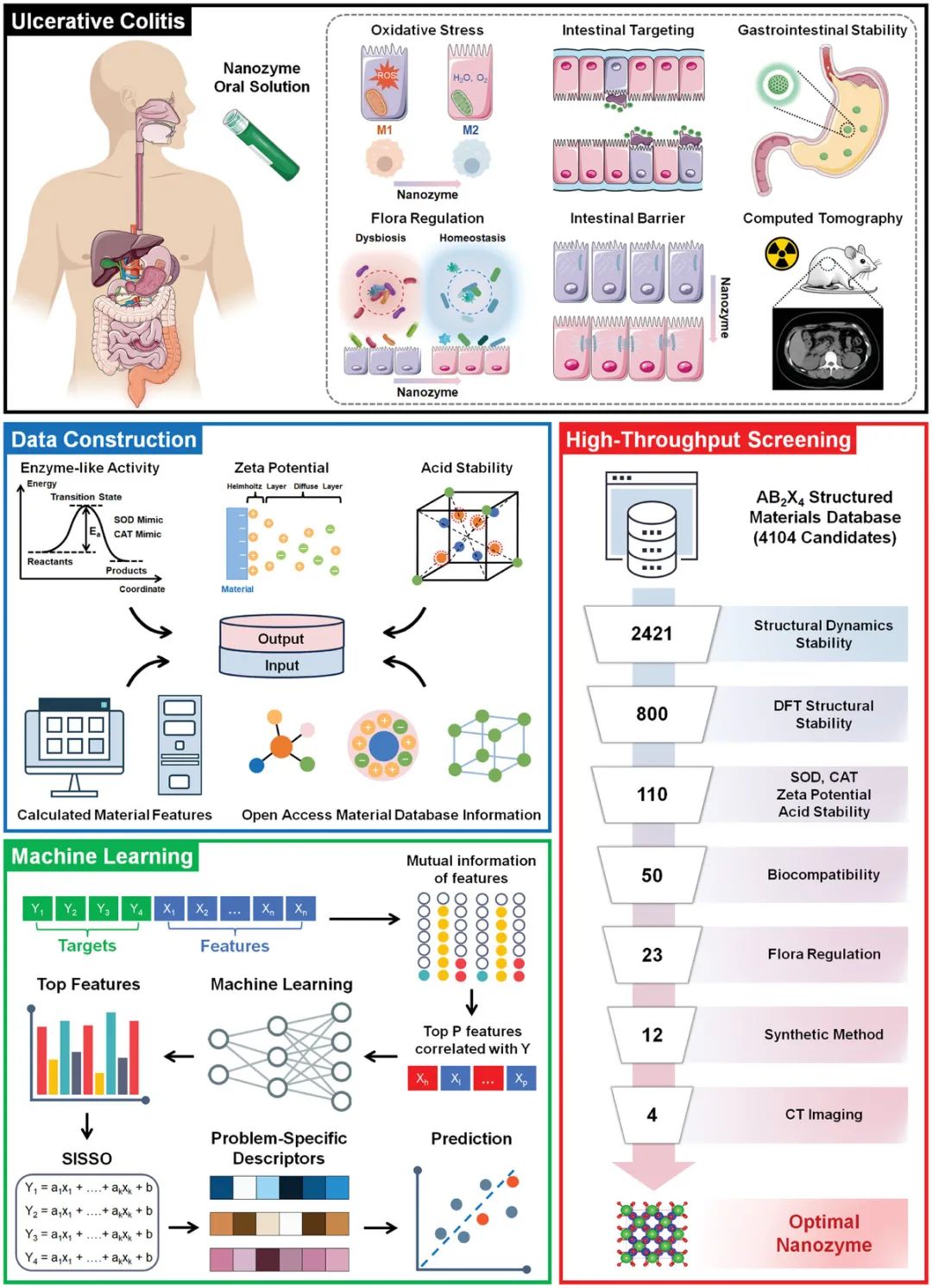
图1 用于UC治疗的多功能纳米酶的设计过程(摘自Advanced Materials)
机器学习(ML)和数据科学的发展推动了数据驱动在纳米酶领域的广泛应用。不仅预测和优化了类酶纳米材料的活性和稳定性,而且通过高效的算法和大数据分析,显著提高了设计效率和预测精度。如确定独立性筛选和稀疏化运算符(SISSO)方法通过结合符号回归与稀疏性选择来构建简洁而强大的预测模型,有效地从大规模候选描述符中筛选出最具影响力的特征。该方法提供了高度的模型可解释性,并在非线性复杂交互中表现出很高的准确性。通过精确控制输入数据的质量,利用SISSO方法的精细特征选择,可以处理复杂UC微环境中的结构-活性关系,准确预测和设计具有特定催化活性的纳米酶。因此,将ML整合到纳米酶设计中简化了开发过程,并推动了UC治疗药物的筛选。
该研究使用ML辅助高通量筛选策略,定了一种适用于UC治疗的新型多特征纳米酶。该策略利用AB2X4,一个材料空间大、场地可控的材料系统。使用第一性原理计算筛选尖晶石结构中A、B和C位点的潜在元素组合,进行波函数分析以提取关键的电子特征,如轨道能级和电子密度。获得的高精度电子属性数据为构建ML模型提供了可靠的基础,保证了其预测的准确性和稳定性。使用数据收集和高通量计算建立AB2X4结构的材料数据库。通过结合ML和SISSO,将材料特征重新组织为新的结构描述符,该结构描述符将这些特征与类超氧化物歧化酶(SOD)和过氧化氢酶(CAT)活性、酸稳定性和ζ电位联系起来,分析AB2X4的结构参数与其用于UC治疗的多特征性质之间的半定量结构-活性关系,快速进行材料预测。
因此,筛选出一种具有强酸稳定性、在UC部位高效活性氧(ROS)清除性能的新型纳米酶SrDy2O4,远远超过一线药物5-ASA的治疗效果。此外,SrDy2O4能够准确定位UC炎症部位,在电子计算机断层扫描(CT)中优于传统的碘造影剂。转录组和16srRNA测序揭示了SrDy2O4缓解UC的内在机制。SrDy2O4通过显著降低氧化应激损伤、恢复线粒体复合物氧化磷酸化的生理水平、改善受损的肠道屏障功能、平衡肠道微生物区系和调节肠道免疫,有效稳定肠道微环境。
参考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202417536


