CDH17:消化道肿瘤新兴靶点
时间:2025-01-10 12:10:53 热度:37.1℃ 作者:网络
2024年8月23日,普众发现1类新药注射用AMT-676在国内获得临床试验默示许可,用于治疗晚期实体瘤。据公开资料,AMT-676是普众发现研发的一款CDH17靶向抗体偶联药物(ADC),其针对晚期实体瘤的1期临床研究已在澳大利亚启动。在肿瘤组织中,CDH17在胃、胰腺、肝、食道、胆管癌和结直肠癌中过表达,被认为是消化道肿瘤药物研发的潜力靶点。
关于CDH17
钙粘素(cadherin, 钙粘蛋白,钙粘合素)是一类依赖于Ca2+的细胞粘附分子的超家族,它在维持组织结构和形态中发挥着关键作用。
Cadherin的表达失调往往与疾病有关,包括组织发育不良、肿瘤形成和转移。典型Cadherin胞外域由5个重复序列构成;胞内域由150-160个氨基酸组成,高度保守。
CDH17(Cadherin 17,LI-cadherin),也称为肝肠钙粘蛋白,是钙依赖性蛋白质CDH超家族的非经典成员。CDH17序列由七个细胞外钙粘蛋白结构域和一个非常短的细胞质结构域形成。与其他经典的钙粘蛋白不同,CDH17是一种钙依赖性跨膜糖蛋白,可介导细胞在肠上皮中的细胞粘附。

图1.钙粘蛋白-17 (CDH17) 的结构特征
(即在细胞外氨基末端 (NH2) 具有 7 个钙粘蛋白重复序列(EC1-EC7),随后是跨膜区和羧基处的短胞质结构域-终点(COOH)。钙离子(用红点表示)位于哺乳动物 CDH17 的钙粘蛋白重复序列之间)
CDH17的生物学功能与表达
CDH17主要在肠上皮细胞及部分胰腺导管上皮细胞中表达,健康成人的肝细胞、食管和胃黏膜中几乎不表达。其主要功能是通过介导钙依赖性粘附在细胞间保持结构和形态的完整性。研究表明,CDH17在胃癌、结直肠癌、肝癌、胰腺癌和胆管癌等多种肿瘤中均有高表达,且其表达水平与患者的预后和治疗反应密切相关。
CDH17与肿瘤发展的关系
CDH17的功能紊乱与肿瘤细胞的浸润和转移密切相关。
在胃癌中,CDH17的上调可通过激活NF-κB和促进MAPK信号通路来促进癌细胞的增殖和侵袭。同时,其在肝癌中的expression与Wnt/β-catenin信号通路的激活相联系,提示其可能在肝细胞癌的进展中发挥作用。
此外,CDH17也被证明能与α2β1整合素相互作用,并且是α2β1整合素活性调控细胞粘附和增殖的关键决定因素,以及能促进结肠直肠癌细胞获得肝转移的能力。
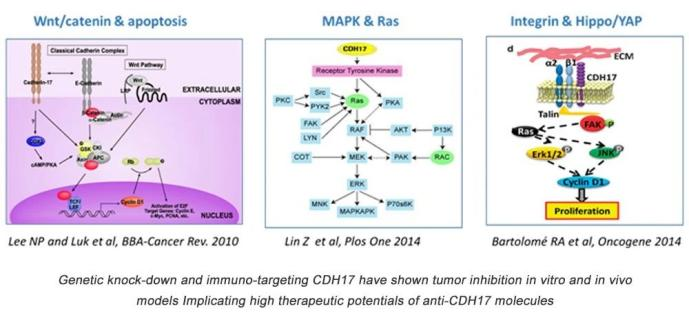
CDH17在肿瘤中的作用机制以及在癌症治疗中的具体作用虽然尚未清楚,但已经有新型靶向治疗药物(如BI 905711和ARB102等)处于临床研究阶段,用于治疗胃癌、胰腺癌、食管癌、胆管癌等胃肠道癌。这些药物可同时结合肿瘤细胞表面的CDH17和死亡受体TRAILR2,诱导肿瘤细胞凋亡,对表达CDH17的正常细胞无损伤。
目前在研格局
相较于其他靶点,CDH17靶点进展较慢,在研药物大多处于临床早期阶段,但CDH17靶向药类型比较丰富,涵盖单抗/双抗、ADC、细胞疗法等,尚未有相关产品获批。
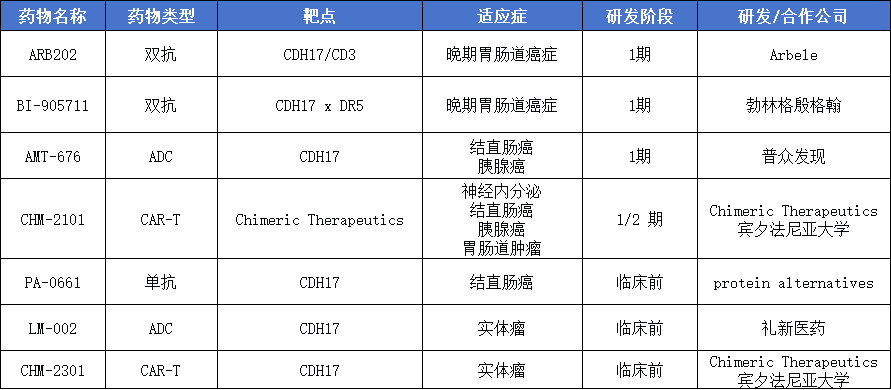
1、ARB202
ARB202是利用TriAx技术构建的一种人源化抗CDH17xCD3的IgG4双抗, 是一款潜在“同类首创”药物,其具备独特亲和力抗 CDH17 和抗 CD3 差异化的结构,在保证高特异性和高杀伤活性的同时,避免过度激活T细胞所引起的全身免疫反应风险。
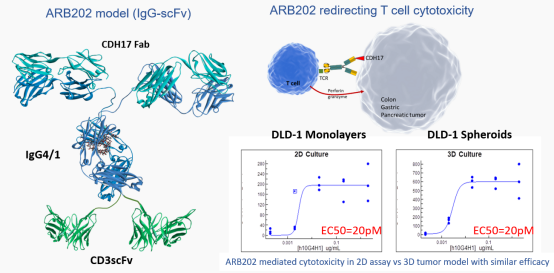
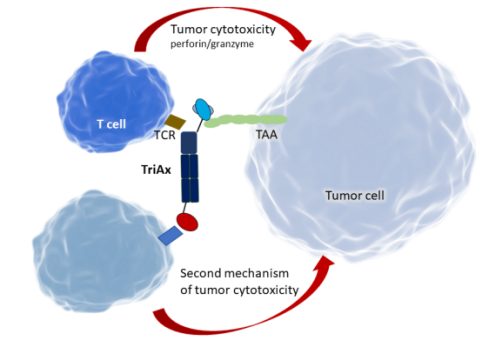
Arbele的TriAx抗体设计是为了通过结合多种抗肿瘤机制在消化道癌症治疗中获得更大的疗效,具有低抗原性、稳定性、理想的生物分布和药代动力学特性。纳入TriAx抗体的抗肿瘤机制包括重新引导T/NK细胞的细胞毒性,抑制免疫检查点,吞噬作用和增强适应性免疫反应。
临床前数据显示:ARB202能有效增强T细胞与表达CDH17的胃肠道肿瘤细胞系之间的相互作用,从而导致T细胞的活化并释放IL-2,有效的产生肿瘤细胞杀伤,通过体内注射低剂量ARB202 抗体可以有效地抑制肿瘤的生长。1a期研究的初步数据显示:ARB 202在血液循环中的耐受性Cmax高达150ng/ml,这表明在这些浓度下没有临床显著的脱靶T细胞活化。
2、BI-905711
BI905711是勃林格殷格翰公司首创的双特异性、四价治疗性抗体,靶向TRAILR2和CDH17的四价双抗,TRAILR2与CDH17交联诱导CDH17依赖性TRAILR2聚集,在共表达TRAILR2和CDH17的肿瘤细胞中诱导选择性凋亡。
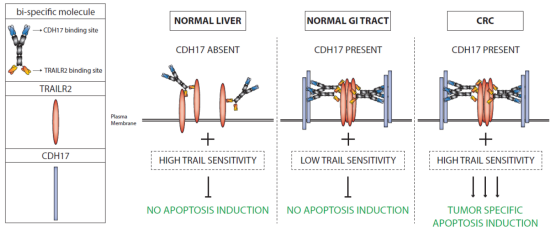
BI 905711已推进至首次人体临床试验。在一项针对晚期胃肠道癌症患者的Ia/b 期研究中,48 名患者接受了BI 905711治疗,13 名患者病情稳定 (SD),8 名患者无进展生存期≥4 个月 (PFS4)。CRC 患者中,6 名患者病情稳定,3 名患者无进展生存期为 4 个月;非CRC 患者中,7 名患者病情稳定 (PDAC:n = 6),5 名患者无进展生存期为4 个月 (PDAC:n = 4)。未观察到 DLT 且未达到 MTD。
3、CHM-2101
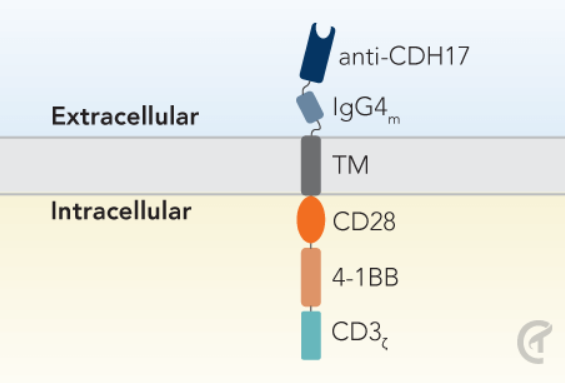
CHM 2101 (CDH17 CAR T)是世界知名的宾夕法尼亚大学细胞治疗中心发明的同类首创第三代 CDH17 CAR T,具有CD28和4-1BB共刺激结构域。CHM 2101的临床前证据于2022年3月发表在《Nature Cancer》杂志上,证明在7种癌症中完全根除肿瘤。
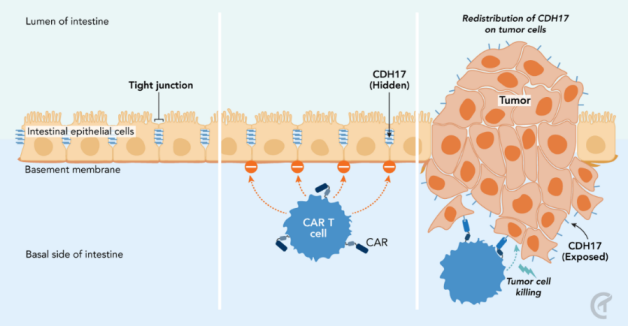
CDH17 CAR-T细胞仅浸润肿瘤细胞,尽管正常细胞表达CDH17也不受影响。在正常细胞中,CDH17隐藏在正常细胞屏障的紧密连接之下;而在癌症中,CDH17上调导致其暴露在癌细胞膜上,允许CAR-T检测并结合它。
目前针对晚期结直肠癌、胃癌和神经内分泌肿瘤患者正在开展一项多中心、开放标签1A/B期临床试验。临床前证据表明,CHM-2101具有完全根除肿瘤细胞而不复发的实体肿瘤的独特效力,并对正常组织没有毒性。
4、AMT-676
2024年8月23日,普众发现1类新药注射用AMT-676在国内获得临床试验默示许可,用于治疗晚期实体瘤。据公开资料,AMT-676是普众发现研发的一款CDH17靶向抗体偶联药物(ADC),其针对晚期实体瘤的1期临床研究已在澳大利亚启动。

总结
CDH17作为一个新兴的肿瘤靶点,具有良好的肿瘤特异性及较低的毒性风险,其药物市场未来展望相当广阔,有望在不久的将来为癌症患者带来新的治疗选择和希望。


