【协和医学杂志】免疫检查点抑制剂相关免疫性膀胱炎一例
时间:2026-05-05 17:08:22 热度:37.1℃ 作者:网络
免疫检查点抑制剂(ICIs)通过阻断程序性死亡受体 1(PD-1)、程序性死亡受体配体 1(PD-L1)及细胞毒性T 淋巴细胞相关抗原4(CTLA-4)等信号通路,解除肿瘤细胞对机体免疫系统的抑制,激活自身抗肿瘤免疫应答[1-2],已成为肝胆管癌[3-4]、黑色素瘤[5]、非小细胞肺癌[6-7]等多种恶性肿瘤的重要治疗手段,显著改善晚期肿瘤患者的生存预后。随着ICIs临床应用的日益广泛,其相关免疫不良反应(irAEs)也逐渐凸显[8]。irAEs可累及全身多个器官系统,其中皮肤、胃肠道及内分泌系统受累较为常见[9],而泌尿系统irAEs相对少见,免疫性膀胱炎的发病率更是不足1%[8,10]。
本文报道1例肝胆管恶性肿瘤患者在接受帕博利珠单抗治疗后发生迟发性免疫性膀胱炎的诊疗经过,结合实验室检查、影像学、膀胱镜及病理活检结果,探讨该疾病的发病机制、鉴别诊断要点及治疗策略,旨在提高临床医师对ICIs相关泌尿系统irAEs的认识,为临床早期识别与规范处理提供参考依据。
1 病例资料
患者女性,55岁,主诉尿频、尿急、尿痛1个月。患者于1个月前(2025年10月17日)无明显诱因出现尿频、尿急、尿痛等尿路刺激症状。
外院查尿常规示:白细胞酯酶(3+),白细胞计数781个/μL,未行尿培养,予左氧氟沙星治疗2周后症状无缓解。1周前于外院复查尿常规:白细胞酯酶(3+),白细胞计数3360 个/μL,红细胞3960 个/μL,尿培养阴性。
泌尿系彩超提示:膀胱壁及尿道内口不均匀增厚,考虑慢性膀胱炎可能。先后予多种抗生素抗感染治疗,症状仍无明显改善,且逐渐加重,排尿间隔为5~10min 1次,伴明显尿痛。2d前出现终末红色血尿,无血凝块,伴下腹坠胀感。自起病以来,患者精神、食欲、睡眠一般,小便如前述,大便正常,体重无明显变化。
既往史:患者1年前(2024年7月15日)诊断为肝胆管恶性肿瘤,确诊后即行卡培他滨联合帕博利珠单抗治疗(21 d为1个疗程)。10个月前(2025年1月8日)行胆道切除术+胆囊切除术+胆肠吻合术,术后继续原方案治疗。4个月前(2025年7月)停用卡培他滨,1个月前(2025年10月23日)末次使用帕博利珠单抗。化疗期间血肌酐波动于80~110 μmol/L。既往有血小板减少病史,长期口服利可君片。否认高血压、糖尿病、冠心病等慢性病史,否认乙肝、结核等传染病病史。否认外伤、输血史。否认食物、药物过敏史。个人史:无吸烟、饮酒嗜好,无特殊化学品、放射线接触史。月经及婚育史:已绝经,已婚已育,配偶及子女体健。家族史:父母健在,否认家族遗传病及传染病史。
入院查体:体温36.2 ℃,心率98次/min,呼吸频率20次/min,血压118/74 mm Hg(1 mm Hg=0.133 kPa),体质量指数为20 kg/m2。神志清,精神可,全身皮肤黏膜无黄染、皮疹,浅表淋巴结未触及肿大,心肺腹未见异常,双肾区无叩痛,双下肢无水肿。实验室检查:血常规示白细胞6.52×109/L,淋巴细胞1.21×109/L,血红蛋白107 g/L,血小板91×109/L;血肌酐100 μmol/L,超敏C反应蛋白12.42 mg/L。
尿沉渣定量示红细胞 46个/μL,白细胞 381个/μL,粒细胞酯酶(2+),尿蛋白(±);尿红细胞位相:正形红细胞20 000/mL,畸形红细胞0/mL,总红细胞 20 000/mL。多次尿培养、结核分枝杆菌检测、解脲支原体培养均为阴性。膀胱穿刺尿病原体靶向高通量测序(NGS)提示JC多瘤病毒、人疱疹病毒4型阳性;尿液JC多瘤病毒核酸检测为2.86×105copies/mL,血液检测为阴性。
外周血淋巴细胞亚群绝对计数:T淋巴细胞 520.59个/μL、CD4+T 细胞 277.09个/μL、CD8+T 细胞 239.63个/μL,均低于参考范围。腹部+盆腔CT平扫示:膀胱壁增厚伴周围渗出,双侧肾盂及输尿管壁稍增厚,右侧肾盂轻度积液。经积极治疗后复查腹部+盆腔CT,提示膀胱壁较前明显变薄(图 1)。
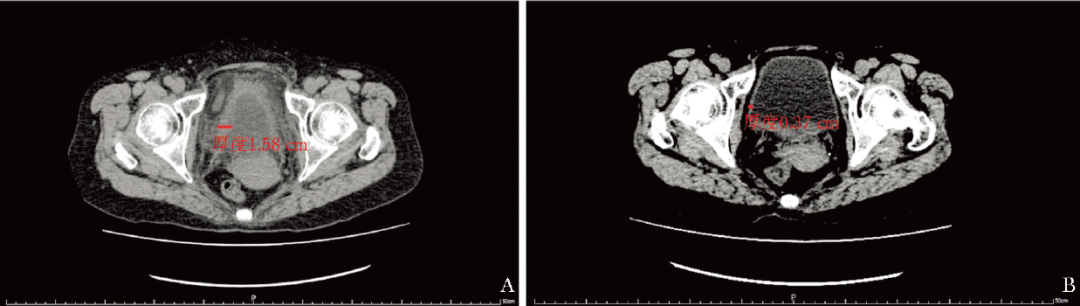
图1 腹部+盆腔CT
A.治疗前提示膀胱壁增厚伴周围渗出;B.治疗后提示膀胱壁稍增厚,较前减轻
患者存在持续尿路刺激症状伴血尿,反复抗感染治疗无效,泌尿系CT提示膀胱壁增厚,为排除膀胱肿瘤、膀胱结石等器质性病变,并进一步明确特异性感染及潜在免疫性损伤可能,遂行膀胱镜检查+黏膜活检术。膀胱镜术中见双侧输尿管口显示不清,膀胱内可见少量絮状物,膀胱各壁黏膜未见新生物、溃疡及结石。
术后病理结果提示:
1 膀胱三角区黏膜组织:尿路上皮大部分脱落,残留上皮呈反应性改变,伴炎症细胞浸润;固有层间质显著水肿,小血管扩张,可见大量淋巴细胞及中性粒细胞浸润,符合慢性活动性炎症,免疫组化示尿路上皮SV40 T Ag(-)(图2);
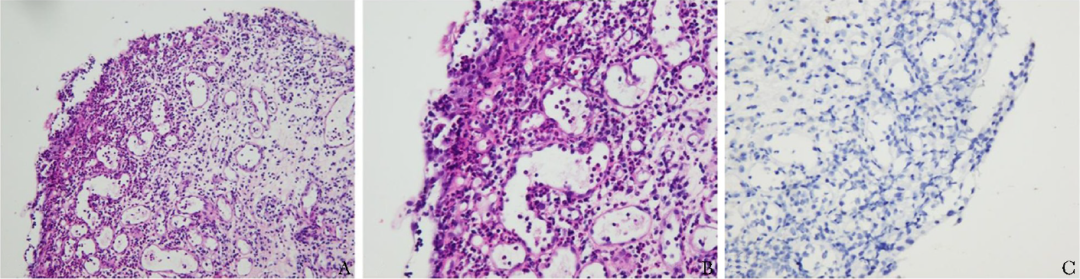
图2 膀胱三角区黏膜组织染色
A~B.HE染色显示,膀胱三角区黏膜固有层间质水肿,可见大量淋巴细胞及中性粒细胞浸润,小血管扩张(A:×200;B:×400);C.免疫组化染色显示尿路上皮SV40 T Ag(-)
2 膀胱后壁黏膜组织:尿路上皮完全脱落,大量中性粒细胞渗出;固有层间质显著水肿、小血管扩张,散在中性粒细胞浸润,局部小灶淋巴细胞聚集,符合慢性活动性炎症,免疫组化示 SV40 T Ag(-)(图3)。
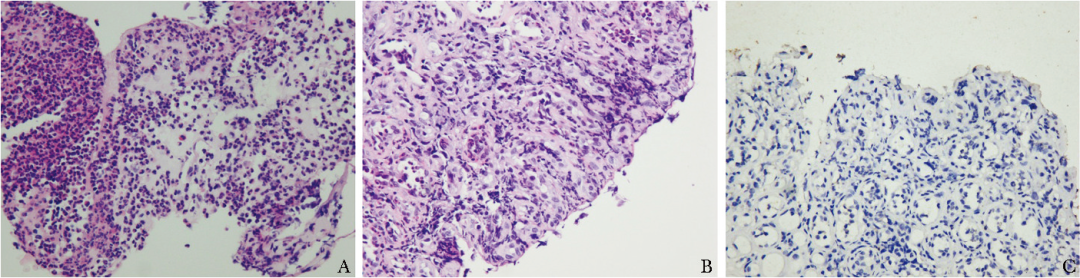
图3 膀胱后壁黏膜组织染色
A~B.HE染色显示,膀胱后壁黏膜尿路上皮完全脱落,大量中性粒细胞渗出,固有层间质显著水肿、小血管扩张,局部小灶淋巴细胞聚集(A:×200;B:×400);C.免疫组化显示尿路上皮SV40 T Ag(-)
患者入院后完善上述检查,排除细菌、结核、支原体等感染,结合帕博利珠单抗用药史及病理结果,临床诊断为ICIs相关免疫性膀胱炎。明确诊断后,予甲泼尼龙40 mg静脉滴注,患者尿路刺激症状逐渐缓解,复查尿沉渣示尿红细胞、尿白细胞计数呈进行性下降。用药5 d后,患者尿频、尿急、尿痛等症状基本消失,排尿间隔延长至3 h,无血尿及腹部不适。复查血肌酐降至72 μmol/L,腹部CT提示膀胱壁厚度较前明显减轻。
出院时予口服足量激素(强的松50 mg,每日1次)。出院后一周,患者症状完全缓解,复查尿沉渣示尿白细胞、尿红细胞均阴性。口服足量激素1周后,减量为强的松25 mg,每日1次。此后定期随访,尿检均正常,血肌酐波动于80~90 μmol/L,按每月减量5 mg的方案逐步减停。目前维持强的松15 mg,每日1次。本例患者完整诊疗时间线见图4。
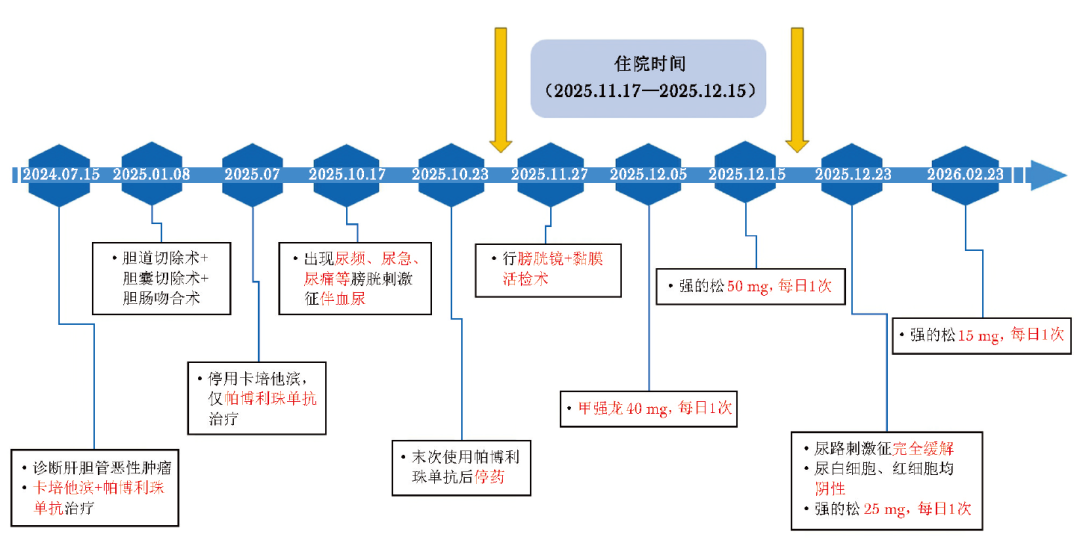
图4 本例患者完整诊疗时间线
2 讨论
ICIs 通过阻断PD-1/PD-L1 等免疫检查点通路,解除肿瘤细胞对机体免疫系统的抑制以激活抗肿瘤免疫应答,已成为肝胆管癌、黑色素瘤等多种恶性肿瘤的重要治疗手段,但随之而来的 irAEs 也成为临床诊疗的重要挑战。irAEs 可累及全身多器官系统,其中免疫性膀胱炎的发病率较低,因缺乏特异性临床表现,临床易误诊为感染性膀胱炎,延误治疗时机[8]。
2.1 ICIs相关免疫性膀胱炎的发病机制
ICIs相关免疫性膀胱炎的核心机制为免疫失衡[11]。帕博利珠单抗等PD-1抑制剂解除了对T细胞的抑制作用[1],活化的T细胞不仅攻击肿瘤细胞,还可能对膀胱黏膜正常组织产生免疫攻击[12],导致尿路上皮损伤、间质炎症浸润及水肿,进而出现尿路刺激症状[13]。本例患者外周血T淋巴细胞、CD4+T 细胞、CD8+T 细胞计数均显著降低,提示存在全身免疫功能紊乱,这与研究报道的 irAEs 患者免疫细胞亚群异常特征一致[8]。
值得注意的是,本例为迟发性irAEs,在使用帕博利珠单抗治疗后1年才出现相关临床表现,与多数irAEs在用药后数周至3个月内发生的特点不同[8-10],其延迟发生的可能原因如下:
1 手术创伤对免疫状态的影响:手术创伤可导致机体免疫细胞一过性耗竭,使免疫损伤的发生时间延迟,这与 Michot等[12]在研究中提出肿瘤患者术后继发免疫重构可影响 irAEs 发生时序的观点相符;
2 ICIs的长效免疫激活作用:帕博利珠单抗对 T 细胞的激活具有持续性,即使停药后,活化的免疫细胞仍可在体内维持低水平活性,在机体免疫平衡重建过程中引发迟发性靶器官损伤[12,14],但目前关于 ICIs迟发性泌尿系统 irAEs的报道较少,其具体机制尚需更多研究证实。
2.2 临床鉴别诊断
ICIs相关免疫性膀胱炎缺乏特异性免疫学诊断标志物,其诊断需结合ICIs 用药史、临床表现、辅助检查及治疗反应综合判断,因无法通过单一指标确诊,需在排除感染、肿瘤、放射性损伤等所有可能病因后,结合ICIs用药的时序关系作出临床诊断[9]。
本例患者有明确的ICIs用药史,存在尿频、尿急、尿痛等尿路刺激症状伴血尿表现,多次尿培养、结核分枝杆菌检测、解脲支原体培养结果均为阴性,腹部CT提示膀胱壁增厚伴渗出,膀胱镜未见膀胱肿瘤,膀胱黏膜病理可见尿路上皮脱落,固有层水肿,间质炎症细胞浸润等非特异性炎症表现,是支持临床诊断并排除肿瘤及特异性感染的重要依据。且患者抗感染治疗无效及对糖皮质激素治疗明显有效的治疗反应,更进一步支持了ICIs相关免疫性膀胱炎的诊断。但本例患者尿液中检测到JC多瘤病毒,是否有病毒感染因素的潜在参与是本例患者诊疗过程中的关键迷惑点及鉴别诊断难点。
首先,JC多瘤病毒相关出血性膀胱炎极罕见,远少于BK多瘤病毒感染,目前尚无统一的尿液核酸检测诊断阈值,临床及部分个案报道多参考BK多瘤病毒相关出血性膀胱炎的通用阈值,尿液病毒核酸载量≥ 107 copies/mL[15-17],若采用此标准,本例患者拷贝数为 2.86×105 copies/mL,未达到致病阈值,提示病毒载量可能不足以引发膀胱黏膜的感染性损伤;
其次,SV40 T Ag是反映多瘤病毒激活、复制启动及致病潜能的重要分子标志物,其阳性结果提示病毒处于非潜伏的致病性感染状态[18-20]。本例患者膀胱黏膜免疫组化 SV40 T Ag(-),结合血液 JC多瘤病毒核酸阴性结果,可基本排除JC多瘤病毒血行感染及膀胱黏膜的活动性感染;
最后,患者患有肝胆管恶性肿瘤,长期接受化疗及 ICIs治疗,免疫功能低下,膀胱黏膜屏障因免疫损伤受损,易出现病毒局部定植[21-22]。
综上,本例中JC多瘤病毒更可能为免疫功能紊乱状态下的局部定植,而非膀胱炎的致病原因。但由于尿液病毒核酸的检测阈值尚未有统一标准,病毒因素的潜在参与尚不能完全排除,JC多瘤病毒的定植可能作为共刺激因素,加重膀胱黏膜的免疫性炎症损伤,其与ICIs相关免疫性膀胱炎的相互作用仍需更多临床研究探讨。
除感染性膀胱炎和膀胱肿瘤外,ICIs相关免疫性膀胱炎还需与放射性膀胱炎相鉴别。放射性膀胱炎伴有盆腔放疗史,病理表现以血管扩张、纤维化、黏膜坏死为特征,糖皮质激素治疗效果有限[23]。本例患者无盆腔放疗史,暂不考虑放射性膀胱炎。
2.3 治疗策略
ICIs 相关免疫性膀胱炎的治疗以糖皮质激素为一线方案,通过抑制异常的免疫反应,减轻膀胱黏膜的炎症损伤[9,24-25]。本例患者予甲泼尼龙静脉滴注后,尿路刺激症状在5 d内快速缓解,尿沉渣、肾功能及影像学指标均显著改善,验证了激素治疗的有效性。对于糖皮质激素治疗效果不佳的中重度 irAEs 患者,可考虑加用免疫抑制剂[24],同时需重视对症支持治疗,包括碱化尿液、止痛、纠正电解质紊乱等,合并机会性感染时需及时予以抗感染治疗。
ICIs 停药后是否重启是临床决策的难点,需结合肿瘤病情、irAEs 严重程度、治疗反应及患者免疫功能状态进行个体化评估。本例患者的重启评估依据如下:
1 肿瘤病情:患者肝胆管恶性肿瘤术后,目前无肿瘤复发征象,但仍有继续抗肿瘤治疗的需求;
2 rAEs 严重程度:本例患者irAEs为中度,无肾功能严重损伤及其他器官系统受累,糖皮质激素治疗后症状快速缓解,且在激素规律减量过程中暂无复发迹象。
基于以上因素,本例患者后续需由肿瘤科、肾内科组成的多学科团队(MDT)进行评估,拟于强的松减至最低剂量(10 mg,每日1次)后,根据患者免疫功能恢复及肿瘤复发情况,必要时考虑重启单药低剂量帕博利珠单抗治疗。重启后需密切监测泌尿系统症状及免疫功能指标,以便及时发现并处理可能的irAEs复发[24]。有研究表明,轻、中度irAEs 经糖皮质激素治疗缓解后,重启ICIs 治疗的复发率约20%~30%[26],因此在重启治疗前仍应由MDT团队谨慎评估。
目前国内外关于ICIs相关免疫性膀胱炎的报道多集中于黑色素瘤[5]、非小细胞肺癌[6]等肿瘤类型,肝胆管肿瘤背景下的报道较为罕见。目前仅有少数肝胆管肿瘤患者发生 PD-1 抑制剂相关免疫性膀胱炎[27-28],且均未合并尿液JC多瘤病毒阳性,本例为肝胆管恶性肿瘤合并尿液JC多瘤病毒阳性的延迟性 ICIs 相关免疫性膀胱炎,丰富了该疾病的肿瘤谱,为临床认识不同肿瘤类型irAEs 的特征提供参考。
综上所述,临床医师需提高对ICIs相关泌尿系统irAEs的认识,尤其是延迟性 irAEs。对于使用ICIs的肿瘤患者,用药3个月以上出现尿路刺激症状且抗感染治疗无效时,应及时考虑免疫性膀胱炎的可能,避免误诊。
此外,膀胱镜检查联合黏膜活检在 ICIs 相关免疫性膀胱炎的诊断中具有核心价值,可直接观察膀胱黏膜形态,排除肿瘤等器质性病变,同时黏膜活检为免疫性损伤及排除特异性感染提供依据,临床应尽早开展。
对于 irAEs 合并病毒学指标阳性的病例,需结合病毒检测诊断阈值、病毒复制标志物、血行感染证据及治疗反应综合判断。ICIs 停药后是否重启治疗,需由MDT进行个体化评估,平衡抗肿瘤治疗的获益与 irAEs的复发风险,重启后需加强临床监测,以确保治疗安全性。
专家点评
施潇潇 副主任医师
免疫性膀胱炎是ICIs相关irAEs的罕见类型,因发病率低、临床表现缺乏特异性,易漏诊误诊。本病例为临床医师提供了关键诊疗提示:在接受ICIs治疗后出现无菌性脓尿、常规抗感染治疗无效者,需高度警惕此类疾病。确诊一方面需充分鉴别诊断,逐一排除泌尿系感染、膀胱肿瘤、放射性膀胱炎等,在排查感染时,不局限于常规尿培养,还需结合肿瘤患者化疗及免疫抑制状态的特殊性,排查不典型病原体感染如多瘤病毒筛查、病原体靶向NGS等;另一方面联合影像学、膀胱镜及病理检查积极寻找免疫性膀胱炎证据。在确诊后及时予糖皮质激素治疗,从症状、尿常规及影像学表现多方面可证实治疗有效。本病例诊疗规范、鉴别诊断全面、治疗思路清晰,为临床规范诊治ICIs相关免疫性膀胱炎提供了宝贵参考。
参考文献
[1]Pardoll D M. The blockade of immune checkpoints in cancer immunotherapy[J]. Nat Rev Cancer, 2012, 12(4): 252-264.
[2]Topalian S L, Drake C G, Pardoll D M. Immune checkpoint blockade: a common denominator approach to cancer therapy[J]. Cancer Cell, 2015, 27(4): 450-461.
[3]Kelley R K, Ueno M, Yoo C, et al. Pembrolizumab in combination with gemcitabine and cisplatin compared with gemcitabine and cisplatin alone for patients with advanced biliary tract cancer (KEYNOTE-966): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2023, 401(10391): 1853-1865.
[4]Zhu A X, Finn R S, Edeline J, et al. Pembrolizumab in patients with advanced hepatocellular carcinoma previously treated with sorafenib (KEYNOTE-224): a non-randomised, open-label phase 2 trial[J]. Lancet Oncol, 2018, 19(7): 940-952.
[5]Hodi F S, O'Day S J, McDermott D F, et al. Improved survival with ipilimumab in patients with metastatic melanoma[J]. N Engl J Med, 2010, 363(8): 711-723.
[6]Reck M, Rodríguez-Abreu D, Robinson A G, et al. Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer[J]. N Engl J Med, 2016, 375(19): 1823-1833.
[7]Brahmer J, Reckamp K L, Baas P, et al. Nivolumab versus docetaxel in advanced squamous-cell non-small-cell lung cancer[J]. N Engl J Med, 2015, 373(2): 123-135.
[8]Postow M A, Sidlow R, Hellmann M D. Immune-Related adverse events associated with immune checkpoint blockade[J]. N Engl J Med, 2018, 378(2): 158-168.
[9]Brahmer J R, Lacchetti C, Schneider B J, et al. Manage-ment of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: American Society of Clinical Oncology clinical practice guideline[J]. J Clin Oncol, 2018, 36(17): 1714-1768.
[10]Martins F, Sofiya L, Sykiotis G P, et al. Adverse effects of immune-checkpoint inhibitors: epidemiology, management and surveillance[J]. Nat Rev Clin Oncol, 2019, 16(9): 563-580.
[11]June C H, Warshauer J T, Bluestone J A. Is autoimmunity the Achilles' heel of cancer immunotherapy?[J]. Nat Med, 2017, 23(5): 540-547.
[12]Michot J M, Bigenwald C, Champiat S, et al. Immune-related adverse events with immune checkpoint blockade: a comprehensive review[J]. Eur J Cancer, 2016, 54: 139-148.
[13]Naidoo J, Page D B, Li B T, et al. Toxicities of the anti-PD-1 and anti-PD-L1 immune checkpoint antibodies[J]. Ann Oncol, 2015, 26(12): 2375-2391.
[14]Fletcher K, Johnson D B. Chronic immune-related adverse events arising from immune checkpoint inhibitors: an update[J]. J Immunother Cancer, 2024, 12(7): e008591.
[15]Jandial A, Mishra K, Sandal R, et al. Management of BK virus-associated haemorrhagic cystitis in allogeneic stem cell transplant recipients[J]. Ther Adv Infect Dis, 2021, 8: 2049936121991377.
[16]Kotton C N, Kamar N, Wojciechowski D, et al. The second international consensus guidelines on the management of BK polyomavirus in kidney transplantation[J]. Transplantation, 2024, 108(9): 1834-1866.
[17]Franzén J, Ramqvist T, Bogdanovic G, et al. Studies of human polyomaviruses, with HPyV7, BKPyV, and JCPyV present in urine of allogeneic hematopoietic stem cell transplanted patients with or without hemorrhagic cystitis[J]. Transpl Infect Dis, 2016, 18(2): 240-246.
[18]Vilchez R A, Butel J S. Emergent human pathogen simian virus 40 and its role in cancer[J]. Clin Microbiol Rev, 2004, 17(3): 495-508.
[19]Eash S, Manley K, Gasparovic M, et al. The human polyomaviruses[J]. Cell Mol Life Sci, 2006, 63(7/8): 865-876.
[20]Boothpur R, Brennan D C. Human polyoma viruses and disease with emphasis on clinical BK and JC[J]. J Clin Virol, 2010, 47(4): 306-312.
[21]Lv Y J, Liu X P. Hemorrhagic cystitis induced by JC polyomavirus infection following COVID-19: a case report[J]. BMC Urol, 2024, 24(1): 87.
[22]Mendoza M A, Imlay H. Polyomaviruses after allogeneic hematopoietic stem cell transplantation[J]. Viruses, 2025, 17(3): 403.
[23]Marks L B, Carroll P R, Dugan T C, et al. The response of the urinary bladder, urethra, and ureter to radiation and chemotherapy[J]. Int J Radiat Oncol Biol Phys, 1995, 31(5): 1257-1280.
[24]Schneider B J, Naidoo J, Santomasso B D, et al. Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: ASCO guideline update[J]. J Clin Oncol, 2021, 39(36): 4073-4126.
[25]Haanen J B A G, Carbonnel F, Robert C, et al. Management of toxicities from immunotherapy: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2017, 28(suppl_4): iv119-iv142.
[26]Pollack M H, Betof A, Dearden H, et al. Safety of resuming anti-PD-1 in patients with immune-related adverse events (irAEs) during combined anti-CTLA-4 and anti-PD1 in metastatic melanoma[J]. Ann Oncol, 2018, 29(1): 250-255.
[27]Zhu S H, Bian L J, Lv J, et al. A case report of non-bacterial cystitis caused by immune checkpoint inhibitors[J]. Front Immunol, 2021, 12: 788629.
[28]Yuan Y Y, Lou L Q, Zhu S H, et al. Immunotherapy-related cystitis induced by nivolumab: a case report and review of the literature[J]. Urol Case Rep, 2025, 62: 103132.


